金属配位下吡啶环上α位C-H键活化途径
李邦玉,王耀荣
1.苏州市职业大学应用化学研究室,江苏苏州,215104;2.苏州大学材料与化学化工部,江苏苏州,215123
C-H键功能化是有机化学和金属有机化学最具吸引力的课题之一[1-2],而吡啶和喹啉等衍生物α位C-H键活化反应是其中重要的一类反应[3-4]。吡啶环广泛存在于生物碱中,它具有芳香性,易进行亲核取代反应,特别是在α位(2-位)与烷基锂或芳基锂发生烷基化、芳基化反应,与氨基钠发生氨基化反应等[5]。吡啶(喹啉环)配位到金属原子上后,环上电子云密度会进一步降低,更易发生亲核取代反应。本文结合笔者本人及所在课题组的科研成果,参考相关文献,论述在还原剂如活泼金属M、低价金属配合物、金属氢化物(M-H)、金属氨化物(M-N)和金属有机化物(M-C)等作用下,吡啶和喹啉环上N邻位C-H键的活化反应。
1 金属还原活化C-H键
1.1 活泼金属钠还原活化C-C偶联反应

1.2 低价金属配合物分子内还原活化
1.2.1 低价稀土元素还原活化C-H键
2010年,沈琪课题组发现,在席夫碱配体相同的情况下,可以制备出还原能力较弱的铕的相应二价席夫碱铕配合物;而难以得到还原能力较强的镱和钐等相应二价席夫碱稀土配合物,因为它们容易发生氧化还原反应生成三价稀土席夫碱配合物[7]。在-60℃下,将三齿席夫碱配体HL1的THF溶液慢慢滴加到二价稀土胺化物Ln[N(SiMe3)2]2(THF)2(Ln=Yb,Sm)的THF溶液中(摩尔比为2∶1),结果喹啉环和C=N基团之间形成C-C键而偶联起来。笔者推测形成机理见图2。席夫碱配体HL1与二价稀土胺化物Ln[N(SiMe3)2]2(THF)2按2∶1摩尔比反应得到理论上的配合物A;该二价席夫碱配合物稳定性差,在碱性条件下,中心二价稀土离子迅速活化喹啉环上α位的C-H化学键,消去二分之一H2分子,转变为含有Ln-C活性键的金属有机中间体B,中心离子由二价氧化为三价离子;接着活泼的Ln-C键加成到另一配体分子中的C=N双键中,形成最终的偶联配体稀土配合物。

图1 反应图示1
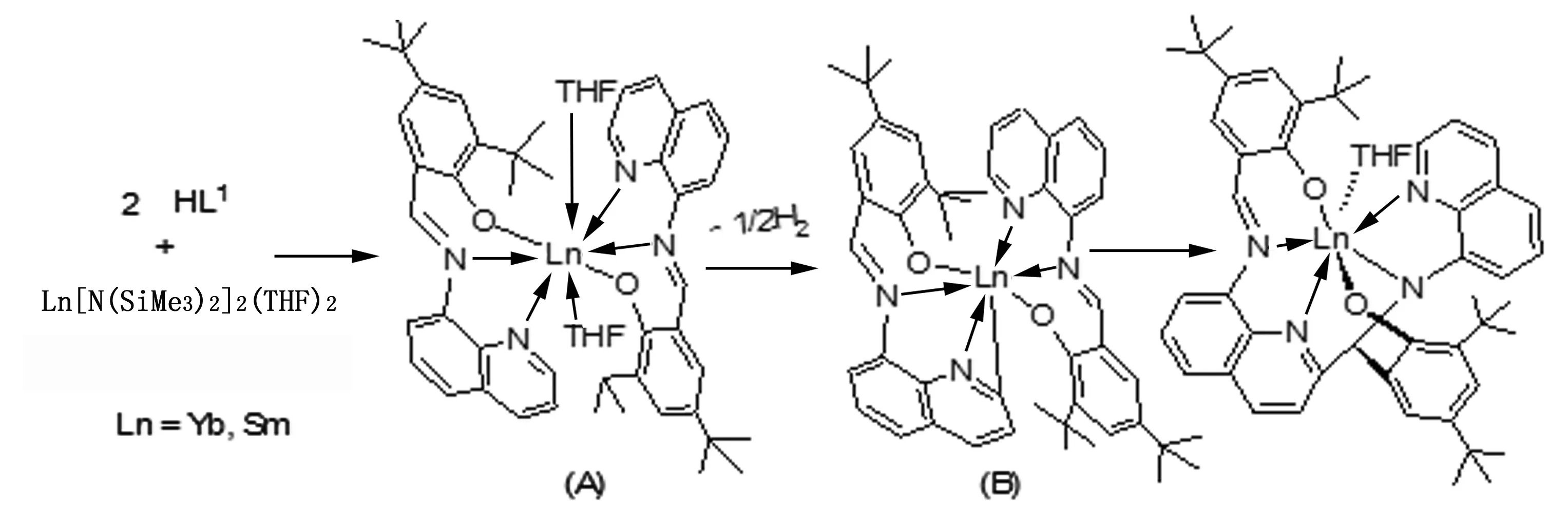
图2 反应图示2
1.2.2 第七副族零价金属元素还原活化C-H键
2008年,Zuhayra等报道了羰基锝A在室温下和吡啶反应,得到两个羰基被吡啶置换的产物B,B在加热下半小时就会氧化加成为C[Tc2(μ-H)(μ-NC5H4)(NC5H5)2(CO)6][8],即两个桥连的羰基被吡啶基和吡啶N邻位脱下来的H桥连(图3)。

图3 反应图示3
其中A、B中锝为零价,而产物C中锝显正一价,吡啶N邻位C-H键被低价金属锝(0)活化。同是第七副族的铼,也可发生类似的反应。1983年,Nubel课题组由羰基铼合成了H负离子和吡啶基负离子双桥连的配合物[Re2(μ-H)(μ-NC5H4)(CO)8](图4)[9]。
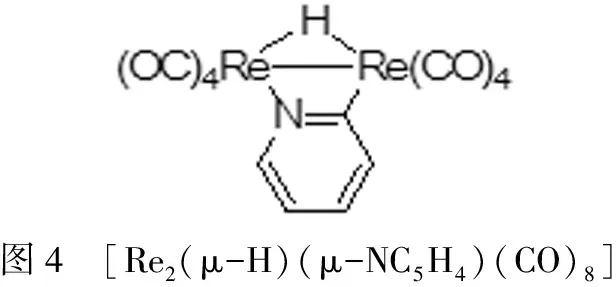
图4 [Re2(μ-H)(μ-NC5H4)(CO)8]
2 金属胺化物中氨基活化C-H键
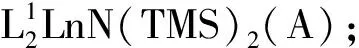

图5 反应图示4
3 金属氢化物活化C-H键

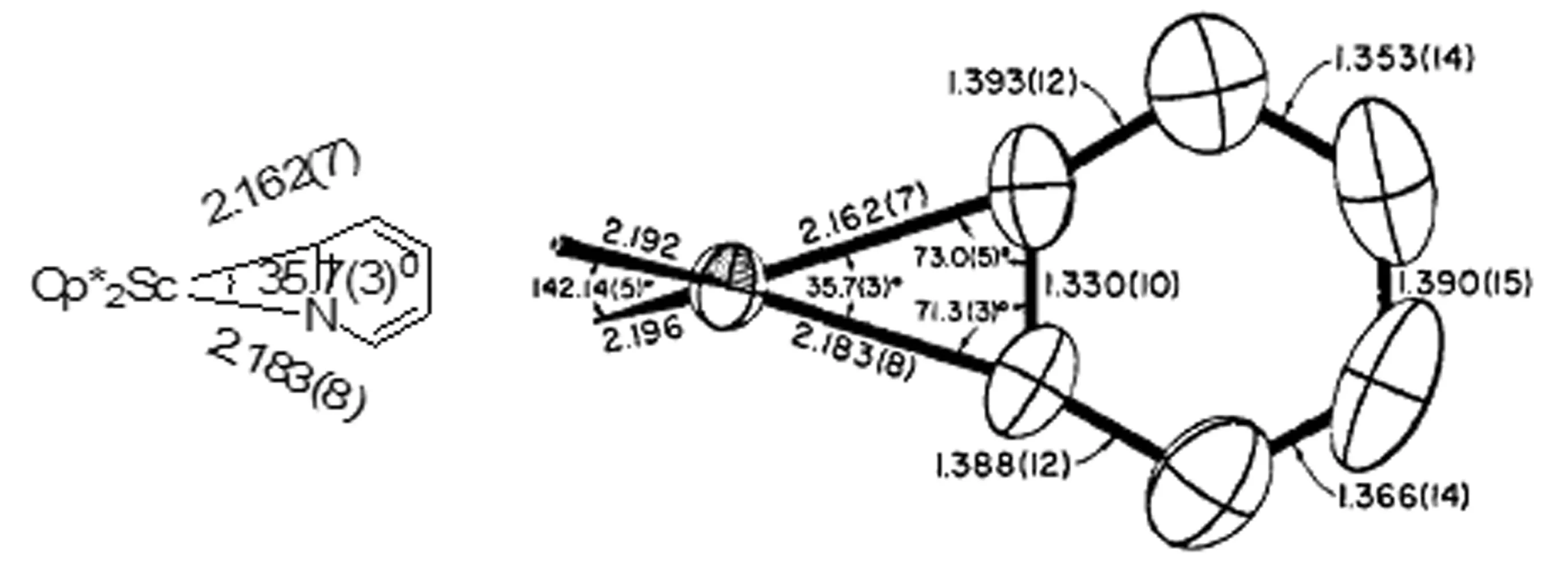
图6 配合物Cp*Sc(C,N-η2-C5H4N)结构图
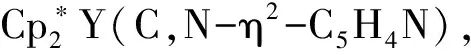
Watson等[13]在1983年就发现二甲茂镥氢化合物Lu(η5-C5Me5)2H也可以和吡啶等反应,生成吡啶2-位C-H键活化衍生产物Lu(η5-C5Me5)2(C,N-η2-C5H4N),反应式如下:
Lu(η5-C5Me5)2H+C5H5N=Lu(η5-C5Me5)2(C,N-η2-C5H4N)+H2
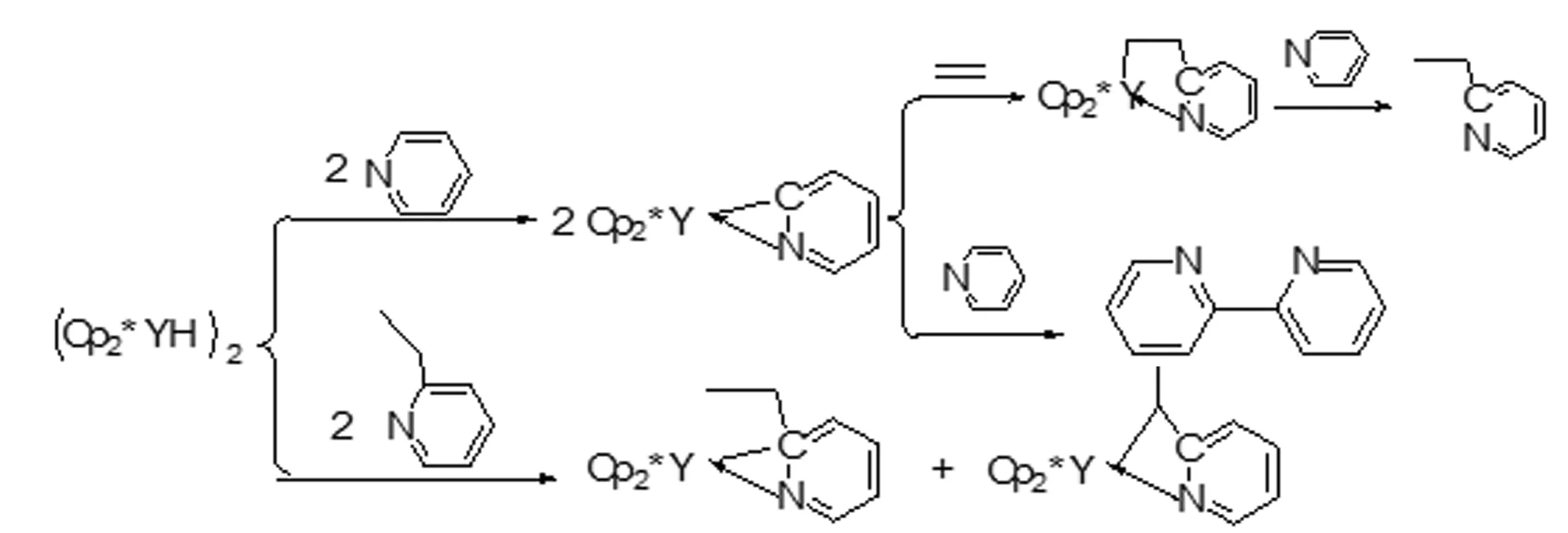
图7 反应图示5
4 金属有机化合物活化C-H键
4.1 稀土金属有机配合物活化C-H键
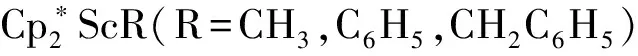
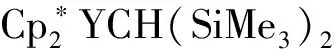
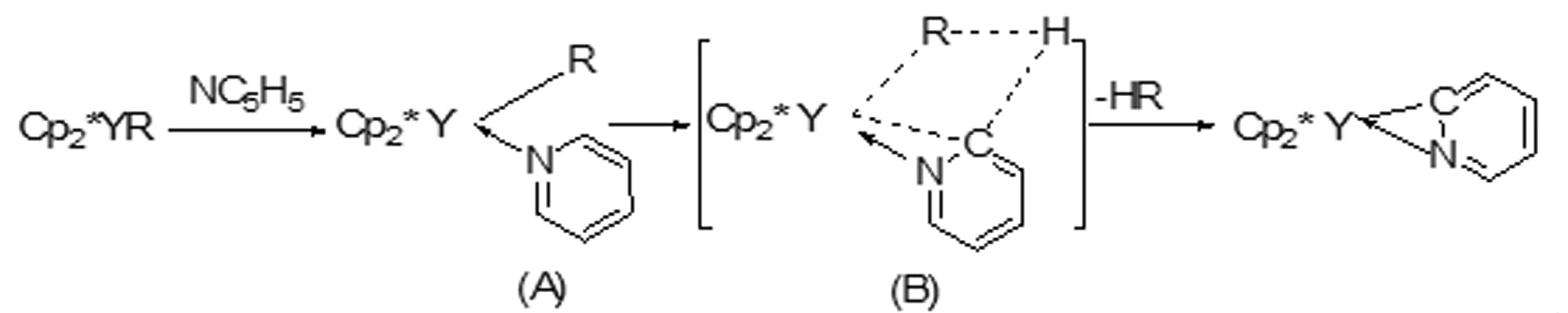
图8 反应图示6
2006年,Stefan等[15]用含Y-C键的离子对配合物[YMe(THF)6]2+[BPh4]2-和吡啶反应,配位的THF被吡啶置换,生成A,A中一个吡啶的2-位C-H键被相邻的甲基活化形成过渡态B,最后消除甲烷得到含Y-C键的吡啶配合物(图9)。

图9 反应图示7
Watson等[13]在1983年就发现二(五甲基茂)镥甲基化合物Lu(η5-C5Me5)2Me可以和吡啶等反应,生成吡啶2-位C-H键活化产物Lu(η5-C5Me5)2(C,N-η2-C5H4N),反应式如下:
Lu(η5-C5Me5)2Me+C5H5N=Lu(η5-C5Me5)2(C,N-η2-C5H4N)+CH4
2004年,Thomas小组[16]发现(联吡啶)镥(五甲茂基)(烷基)(胺基)稀土配合物与CO反应时,Lu-C活性键插入C-O键的同时活化了吡啶N邻位的C-H键,同时发生三个化学键的反应,结果由CO把联吡啶和三甲基硅基甲基偶联起来,形成一个新三齿配体配位到金属镥上。类似地,(联吡啶)镥(五甲茂基)(双烷基)稀土配合物也可以与CO反应,其中CO也把联吡啶和其中一个烷基偶联起来,说明反应中,也存在Lu-C键活化联吡啶N邻位C-H共价键的情况(图10)。
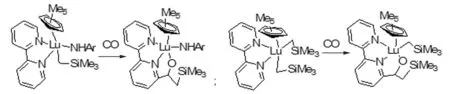
图10 反应图示8
其反应中间体可能是生成了含Lu-C键的Lu(联吡啶)(C,N-η2-C5H4N)配合物。如2007年,Jantunen课题组[17]发现,含一个THF、两个吡啶配位的五甲茂基镥双烷基配合物不稳定,特别是当通过抽真空的方式将配位在镥上的四氢呋喃脱去后,该配合物就转变为吡啶N邻位C-H键活化后产物A,其中,镥离子和吡啶上N邻位的C原子形成了Lu-C活性键,对此,他们通过配合物的X-射线单晶衍射图进行了确认。此活化产物A不稳定,他们在-35℃低温下培养出来的单晶放在室温下即会逐步解离,不到2天就基本分解掉了(图11)。

图11 反应图示9
4.2 第四副族金属有机配合物活化C-H键
1981年,Klei等[18]用Cp2TiR(R=alkyl)和2-取代吡啶或喹啉反应,2-位的C-H键被活化,生成含Ti-C的吡啶Ti配合物,如(η5-C5H5)2Ti(C,N-η2-C5H4N)。1989年,Richard等[19]用Cp2Zr(CH3)(THF)(A)和甲基吡啶反应,常温下,在二氯甲烷中反应20分钟,得到两种异构体B(含量比为1∶1),分离产率达84%(核磁监测产率达90%),反应过程如图12。B和丙烯常温常压下反应45分钟可得到插入产物C,产率接近100%。在常温和低压下催化甲基吡啶和丙烯偶联,得到单一产物D。
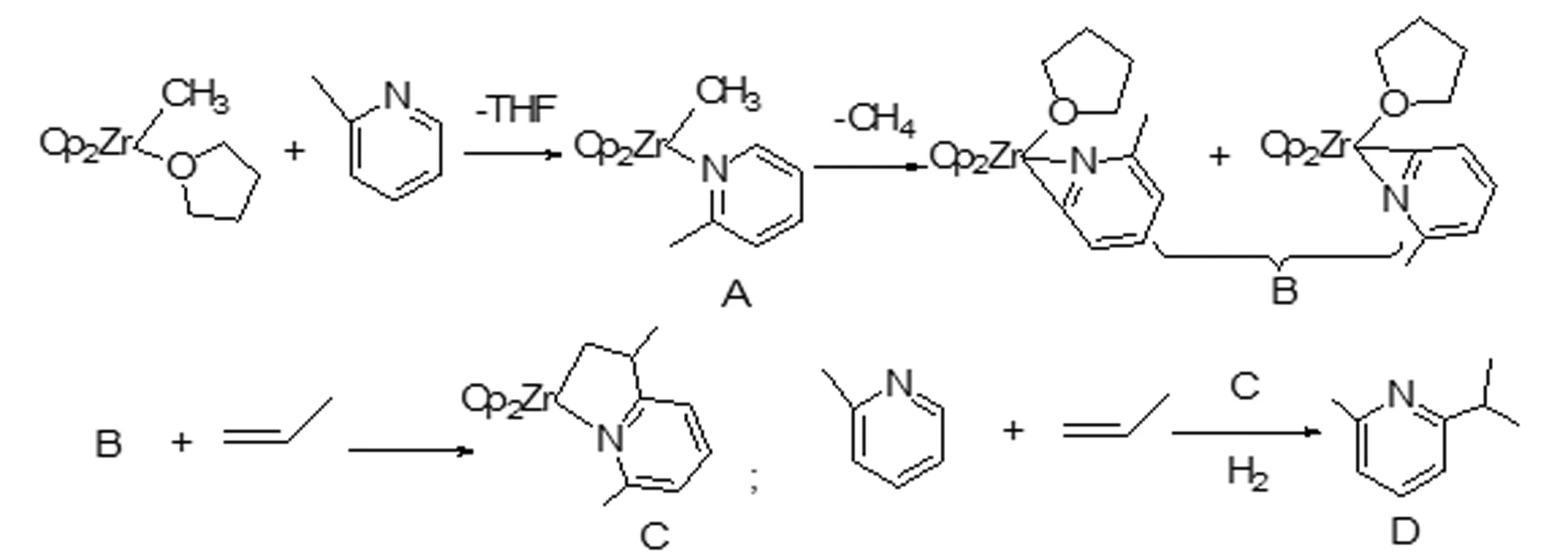
图12 反应图示10
综上所述,当吡啶和喹啉等衍生物在配位到金属上后,通过活泼金属还原剂、低价金属配合物、金属氢化物、金属氨化物和金属有机化物等可以活化N邻位C-H键,导致C-H键断裂,进而得到各种取代吡啶化合物及其配合物。随着研究的深入,人们将会发现更多、更好的活化试剂,活化研究会更系统、更有规律可循。
参考文献:
[1]Ritleng V,Sirlin C,Pfeffer M.Ru-,Rh-,and Pd-Catalyzed C-C Bond Formation Involving C-H Activation and Addition on Unsaturated Substrates:Reactions and Mechanistic Aspects[J].Chem Rev,2002,102:1731-1770
[2]Tsuchikama K,Kuwata Y,Tahara Y-K,et al.Rh-Catalyzed Cyclization of Diynes and Enynes Initiated by Carbonyl-Directed Activation of Aromatic and Vinylic C?H Bonds[J].Org Lett,2007,9:3097-3099
[3]Chen D,Li Y,Wang B Q,et al.Reactions of Pyridyl Side-Chain-Functionalized Cyclopentadienes with Metal Carbonyl:Intramolecular C-H Activation of Pyridine[J].Organometallics 2006,25:307-310
[4]Machado R A,Goite M C,Arce A J,et al.Two isomeric products [Os3(μ-H)(C14H9N4)(CO)9] formed by orthometallation of the luster [Os3(C14H10N4)(CO)10].containing the chelating ligand 2,3-bis(2-pyridyl)pyrazine[J].J Organomet Chem,2005:690,622-628
[5]邢其毅,徐瑞秋,周政.基础有机化学[M].北京:高等教育出版社,1991:1038-1054
[6]Li B Y ,Yao Y M,Wang Y R,et al.Reduction of imine of samarium Schiff base chloride by sodium-Formation of a novel samarium complex through unprecedented C-C coupling and hydrogen transfer reaction [J].Inorg Chem Commun,2008,11(3):349-352
[7]Han F B,Li B Y,Zhang Y,et al.Quinoline Ring C-H Bond Activation in Bis(3,5-di-tert-butylsalicylidene)-8aminoquinoline Bis(trimethylsilyl)amido Lanthanide Complexes[J].Organometallics 2010,29:3467-3470
[8]Zuhayra M,Lützen U,Lützen A,et al.C-H bond activation of coordinated pyridine:Ortho-pyridyl-di-technetiumhydridocarbonyl metal cyclus.Crystal structure and dynamic behaviour in solution[J].Inorg Chem,2008,47:10177-10182
[9]Nubel P O,Wilson S R,Brown T L.Crystal and molecular structure and substitution reactivity of (μ-hydrido)(μ-pyridyl)dirhenium octacarbonyl,(μ-H)Re2(CO)8(μ-NC5H4).Crystal and molecular structure of (μ-hydrido)( μ-pyridyl)(trimethylamine N-oxide)dirhenium heptacarbonyl,(μ-H)Re2(CO)7(μ-NC5H4)(Me3NO)[J].Organometallics 1983,2:515-525
[10]Han F B,Teng Q Q,Zhang Y,et al.Influence of Schiff Base and Lanthanide Metals on the Synthesis,Stability and Reactivity of Monoamido Lanthanide Complexes Bearing Two Schiff Bases[J].Inorg Chem,2011,50:2634-2643
[11]Mark E T,Steven M B,Bulls A R,et al.“σ Bond Metathesis” for C-H Bonds of Hydrocarbons and Sc-R(R=H,alkyl,aryl) Bonds of Permethylscandocene Derivatives.Evidence for Noninvolvement of the π System in Electrophilic Activation of Aromatic and Vinylic C-H Bonds[J].J Am Chem Soc,1987,109:203-219

[13]Watson P L.Facile C-H activation by lutetium-methyl and lutetium-hydride complexes[J].J Chem SOC,Chem Commun,1983:276-277
[14]Klaas H H,Ytsen W.Reactions of Yttrium-Carbon Bonds with Active Hydrogen-Containing Molecules.A Useful Synthetic Method for Permethylyttrocene Derivatives[J].Organometallics 1987,6:2053-2060
[15]Stefan A,Benjamin R E,Peter M,et al.Formation of a Dicationic Yttrium η2-Pyridyl Complex from an Yttrium Methyl Dication by C-H Activation of Pyridine[J].Organometallics 2006,25:793-795
[16]Thomas M C,John C G,Brian L S,et al.C-H activation of a 2,2′-bipyridine ligand within (mono)pentamethylcyclopentadienyl lutetium complexes[J].Chem.Commun,2004:1398-1399
[17]Jantunen K C,Scott B L,Gordon J C,et al.Reactivity of (C5Me5)Lu(CH2SiMe3)2(THF) with Pyridine Ring Systems:Synthesis and Structural Characterization of an η2-(N,C)-Pyridyl (Mono)pentamethylcyclopentadienyl Lutetium(III) Complex[J].Organometallics 2007,26:2777-2781
[18]Klei E,Teuben J H.reaction of titanocene alkyls with pyridines;a novel type of cyclometallation reaction[J].J Organomet Chem,1981,214:53-64
[19]Richard F J,Dennis F T.Zirconium-catalyzed coupling of propene and.alpha.-picoline[J].J Am Chem Soc,1989,111(2):778-779

