盐湖卤水硼镁分离工艺及高纯氧化镁的制备
于培峰,杨喜云,徐 徽,石西昌,陈 亚,颜果春
(中南大学 冶金科学与工程学院,长沙 410083)
青海察尔汗盐湖是一个大的钾肥生产基地, 在生产钾肥的同时排出大量富含硼、镁、锂的老卤,若不加以利用,将给盐湖的生态造成严重破坏,同时造成资源的严重浪费[1−3]。近年来,随着锂辉石等矿石资源的日益贫乏和枯竭,盐湖卤水锂资源的研究和开发越来越受到人们的关注和重视,科技界做了大量的工作,现已开发出4种工艺技术路线,即煅烧法[4−5]、膜分离法[6−7]、离子交换吸附法[8−9]和硼、镁、锂联合提取法[10]。资源的开发利用不仅仅是一项技术开发,更是一项系统工程,在提取一种资源的同时,要兼顾对其他资源的影响,做到盐湖资源综合开发和利用,在这4种方法中,镁、锂、硼联合提取法是最有发展前景,最有可能实现低品质盐湖资源高效利用的方法。联合提取硼、镁、锂的关键是彻底分离硼与镁锂、镁与锂。由于硼在沉镁时易被 Mg(OH)2吸附而共沉,硼在Mg(OH)2煅烧过程中转变为B2O3进入氧化镁。混杂在氧化镁中的B2O3在高温下可与CaO生成低共熔物,同时与CaO·SiO2生成三元低共熔物(熔点1 000 ℃左右),对氧化镁的高温性能产生不利影响,卤水彻底分离硼成为制备高纯氢氧化镁和氧化镁的技术关键。
目前,从卤水中提取硼酸,使硼镁分离的主要方法有酸化法[11]、沉淀法[12]、溶剂萃取法[13]、离子交换法等,其中酸化法、沉淀法、溶剂萃取法在国外已应用于工业化生产,而在国内尚处于研究阶段。本文作者根据盐湖老卤卤水硼、镁含量高的特点,采用硫酸法−离子交换法联合提硼,使硼与镁锂高效分离;采用氨法沉镁实现镁与锂分离,详细研究卤水 pH值、吸附温度、吸附时间、树脂用量对硼分离效果的影响,用动态法研究卤水流速、交换柱高径比对硼分离效果的影响,同时考察卤水硼浓度对氢氧化镁硼含量的影响。
1 实验
1.1 实验原料
实验采用的卤水为青海察尔汗盐湖中提取钠、钾盐后的老卤,对其进行ICP-AES全分析,其成分如表1所示。卤水pH值为4.20,密度为1.32 g/mL,镁离子浓度为110.92 g/L,锂离子浓度为2.50 g/L,镁锂比为 44.30。在离子交换法吸附硼过程中使用硼特性吸附树脂—XSC-700,其各项参数见表2。
1.2 实验过程
1.2.1 酸法提硼
向250 mL卤水中加入适量的浓硫酸(98%),在搅拌速度为100 r/min、反应温度60 ℃下反应1 h,然后置于恒温冷却槽中冷却一段时间过滤,测定固体中硼酸含量,计算硼的提取率。
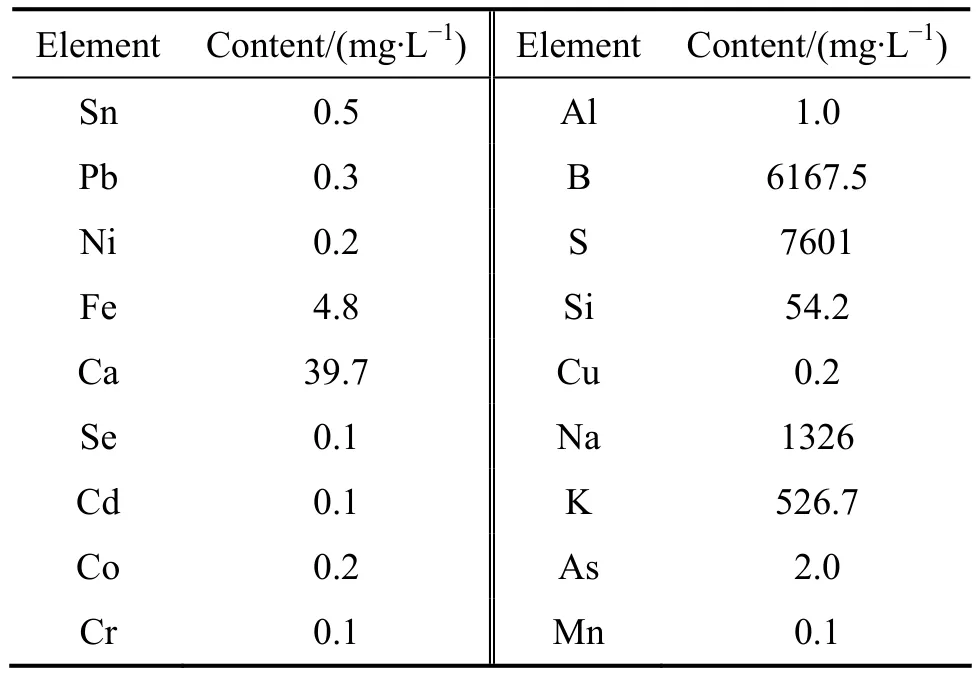
表1 卤水的ICP-AES分析结果Table 1 ICP-AES analysis results of brine

表2 XSC-700树脂的物理化学性质Table 2 Physical and chemical properties of XSC-700
1.2.2 离子交换法提硼
分为静态法和动态法两种。静态法是量取100 mL酸法提硼后卤水,加入一定体积的湿树脂,吸附一定时间,用ICP分析吸附前后卤水中的硼含量,计算吸附率。动态法是在离子交换柱中进行的,交换柱直径为23 mm,长500 mm,卤水经恒流泵以一定的流速从下至上通过交换柱,用自动取样器收集适量的卤水,用ICP分析硼含量。
1.2.3 氨法沉镁
对离子交换法提硼后卤水氨法沉镁。首先将底液(300 mL纯水,15 g Mg(OH)2,5.1 g NH4Cl)加入到2 L三口烧瓶。待底液温度升至 50 ℃时往烧瓶中以 20 mL/min速度滴加卤水,同时滴加浓氨水,控制pH值为10,开启搅拌,控制搅拌速度为100 r/min,待500 mL卤水滴加完毕后,继续滴加浓氨水(按物质的量计过量20%),反应结束后60 ℃恒温陈化30 min,过滤、洗涤、烘干得到氢氧化镁。
1.2.4 氢氧化镁煅烧
将氢氧化镁分别在950 ℃、1 100 ℃、1 200 ℃、1 500 ℃温度下煅烧2 h,得到氧化镁产品。
1.3 分析检测
镁离子浓度采用EDTA滴定法分析,高硼卤水中的硼采用甘露醇滴定,低硼卤水中的硼以及氢氧化镁、氧化镁中杂质元素采用电感耦合等离子光谱发生仪 ICP-OES(American Intrepid ⅡXSP)分析。
氢氧化镁的物相采用日本理学D/max−2550 X射线衍射仪进行检测分析,辐射源为Cu Kα(λ=0.154 06 nm),石墨为单色器,管压为40 kV,管电流为40 mA,扫描范围为10°~80°;用 JEOL公司JSM 5600−LV扫描电子显微镜观察氢氧化镁产品形貌特征。
2 结果与讨论
2.1 卤水提硼
由于卤水中硼浓度高,先采用硫酸法提硼。在条件试验的基础上,确定酸法提硼的最佳工艺条件为:浓硫酸用量14 mL/L卤水、反应温度60 ℃、反应时间1 h、冷却温度−5 ℃、冷却时间4 h,硼的提取率达到80%,提硼后卤水硼含量为1 200 mg/L。
硼酸在水中有一定的溶解度(表3),0 ℃时溶解度为2.77 g,−5 ℃时溶解度为2.51 g,酸法不能完全提取卤水中的硼,需用离子交换法对酸法提硼后的卤水深度提硼,论文主要讨论离子交换法提硼的主要影响因素。
2.1.1 吸附时间对硼吸附率及吸附性能的影响
在100 mL卤水中树脂的量为62 mL、温度为25℃、卤水pH为6.0的条件下,吸附时间对硼提取的影响结果如图1所示。

表3 硼酸在水中的溶解度Table 3 Solubility of boric acid
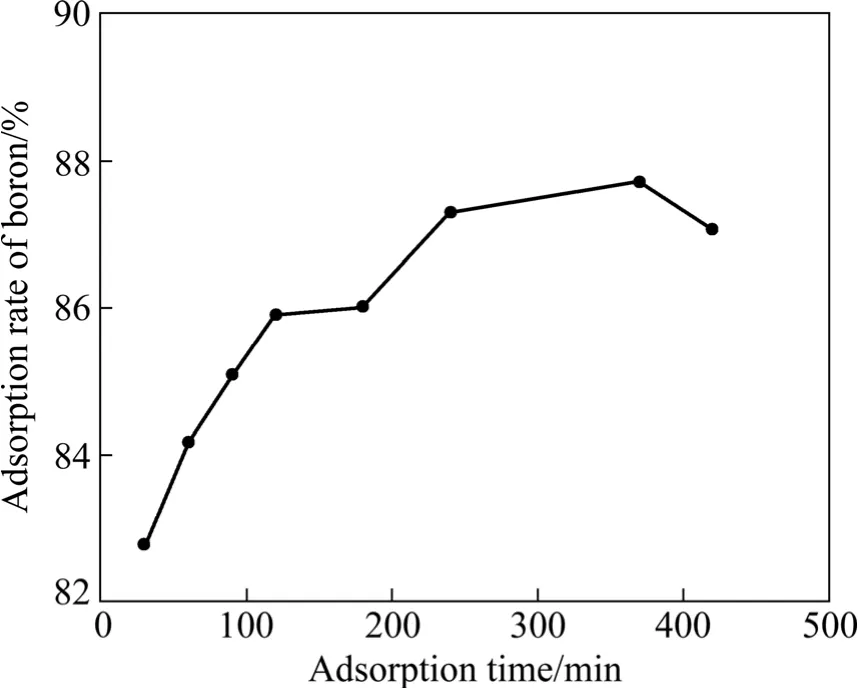
图1 不同吸附时间的硼吸附率Fig.1 Adsorpition rate of boron at different adsorption times
由图1可以看出,当吸附时间小于240 min时,随着吸附时间的延长,硼吸附率增大,当吸附时间大于240 min时,硼吸附率增加缓慢,吸附过程已经达到平衡。因此,吸附时间可以定为4 h。
采用准一级动力学模型和准二级动力学模型对吸附实验结果进行模拟得到相应的反应动力学参数,进而得到吸附过程的反应级数。两种模型方程分别为[14−15]
Lagergen准一级动力学模型:
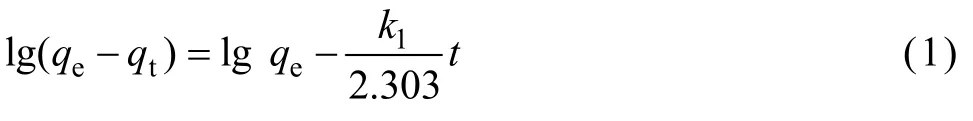
准二级动力学模型:

式中:qe和 qt分别为平衡和时间 t时的吸附容量,mg/mL;k1、k2分别为准一级、准二级动力学速率常数。
图2所示为不同吸附时间单位树脂的吸附容量,分别以lg(qe−qt)和t/qt对t作图可得两条直线,模拟结果如图3所示,表4所列为两种动力学模型的相关参数。
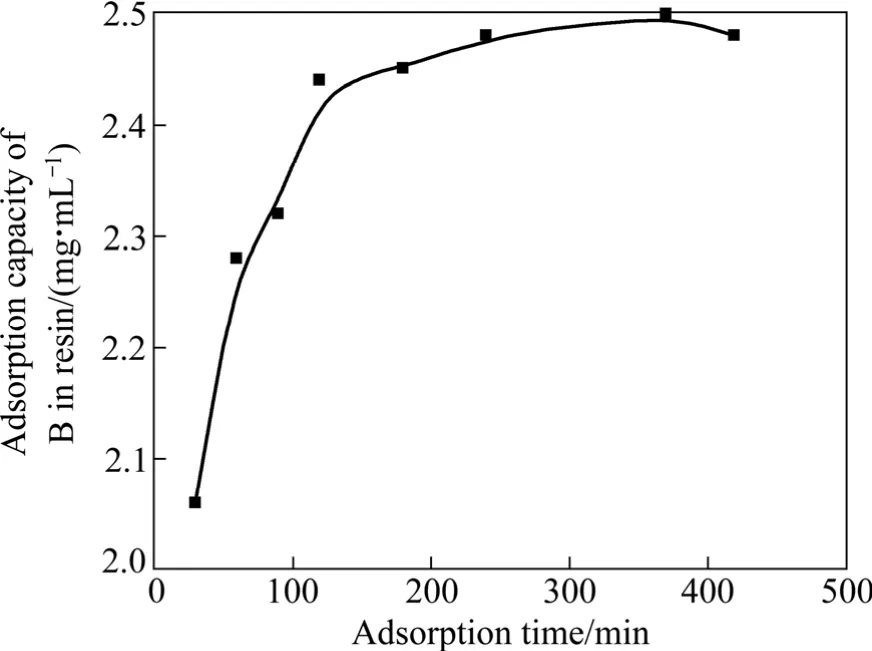
图2 不同吸附时间单位树脂的吸附容量Fig.2 Adsorption capacity of B in resin at different adsorption times
由表4可知,采用准二级动力学模型进行模拟时,相关系数R2可达0.99以上,表明吸附过程类似于化学吸附特性,与浓度关系密切。
2.1.2 卤水pH值对硼吸附的影响
卤水在碱性环境中析出氢氧化镁沉淀,它吸附卤水中的硼,干扰实验,本文作者只考察pH值为2、3、4、5、6时硼的吸附效果。实验条件为:100 mL卤水中树脂的量62 mL,吸附时间4 h,温度25 ℃,结果如图4所示。

图3 吸附动力学模型模拟Fig.3 Adsorption kinetic models∶ (a)Pseudo-first order model; (b)Pseudo-second order model

表4 动力学模型相关参数Table 4 Parameters of kinetic model
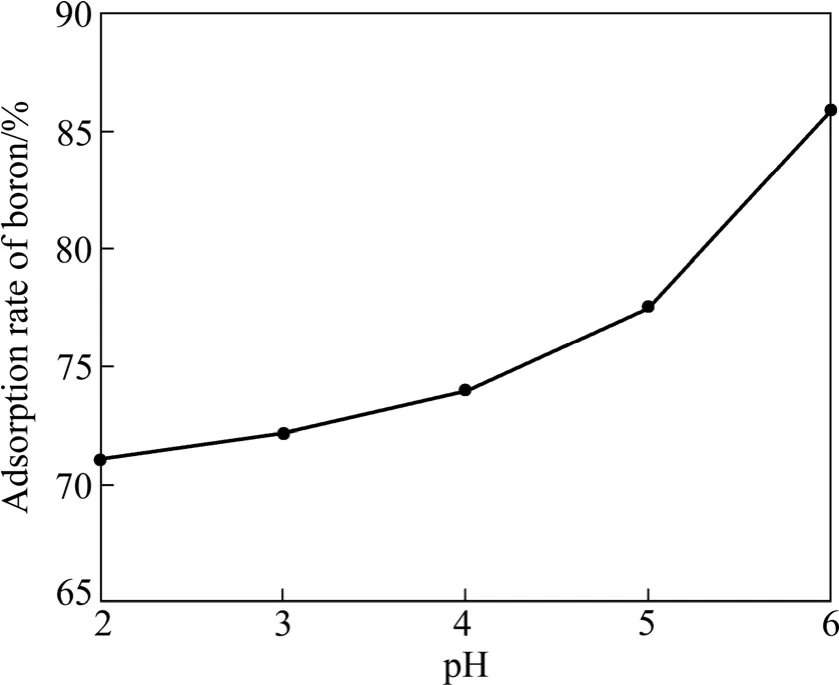
图4 卤水pH值对硼吸附效果的影响Fig.4 Effect of pH of brine on adsorption efficiency of B
从图4可以看出,随pH值增大,硼吸附率升高。树脂对硼的吸附量与pH值的依赖关系与硼的存在形式和树脂吸附作用机理有关[16−17]。硼在溶液中以B(OH)3、 B(OH)4−、 B3O3(OH)4−、 B3O3(OH)32−、B4O5(OH)42−和B5O6(OH)4−形式存在,当硼浓度低于0.1 mol/L时,主要以B(OH)3和B(OH)4−的形式存在, pH较低时,B(OH)4−含量较低,主要以B(OH)3的形式存在,pH较高时,主要以B(OH)4−的形式存在,且溶液中B(OH)3与B(OH)4−可以相互转化。当含硼液与吸附树脂作用时,只有 B(OH)4−能与树脂上的官能团形成稳定络合物[18−19],故随着pH值增加,B(OH)4−浓度增加,树脂对硼的吸附量也增大;pH值较低时,树脂对硼也有一定的吸附量,由于树脂中的 OH−促进了B(OH)3向B(OH)4−转化,进而提高树脂对硼的吸附量。因此,选定离子交换深度提硼时卤水pH值为6.0。
2.1.3 树脂量对硼吸附的影响
在卤水pH值6、吸附时间4 h、温度为25 ℃的条件下,进行不同树脂量的吸附实验,结果如图5所示。
由图5可知,树脂加入量越多,硼吸附率越高,100 mL卤水中树脂加入量达到66时,硼的吸附率即可达95%以上。但随着树脂量的加大,树脂的单位吸附容量呈下降趋势。1 mL树脂对B的最低吸附容量为1.77 mg,最高为3.20 mg,1 mL树脂对B的理论吸附容量为 5.00 mg,实际吸附量仅为理论吸附量的35.4%~64.0%。XSC-700树脂在吸附硼酸根离子的同时会释放出氢离子,碱性条件有利于硼离子的吸附,由于卤水呈酸性,因此降低了树脂从卤水中吸附硼的容量,同时卤水中存在大量的Mg2+,Cl−和SO42−干扰硼的吸附。

图5 树脂加入量对硼吸附效果的影响Fig.5 Effect of resin volume on adsorption efficiency of B
2.1.4 温度对硼吸附的影响
100 mL卤水中树脂用量为66 mL,pH值为6,吸附时间为4 h,温度对硼吸附率的影响结果如图6所示。
从图6可以看出,温度对硼的吸附率影响不大,硼的吸附主要受扩散控制[20],升高温度,卤水黏度降低,硼酸根离子的扩散速率增大,达到吸附平衡的时间短。由图6可知,20 ℃时,吸附4 h后硼的吸附率已到了97%,所以吸附过程在常温25 ℃进行即可。

图6 吸附温度对硼吸附效果的影响Fig.6 Effect of adsorption temperature on adsorption efficiency of B
2.1.5 流速对硼吸附的影响
采用离子交换柱进行卤水的吸附在实际应用中可操作性强。研究表明:时间、温度、pH值和树脂量的交换柱实验结果与静态结果是一致的,所以在交换柱实验研究中只考察了卤水流速和交换柱高径比对硼吸附效果的影响。
酸化脱硼后卤水硼浓度为1 200 mg/L、pH值为6、交换柱高径比为17(树脂量为162 mL),在25 ℃下进行操作,分别考察流速为1、2、3 mL/min时硼吸附效果,得到相应的流出液中硼浓度随时间的变化曲线,如图7所示。
由图7可知,卤水流速增大,穿透点(流出液硼浓度为1 mg/L时为穿透点)出现越早。由于卤水流速增大,卤水和树脂的接触时间缩短,卤水中的硼没有足够的时间和树脂发生吸附反应。流速为 1、2、3 mL/min时,1 mL树脂穿透吸附B的容量分别为4.89、3.34、2.00 mg,说明树脂的穿透吸附容量随着卤水流速的增大而下降。由于流速低,单位时间吸附的卤水少,生产效率低,综合考虑选择流速为2 mL/min。
2.1.6 交换柱高径比对硼吸附的影响
在卤水硼浓度为1 200 mg/L、pH为6.0,卤水流速为2 mL/min、25 ℃的条件下,分别考察高径比(H/D)为11、14、17时硼吸附效果,得到了硼的穿透曲线如图8所示。

图7 卤水流速对硼吸附的影响Fig.7 Effect of flow rate of brine on adsorption efficiency of B

图8 高径比对硼吸附的影响Fig.8 Effect of ratio of height to diameter (H/D)of exchange column on adsorption efficiency of B
由图8可知,交换柱高径比越小,穿透点出现越早。交换柱高径比越小,交换柱内树脂高度降低,在同样的卤水流速下,卤水的吸附时间越短。高径比(H/D)为11、14、17时,1 mL树脂穿透吸附B的量分别为1.56、1.78、3.34 mg,说明交换柱高径比增加,树脂穿透吸附容量增大。
卤水成分复杂,含有许多其他离子,为考察树脂对硼的吸附选择性,分别测定流出液 Mg2+、Na+、SO42−、K+的穿透曲线,结果如图9~10所示。实验条件:交换柱高径比为17,卤水流速为2 mL/min,酸化后卤水pH值调至6.0,酸化后卤水的硼浓度为1 200 mg/L,镁离子浓度为 85.81 g/L。由图9~10 可知,Mg2+、Na+、SO42−、K+在起始50 min有较大的吸附,当吸附时间达到100 min后,基本不被吸附。由于XSC-700硼特性吸附树脂是一种多孔结构,有比较大的比表面、并且卤水黏度较大,对Mg2+、Na+、SO42−、K+有一定的截留作用,但是这种作用不同于紧密的化学键,用去离子水淋洗时很容易把这些离子洗下来,可以实现硼与 Mg2+、Na+、SO42−、K+的分离。

图9 Mg2+和SO42−的穿透曲线Fig.9 Penetration curves of Mg2+ and SO42−
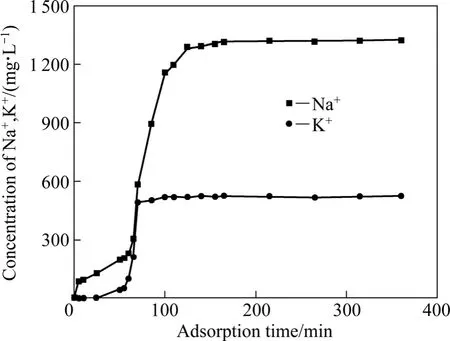
图10 Na+和K+的穿透曲线Fig.10 Penetration curves of Na+ and K+
2.1.7 XSC-700树脂的洗脱
取吸附饱和后的 50 mL XSC-700螯合树脂先水洗,再采用不同浓度的盐酸溶液在室温下进行洗脱30 min,考察不同浓度的盐酸对硼洗脱的影响,其结果如图11所示。
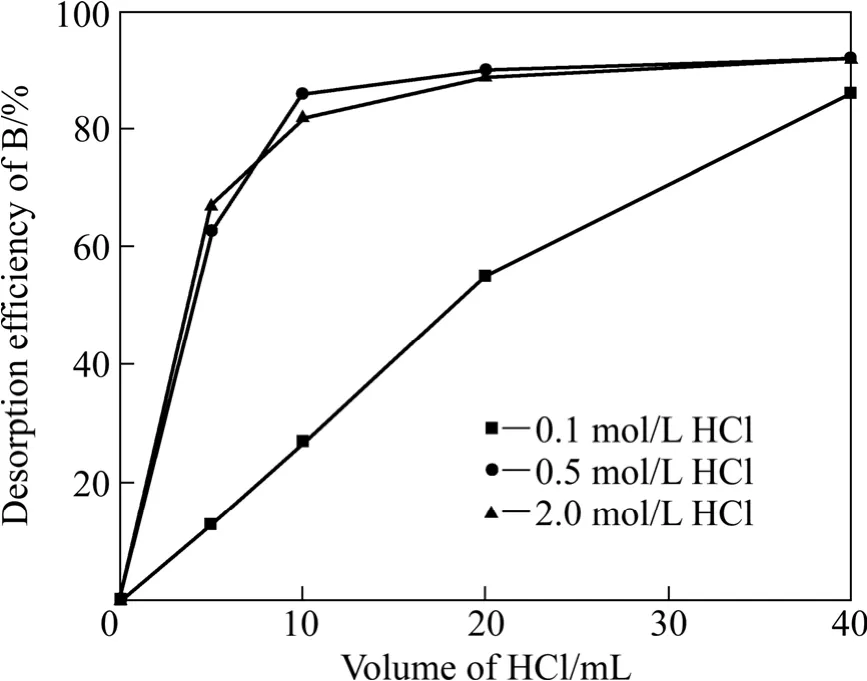
图11 不同浓度盐酸对硼洗脱率的影响Fig.11 Effects of different concentrations of HCl on desorption efficiency of B
由图11可知,3种浓度的盐酸均可使树脂中硼的洗脱率达到90%。XSC-700螯合树脂对B(OH)4−吸附能力很强,在酸性溶液中 B(OH)4−将转化为 H3BO3,从而解吸下来,故选择20 mL 0.5 mol/L HCl作为洗脱剂可以使硼的洗脱率达92%,而解吸液中硼浓度为1.8 g/L,经浓缩后可直接制取硼酸。
2.2 氨法沉镁
由上述实验结果可知,卤水中硼提取率受树脂的使用量、吸附时间和卤水流速等因素影响。通过调整这些参量可以得到一系列不同硼浓度的卤水,研究卤水中硼浓度对氢氧化镁中硼含量的影响,结果见表5。为了研究卤水中的硼是否沉淀进入氢氧化镁产品,假设硼全部进入氢氧化镁,通过卤水中镁的浓度和氢氧化镁的产率可以计算出氢氧化镁产品中硼的理论含量,将理论硼含量也一并列在表5中。

表5 不同硼浓度卤水条件下所得氢氧化镁的浓度Table 5 Mg(OH)2 concentration prepared from brine under different boron concentrations
比较表5中氢氧化镁的理论硼含量与ICP所测硼含量可以发现,卤水中的硼大部分进入氢氧化镁产品中,对其纯度影响不大,但硼的存在影响氢氧化镁的性能,所以得到硼浓度低的卤水是制备高纯氢氧化镁的必备条件,控制卤水硼浓度低于 5 mg/L,氢氧化镁纯度可达98%。
对纯度为98%的氢氧化镁产品进行X射线衍射和扫描电镜分析,其衍射谱和SEM像分别如图12和13所示。由图12可知,所得氢氧化镁的结晶状态良好、无杂相。在氨法沉镁的过程中,采用氯化铵−氨水缓冲体系来调节反应的 pH值,氢氧化镁的过饱和度相对较小,粒子成核数目减少,生长速度加快,所得氢氧化镁颗粒较大(见图13),过滤性能较好。
对氨法沉镁的母液进行分析,镁离子浓度为22.18 g/L,锂离子浓度为2.5 g/L,镁锂比由44.3(原卤水)降低到8.8。采用碳酸氢铵二段沉镁可以将镁彻底除尽,为后续制备碳酸锂提供有利条件[20]。

图12 氢氧化镁的XRD谱Fig.12 XRD pattern of Mg(OH)2

图13 氢氧化镁的SEM像Fig.13 SEM image of Mg(OH)2
2.3 氢氧化镁煅烧
将纯度为98.0%的氢氧化镁分别在950 ℃、1 100℃、1 200 ℃、1 500 ℃下煅烧2 h,所得氧化镁产品的硼含量如表5所列,对在950 ℃和1 500 ℃下煅烧得到的氧化镁产品进行ICP-AES全分析,其结果分别如表6和7所列。

表5 不同煅烧温度下氧化镁纯度及硼含量Table 5 Mg(OH)2 purity and boron content at different calcining temperatures
由表5可知,煅烧温度从950 ℃提高至1 500 ℃时,氧化镁的纯度明显提高。由表6和7可知,煅烧温度升高,硫含量显著降低。硫主要以硫酸镁形式存在于氢氧化镁中,硫酸镁在1150℃时会分分解成氧化镁、二氧化硫和氧气。硼在煅烧过程分解很少,因此氧化镁纯度的提高是由于硫酸盐杂质分解所致,卤水彻底除硼是得到低硼含量氧化镁的保证。

表6 950 ℃煅烧所得氧化镁的ICP-AES分析结果Table 6 Analysis results of ICP-AES of MgO by calcination at 950 ℃(μg/g)

表7 1 500 ℃煅烧所得氧化镁的ICP-AES分析结果Table 7 Analysis results of ICP-AES of MgO by calcination at 1 500 ℃(μg/g)
在最佳工艺条件下煅烧氢氧化镁所得氧化镁产品纯度达到99.8%,氧化镁的化学成分超过电工级(纯度为 98.2%~99.2%)、陶瓷级(纯度为 94.0%~99.0%)和耐火材料级(纯度为 97.3%~99.1%)氧化镁产品的标准,符合高纯氧化镁的要求。
3 结论
1)采用硫酸法提硼,使硼镁初步分离,硼的提取率达80%,卤水硼浓度降至1 200 mg/L。
2)采用离子交换树脂对酸化后卤水深度除硼,当卤水pH值为6,100 mL卤水中树脂用量为66 mL,常温下吸附4 h时后,硼吸附率达95%以上,实现了硼与镁、锂的分离;在卤水流速为2 mL/min、交换柱高径比为17、卤水硼浓度为1 200 mg/L、pH值为6的条件下,硼的穿透吸附容量达3.34 mg。
3)采用氨法沉镁,卤水的镁锂质量比由原来的44.3降低到8.8,实现镁、锂的初步分离。
4)由硼浓度为5 mg/L的卤水可制得纯度为98%、过滤性能良好的氢氧化镁,1 500 ℃下煅烧氢氧化镁可以得到纯度为 99.8%的氧化镁产品,符合高纯氧化镁的要求。
5)该工艺综合利用了卤水中的硼与镁,实现了硼、镁、锂高效分离,为后续制备碳酸锂创造了有利条件。
[1]李 浩, 唐中凡, 刘传福, 雷光元.新疆罗布泊盐湖卤水资源综合开发研究[J].地球学报, 2008, 8(4)∶ 517−524.LI Hao, TANG Zhong-fan, LIU Chuan-fu, LEI Guang-yuan.Comprehensive exploitation and research of brine resources[J].Journal of Acta Geoscien Sinica, 2008, 8(4)∶ 517−524.
[2]许荣辉, 李海民.高纯氧化镁制备原理初探[J].盐湖研究,2003, 11(4)∶ 39−41.XU Rong-hui, LI Hai-min.The principles in preparing of high purity magnesium oxide[J].Journal of Salt Lake Research, 2003,11(4)∶ 39−41.
[3]杨建元, 程温莹, 邓天龙, 高晶岩.东台吉乃尔湖晶间卤水综合利用研究(煅烧法提锂工艺)[J].无机盐工业, 1996(2)∶29−33.YANG Jian-yuan, CHENG Wen-ying, DENG Tian-long, GAO Jing-yan.Comprehensive exploitation and research on brines from Jilaier salt lake of Dongtai (extraction of lithium by calcination)[J].Inorganic Chemicals Industry, 1996(2)∶ 29−33.
[4]张占良, 索智录.盐湖卤水煅烧制取含锂氧化镁的实验研究[J].内蒙古石油化工, 2008(8)∶ 19−20.ZHANG Zhan-liang, SUO Zhi-lu.Experimental study on manufacturing magnesium oxide containing lithium with calcining the bittern of salt lake[J].Inner Mongulia Petrochemical Industry, 2008(8)∶ 19−20.
[5]WEN Xian-ming, MA Pei-hua, ZHU Chao-liang, HE Qiong,DENG Xiao-chuan.Preliminary study on recovering lithium chloride from lithium-containing waters by nanofiltration[J].Separation and Purification Technology, 2006, 49∶ 230−236.
[6]宋卫得, 王海增, 邢 坤, 郭鲁钢, 李冬梅.纳滤膜分离技术及其在盐湖卤水资源开发中的应用[J].盐湖研究, 2006, 14(4)∶56−60.SONG Wei-de, WANG Hai-zeng, XING Gun, GUO Lu-gang, LI Dong-mei.Nanofiltration technology and its application in the comprehensive utilization of bittern resources[J].Journal of Salt Lake Research, 2006, 14(4)∶ 56−60.
[7]NADAV N.Boron removal from seawater reverse osmosis permeate utilizing selective ion exchange resin[J].Desalination,1999, 124∶ 131−135.
[8]ACOB C.Seawater desalination∶ Boron removal by ion exchange technology[J].Desalination, 2007, 205∶ 47−52.
[9]徐 徽, 许 良, 陈白珍, 石西昌, 杨 鑫.高镁锂比盐湖卤水镁锂分离工艺[J].中南大学学报∶ 自然科学版, 2009, 40(1)∶36−40.XU Hui, XU Liang, CHEN Bai-zhen, SHI Xi-chang, YANG Xin.Separating technique for magnesium and lithium from high Mg/Li ratio salt lake brine[J].Journal of Central South University∶ Science and Technology, 2009, 40(1)∶ 36−40.
[10]杨 鑫, 徐 徽, 陈白珍, 石西昌, 徐 良.盐湖卤水硫酸法提取硼酸的工艺研究[J].湖南师范大学自然科学学报, 2008,31(1)∶ 72−77.YANG Xin, XU Hui, CHEN Bai-zhen, SHI Xi-chang, XU Liang.Study on the extraction of boric acid from aalt lake B rine by vitriol method[J].Journal of Natural Science of Hunan Normal University, 2008, 31(1)∶ 72−77.
[11]王路明.Mg(OH)2对海水中硼的吸附效果[J].海湖盐与化工,2003, 32(5)∶ 5−7.WANG Lu-ming.Absorption effect of magnesium hydroxide on boron in seawater[J].Journal of Sea Lake Salt & Chemical Industry, 2003, 32(5)∶ 5−7.
[12]杨卉芃, 李 琦, 王秋霞, 余丽秀, 曹耀华.从卤水中回收硼的试验研究[J].矿产保护与利用, 2002(4)∶ 39−42.YANG Hui-peng, LI Qi, WANG Qiu-xia, YU Li-xiu, CAO Yao-hua.Experimental research on recovering boric from a bittern liquid[J].Conservation and Utilization of Mineral Resources, 2002(4)∶ 39−42.
[13]UNLU N, ERSOZ M.Removal of heavy metal ions by using dithiocarbamated-sporopollenin[J].Separation and Purification Technology, 2007, 52(3)∶ 461−469.
[14]NAIYA T K, BHATTACHARYA S K.Removal of Cd from aqueous solutions using clarified sludge[J].Journal of Colloid and Interface Science, 2008, 325(1)∶ 48−56.
[15]KOSEOGLUA H, KABAYB, YÜKSELB M.The removal of boron from model solutions and seawater using reverse osmosis membranes[J].Desalination, 2008, 223∶ 126−133.
[16]EDWARDS J O, ROSS V J.Structural principles of the hydrated polyborates[J].Journal of Inorganic and Nuclear Chemistry,1960, 15(4)∶ 329−337.
[17]BYRNE R H, YAO W, KLOCHHO K, TOSSELL J A,KAUFMAN A J.Experimental evaluation of the isotopic exchange equilibrium10B(OH)3+11B(OH)4−=11B(OH)3+10B(OH)4−in aqueous solution[J].Deep-Sea ResearchⅠ, 2006,53∶ 684−688.
[18]肖应凯, 刘卫国, 肖 云.硼特效树脂离子交换法分离硼的研究[J].盐湖研究, 1997, 5(2)∶ 1−6.XIAO Ying-kai, LIU Wei-guo, XI yun.The investigation of ion exchange technique for extracting boron from aqueous fluids by boron specific ion exchange resin[J].Journal of Salt Lake Research, 1997, 5(2)∶ 1−6.
[19]孔亚杰, 韩丽娟, 李海民.D403树脂从盐湖卤水中提取硼酸的探索试验[J].无机盐工业, 2006, 38(2)∶ 10−11.KONG Ya-jie, HAN Li-juan, LI Hai-min.Experiment of extracting boric acid from salt lake brines by D403 resin[J].Journal of Inorganic Chemical Industry, 2006, 38(2)∶ 10−11.
[20]许 良, 徐 徽.盐湖卤水镁锂分离及制取碳酸锂工艺研究[D].长沙∶ 中南大学, 2008∶ 1−71.XU Liang, XU Hui.Studies on magnesium and lithium separation technology and extracting lithium by sodium carbonate[D].Changsha∶ Central South University, 2008∶ 1−71.

