以猪角膜脱细胞基质为载体培养人脐静脉内皮细胞构建实验性角膜后板层*
祁 冰, 侯光辉△, 李 柳, 季青山, 吴 静, 周 清
(1暨南大学附属第三医院,珠海市人民医院眼科,广东珠海519000;2南昌大学附属第三医院,南昌市第一医院眼科,江西南昌330038;3暨南大学附属第一医院眼科,广东广州510630;4暨南大学医学院眼科研究室,广东广州510632)
角膜盲是我国主要致盲性眼病之一。据2006年第2次全国残疾人抽样调查统计显示,因角膜病致盲患者约400万人[1]。角膜移植是治疗角膜盲的重要手段之一,但因材料供不应求且角膜内皮损伤后不可再生修复等因素限制了其在临床的应用。我国早在2002年就已建立深低温保存活性角膜技术使角膜内皮细胞活性达92.6%,保存期也可长达一年以上[2]。但由于社会、文化和宗教等原因,我国的角膜供体资源仍极其短缺,因此人们开始尝试寻找更多有利于代替角膜内皮细胞的种子细胞及其体外培养的生物载体[3-6],用以构建组织工程角膜。本实验以人脐静脉内皮细胞(human umbilical vein endothelial cells,HUVECs)为种子细胞,在冷冻脱水保存的猪角膜后弹力膜/基质载体上进行体外诱导,观察其向角膜内皮样细胞分化的潜能,并尝试利用构建的组织工程角膜进行兔的角膜后板层移植。
材料和方法
1 种子细胞的来源及分离培养
人脐带取自暨南大学附属第一医院产科。无菌状态下剪取健康新生儿脐带,长度>20 cm,立即放入灭菌的PBS缓冲液中,4℃保存,2 h内进行分离。超净台内剪除破损部分,找到脐静脉口,插入去掉针尖的16号注射针头,用止血钳夹住,PBS冲洗脐静脉腔至无血迹。从针头向静脉内灌注0.1%I型胶原酶,待液体从另一端流出后,止血钳夹闭此端,使静脉完全充盈。将脐带放入盛有约300 mL PBS的烧杯中,置37℃的水浴中约12 min。消化后取出脐带。轻柔按摩血管以增加内皮细胞脱落,打开一端止血钳收集消化液于烧杯中,用含10%胎牛血清的M199培养液(含1×105U/L青霉素和100 mg/L链霉素)冲洗脐静脉2次,将冲洗液收集后置于离心管中,1 000 r/min离心5 min,弃上清液,向沉淀中加入含20%胎牛血清的M199培养液,用吸管轻轻吹打制成均匀的细胞悬液,接种于25 mL的培养瓶,放入37℃、5%CO2培养箱中,24 h后换液,以后每2 d换液1次。待原代细胞培养至80%以上融合时,倾去培养液,用PBS液冲洗2遍,然后加入0.25%胰蛋白酶,常温下消化2 min,当见细胞出现皱缩,细胞间隙增大时,加入含20%胎牛血清的M199培养液终止消化。将细胞悬液收集于离心管中,1 000 r/min离心5 min后,1∶2比例接种于新的培养瓶中[7-9]。
2 载体的制备与保存
取新鲜猪眼球,生理盐水反复冲洗,剪去球周组织,浸泡于含庆大霉素(4×105U/L)的PBS缓冲液中,置4℃冰箱30 min,再用含青霉素、链霉素(各2×105U/L)的PBS冲洗3次。无菌纱布包裹眼球,仅暴露角膜部分,眼科穿刺刀斜行向上进入眼球做微型切口;无菌虹膜恢复器从切口处沿角膜缘完整分离板层角膜基质后,眼科剪沿角膜缘处剪除角膜上皮层和前弹力层组织,再用穿刺刀平行进入眼球,沿角膜缘内1 mm处剪下剩余角膜板层(包括基质层、后弹力层和内皮层),将角膜基质深板层内皮面朝上置于无菌培养皿中-80℃冻存3 d。解冻后加入1.2×103U/L中性蛋白酶II 37℃孵育5 min,体视显微镜下用细胞刮子刮除内皮细胞,并在倒置显微镜下观察,确保角膜内皮细胞去除干净。余下的角膜组织(约占猪角膜厚度的1/4~1/3)放入PBS液中冲洗2~3次,置纯甘油中4℃脱细胞48 h。经上述处理的角膜组织后弹力层面朝上,用6.2 mm环钻钻穿后取下,于纯甘油中4℃密封保存6个月[10]。接种细胞前进行水、紫外线两面灭菌各30 min,平铺置96孔培养板,角膜后弹力面朝上,接种血管内皮细胞[11]。
3 HUVECs的CM-DiI标记及移植片的接种
培养的第2代HUVECs贴壁融合达80%时加入含4 mg/L CM-DiI的培养基,37℃孵育30 min,PBS洗2遍后,荧光显微镜下观察细胞标记情况并拍照,然后消化细胞传代培养。将标记的2~3代血管内皮细胞胰酶消化后,用含20%胎牛血清的M199培养液调整细胞密度为每孔1×105,吹打均匀,接种于96孔培养板中附有预处理过的角膜组织片上[12],液体量每孔约200μL,置于5%CO2、37℃培养箱内培养,避免搬动。3 d后首次换液,以后每2 d换液1次,培养1周至细胞形成集落后,部分固定行形态学观察及密度测定,组织切片扫描电镜观察细胞的超微结构,另一部分行角膜深板层移植。
4 角膜深板层移植
24只正常健康新西兰大白兔按照随机处理原则分成实验组和对照组各12只,均设左眼为实验眼。角膜移植术前以3%戊巴比妥钠给家兔行全身麻醉,耳缘静脉进针,用量为1~1.5 mL/kg。0.4%奥布卡因滴眼液结膜囊表面麻醉,含庆大霉素的PBS缓冲液冲洗眼球,消毒铺巾,开睑器开睑。固定眼球后,参考Fernandez等[13]的方法进行角膜后板层移植,角膜中央以角膜环钻切除约7.5 mm、1/4厚角膜上皮板层,待用。角膜中央再以角膜环钻切除约6.2 mm余下全层角膜,实验组移植种植有HUVECs的猪角膜基质深板层,且将负载有血管内皮细胞的板层面朝下。对照组移植单纯猪角膜基质深板层片(未种植血管内皮细胞的基质板层)。10-0尼龙缝线连续环形缝合12~16针。术后,2组实验兔均每天用四环素可的松眼膏点眼,观察移植眼角膜透明度。
5 扫描电镜观察
用PBS缓冲液冲洗干净实验组与对照组猪角膜基质板层片后将其浸泡在装有2.5%戊二醛培养瓶中,置4℃冰箱中过夜。次日用PBS液冲洗3遍,分别以50%、70%、80%和90%梯度逐级递增的乙醇进行脱水处理,各浓度中都需浸泡10 min,最后放入100%乙醇中脱水3次,中间更换新的乙醇,每次10 min。脱水后转入中间液(醋酸异戊酯)中以便将其中的乙醇置换出来,时间约15~30 min,操作中间需更换1次新的中间液,共2次,然后临界点干燥法行干燥处理,继而贴铜台,扫描电镜观察细胞表面结构,并拍照记录。
6 取材固定
移植8周后空气栓塞法处死实验兔,剜除实验眼,浸泡于含庆大霉素(4×105U/L)的PBS溶液中,置4℃冰箱30 min。超净台内剪下角膜组织,PBS缓冲液冲洗干净,角膜组织标本用OCT(optimal cutting temperature)包埋剂封固,行冰冻切片处理。
7 免疫荧光染色检测角膜内皮细胞抗原标志物神经元特异性烯醇化酶(neuron-specific enolase,NSE)和紧密连接蛋白1(zonula occludens-1,ZO-1)
上述制成的切片用冷丙酮室温固定10 min后用PBS缓冲液冲洗3次,每次3 min。切片组织覆盖处滴加驴血清,置室温中30 min,PBS冲洗3次,每次3 min。接着滴加1∶100的山羊抗人NSE单克隆抗体,4℃冰箱中过夜,次日PBS冲洗3次,每次3 min。再以1∶50的驴抗山羊Ⅱ抗滴加,37℃避光孵育30 min,同样用PBS冲洗3次,3 min/次后避光保存,尽快行荧光显微镜下拍照记录。ZO-1检测也需将制备好的切片组织以上述方法滴加1∶100的小鼠抗人ZO-1单克隆抗体,4℃冰箱中过夜,避光孵育30 min,同样用PBS冲洗3次,每次3 min,避光保存,拍照记录。
结 果
1 HUVECs的形态学观察
倒置显微镜下观察可见,早期细胞呈小多角形、球形、呈团状,少数细胞伸展,24 h后可见细胞贴壁,逐渐生长呈短梭状或鹅卵石样镶嵌排列,见图1A。脐静脉内皮细胞胞膜完整,胞核清晰,呈圆形或椭圆形,核分裂相多见,1~2个核仁,胞浆丰富,3~4 d后融合,呈多角形,为单层呈铺路石状排列,见图1B。

Figure 1.Morphology of human umbilical vein endothelial cells(HUVECs)observed under inverted microscope(A:×100;B:×200).图1 镜下人脐静脉内皮细胞的形态特征
2 原代HUVECs的生长曲线
每次经胰蛋白酶消化而获得的血管内皮细胞,活细胞百分率>95%。接种后24 h内细胞贴壁率为80%,以后细胞以对数形式增殖,倍增时间为2.5 d,见图2。

Figure 2.The growth curve of HUVECs determined by MTT assay.图2 MTT法绘制HUVECs生长曲线
3 HUVECs CM-DiI标记后的细胞形态及传代后的荧光表达情况
CM-DiI标记HUVECs,标记率达90%以上,染色后的细胞呈现红色环状的荧光颗粒,形态表现为短梭形、椭圆形,同未染色的细胞形态大致相同,而中间未染色区域为细胞核,见图3A。细胞传3代时红色荧光表达仍很强,但较前相对减弱,见图3B。
4 猪角膜深板层的处理情况
经甘油处理后的猪角膜基质深板层在倒置显微镜下可见其表面光整,无内皮细胞残留,见图4A。在光镜下同样可见,处理后的角膜基质深板层仅保留了支架的完整网状结构,见图4B。扫描电镜显示去除内皮细胞的猪角膜基质深板层面光滑平坦,未见有细胞生长,见图4C。

Figure 3.HUVECs labeled with CM-DiI(×100).A:under fluorescence microscope,red granular particles were CMDiI-labeled HUVECs;B:passage tracing of HUVECs by CM-DiI labeling.图3 CM-DiI标记的人脐静脉内皮细胞

Figure 4.Preparation of porcine corneal posterior lamellae.A:under inverted microscope,porcine corneal posterior lamellae were treated with 100%glycerinum(×50);B:light microscopy showed porcine corneal posterior lamellae did not have endothelial cell residue,only the complete mesh structure was observed(×100);C:as shown by electron microscopy,the surface of porcine corneal posterior lamellae was smooth and flat(×2 500).图4 猪角膜基质深板层的处理情况
5 种植在猪角膜基质深板层上HUVECs的生长情况
镜下观察显示,种植在猪角膜基质深板层上的HUVECs经培养7 d后,细胞间紧密连接相互融合呈铺路石状并逐渐与板层组织相互贴合形成单层,见图5A。电镜下,实验组种植有HUVECs的猪角膜基质深板层表面细胞呈圆形或多角形,连接成片,表面有微绒毛,富有立体感,见图5B。

Figure 5.Growth of HUVECs seeded on porcine cornea acellular matrix.A:as shown by inverted microscopy,the HUVECs formed a monolayer on the Descemet's membrane of dehydrated porcine corneal stroma(×100);B:by electron microscopy,microvilli were observed on the surface of cells and the nuclei were clear to see(×2 500).图5 种植在猪角膜基质载体上的人脐静脉内皮细胞的生长情况
6 猪角膜基质深板层移植术及术后兔角膜透明度的观察
手术显微镜下为新西兰大白兔行猪角膜基质深板层移植,见图6,并于术后每天为其实验眼涂抹抗生素眼膏,术后8周观察可见,猪角膜基质深板层面种植有HUVECs的实验组,其角膜基本透明,周边角膜略有水肿,角膜的透光率和吸光度与未手术角膜比较无显著差异,见图7A。而未载有血管内皮细胞的单纯猪角膜深板层移植术后,角膜明显水肿,混浊,并逐渐形成溃疡,见图7B。
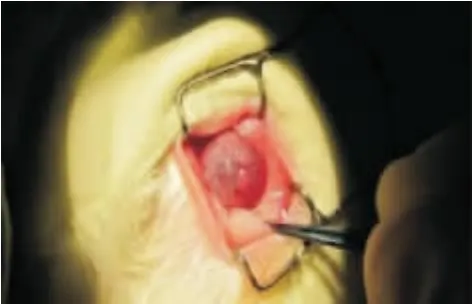
Figure 6.HUVECs were seeded onto Descemet's membrane and cultured in vitro for 7~10 d,and then were used for transplantation.图6 显微镜下行猪角膜基质深板层移植
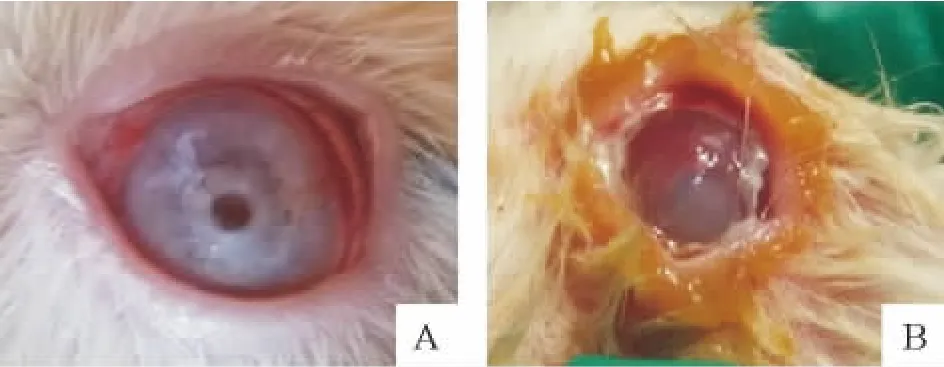
Figure 7.Observation of rabbit corneal transparency after lamellar keratoplasty.A:experimental group;B:control group.图7 板层角膜移植术后兔角膜透明度的观察
7 移植术后角膜板层组织免疫荧光染色
移植术8周后空气栓塞法处死实验兔,取出实验眼角膜板层组织行免疫荧光染色,镜下观察可见实验组猪角膜基质深板层上的HUVECs表达角膜内皮相对特异性蛋白NSE,并发绿色荧光,见图8A,将其同一视野内细胞核以DAPI复染后,发蓝色荧光,见图8B。实验组猪角膜基质深板层上的HUVECs经ZO-1染色结果同样表现为阳性,发绿色荧光,见图9A,对同一视野内细胞核行DAPI复染后,发蓝色荧光,见图9B。

Figure 8.NSE expression examined by immunofluorescent staining in porcine corneal posterior lamellae from experimental group(×200).A:HUVECs expressed NSE(green fluorescence);B:in the same visual field,the nuclei showed blue fluorescence by DAPI counterstaining.图8 实验组猪角膜基质后弹力层面上NSE的表达

Figure 9.ZO-1 expression examined by immunofluorescent staining in porcine corneal posterior lamellae from experimental group(×200).A:HUVECs expressed ZO-1(green fluorescence);B:in the same visual field,the nuclei showed blue fluorescence by DAPI counterstaining.图9 实验组猪角膜基质后弹力层面上ZO-1的表达
讨 论
本研究选用的异种生物载体[14]为除去上皮和内皮层的猪角膜基质深板层,是一种低免疫原性生物载体材料,含有丰富的细胞外基质成分(包括Ⅰ、Ⅲ、Ⅴ型胶原蛋白、糖蛋白、蛋白多糖)、其间散布有角膜基质细胞和极少数游走的白细胞,这与人类角膜的结构类似。张米等[15]将自体脂肪干细胞体外种植在猪角膜基质上并行板层角膜移植治疗碱烧伤,术后角膜基本恢复透明,未发生排斥反应。邵春益等[16]以猪角膜脱细胞基质为载体培养猫骨髓内皮祖细胞,所获得的猫骨髓内皮祖细胞可在猪角膜脱细胞基质上单层生长,黏附较好,形态上呈多边形,至少可维持1个月。因此相比上皮层和内皮层,基质层的成分复杂但免疫原性低[17],可作为种子细胞的理想载体,且该载体与人角膜基质结构类似,具有良好的屈光作用,来源广泛、细胞自然生长环境、具有一定形状与厚度、便于移植等优点。
进行组织工程选用的种子细胞应当具有容易获得、能够长期维持其生理功能和生物活性、抗原性小等特性[18-19]。从上世纪70年代起学者们就开始寻求治疗角膜内皮损伤的新材料和新方法,并曾尝试利用正常的异体角膜内皮细胞进行替代移植。但因人体角膜内皮细胞在体内并不具增殖性,而且在体外增殖也有限,因此其应用受到很大的限制。Gospodarowicz等[20]认为血管内皮细胞和角膜内皮细胞存在许多相似之处,故应用这2种细胞进行相关的联合移植实验,获得了一定的成功。吴小莉等[21]和罗哲文等[22]用人脐静脉内皮细胞种植在处理过的羊膜上,待形成单层后用于猫眼角膜内皮细胞移植,植片在1周内保持完全透明,说明该细胞可行使角膜内皮细胞的屏障及液泵功能。
种子细胞的移植示踪是确定移植是否成功的重要依据。目前通过细胞移植示踪研究其能否在受损器官上定植,方法有多种。本实验采用一种较新的细胞膜荧光染料CM-DiI(氯苯甲酰氨-1,1’-双十八烷基-3,3',3',3'-四甲基吲哚羰基花青高氯酸盐)标记HUVECs,并在体外传代培养,观察它的标记情况。由于它是一种亲脂性的碳花青荧光膜染料,容易嵌进生物质膜内并在膜内做定向扩散运动从而可有效地标记整个细胞,是目前最好的荧光染料。它的荧光激发波长为553 nm,发射波长为570 nm,在绿色光激发下,发出红色荧光。有研究表明,低浓度CMDil标记细胞无毒性,细胞免疫表型或分化状态等改变均不影响细胞标记,标记后的细胞生物学特性包括增殖、迁移、分化能力、旁分泌作用等均无改变,而且不出现细胞间传递的现象[23-24]。
角膜内皮细胞是附着在后弹力层面上的单层六角形扁平细胞。本课题组所设计的异种生物载体[25],是内皮细胞的自然生长环境,以CM-DiI标记的HUVECs为种子细胞构建角膜后板层,可见到细胞在载体上生长良好,并由短梭状、鹅卵石样排列逐渐融合,最后紧密连接形成单层。
本实验移植术后的角膜在位,未发生排斥反应,说明猪角膜基质深板层片在兔角膜上移植能存活。并观察实验组和对照组新西兰大白兔的术眼角膜透明度,可明显看到种植有血管内皮细胞的猪角膜基质深板层实验组,术眼角膜基本透明,而对照组,单纯猪角膜板层移植的术眼角膜仍然水肿混浊,说明HUVECs已经部分向角膜内皮方向转化,同时已具有一定的角膜内皮泵水功能[26],并在一定程度上改善了损伤兔角膜的眼表形态[27]。Böhnke 等[28]报道,用抗人的NSE单克隆抗体对人眼组织进行免疫组化检测,发现体外培养的人角膜内皮细胞染色结果阳性,而人基质细胞筋膜囊成纤维细胞和角膜上皮均不能被染色,证明其是眼范围内内皮细胞所特有的。Zhu等[29]用抗体ZO-1免疫染色显示出了角膜内皮细胞的规则多边形结构。因此NSE和ZO-1均是角膜内皮相对特异性蛋白,对实验组种植后的血管内皮细胞行 NSE及ZO-1染色,其结果均为阳性,也同样证明了猪角膜基质深板层的微环境用以诱导脐静脉内皮细胞向角膜内皮细胞方向转化的可行性。

