基于流动注射的高速医用电解质分析模块研制
张会生 张小飞 刘昕宇 饶 捷 钟彩青 李乔亮*齐素文 林淑梅 陈思平 汪天富
1(广东省生物医学信息检测与超声成像重点实验室,深圳大学生物医学工程系,深圳 518000)
2(深圳市新产业生物医学工程股份有限公司,深圳 518000)
引言
电解质测定是临床检测中重要的一项,通过检测人体血液、尿液或脑脊液中的Na+、K+、Cl-、Ca2+等离子的溶度[1],便可判断血液中阴、阳离子是否平衡,这对临床医生诊断疾病和实施手术十分重要[2]。
目前临床上就电解质浓度的测量主要有两种方法,即通过电解质分析仪测量与全自动生化分析仪的电解质分析模块测量[3]。其中,电解质分析仪只能测量电解质,而全自动生化分析仪不但能测量电解质而且还能测量其它的生化项目。
传统电解质分析仪测量项目单一,并且在国内临床上测量血液中 Na+、K+、Cl-、Ca2+采用离子选择电极法,测量速度较慢,因此主要应用在中小医院。为了满足广大基层医院与大型医院对各种生化项目快速测量的需求[4],节省患者就诊与医院诊断时间,尤其是当发生传染病疫情(如SARS、禽流感)的时候,嵌入电解质模块的高速生化分析仪将大大提高医院的诊断效率,因此,在全自动生化分析仪中添加高速电解质分析模块是必要的选择[5]。
目前,我国在自主研发电解质分析方面取得了较大的发展,国内涌现了如深圳越华、康立、航创、希莱恒、上海迅达等生产电解质分析仪公司,但均没有公司研制商品化的电解质分析模块。由于我国尚未掌握高速电解质分析模块的关键技术,国内的公司只能购买国外相关公司的电解质分析模块。依赖这种进口的电解质分析模块,不但电极和试剂价格昂贵[6],而且在技术上相对被动。
针对全自动生化分析仪中对电解质的快速诊断需求,迫切需要研发一种嵌入到全自动生化分析仪中的电解质模块。为此,本研究结合流动注射分析法(FIA)与离子选择电极法(ISE),提出了一种新的高速电解质研制方法。传统电解质分析仪虽然也拥有离子选择电极法(ISE)易于流动监测和自动化检测[7-8]的特点,但其试剂和样品需混合反应一定时间后再进行采样分析,而采用流动注射分析法(FIA)无反应停留时间,因此,具有速度快、精度高、耗试剂量少等优点[9-10]。在嵌入式软硬件技术的条件下,成功研制了能嵌入全自动生化分析仪的高速电解质模块。
1 测量原理
1.1 流动注射分析法(FIA)
在热力学非平衡的条件下,液流中重现地处理试样或试剂区带的定量流动分析技术[11-12]为流动注射分析法。
分散系数D是在分散过程发生前后,产生读出信号的流体元中待测组分的浓度比如式(1)。

式中:Co是为待测液本来的浓度,C是在分散后某一段流体元中的待测液的浓度。
根据最大峰值处所得到的D值的大小将FIA的流路划分为高、中、低分散体系[13]。
为了能准确研究受控的分散,对反应管长、管径、试样体积、流速、扩散系数等[14]进行数学模型分析。
(1)注入试样体积与分散系数D关系如式(2)。

式中,K表示与流路有关的常数,V为注入体积。
在D值较高时注入体积V与D基本成反比关系,所以降低区带分散简便的方式便是增大注入体积。
(2)载流速度与分散系数D的关系
试样带的分散将随着流速的降低而降低[15]。
(3)反应管道长度与分散系数D的关系
D与反应管道长度L的关系符合式(3)。

式中,K为与管道孔径和注样体积相关的常数。当孔径大,体积小时,K值就大,反之则小。
(4)反应管道孔径与分散系数D的关系表示为

式中,K为FIA体系中与注样体积、反应管道孔径和反应管长等有关的常数,R一般为毫米级。
在高速电解质分析模块的研发过程中,根据以上4点要求,结合电化学分析法的应用实际,合理地设计液路中的注样体积、反应管长、载流速度、反应孔径等参数。
1.2 离子选择电极法(ISE)
离子选择电极是一类电化学传感器[16],也称为膜电极,用来指示离子的活度。
如图1所示,离子选择电极一般由内参比电极、内参比液和敏感膜3个部分组成,其中内参比液和膜材料中均含有和待测离子相同的离子。当电极置于溶液中时,在溶液界面和电极膜间将发生离子交换和扩散作用,这样就改变了两相界面的原有的电荷分布,从而形成了双电层,并产生了膜电位。离子选择电极电位会随溶液中待测离子的活度变化而变化,且两者的关系符合能斯特(Nernst)方程[17]。

图1 离子选择电极的结构Fig.1 Architecture of ion-selective electrode
在实际测量中,需克服温度、液接电位等因素对测量结果的影响。在量样品前,还需对电极进行标定。
分别测定已知溶度为CA和CB的标准液A和标准液B的对应电位为EA和EB,算出电极的实际斜率S为:
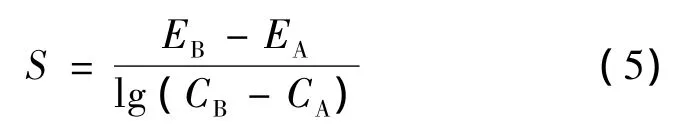
定标完成后,只要测量出待测溶液中的离子对应的电极电位 Ex,就可求出待测溶液的离子溶度Cx:

将 Na+、K+、Cl-、Ca2+和 pH 等多种电极组合起来,即可同时测定待测样品中Na+、K+、Cl-、Ca2+等离子的含量以及pH值。
1.3 FIA与ISE联用
影响电解质模块分析速度的主要因素有离子选择电极响应时间、测试方法和测试的流程等。目前的电解质分析仪测量,均是基于样品在物理和化学平衡条件并在静止的情况下进行的,我们称这种分析方法为静态分析法。测量中达到平衡状态需要一定的等待时间,因此无法达到高速测试要求。电解质分析过程中的加样、采集数据、清洗等动作的先后顺序及配合紧凑程度(即测试的流程)也会对分析速度造成一定的影响。而流动注射法采用是连续的动态抽样分析,这样可以大大提高测试时间。
在仪器测试中,取AD转换器采集电位信号的波峰(波谷)值作为离子浓度的参考标准。AD转换器采集电位如式7所示。

式中,E(t)AD为AD转换器在周期T内,时间t下采集的 波峰(波谷)值,e(t)为时间t时AD转换器采集的离子电位,Mt为最大值Maxt或最小值MinT。
根据式(6)与式(7)知,待测溶液的离子溶度Cx为

采用流动注射与离子选择联用时,AD采集次数与 Na+、K+、Cl-、Ca2+与 pH 值的浓度关系如图2。图中,波峰(波谷)值已标出,采用 Na+、K+、Cl-、Ca2+和pH值波峰(波谷)附近的10个值并求平均值为仪器测量样品浓度。上图中,Na+、K+、Cl-、Ca2+和 pH 值浓度分别为 74.5、70.2、111.8、94.1、103.4 mmol/L。
同时,采用流动注射分析法与离子选择电极法联用,对于研制高性能高测试速度的电解质分析模块具有减少样本用量、减少离子选择电极对测量样本的响应时间、克服基点漂移、实现电极管路自动清洗等优点[19],两者的结合则是我们研发高速电解质模块的理论基础。
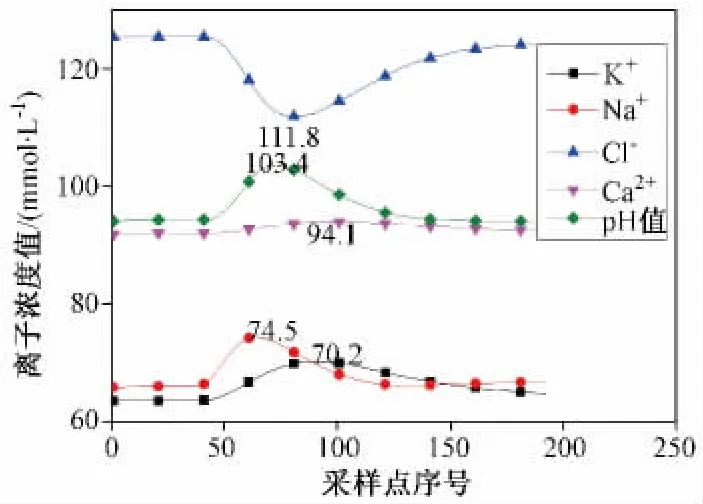
图2 流动注射与离子选择联用时数据采集端离子浓度Fig.2 Data acquisition terminal ion concentration based on flow injection and ion selective
2 高速电解质分析模块总体结构设计
合理的液路设计对高速电解质分析模块的研发至关重要[20],经过实验数据分析,设计液路架构如图3。

图3 高速电解质分析模块的液路图Fig.3 Liquid road map of high-speed electrolyte analyzer
液路由进样杯、旋转换向阀、A标蠕动泵、B标蠕动泵、样本蠕动泵、载流蠕动泵、多个液流检测器、试剂及管路等组成。进样杯中是采样针采集的样本。旋转换向阀通过旋转阀体实现任意一个外圈和内圈的孔位连接以形成不同的流路。蠕动泵用来推动试剂或试样流动。A标蠕动泵用来抽取标准液A到进样杯,B标蠕动泵用来抽取标准液B到进样杯。样本蠕动泵用来抽取样本或标准液到达采样杯,载流蠕动泵用来推动载流不间断地流通于整个测量管路中,以实现流动注射。换向阀定位光耦用来定位换向阀旋转位置,样本检测器用来确保样本或标准液充满采样杯,便于定量测量。气泡检测器用来检测在样本测量过程中流过离子选择电极管路的待测液中是否有气泡,并判断结果异常原因。ISE检测器用来定位去蛋白液或活化液是否到达离子选择电极管路。
测量样本时,首先由加样针将样品采集到进样杯,然后由样本蠕动泵抽取样本到样本检测器。其次通过转动旋转换向阀使样本与载流管路相接,并且由载流蠕动泵将样本和载流混合液送到离子选择电极组并进行电位检测(此时前段进样管路也自动进行清洗)。最后,混合液排出到废液管路[21-24]。
根据设计架构要求,完善设计功能,设计出的高速电解质分析模块如图4所示。
3 高速电解质分析模块硬件设计

图4 高速电解分析模块实物图Fig.4 Physical set up of high-speed electrolyte analyzer
数据采集系统是设计中的关键模块[15]。当通过读卡器读取RFID电子标签后,启动高速电解质分析模块,此时,液路控制模块开始工作。采用外接A/D转换芯片,对离子选择电极数据进行转换后送到ARM中进行处理,再通过串口传到上位机。数据采集端总体设计结构如图5。
分析模块的微控制器选用的是NXP公司推出的LPC2387,LPC2387具有非常丰富的硬件资源并且功耗极低,包括4个32位定时器、8路10位逐次逼近式的模数转换器、4个异步串口、3个IIC接口、1个SPI接口和1个SSP接口等,在工业控制和医疗系统上具有广泛的应用。设计中,LPC2387是电解质分析模块的中央控制单元,能保证与上位机通信的实时性、准确性、完整性,实现电解质分析模块的进样和清洗功能以及控制数据采集模块的工作模式并接收数据信息。

图5 数据采集端硬件总体设计Fig.5 Overall design of hardware data collection
RFID系统由Mifare的标准IC卡MF1 IC S50和集成了天线的读写器M104A模块组成。在系统设计中,将读写器的WAKE信号接至LPC2387的一个定时器捕获输入引脚,当读卡器的有效识别区域中出现了RFID电子标签时,读写器的WAKE信号将会触发一次中断,LPC2387在处理该中断请求时调用针对电子标签的相关程序,便可实现对电子标签的各种操作。
液路控制模块主要包括蠕动泵(A标蠕动泵、B标蠕动泵、样本蠕动泵、载流蠕动泵,即图4中从左到右4个蠕动泵)电路、液面检测(A标液位检测、B标液位检测、载流液位检测)电路、液路检测(换向阀归零检测器、B标检测器、气泡检测器、ISE检测器)电路。整体液路的动力装置采用日本信浓公司的步进电机,驱动 IC采用 Allegro公司的 A3983,A3983是一款DMOS的微步细分电动机的驱动芯片,带有内置转换器,操作简单。选用以红外发光二极管作为发射器,并且以红外光敏三极管作为接收器的关电耦合器作为液流定位检测模块的关键器件。
电极模块包括 K+电极、Cl-电极、Na+电极、Ca2+电极以及pH值电极,均采用希莱恒公司专业的离子电极产品,用来检测相应的离子电位。
模数(A/D)转换IC采用TI公司的ADS1114,一款高精度、低功耗以及操作便捷的模数转换芯片,采样频率860 Hz,而耗电电流仅为150 μA(典型标准值),工作电压可低至2 V。在高速电解质分析模块中,ADS1114作为离子电极电位的模数转换芯片。
4 高速电解质分析模块软件设计
4.1 软件总体结构设计
高速电解质分析模块软件包括上位机、中控(COP-Central of Process)、下位机等3个部分。如图6所示。

图6 软件设计总体结构图Fig.6 Overall structure of the software design
上位机与下位机之间通过独立的通信协议进行相互通信,通信中产生的错误码用来判断机器故障情况。其中,上位机负责整机时序的设计和产生相关动作命令。COP负责接收上位机命令并对一些大指令进行拆分并发给对应的下位机执行部件,同时,协同各个下位机模块完成上位机下发的指令。下位机则负责对其接收到命令进行解析并执行相应动作。大部分的功能由下位机单独完成,例如初始化、定标、清洗和保养等功能,而COP作为电解质模块和上位机通信数据的中转站,对电解质分析模块的相关命令只做转发。
4.2 软件功能设计
上电后,判断是否使用电解质模块后必须对电解质模块进行仪器的复位及初始化,软件功能设置如图7所示。
上电以后,通过上位机发送电解质模块指令来确定是否要进行初始化电解质模块。若使用,则进行初始化;若不使用,则进行ISE管路排空(上次仪器不正常关机时可能会有试剂浸泡电极)。为了减少初始化与定期保养电极试剂消耗,上电后必须对是否使用电解质模块进行判断。
在实际的测量中,具体做法是软件初始化后抽取一定量的A标采样杯,然后将旋转换向阀转到测试档位,并转动载流蠕动泵,将样本和载流一起推到ISE管路并不断采集电极电位值,将得到的峰值上传给上位机[25]。

图7 软件初始化设置Fig.7 Software initialization Settings
同时软件设计中,在上位机中加入了实验说明、电极保养以及上传实验结果等选项,便于广大使用者按须知操作[26]。
4.3 串口通信及数据采集模块软件设计
串口通信模块用于上位机和下位机之间指令的收发,因此,必须保证通信的稳定可靠[27]。本系统的串口通信模块的软件设计采用队列结构,分别创建串口接收队列和发送队列,用来处理接收到的命令和待发送的数据;串口通信流程如图8所示。

图8 串口通信软件设计图Fig.8 Design of serial interface communication software
数据采集模块中采用I2C(Inter-integrated circuit)总线操作A/D转换器,I2C总线是Philips公司推出的芯片间串行传输总线,以2根连线实现了完善的全双工同步数据传送,可以方便地构成多机系统和外围器件扩展系统。本系统将主控芯片LPC2387设置为I2C主机,ADS1114设为I2C从机。由主机LPC2387产生时钟信号、发送起始位及停止位。数据在SDA线上必须是8位传输,每次传输可以发送一个或多个字节数据。传输过程中最先传输最高位并且传输完一个字节后必须跟一个应答位[28]。
I2C的操作包括4种模式:主发送模式、从发送模式、主接收模式和从接收模式。而本设计中ADS1114作为从机接收来自主控板上微控制器的操作指令,然后往主控模块发送转换结果。
5 评价方法
参照国家行业标准《中华人民共和国医药行业标准 YY/T0589-2005——电解质分析仪》,并在18℃ ~25℃温度下,无凝露,标准大气压,电网电压为220±5V等环境下使用高速电解质分析模块进行大量的实验,并对准确度、精密度、线性、稳定性、携带污染率等5个方面的评价。
根据行业标准的要求,配置朗道(RANDOX)5点定值质控液及质控血清液,离子浓度含量如表1和表2。
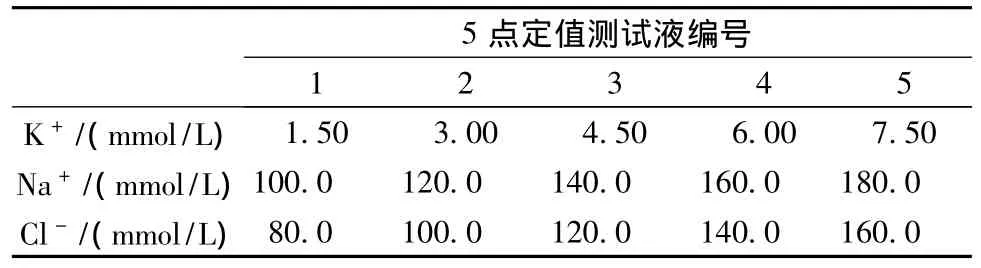
表1 RANDOX 5点定值测试液离子含量Tab.1 Purity of ion in RANDOX five fixed value test fluid

表2 血清质控液离子含量Tab.2 Purity of ion in serum quality control liquid
根据配置的点定值质控液及质控血清液,下面对研制模块从准确度、精密度、线性、稳定性与交叉污染率进行实验评价。
5.1 准确度评价
本实验选用RANDOX CAL 3定标液和RANDOX Control 2质控液作为测试样本,以其靶值作为准确性的参考值。分析仪在正常工作情况下先用校正液进行两点校正。然后对给定定值参考物质联续测试5次,分别求得各元素测定的平均值,根据式(9)计算分析各元素测定值与参考物质定值的偏差(ΔB),应符合性能指标要求。

5.2 精密度评价
分析仪在正常工作下,校正后对定值参考物质连续测定11次,根据白塞尔公式[29]计算精密度如式(10)。
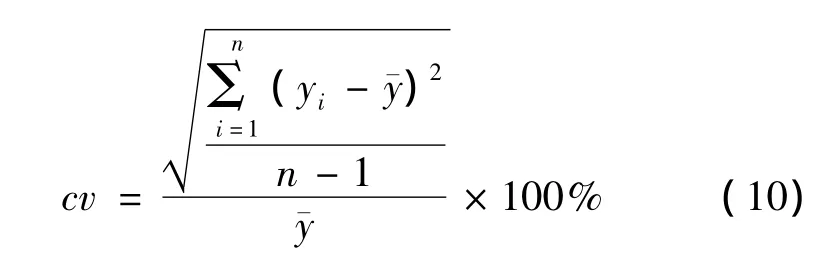
5.3 线性评价
各分析元素均得到一组不同溶度的实测值。用线性回归分析方法分别计算各元素的线性回归参数a(拟合斜率)和b(拟合截距),导出线性回归方程Y=aX+b,将各元素的标准值X代人方程求出相应的线性回归值Y,然后按照公式计算线性误差

式中,Δi为线性误差;Yi为测试值;Y为线性回归值。
5.4 稳定性评价
仪器在正常工作条件下按常规测试程序先行校正,然后对定值质控测试液3进行测试,每隔2 min测试一次并记录下各分析元素的测定值,10 min内共测试6次,各分析元素均分别得到6个测定值,挑出其中最大值Xmax和最小值Xmin,根据式(12)分别计算各分析元素的波动百分比ΔD,本标准把ΔD的值定为稳定性,结果应符合性能指标要求。
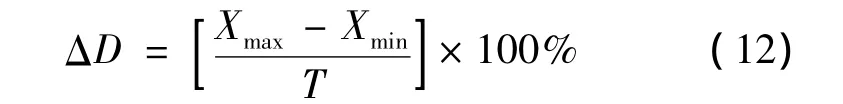
式中,T标称参考值;Xmax最大测定值;Xmin最小测定值。
5.5 交叉污染率评价
分析仪正常工作下,校正后,将各分析元素的高、低溶度的标称值溶液分别交替进行测试。先对低溶度的标称值溶液连续测4次,再对高溶度的标称值溶液连续测4次,最后再对低溶度的标称值溶液连续测4次,这样,每一分析元素均得到2组低溶度值和1组高溶度值,按式(13)和式(14)分别计算从低溶度到高溶度的交叉污染CLH和从高溶度到低溶度的交叉污染CLH
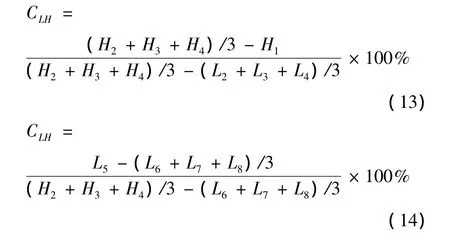
式中,L1~L8为低浓度溶液第1~8次的测试值;H1~H4为高浓度容液第1~4次的测试值。
6 结果
6.1 准确度实验结果
数据处理后求得高速电解质模块准确度相关参数如表3和表4所示。分析可知采用RANDOX CAL 3定标液和RANDOX Control 2质控液作为测试样本,其准确性测试结果均呈线性,因此测试结果稳定可靠。相对偏差值B均在要求指标3%的范围内,说明本仪器的准确度达标。

表3 Randox Cal 3准确度测试数据计算结果Tab.3 Accuracy test data calculation results of Randox Cal 3

表4 Randox Control 2准确度测试数据计算结果Tab.4 Accuracy test data calculation results of Randox Control 2
6.2 精密度实验结果
对实验数据进行计算处理求得精密度相关参数如表5所示。血清质控液3进行11次的测试结果,K+、Na+、Cl-精密度测试结果线性稳定可靠;3个项目的变异系数都优于仪器标准指标,说明本仪器的精密度达标。

表5 精密度测试数据计算结果Tab.5 Data calculation results of precision tests
6.3 线性实验结果
高速电解质分析模块线性测试结果如表6所示。由表6可知,3个项目的线性误差均小于仪器指标要求值,说明本仪器的线性达标。

表6 线性测试数据结果处理Tab.6 Data calculation results of linear
6.4 稳定性实验结果
高速电解质分析模块稳定性测试结果如表7所示。对定值质控测试液进行测试数据稳定可靠,从处理后的数据结果(见表7)可知K+、Na+、Cl-稳定性(ΔD)分别为1.11%、0.76%、1.39%均小于要求指标1.50%,符合稳定性测试,说明仪器稳定性达标。
6.5 交叉污染率实验结果
高速电解质分析模块交叉污染率测试结果如表8所示。

表8 交叉污染率数据计算结果Table 8 Data calculation results of cross contamination
由表8可以看出,3个项目的交叉污染都优于仪器标准指标要求,说明本测量模块的交叉污染率达标。
临床检验仪器研制中,检测系统性能评价对实验室工作十分重要,是临床实验室选购仪器的重要参考指标[1]。
6.6 临床验证结果
本模块研制成功后,在深圳市南山医院做了K+、Na+、Cl-等离子的临床测试,并与医院现有产品(航创 HC9886)做了临床比对,从大量的临床数据中选取10个样本进行比对如表9所示。
7 讨论和结论
采用流动注射法和离子选择电极法联用研制的高速电解质分析模块研发成功后在准确度、精密读、线性、稳定性、交叉污染率五方面测试均达到国家行业标准《中华人民共和国医药行业标准YY/T0589—2005——电解质分析仪》。通过临床试验,所测K+、Na+、Cl-浓度结果准确可靠,验证了模块的临床可靠性,但限于实验条件(时间限制等),模块在长时间的运行过程中可能产生不可预测的错误或误差。同时在实验总结得出载流的配方对仪器的测试速度与其他性能具有重要意义,后期工作可以不断优化载流配方以提高仪器相关性能;蠕动泵的脉动对实验可能产生影响,需要长期的临床实验验证与方法改进。

表9 临床试验数据比对Tab.9 Clinical trial data comparison
在深圳南山医院做了2个月的临床对比试验,整体效果良好,检测数据和医院现有的航创HC9886电解质分析模块数据对比,数据准确可靠(见表9)。但鉴于条件限制(医护人员参与实验时间有限),只做了200组实验对照,显然,仪器长期的运作将无法保障,因此,在临床应用上,本模块还需要长期的实践应用,改善不足,提高相关性能。
总之,该模块的研制成功与不断改进,将在临床上通过对电解质浓度的测定为医生判断病情、解释病症、进行治疗、评价疗效等提供科学依据,与生化分析仪联用可提高临床诊断效率。
[1]罗浔阳,张劼,孙兵,等.日立7600-020E生化分析仪电解质模块应用评价[J].医疗设备信息,2007,22(5):53 -54.
[2]张会生.HC-9886型全自动多参数电解质分析仪的研制[J].现代科学仪器,2004,(2):26 -29.
[3]王拥军.两种分析仪测定血清电解质的方法学对比与评估[J].齐齐哈尔医学院学报,2008,29(17):2063 -2064.
[4]宋延荣,张萍.基层医院生化分析仪使用情况调查及对策[J].实用医技杂志,2011,18(11):1024.
[5]刘玮,刘克芹.日立7600-110生化分析仪电解质模块应用评价[J].河北北方学院学报,2010,27(1):48 -50.
[6] 朱世银,刘玲.日立生化分析仪H,D液的研制与应用[J].临床军医杂志,2001,29(2):124.
[7]National Committee for Clinical Laboratory Standard.Evalu-ation of the linearity of quantitative measurement procedures:a statistical approach.Approved Guideline[S].NCCLS docu-ment EP6A.Wayne,Pennsylvania:NCCLS,2003,1(100):9 -47.
[8]National Committee for Clinical Laboratory Standard.Method comparison and bias estimation using patient samples[S].Approved Guideline,EP9A,Pennsylvania,1995,15(7):1 -2.
[9]金绍祥.流动注射分析法与多种仪器分析联用的进展[J].理化检验 - 化学分册,2009,45(2):238 -240.
[10]龙波,吕薇,陈梨春.日立7180E生化分析仪电解质模块性能评价指标的研究[J].激光杂志,2011,32(4):96 -97.
[11]Ruzicka J,Hansen EH.Flow Injection Analysis[M].(2nd Edition).New York:John Wiley & Sons,1988.
[12]方肇伦.流动注射分析法[M].北京:科学出版社,1999.
[13]Ruzicka J,Hansen EH..Flow Injection Analysis[M].New York:John Wiley&Sons,1981.
[14]Ukeda H.FIA Bibliography[J].Flow Injection Anal,2004,(21):69-79.
[15]董慧如.流动注射分析的原理及影响因素[J].化学通报,1987,(3):34-79.
[16]杨根元.使用仪器分析[M].北京:北京大学出版社,2001.
[17]崔云龙.酶法测定血清碳酸氢盐[J].临床检验杂志,1993,11(3):134-135.
[18]Alexander PW,Dimitrakopoulos T,Hibert DB.Operational assessment of a protentiometric eight-sensor f-low cell in a portable flow injection analyzer[J].Field Analytical Chemistry And Technology,1996,1(1):31 -37.
[19]Martinotti V,Balordi M,Ciceri G.A flow injection analyser conductometric coupled system for the field analysis of free dissolved CO2and total dissolved inorganic carbon in natural waters[J].Anal Bioanal Chem,2012,403:1083 -1093.
[20]Li Qingyang,Morris KJ,Dasgupta PK.Part-able flow-injection analyzer with liquid-core waveguide bas-ed fluorescence,luminescence,and long path length absorb-ance detector[J].Analytica Chimica Acta,2003,479:151 -165.
[21]Han Bin, Cao Lei. Flow injection-spectrophotometric determination of total dissolved nitrogen in seawater based on quantificational solenoid valves[J].Spectros-Copy and Spectral Analysis,2012,32(1):219 -222.
[22]Wehe CA,Bornhorst J,Holtkamp M.Fast and low sample consuming quantification of manganese in cell nutrient solutions by flow injection ICP-QMS[J].Metallomi,2011,3(12):1291-1296.
[23]Mao Lisha,Chen Huiling,Liu Guihua.Flow injection analysis method for hygienic examination of volatile phenol co-mpounds in the air of residential area [J].Journal of hygiene Research,2011,40(6):773-775.
[24]叶华俊,夏阿林,张学锋,等.基于长波近红外的便携式品质分析仪的研制及应用[J].仪器仪表学报,2012,33(1):86-89.
[25]杨邱青,朱智甲,赵爱东.直管型智能流动注射化学发光分析仪的研制[J].仪器仪表学报,2005,26(10):1024 -1026.
[26]黄志敏,李科杰,许海平.流动注射式水质在线测控系统的研究[J].仪器仪表学报,2005,26(4):344 -346.
[27]刘伯强,马登程,王明时,等.一种基于DSP结构的电解质分析仪的设计与实现[J].仪器仪表学报,2006,27(4):410-412.
[28]Atia MJ,Zeng Jiang.An explicit foumula for the linearization coefficients of Bessel polynomials [J].Ramanujan Journal,2012,28(4):211 -221.
[29]杨昌国.精密度评价和方法比较中NCCLS评价方案的应用[J].临床检验杂志,1993(1):47 -49.

