抗红花花粉蛋白单克隆抗体的研制Δ
张庆生,李 波,张凤兰,裴新荣,陈志蓉,王钢力,达 晶,王春香,林瑞超(.中国食品药品检定研究院,北京 00050;.北京康为世纪生物科技有限公司,北京 006))
红花为菊科植物红花Carthamus tinctorius L.的干燥花,具有活血通经、散瘀止痛的作用,是一种应用非常广泛的传统中药材[1]。随着科技进步和制药业的发展,红花注射液被广泛应用于闭塞性脑血管病、冠心病、脉管炎等疾病的治疗,并取得了一定的疗效,但中药注射剂的安全问题逐渐浮出水面,主要表现在因中药注射剂引起的各种过敏反应,轻者引起皮疹、呼吸苦难,重者可导致过敏性休克[2-4]。这既威胁患者的身体健康,也对我国中药制药业的发展造成了严重的伤害。因此,构建一个监测中药制剂、尤其是中药注射剂的过敏性反应监控、评价平台,对筛查中药制剂过敏原残留、优化制剂工艺、预防过敏反应的发生具有重要意义。食物、植物、药物、制药杂质残留等都可能诱导过敏反应,而花粉是自然界最常见的过敏原之一[5-6]。本实验应用红花花粉蛋白免疫小鼠,通过筛选针对花粉蛋白的特异性单克隆抗体,尝试构建针对红花注射液的过敏原筛查平台,为优化红花制剂生产工艺、加强质量控制及预防临床过敏反应提供新的思路和方法。
1 材料
1.1 仪器
酶标仪(BIO-RAD 680),DEM-3型自动洗板机(北京拓普分析仪器有限责任公司生产),二氧化碳培养箱SANYO,HD-4层析工作站(上海沪西仪器厂生产),层析柱(Phamacia),蛋白电泳装置(BioRadⅡ),蛋白定量检测仪(Amersham Biosciences)
1.2 药品与试剂
弗氏完全佐剂、弗氏不完全佐剂、HAT(次黄嘌呤H、氨基喋呤A、胸腺嘧啶脱氧核苷T)培养基、100×HT(次黄嘌呤H、胸腺嘧啶脱氧核苷 T)培养基(、聚乙二醇(PEG)4000、RPMI 1640培养基、胎牛血清、二甲基亚砜(DMSO)、山羊抗小鼠IgG(H+L)-HRP、Sp2/0细胞株(由北京康为世纪生物科技有限公司提供)。抗体亚型检测试剂盒(SBA Clonotyping System/HRP)(购自 SouthernBiotech公司),透析袋(购自 BLUEBIRD公司),超滤管(购自Millipore公司),Bradford蛋白浓度测定试剂盒(Bradford Protein Assay Kit)(购自Pierce公司)。红花花粉由山西太原华卫药业有限公司提供。
1.3 动物
BABL/c小鼠购自扬州大学,清洁级,合格证号:SCXK苏2012-0004。
2 方法
2.1 实验药品的制备
称取红花花粉50 g,加入250 ml水,煮2 h,过滤后取滤液80 ml,加入预冷的无水乙醇120 ml(60%),放置4℃过夜(17 h),5000 rpm/min离心20 min,弃上清液,沉淀即为红花花粉总蛋白,应用Bradford方法检测蛋白含量。将红花花粉总蛋白作为免疫原。
2.2 免疫方案
选取5只雌性BLAB/c小鼠进行免疫,具体免疫流程如下:第 1 次免疫,按蛋白量 80 μg/只,250 μl/只,配合应用完全弗氏佐剂,背部皮下多点免疫;第2次加强免疫,按蛋白量40 μg/只,250 μl/只,配合应用不完全弗氏佐剂在初次免疫后一周加强免疫;第3、4次加强免疫方案与第1次加强免疫相同;第 5 次加强免疫按蛋白量 80 μg/ml,100 μl/只,采用脾内加强免疫方式进行。
2.3 细胞融合和克隆
第5次加强免疫后3 d,取小鼠脾细胞,采用PEG常规融合方法,将小鼠脾细胞和骨髓瘤细胞Sp2/0细胞株进行融合。采用间接酶联免疫吸附剂测定(ELISA)方法对融合细胞上清进行筛选,经过2次筛选确认阳性细胞孔后,采用有限稀释法对阳性细胞株进行克隆。
2.4 抗体亚型检测
SBA Clonotyping System/HRP购自Southern Biotech公司,按试剂盒操作说明进行检测。
2.5 腹水制备
取BALB/c小鼠,每只注射0.5 ml石蜡油,7 d后将杂交瘤细胞按1×106个细胞/0.5 ml/只给小鼠接种,接种细胞约7~14 d后收集腹水备用。
2.6 抗体纯化
采用结合缓冲液(Binding Buffer)平衡Protein G亲和柱至基线平稳;将腹水样品上柱,收集流穿液;将流穿液再次上柱,继续平衡至基线平稳;加入洗脱缓冲液(Eluting Buffer)洗脱,收集洗脱峰,检测纯度;用0.01 M,pH值为7.2的磷酸盐缓冲液(PBS)透析收集的洗脱峰,使纯化后的抗体保存在0.01 M,pH值为7.2的PBS中;用蛋白定量检测仪测定纯化后单抗的浓度;对纯化后的抗体进行SDS-聚丙烯酰胺凝胶电泳(SDSPAGE),上样量 8 μg/抗体。
2.7 抗体特异性鉴定
将红花蛋白按 10 μg/ml,100 μl/孔,4 ℃ 包被过夜。洗涤3次后,加入150 μl/孔3% 牛血清白蛋白(BSA),37℃封闭2 h;洗涤3次后,将单克隆抗体按 1:3000稀释,100 μl/孔37℃孵育2 h;洗涤3次后,将辣根酶标记的羊抗鼠IgG按1∶5000 稀释后,100 μl/孔,37 ℃ 孵育 1 h;加入 1 × TMB,37℃显色15~30 min,加入50 μl/孔 2 M 硫酸(H2SO4)终止反应。以450 nm单波长测定各孔OD值,以与阴性对照孔OD值的比值(P/N)>2.1为限,作为判断抗体阳性、效价或特异性的临界点。
3 结果
3.1 免疫后血清效价检测结果
经过4次免疫后,5只小鼠血清效价的检测结果见表1(应用硫酸盐缓冲液作为空白对照)。结果显示,5只小鼠均已达到融合标准,其中3号小鼠的效价最高。
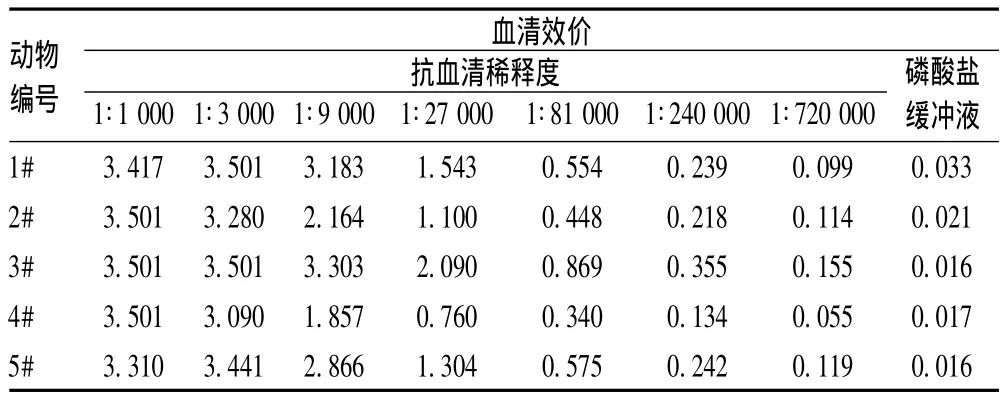
表1 红花花粉蛋白免疫血清效价检测结果(OD450 nm)Tab 1 Determination results on antisera titration of safflower pollen protein(OD450 nm)
3.2 单克隆细胞株的筛选
细胞融合后第3、6 d对融和板进行换液,于第7 d对融合细胞进行筛选。共有3个阳性细胞孔,为保证阳性率的稳定,再扩至24孔以再次检测确定。检测结果表明3株均为阳性。应用有限稀释法进行亚克隆,经过3次亚克隆后阳性率达100%,得到1B6,2A11,6H11共3个单克隆细胞株。
3.3 抗体亚型的鉴定
按试剂盒提供方法对所获得的3个单克隆抗体进行亚型鉴定,鉴定结果见表2。1B6、2A11、6H11表示3株细胞克隆的编号,产生的单克隆抗体应用相同编号。检测结果表明所获3株细胞产生的抗体亚型均为IgG1型。
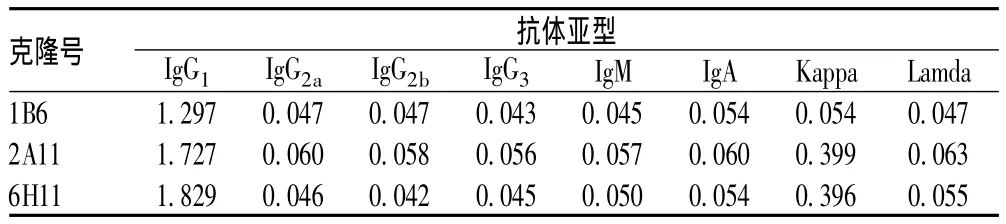
表2 单克隆抗体亚型鉴定(OD450 nm)Tab 2 Subtype identification of monoclonal antibodies(OD450nm)
3.4 抗体特异性鉴定
应用间接ELISA方法,进一步检测各单克隆抗体对红花蛋白抗原识别的特异性,检测结果见表3。单克隆抗体1B6、2A11、6H11较相应空白对照组(应用硫酸盐缓冲液作为空白对照)分别增加了9.63、9.59和6.61倍,结果见图1。结果显示,各单克隆抗体均能特异性识别红花蛋白抗原,均具有较强的特异性。

表3 单克隆抗体对红花花粉蛋白的特异性识别(OD450 nm)Tab 3 Specificity recognition of monoclonal antibodies on safflower pollen protein(OD450nm)
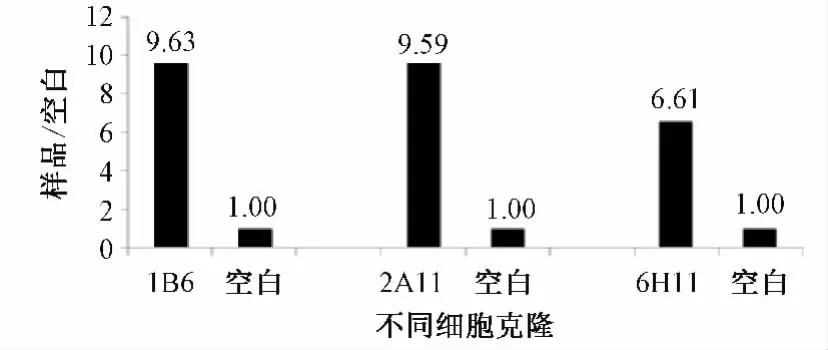
图1 单克隆抗体对红花花粉蛋白的特异性识别Fig 1 Specificity recognition of monoclonal antibodies on safflower pollen protein
4 讨论
4.1 中药注射剂引起的过敏问题
传统中药主要通过口服、外敷等方式应用,再则中药强调辨证论治、君臣佐使,单种药物成分浓度相对较低,因此,历来认为中药毒副作用较小,比较安全。随着科技进步和制药业的发展,中药注射剂、滴丸、喷雾剂等多种剂型在临床应用越来越广泛。但传统中药应用过程中较少出现的毒副作用,如中药注射剂引起的过敏性休克时常发生,并逐渐成为阻碍中药应用、制约企业发展的关键因素。因此,探索中药注射剂致敏的主要原因和发生机制,以改善制药工艺,消除过敏反应的发生成为当前亟待解决的关键问题。
4.2 中药注射剂诱导过敏的机制
与西药注射剂相比,中药注射剂常常成分复杂,诱导过敏反应发生的原因也更为复杂。有研究认为[7],中药过敏发生的原因与年龄、性别无关,主要与给药途径有关,尤其是注射用药最易诱发过敏反应。于风平等[8]用间接ELISA的方法筛查刺五加注射液中的过敏性杂质成分,并建议应用超滤技术去除过敏性杂质。红花、清开灵、双黄连注射剂等[4,9]均有诱发过敏反应的报道,另外制药中使用的聚氧乙烯脱水山梨醇单油酸酯(吐温-80)等还可诱导类过敏反应的发生[10]。中药药物成分、制药杂质和给药途径都是引起过敏或类过敏现象发生的重要原因。
4.3 构建过敏反应评价平台的目的和意义
由于缺乏适宜的中药注射剂过敏和类过敏反应评价模型,这成为制约中药注射剂发展的重要瓶颈。植物花粉是最为常见的致敏原之一,本研究以红花花粉蛋白作为研究的突破口,希望通过构建针对红花花粉蛋白的特异性细胞克隆、制备特异性单克隆抗体,作为研究红花注射剂过敏原鉴定、筛选的重要工具,也为改良红花注射剂制药工艺、降低过敏反应的发生提供技术支撑。目前,我们已经构建了3株针对红花花粉蛋白的细胞克隆,经鉴定均产生IgG1型抗体,效价较高。应用ELISA的方法,进一步证明这3个单克隆抗体均能识别红花花粉蛋白,并且具有较好特异性。今后,我们将以3个单克隆抗体作为研究工具,首先鉴定单克隆抗体识别红花花粉蛋白的免疫原结构,再探索红花花粉蛋白与红花注射剂诱导过敏反应发生之间的关系,研究红花注射剂关键的致敏原因,并希望研发出能够快速筛查红花注射剂过敏原残留的试剂盒,用于改善红花制剂工艺、降低过敏反应发生风险。期望以此作为工作基础,研究开发出针对多种中药成分的单克隆抗体,将我们的过敏反应评价体系,逐步拓展成为研究和评价各类中药注射剂过敏反应的通用平台,这将对我国中药制药的发展产生积极的推动作用,具有非常重要的意义。
[1]国家药典委员会.中华人民共和国药典:一部[S].2010年版.北京:中国医药科技出版社,2010:141-142.
[2]马飞,王丽莉,丁莉莉.红花注射液致过敏性皮疹1例[J].中国药物滥用防治杂志,2005,11(2):92.
[3]胡斌,谭志萍,王卉川.红花注射液致过敏性呼吸困难1 例[J].药物流行病学杂志,2006,15(5):309-310.
[4]葛红星,刘艳红,雷招宝.红花注射液致过敏性休克16例文献分析[J].中成药,2012,34(9):1836-1838.
[5]宋绍雄,高祥文,夏波.200例儿童食物过敏的原因分析[J].求医问药:学术版,2013,11(1):71-72.
[6]刘志华.花粉过敏的原因、预防和治疗[J].生物学教学,2013,38(1):52-53.
[7]冯艳霜.187例中药致过敏反应文献分析[J].药物不良反应杂志,2002,4(2):81-83.
[8]于风平,胡昌勤,崔生辉,等.刺五加注射液中过敏性杂质的分析[J].中国药学杂志,2008,43(5):384-387.
[9]翁维良,林洪生,高蕊,等.4种中药注射剂皮肤过敏试验方法与意义的探讨[J].中国中药杂志,2007,32(24):2649-2652.
[10]李黎明,金若敏,李小月.中药注射剂类过敏反应实验研究进展[J].中药药理与临床,2012,28(1):187-190.

