老年患者发生药品不良反应的相关因素分析
江 佳,刘 俊(皖南医学院弋矶山医院药剂科,安徽芜湖 241001)
随着我国医疗卫生事业的发展和人们生活水平的提高,截至2005年底我国≥65岁老年人口达10055万人,占全国总人口的7.7%,占世界老年人口的1/5,占亚洲老年人口的1/2[1],我国已经步入老龄化社会。老年人特殊的生理特点决定了其用药的特殊性,加之老年人对药品敏感性较高,故其容易发生药品不良反应(ADR)。国外有文献报道,老年患者ADR发生率明显高于年轻患者,70~79岁者ADR发生率较20~29岁增加了近7倍。国内也有相关报道,在所有发生ADR的人群中,老年患者发生ADR的构成比较高[2,3],因此,老年人用药的安全性应当受到人们的关注。笔者通过对我院老年患者发生的ADR进行分析,了解其发生的特点及规律,以便引起临床重视而减少或避免ADR的发生,保障老年患者用药安全。
1 资料与方法
采用回顾性调查的方法,利用全国ADR监测网络数据库检索出我院2011年收集上报的746例ADR报告,从中筛选出60岁及以上的患者作为研究对象,共计333例,构成比为44.64%。对其进行因果关系评价:肯定28例,很可能25例,可能280例。利用Excel表格登记患者年龄与性别、ADR名称、一般情况及主要临床表现、药品名称与给药方式等,对上述资料进行分类汇总、分析。
2 结果
2.1 患者一般情况
男性150例,女性183例,男女比例为1∶1.22;年龄分布为60~87岁,平均年龄为(69.36±6.80)岁,其中60~69岁者171例,70~79岁者130例,80~87岁者32例。
2.2 ADR一般情况
ADR发生程度较轻以一般反应为主有307例(占91.29%),另外新的ADR有12例(占3.60%),严重的ADR有14例(占5.11%);ADR预后良好,好转270例(占81.08%)、治愈61例(占18.32%)、有后遗症2例(占0.60%),未出现死亡病例。
2.3 药品使用情况
药品的使用以单一用药为主,有298例,占89.49%;联合用药35例,占10.51%。给药途径以静脉滴注为主,有162例,占总数48.65%;其次为口服给药,有161例,占48.35%,见表1(其他包括舌下含服及眼内用药)。
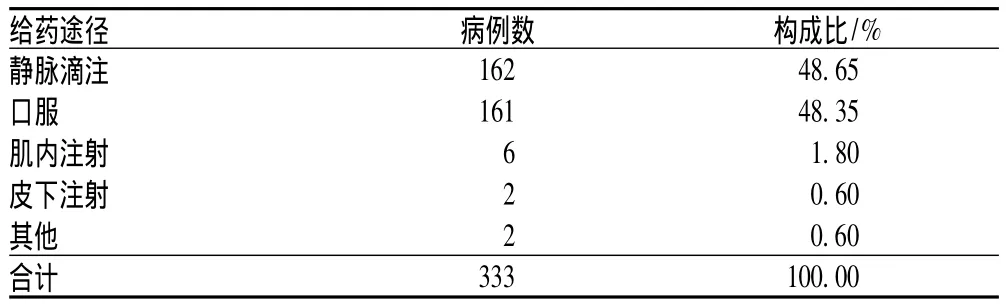
表1 发生ADR的给药途径Tab1 Distribution of route of administration in ADR cases
2.4 引起ADR的药品种类
引发ADR的药品涉及14类166个品种,心血管系统用药发生ADR的例数最多,为78例,占23.42%;其次为抗感染药,为74例,占22.22%;消化系统用药发生ADR 35例,占10.51%,居第3位,见表2。从具体药品分布来看,左氧氟沙星(18例,占23.68%)、中长链脂肪乳(11例,占14.47%)及尼麦角林(8例,占10.53%)发生ADR的例数分别居前3位,见表3。
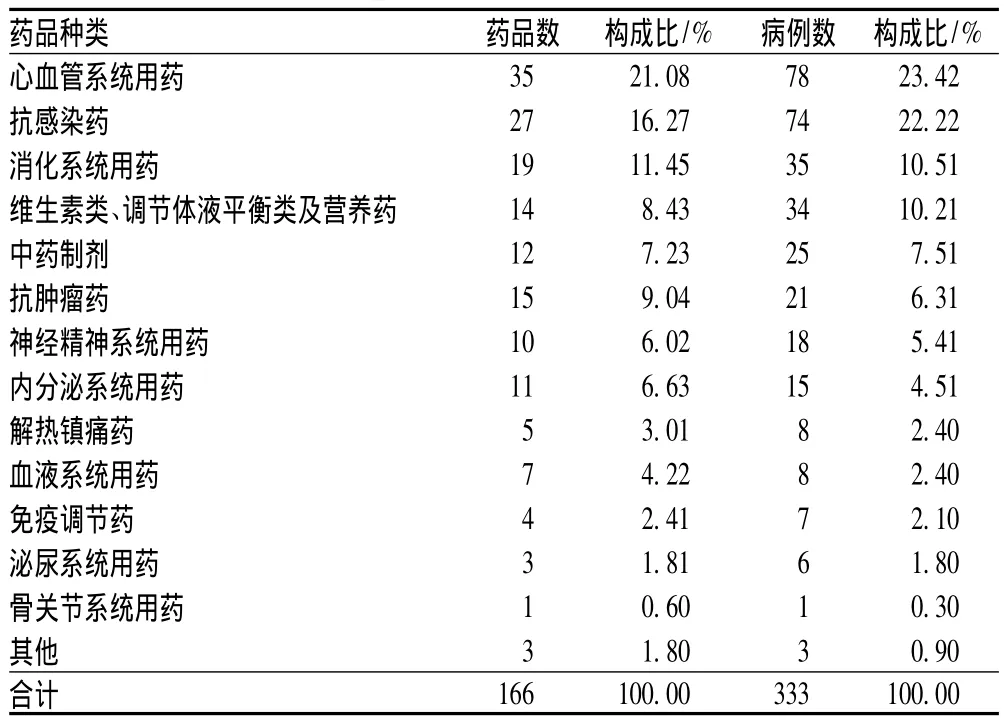
表2 引起ADR的药品种类Tab 2 Types of ADR-inducing drugs
2.5 ADR累及器官和(或)系统及主要临床表现
参考世界卫生组织(WHO)《药品不良反应术语集》对ADR进行分类,ADR可累及全身多个脏器,本次分析结果以消化系统症状最多,共85例,占25.53%;其次为皮肤及附件损害,共55例,占16.52%,见表4。

表3 发生ADR例数排序前10位的药品Tab 3 Top 10 drugs ranked by number of ADR cases
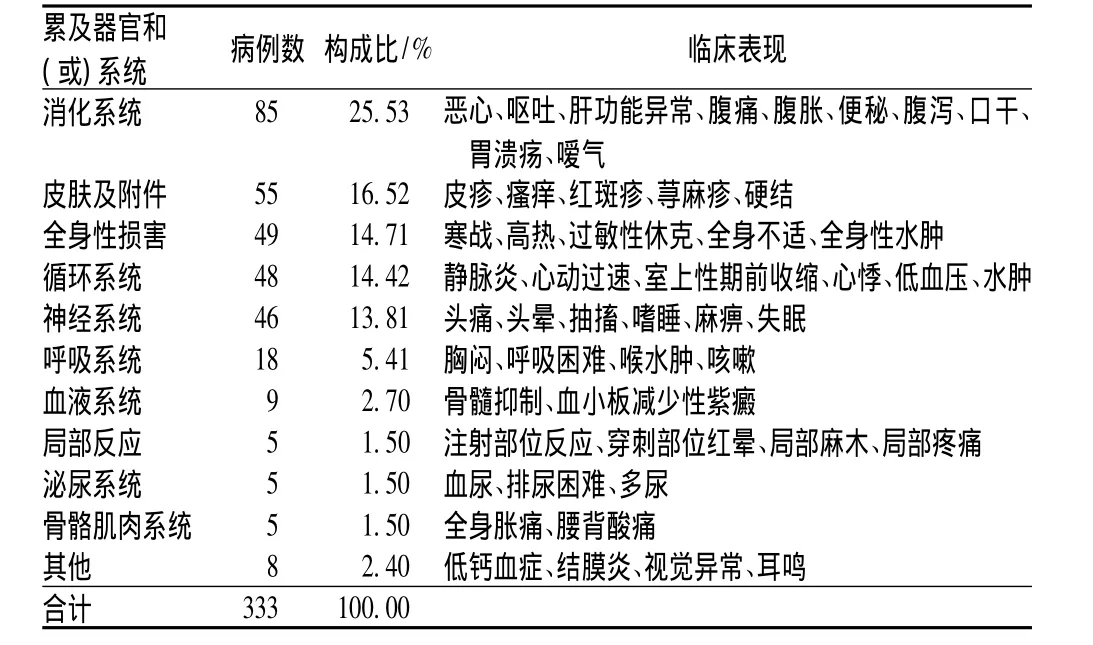
表4 ADR累及器官和(或)系统及主要临床表现Tab 4 Organs and(or)systems involved in ADR and main clinical manifestation
3 讨论
3.1 老年患者发生ADR的原因
老年患者发生 ADR的例数较多,占ADR总例数的44.64%,与文献报道相似[2]。女性ADR发生例数略多于男性,至于性别是否为老年患者ADR诱发因素有待于进一步验证。老年患者生理机能处于不断衰退状态,机体内环境的变化会影响药物的吸收、分布、代谢和排泄过程。老年患者血浆白蛋白含量减少,使得游离型药物浓度增大,药物作用增强而引发ADR;老年患者骨骼肌肉相对减少,可使得在肌肉组织中分布广泛的药物(如地高辛)的血药浓度增加而诱发ADR;老年患者肝脏的血流量比青年人减少40%~50%[4],肝脏代谢酶的合成及活性也显著下降,药物的代谢减慢,血浆半衰期延长;老年患者肾功能亦随着年龄增长而逐渐下降,65岁老年人的肾血流量仅为年轻人的40%~50%[5],直接影响药物在肾脏的排泄,导致药物容易在体内蓄积而诱发ADR。老年患者患病较多且病情复杂,联合用药概率较大,有资料显示:同时使用5种以下药物,ADR发生率为6%~8%;同时用药6~10种时,ADR发生率上升为40%;当用药数达到15~20种,ADR发生率将升至70%~80%[6];老年患者对药物的敏感性较高,尤其是心脑血管系统用药在常规剂量下可表现出较强的药理作用甚至出现ADR。另外,老年患者用药依从性较差,常出现漏服药物、过量服药及不规则用药等,均可诱发ADR。因此,老年患者用药应结合患者具体情况,根据患者的肝肾功能进行剂量调整,建议60岁以上老年患者用药剂量为成人剂量的3/4,有些药物为成人剂量的1/2[7]。
3.2 ADR与给药途径的关系
静脉滴注是导致ADR发生的主要给药途径,占48.65%。由于静脉滴注可避免肝脏的首关效应,药物直接进入血液可迅速达到峰浓度而发挥药理作用,对于急症或重症患者可起到较好的临床效果,临床使用频率较高。但药物溶液除了受本身pH值、渗透压、可溶性微粒、内毒素以及滴注速度等因素的影响,还与药物配制过程、药物浓度、药液放置时间有密切关系[8],这些因素均可导致ADR的发生。静脉滴注致 ADR的程度一般较其他给药方式严重,在上报的14例严重的ADR中,由静脉滴注导致有12例,主要表现为寒战、高热、过敏性休克、呼吸困难及骨髓抑制等,有2例患者在输液过程中出现过敏性休克而导致器官功能衰竭。因此对于老年患者应严格掌握输液指征,在病情允许的情况下尽量采用非静脉用药,遵循“能口服勿注射”的原则。由于口服给药具有服药方便、药物无需特殊处理、患者可自行处理等优点而被广泛采用,其ADR发生例数仅次于静脉滴注居第2位,但ADR发生程度一般较轻,主要表现为消化系统、神经系统反应及皮肤症状。
3.3 ADR与药品的关系
心血管系统用药和抗感染药发生ADR的构成比较高且累及的药品数较多,可能与老年患者心血管系统疾病发病率高及老年患者免疫功能减退易受外界致病因子侵袭使得相关药物使用频率较高有关,另外抗感染药不合理使用如无指征用药、预防及联合用药不当、用药剂量过大及疗程过长等也是诱发ADR的重要因素。随着新型氟喹诺酮类抗菌药物的不断出现,药物的耐药性问题日益显著,由氟喹诺酮类导致的ADR也频繁出现[9],其代表药左氧氟沙星通过破坏细菌DNA拓扑异构酶、干扰细菌DNA的合成而发挥抗菌作用,因具有抗菌谱广、抗菌活性强、组织渗透性好等优点而用于临床各种感染性疾病的治疗,在我院左氧氟沙星的使用量一直居高不下,其ADR发生例数居首位。此外,左氧氟沙星在我院部分老年患者中用法、用量欠妥,如采用 0.6 g、ivd、qd,0.4 g、ivd、bid。老年患者肾脏清除能力减弱,左氧氟沙星1日量1次给予以及大剂量用药,均可加重肾脏负担,尤其对于已经有肾损害的患者,可导致药物在体内蓄积而诱发ADR;左氧氟沙星脂溶性较强,易透过血-脑脊液屏障,与γ-氨基丁酸(GABA)受体结合而诱发神经精神症状,尤其对于老年患者其引发神经精神症状较为常见;左氧氟沙星结构中含有的氟原子可与光线中紫外线结合而诱发光敏性皮炎。另外脂肪乳等营养药引发的ADR也应引起关注,其导致的ADR例数仅次于左氧氟沙星,脂肪乳系由大豆油加入一定量的卵磷脂乳化而成的无菌、无热源的乳剂型注射剂,其较大的微粒可作为外源性异物被机体免疫系统识别而产生剧烈的免疫反应[10],可表现为全身症状及心血管反应,在使用过程中应注意控制滴注速度,在最初 10 min为20 滴/min,30 min 后维持为40 ~60 滴/min[11]。
3.4 ADR临床表现及处理
ADR的症状可表现消化系统反应、皮肤及附件损害、全身性损害、循环系统反应、神经系统反应及呼吸系统反应,其中以消化系统反应和皮肤及附件损害最多见,分别占25.53%、16.52%,与这2类临床症状易于观察和判断有关。消化系统反应主要表现为恶心、呕吐、腹痛等胃肠道反应以及肝功能异常,大部分与滴注速度过快有关,经过减慢滴注速度,症状可缓解,重症患者给予甲氧氯普胺10 mg、im或格拉斯琼50 mL、ivd后好转;阿奇霉素等大环内酯类抗菌药物致胃肠道反应较常见,在输液中加入维生素B6可明显减少胃肠道不适症状;对于肝功能异常的轻症患者经过停药可自行缓解,如症状较重,给予甘草酸制剂等保肝处理后可使肝功能恢复正常。皮肤及附件损害表现为皮疹、瘙痒等过敏反应,与药品本身和皮肤敏感性有关,给予地塞米松10 mg、iv或泼尼松5 mg、po,并给予氯苯那敏等抗组胺药对症处理后可使症状消失;对于抗肿瘤药可在用药前预防性给予糖皮质激素及抗组胺药,可使皮肤过敏反应明显减少。
综上所述,老年患者发生ADR的原因较为复杂,除了与老年患者自身生理及病理因素有关外,还与药物种类、给药方式等外界因素有关。因此临床在接诊老年患者时,应仔细耐心地询问患者或其家属,以尽可能详细地了解患者的病史、过敏史、ADR史及用药情况,结合必要的实验室检查,全面综合分析患者病情,作出正确的诊断,制订出合理的治疗和用药方案,在用药过程中加强ADR监测,以降低老年患者发生ADR的风险。
[1]李 倩,冯端浩,李国栋,等.老年人用药风险分析[J].中国医院用药评价与分析,2012,12(2):175-178.
[2]肇启春.313例老年患者药品不良反应分析[J].沈阳药科大学学报,2009,26(S1):54-56.
[3]崔艳丽.108例药品不良反应报告分析[J].中国医院用药评价与分析,2011,11(9):847-849.
[4]徐叔云,魏 伟.临床药理学[M].3版.北京:人民卫生出版社,2008:119.
[5]陈雅敏.特殊人群的药物警戒[J].药物流行病学杂志,2011,20(6):315-317.
[6]Steele AC,Meechan JG.Pharmacology and the elderly[J].Dent Update,2010,37(10):666-670.
[7]沈 芊,闫素英,王育琴.331例抗感染药致老年人药品不良反应分析[J].药物流行病学杂志,2011,20(6):291-294.
[8]毛疆民,王 勇,毛全高.200例药品不良反应报告分析[J].中国医院药学杂志,2012,32(1):75-76.
[9]刘又宁.关注氟喹诺酮类药物不良反应[J].中国社区医师,2010,7(1):20-21.
[10]杨春艳,蔡 琦.我院32例脂肪乳注射液不良反应报告分析[J].中国药事,2011,25(1):83-84.
[11]陈新谦,金有豫,汤 光.新编药物学[M].17版.北京:人民卫生出版社,2011:814.

