1-甲基-3丙酸咪唑硫酸氢盐在烯烃环氧化中的应用
张阳阳,阎 松,赵 威
(1.辽宁石油化工大学,辽宁 抚顺113001; 2.营口理工学院,辽宁 营口 115000)
环氧化合物是指分子中含有一个或多个环氧基的一类化合物,它是有机合成中应用比较广泛的重要中间体之一[1-3]。目前合成环氧化合物的重要反应是烯烃的环氧化反应。烯烃环氧化反应广泛的应用于很多领域,对其进行研究具有重要的理论及实践意义。对于环氧化反应,绝大部分是需要催化剂的[4]。因此如何选择合适的催化剂进行反应是至关重要的。催化剂不仅要求其具有较高的活性和选择性,对于其环保方面也越来越受到科学家们的重视。而对于许多环氧化反应是对环境有害的,最初的氯醇法生产环氧化合物由于对环境造成污染而逐渐被淘汰[5]。研发环境友好型催化剂来替代常规试剂是绿色化学研究的重要内容[6]。
离子液体是近年来发展起来的并不断壮大的具有优良性能的绿色试剂,它完全由阴阳离子构成,是在室温下或接近室温下呈液态的低温熔融盐。由于其具有可忽略的蒸汽压及较好的热稳定性而被用于很多催化反应[7-10]。离子液体在催化反应中可循环使用次数较多、回收利用率较高、对环境友好,引起了人们越来越多的关注。随离子液体的种类逐渐更新,选择合适的具备特定性能的离子液体进行催化反应将会获得较普通有机溶剂让人满意的结果。
本论文重点研究了以离子液体1-甲基-3-丙酸咪唑硫酸氢盐(简称[C1imCH2CH2COOH]HSO4)和{[(phens)2(H2O)FeⅢ]2(μ-O)}(ClO4)4(后文中以A表示)为催化剂,以30% H2O2为氧化剂,将以1-辛烯为代表的烯烃转化成相应的环氧化物的反应。结果表明,当离子液体用量为0.5 mmol,30%双氧水3 mmol,反应时间15 min,反应温度5 ℃,1-辛烯的转化率达到99%以上,1,2-环氧辛烷的选择性达到92%。表明该催化体系对烯烃环氧化反应具有良好的催化性能,反应结束后,因产物不溶于离子液体而分层,通过倾倒即可分离。
1 实验部分
1.1 离子液体结构
离子液体 1-甲基-3-丙酸咪唑硫酸氢盐(简称[C1imCH2CH2COOH]HSO4)结构见图1。
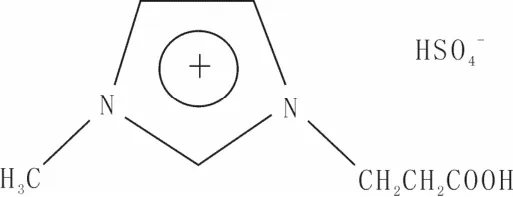
图1 [C1imCH2CH2COOH]HSO4的结构式Fig.1 The structure of [C1imCH2CH2COOH]HSO4
1.2 化合物A的制备
将高氯酸铁(0.197 g,0.56 mmol)溶于0.5 mL水中;将1,10- 啰菲 啉(0.2 g,1.1 mmol)溶于4.5 mL乙腈中;把二者混合加入到50 mL了反应瓶中,室温下在磁力加热搅拌器上搅拌10 min,得到产物A(图2)在-4 ℃下静置以备用。
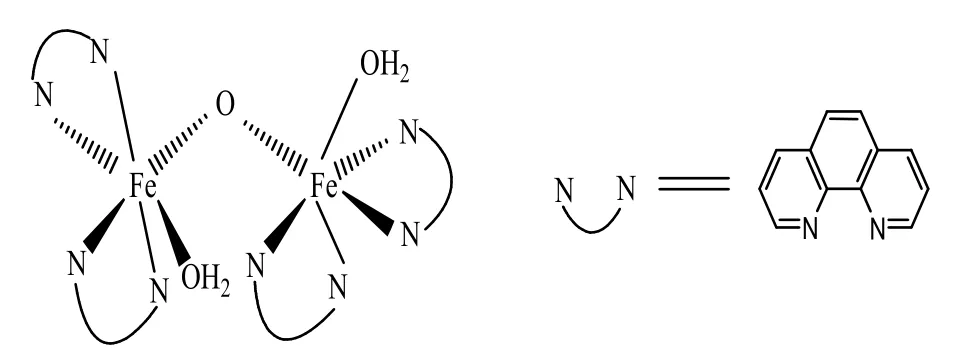
图2 {[(phens)2(H2O)FeⅢ]2(μ-O)}(ClO4)4(化合物A)的结构式Fig.2 The structure of {[(phens)2(H2O)FeⅢ]2(μ-O)}(ClO4)4(complexA)
1.3 烯烃的催化环氧化反应
将离子液体1-甲基-3-丙酸咪唑硫酸氢盐(0.5 mmol)和 30%H2O2(3 mmol)放入 50 mL反应瓶中,室温下在磁力加热搅拌器上搅拌15 min,在5 °C条件下,再加入上述制备的化合物 A(0.28 mmol),向反应瓶中滴加1-辛烯(2.8 mmol),剧烈搅拌调节转速不低于1 000 r/min,反应结束后,在0~5 ℃下静置分层,用正己烷萃取5次,每次1 mL,在0~5℃下静置分层,下层为含有离子液体的水相,上层为油相,取上层有机液进行在Q-Mass910GC/MS上定性分析,在SP-3400气相色谱仪上定量分析,并由仪器自带的色谱软件系统根据不同组分的峰面积直接给出定量数据,含量小于0.5%的产物未计算在内(图 3)。
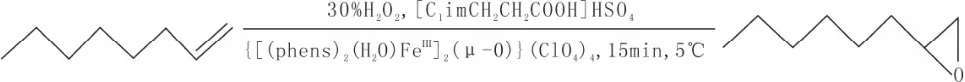
图3 1-辛烯烃的环氧化反应Fig.3 The epoxidation of 1-octene
1.4 定性和定量分析
产物在Q-Mass910GC/MS上定性分析,在SP-3400气相色谱仪上定量分析,并由仪器自带的色谱软件系统根据不同组分的峰面积直接给出定量数据,含量小于0.5%的产物未计算在内。
2 结果与讨论
2.1 离子液体用量
考察了离子液体1-甲基-3-丙酸咪唑硫酸氢盐([C1imCH2CH2COOH]HSO4)用量对 1-辛烯环氧化反应的影响,结果见图4。从图4中可以看出,随着离子液体的用量增加,1-辛烯的转化率和 1,2-环氧辛烷的选择性不断增加;当离子液体的用量为0.5 mmol,1-辛烯的转化率达到99%,此时,1,2-环氧辛烷的选择性为92%;这一结果已经相当好,说明离子液体完全能够代替相转移催化剂或有机酸性配体,而且离子液体对环境更加友好。再增加离子液体的用量,1-辛烯的转化率和 1,2-环氧辛烷的选择性变化不大。因此选择离子液体的用量为0.5 mmol。

图4 离子液体用量对1-辛烯环氧化反应的影响Fig. 4 Influence of the amount of ionic liquids on 1-octene epoxidation
2.2 双氧水用量
考察了H2O2用量对1-辛烯环氧化反应的影响,结果见图5。从图5中可以看出,当双氧水(30%)用量为0.5 mmol时,1-辛烯的转化率仅为48%,1,2-环氧辛烷的选择性为80%。这是由于氧化剂量太小,导致反应的 1-辛烯很少;随着双氧水用量的增加,更多的1-辛烯参加反应,1,2-环氧辛烷的转化率也逐渐的增加;当双氧水的用量为3 mmol时,1-辛烯的转化率达到99%,1,2-环氧辛烷的选择性达到92%,此时1-辛烯基本上完全反应,大部分都转化成了1,2-环氧辛烷;继续增加双氧水的用量,1-辛烯的转化率变化不大,1,2-环氧辛烷的选择性却不断下降,GC/MS检测结果表明这是由于过量的的双氧水使产物1,2-环氧辛烷氧化,生成不稳定的辛二醇,辛二元醇进一步被氧化生成 1-辛酸。由此可以看出过多的双氧水对烯烃的环氧化反应并没有太大好处。因此我们选择双氧水的用量为3 mmol。
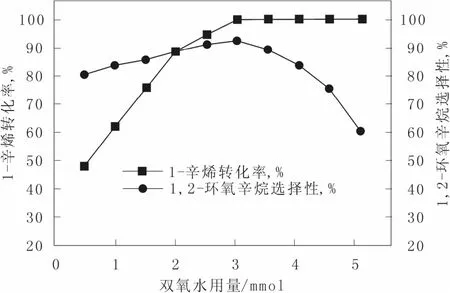
图5 双氧水用量对1-辛烯环氧化反应的影响Fig. 5 Influence of the amount of H2O2 on 1-octene epoxidation
2.3 反应时间
考察反应时间对1-辛烯环氧化反应的影响,结果见图6。从图6可以看出,反应开始时,1-辛烯的转化率比较低,1,2-环氧辛烷的选择性也不高。随着反应时间的增加,反应转化率逐渐升高,当反应时间为15 min时,1-辛烯的转化率已经达到99%,基本上完全反应,此时1,2-环氧辛烷的选择性也达到92%。但当反应时间超过15 min时,延长反应时间,1-辛烯的转化率和1,2-环氧辛烷的选择性基本不变,说明再增加反应时间1-辛烯的转化率和1,2-环氧辛烷的选择性不会再由明显变化。因此,我们选择15 min作为反应的最佳时间。
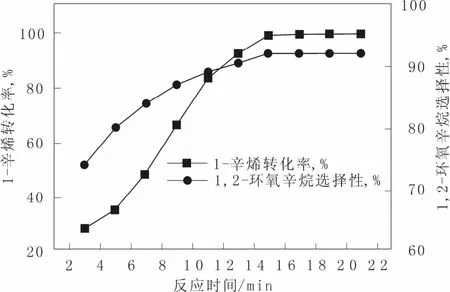
图6 反应时间对1-辛烯环氧化反应的影响Fig.6 Influence of different time on 1-octene epoxidation
2.4 反应温度
考察了反应温度对1-辛烯环氧化反应的影响,结果见图7。从图7中可以看出,反应温度为0℃时,1-辛烯的转化率较低;随着反应温度的增加,1-辛烯转化率逐渐升高,1,2-环氧辛烷的选择性也随之升高;当反应温度为5 ℃时,1-辛烯的转化率达到99%,1,2-环氧辛烷的选择性为92%,再提高反应温度对反应影响不大,因此我们选择5 ℃为最佳反应温度。
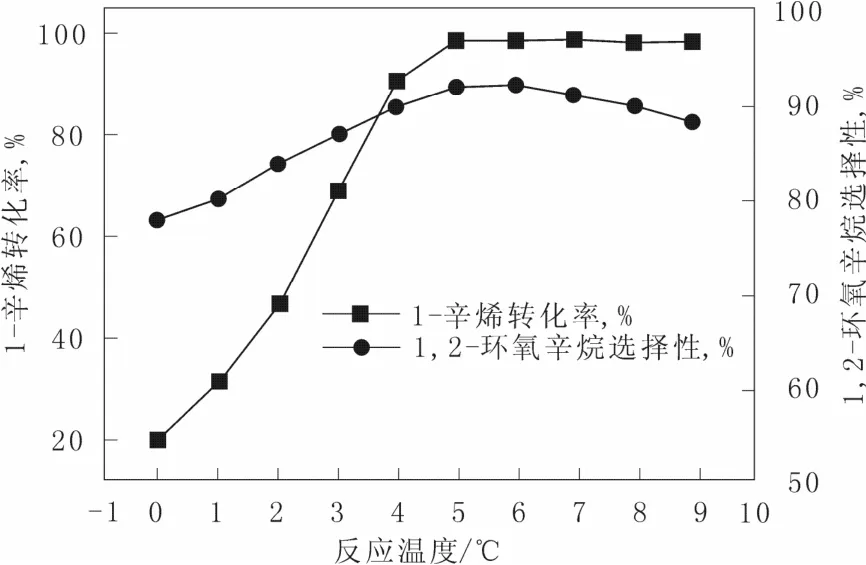
图7 反应温度对1-辛烯环氧化反应的影响Fig.7 Influence of different temperature on 1-octene epoxidation
2.5 催化体系的循环使用
反应结束后,在0~5 ℃下静置分层,用正己烷萃取5次,每次1 mL,在0~5 ℃下静置分层,下层为含有离子液体的水相,上层为油相,将下层滤液减压抽滤,用旋转蒸发仪浓缩到1 mL,然后加入30%H2O2(1 mL)反应15 min,加入1-辛烯按照以前的操作进行,催化体系的循环使用结果见表1。由表1可知,催化剂重复使用7次,催化活性基本不变,表明该催化体系是可以重复使用的。
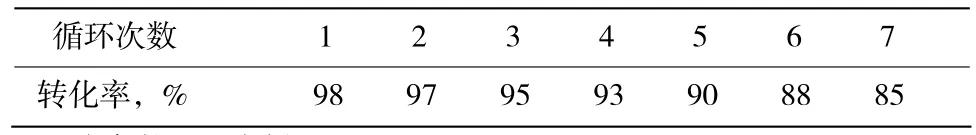
表1 催化剂重复使用Table 1 Recycling of the catalyst
2.6 其它烯烃环氧化反应
考察其他烯烃的环氧化反应,结果见表2。从表2中可以看出,在离子液体[C1imCH2CH2COOH]H SO4中,以化合物A为催化剂,考查了庚烯,辛烯,壬烯,癸烯的环氧化反应,结果表明,以30%H2O2为氧源时,上述烯烃的转化率都达到99%以上,表明该催化体系对多种烯烃具有较高的催化活性。
3 结 论
烯烃的环氧化反应在有机化学反应中非常具有挑战性,许多反应体系都有很多不足,例如:昂贵有毒的催化剂,较长的反应时间,少见的催化剂载体等。本论文研究了以1-辛烯为代表的多种烯烃的环氧化反应,研究表明,在离子液体 1-甲基-3丙酸咪唑硫酸氢盐中,以 30%双氧水为氧化剂,以{[(phens)2(H2O)FeⅢ]2(μ-O)}(ClO4)4为催化剂,在 5 ℃条件下,反应15 min,1-辛烯的转化率高达99%。
该催化体系具有良好的催化性能,它在一系列的烯烃环氧化反应中都显现出良好的活性并且获得了较高的转化率。离子液体可以多次循环使用,是一种极具潜力的对环境友好的催化材料。
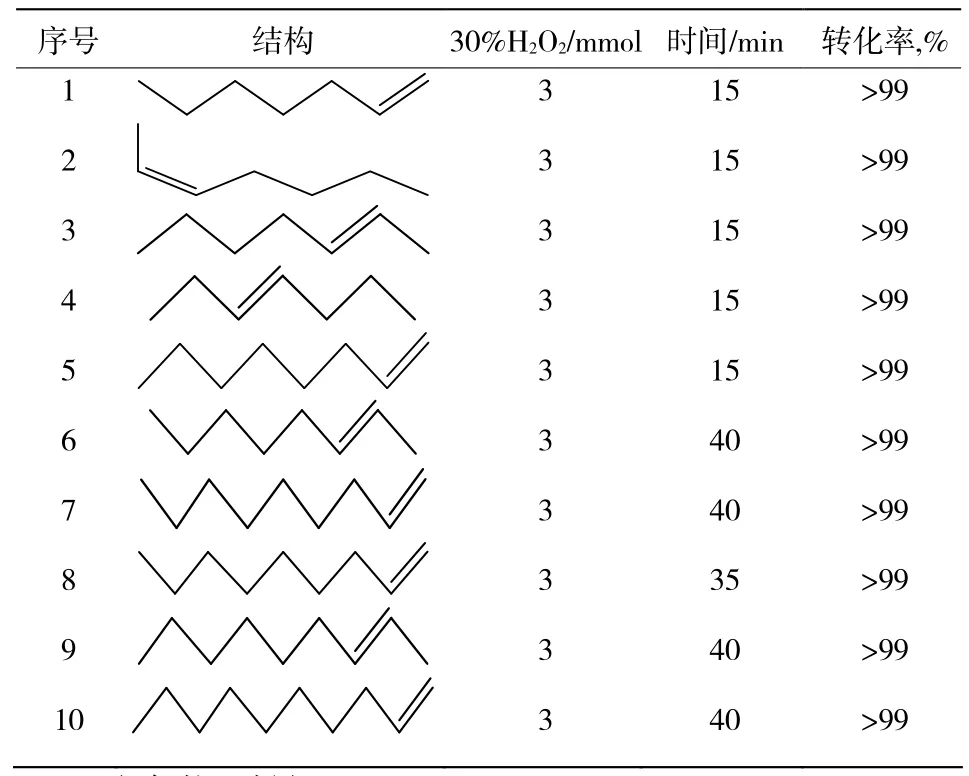
表2 烯烃的环氧化反应Table 2 The epoxidation of other olefins
[1]Maradur S P, Jo C, Choi D H, et al. Mesoporous polymeric support retaining high catalytic activity of polyoxotungstate for liquid-phase olefin epoxidation using H2O2[J]. Chem Cat Chem, 2011, 3 (9):1435-1438.
[2]但年华,但卫华,曾睿,等. 环氧化合物及其在胶原改性中的应用[J].材料导报, 2006, 20 (6) : 119-122.
[3]于松杰,王寿峰,孙伟.新型四氮锰配合物催化烯烃环氧化反应的研究[J].分子催化,2011, 25(3): 209-212.
[4]陈超, 吴显春,宗焕荣,等. 烯烃环氧化催化剂的研究进展[J]. 化工科技, 2007, 15 ( 4) : 48-53.
[5]李学峰,高焕新,陈庆龄.介孔材料在烯烃环氧化中的催化应用[J]. 化学进展,2006, 18(7,8): 849-853.
[6]欧阳小月,江焕峰,等.以双氧水为氧源的烯烃环氧化反应[J].有机化学,2007, 27 (3): 358-367.
[7]GUI J Z,CONG X H,LIU D,et al. Novel Brönsted acidic ionic liquid as efficient and reusable catalyst system for esterification [J]. Catalysis Communications, 2004, 5 (9): 473-477.
[8]GUI J Z, DENG Y Q, HU Z D, et al. A novel task-specific ionic liquid for Beckmann rearrangement: A simple and effective way for product separation [J]. Tetrahedron Letters, 2004,45 (12): 2681-2683.
[9]COLE A C,JENSEN J L,NTAI I,et a1. Novel Brönsted acidic ionic liquids and their use as dual solvent-catalysts [J]. Journal of the American Chemical Society, 2002, 124: 5962-5963.
[10]刘晓飞,陈静,夏春谷. 吗啉基功能化酸性离子液体催化苯酚一叔丁醇选择性烷基化反应[J]. 分子催化, 2008, 22 (5): 392-397.

