9,10-环亚甲基假紫罗兰酮的响应面法合成
赵 扬 ,罗金岳 ,2
(1南京林业大学化学工程学院,江苏 南京 210037;2江苏省生物质绿色燃料与化学品重点实验室,江苏 南京210037)
鸢尾酮(Irone),又名6-甲基紫罗兰酮,存在3种同分异构体,其香气甜香柔和且纯正,已作为国际上公认的、同时也是紫罗兰香料系列中最名贵的高级香料[1-2]。鸢尾酮广泛用于食品、化妆品、香烟、香皂、衣物、纸张和书籍等产品上。其优雅的香气,良好的协调性,突出的定香作用,使得许多高档紫罗兰型香水中都有它的踪影[3]。我国步入鸢尾酮研究领域虽然只是近几年的事情,但由于我国有丰富的山苍子资源,利用柠檬醛半合成鸢尾酮,不仅可以充分利用我国自然资源,而且可以获得丰厚的经济价值[4]。
生产鸢尾酮的方法较多,应根据原料来源情况选择合适的生产方法。目前制得鸢尾酮的研究热点主要为化学合成法。研究学者Delpace用松脂加工副产物异戊二烯经调聚反应、Sommelet反应得柠檬醛[5]。Schinz等[6]借鉴此法,用异戊二烯合成了甲基香叶基氯,通过Sommelet反应得6-甲基柠檬醛,再与丙酮缩合得假性鸢尾酮,经环化获得了鸢尾酮。Barton于1960年提出的假性紫罗兰酮路线[7],1980年经Torii等[8]改进,经5步合成鸢尾酮的α、β、γ混合物,后经刘晓庚、陈梅梅等改进为柠檬醛→假性紫罗兰酮→假鸢尾酮→鸢尾酮(α,β,γ),将甲基定位反应放到环化反应之前,降低了甲基定位反应的难度,是值得借鉴的。而9,10-环亚甲基假紫罗兰酮作为柠檬醛路线的中间体,其研究价值不言而喻。本文旨在以假紫罗兰酮为原料,通过Simmons-Smith反应合成鸢尾酮的重要中间体9,10-环亚甲基假紫罗兰酮,并通过响应面法得到选择性好、产物得率高的9,10-环亚甲基假紫罗兰酮合成工艺。
1 实验部分
1.1 原料及仪器
假紫罗兰酮为自制淡黄色液体,经GC检测纯度为94.02%,具体制作方法参见文献[9]。冰乙酸、氢氧化钠、氯化钠、乙酸铜、无水硫酸钠、锌粉、二碘甲烷(化学纯)、二苯甲酮(化学纯)、钠(化学纯)、二氯甲烷、乙醇、乙醚、无水氯化钙、四氢呋喃、1,2-二氯乙烷、二乙基锌(1.0 mol/L 正己烷溶液)、氢化钙(放氢量>97%)、分子筛 3Å 型(钾-Å型)分子筛,球状Φ3~5 mm、柱层析用硅胶 200~300目、GF254型硅胶板等。未注明试剂药品均为分析纯,层析硅胶由青岛海洋化工试剂厂提供。
巩义市英峪予华仪器厂SHZ-D(Ⅲ)型循环水式真空泵;上海江星仪器有限公司 DF-1型集热式磁力恒温搅拌器;日本SHIMADZU公司7890A型气相色谱仪;美国Agilent公司7890A-5975C型气相-质谱联用仪;美国Thermo Electron公司Nicolet 380 FTIR型红外分析仪。
1.2 试验方法
1.2.1 锌铜偶催化剂的制备[10]
(1)方法Ⅰ 在500 mL锥形瓶中加入49.2 g纯锌粉和40 mL 3 %的盐酸,电磁快速搅拌1 min,放置到沉淀完全,倾去上层清液。同样的操作,依次用3次40 mL 3 %的稀盐酸,5次100 mL水,2次75 mL 2 %硫酸铜水溶液,5次100 mL水,4次100 mL乙醇和5次100 mL无水乙醚处理。最后把所得锌铜偶移到布氏漏斗上,加无水乙醚,覆盖橡皮薄膜,吸气到干。移到真空干燥器中,在五氧化二磷存在下干燥过夜。
(2)方法Ⅱ 2 g一水合乙酸铜和50 mL冰乙酸在接近回流温度下加热溶化,快速搅拌,加入35 g纯锌粉,搅拌0.5 min后,铜沉淀完全。放置1 min,倾去上层清液。用50 mL冰乙酸洗涤,再用无水乙醚100 mL洗涤3~5次。湿的锌铜偶即可直接使用。这种方法制备简单,随制随用。活性较高,不仅可用于二碘甲烷,还可用于二溴甲烷。
进行反应之前,先通过Schlenk装置将体系内空气排空,并对所有反应溶剂和反应体系进行除水操作,整个过程使用氮气保护,创造较为严格无水无氧反应环境后方能开始反应。
1.2.2 以锌铜偶为催化剂合成鸢尾酮的步骤
向三口烧瓶中加入30 mL溶剂和固体催化剂,称取定量二碘甲烷,快速加入装有催化剂的三口烧瓶中,在恒压漏斗中加入定量的假性紫罗兰酮,在磁力搅拌器中加入冰块,使用氯化钠使反应体系内的温度保持在−5 ℃。将各处瓶口用生料带封好,避免水蒸气进入。在冰浴反应温度下保持0.5 h,使卡宾试剂充分形成后开始滴加假紫罗兰酮,滴加时间控制在1 h。继续低温反应一定时间,缓慢回温1 h至20 ℃,后加热至一定温度并保持一定时间,反应在回流条件下进行。
回流结束后,迅速将反应物倒至碎冰上,发生淬灭反应,为保证淬灭反应完全,碎冰体积为反应物的2~3倍,后将反应物倒入布氏漏斗抽滤,并用乙醚充分洗涤。滤液静置分层,将上层乙醚层用1∶10的氨水洗涤3~5次,至乙醚层澄清,后用蒸馏水洗至中性,加入无水硫酸钠除水,过夜,旋蒸除去溶剂,进行检测。
1.2.3 以二乙基锌为催化剂合成鸢尾酮的步骤
先在三口烧瓶中加入一定量的二碘甲烷和溶剂,在恒压漏斗中加入一定量的假紫罗兰酮,将接口用生料带密封,用注射器将一定量的二乙基锌溶液通过N2胶管迅速打入反应体系中,在磁力搅拌器中加入冰块,使用氯化钠使反应体系内的温度保持在−5 ℃,在冰浴反应温度下保持0.5 h后开始滴加假紫罗兰酮,时间控制在1 h。继续低温反应一定时间,缓慢回温1 h至20 ℃,后加热至一定温度并保持一定时间,反应在回流条件下进行。
回流结束后,迅速将反应物倒至碎冰上,发生淬灭反应,后用乙醚萃取,静置分层,取上层乙醚层,加入无水硫酸钠除水,过夜,旋蒸除去溶剂,进行检测。
反应式如式(1)。

1.3 产物的分析鉴定
产物含量测定采用日本 SHIMADZU公司7890A型气相色谱仪,使用DB-5型毛细管柱,初温80 ℃,以5 ℃/min的速率升至250 ℃,面积归一法定量,进样量0.2 μL,气化室温度250 ℃,检测器温度 250 ℃。采用美国 Agilent公司7890A-5975C型气质联用仪对其结构进行初步鉴定,采用HP-5型色谱柱,初温80 ℃,以5 ℃/min的速率升至260℃,FID检测器,载气为N2,气化室与检测其温度均为250 ℃,进样0.2 μL。
2 结果与讨论
2.1 产物的分析鉴定结果
粗品 9,10-环亚甲基假紫罗兰酮的合成经硅胶柱层析进行纯化,洗脱剂为石油醚∶乙酸乙酯体积比 20∶1,收集目标组分,进行浓缩干燥,即得较纯9,10-环亚甲基假紫罗兰酮。
2.1.1 产物的气相色谱分析结果
对产物进行气相色谱分析,面积归一法定量。实验结果显示保留时间为23.944 min和24.921 min,分别对应9,10-环亚甲基假紫罗兰酮的顺反异构体,峰面积之和达到76.2 %。
2.1.2 产物的红外分析结果
产物进行红外图谱分析,由图1显示3051 cm−1为烯烃中—CH2—的伸缩振动峰;2938 cm−1、2865 cm−1为烷烃中—CH3及—CH2—的伸缩振动峰;1686 cm−1与1667 cm−1处为受共轭影响的C=O的伸缩振动峰对应带;1630 cm−1、1588 cm−1为不饱和酮结构中C=C的伸缩振动峰;1453 cm−1、1361 cm−1为—CH2—及—CH3的不对称变形振动峰;1253 cm−1为叔丁基的骨架震动,1165 cm−1为—C—H面内弯曲振动,973 cm−1为多个不饱和 C=C上C—H 的变形振动峰;883 cm−1为环丙烷的变形振动。

图1 产物的红外图谱

图2 产物的质谱图
2.1.3 产物的质谱分析结果
对所得产物进行气质联用分析,其中分子离子峰为 m/z=206,基峰为 m/z=55。主要离子碎片见图2。
2.2 单因素法中各因素对 9,10-环亚甲基假紫罗兰酮得率的影响
2.2.1 催化剂种类对得率的影响
催化剂主要采用不同种类的锌卡宾催化剂,在此基础上对活化锌粉、锌铜偶以及二乙基锌对实验的影响分别作了探讨,实验过程中发现,活化锌粉对反应几乎没有催化作用,因此针对价格较低的锌铜偶以及催化活性较高的二乙基锌分别进行了单因素试验。
2.2.2 溶剂种类对得率的影响
针对不同的催化剂锌铜偶及二乙基锌溶液,选择四氢呋喃、乙醚、二氯甲烷及 1,2-二氯乙烷同时进行实验。锌铜偶催化体系的反应条件为:n (假紫罗兰酮)∶n (二碘甲烷)∶n (锌铜偶) = 1∶1∶4,滴加时间1 h,冰浴时间4 h,冰浴反应温度−5 ℃,缓慢升至回流温度后反应4 h,采用不同溶剂进行反应,原料假紫罗兰酮在溶剂中的摩尔浓度为 0.2 mol/L 。二乙基锌催化体系的反应条件为:n (假紫罗兰酮)∶n (二碘甲烷)∶n (二乙基锌) = 1∶1∶1,滴加时间1 h,冰浴时间2 h,冰浴反应温度−5 ℃,回流时间2 h,原料假紫罗兰酮在溶剂中的摩尔浓度为0.2 mol/L。反应结果见图3。
如图3所示,可知锌铜偶与二乙基锌催化体系在醚类溶剂四氢呋喃及乙醚中反应的得率明显低于在卤代烷烃类溶剂中的得率,而其中二氯甲烷溶剂最利于反应的进行,同时可以看出利用方法Ⅰ制备的锌铜偶催化剂的催化效果不如方法Ⅱ的催化效果理想。就得率来看,二乙基锌在二氯甲烷中的得率明显高于锌铜偶催化剂的得率,且用量少,反应时间短,但考虑到二乙基锌价格昂贵,因此锌铜偶同时作为后续实验的催化剂,达到同二乙基锌作比较的目的。
2.2.3 催化剂用量对得率的影响
锌铜偶Ⅱ催化体系的反应条件为:溶剂选取二氯甲烷,假紫罗兰酮在溶剂中的浓度为0.2 mol/L,原料滴加时间 1 h,冰浴时间 4 h,冰浴反应温度−5 ℃,缓慢升至回流温度后反应4 h。二乙基锌催化体系的反应条件为:溶剂选取二氯甲烷,假紫罗兰酮在溶剂中的摩尔浓度为0.2 mol/L,原料滴加时间1 h,冰浴时间2 h,冰浴反应温度−5 ℃,回流时间2 h。所得结果如表1所示。
由表1可知,随着催化剂用量的增加,锌铜偶Ⅱ与二乙基锌催化体系的得率均呈增加趋势,但锌铜偶Ⅱ的催化反应得率整体偏低,且在n (假紫罗兰酮)∶n (二碘甲烷)∶n (锌铜偶Ⅱ) = 1∶1∶4 时达到最大值。二乙基锌反应体系在 n (假紫罗兰酮)∶n(二碘甲烷)∶n (二乙基锌) = 2∶2∶1 至 1∶1∶1 的过程中有一个骤升现象,当催化剂用量低于该比例时,产物得率极低,而当高于该比例时,产物的得率亦没有明显的升高。故选择该条件进行后续反应,此时产物得率为48.8 %。
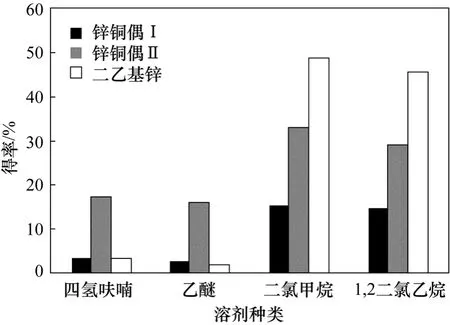
图3 溶剂种类对得率的影响

表1 催化剂用量之比对得率的影响
2.2.4 冰浴时间对得率的影响
锌铜偶Ⅱ催化体系的反应条件为:n (假紫罗兰酮)∶n (二碘甲烷)∶n (锌铜偶Ⅱ) = 1∶1∶4,滴加时间1 h,冰浴反应温度−5 ℃,回流时间4 h,溶剂二氯甲烷,且假紫罗兰酮在溶剂中的浓度为 0.2 mol/L。二乙基锌催化体系的反应条件为:n (假紫罗兰酮)∶n (二碘甲烷)∶n (二乙基锌) = 1∶1∶1,滴加时间1 h,冰浴反应温度−5 ℃,回流时间2 h,溶剂二氯甲烷,且假紫罗兰酮在溶剂中的摩尔浓度为0.2 mol/L。
由表2可知,随着冰浴时间的增加,两催化剂体系的得率均是先上升后下降,且反应过程中并无得率低于锌铜偶Ⅱ催化体系的情况,在该反应条件下,锌铜偶Ⅱ与二乙基锌催化体系分别在冰浴时间为6 h和4 h时达到最大得率,当冰浴时间再延长时,产物得率逐渐降低,可能是由于随着冰浴时间的延长,生成的副产物增加,导致目标产物得率下降。
2.2.5 回流时间对得率的影响
锌铜偶Ⅱ催化体系的反应条件为:n (假紫罗兰酮)∶n (二碘甲烷)∶n (锌铜偶Ⅱ) = 1∶1∶4,滴加时间1 h,冰浴时间6 h,冰浴反应温度−5 ℃,溶剂二氯甲烷,且假紫罗兰酮在溶剂中的摩尔浓度为0.2 mol/L。二乙基锌催化体系的反应条件为:n (假紫罗兰酮)∶n (二碘甲烷)∶n (二乙基锌) = 1∶1∶1,滴加时间1 h,冰浴时间4 h,冰浴反应温度−5 ℃,溶剂二氯甲烷,且假紫罗兰酮在溶剂中的摩尔浓度为0.2 mol/L。
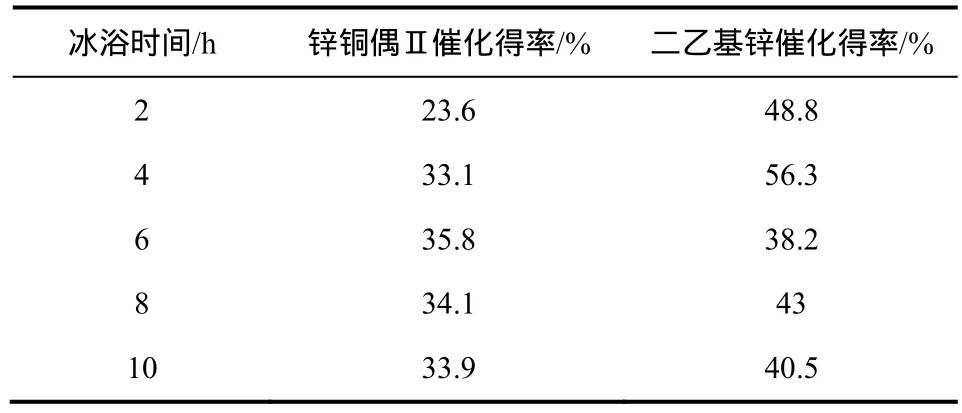
表2 冰浴时间对得率的影响
由表3可知,随着回流时间的增加,二乙基锌催化体系得率呈现先上升后下降的趋势,锌铜偶Ⅱ体系得率趋势则为上升后基本不变,且二乙基锌催化体系得率一直维持在高于锌铜偶Ⅱ催化体系的水平。二乙基锌催化得率在回流4 h达到最大值,为70.5 %;而锌铜偶Ⅱ催化得率在回流6 h时达到最高,为38.4。可见二乙基锌催化效果明显比锌铜偶Ⅱ的催化效果要好,因此,为探索9,10-环亚甲基假紫罗兰酮的最高得率,在后续的响应面法中采用二乙基锌作为催化剂。

表3 回流时间对得率的影响
2.2.6 原料在溶剂中的浓度对得率的影响
总结上述实验条件,使得锌铜偶Ⅱ催化体系的反应条件为:n (假紫罗兰酮)∶n (二碘甲烷)∶n (锌铜偶Ⅱ) = 1∶1∶4,滴加时间1 h,冰浴时间6 h,回流时间6 h,冰浴反应温度−5 ℃,溶剂选取二氯甲烷,探索原料在溶剂中的摩尔浓度对产物得率的影响,从图4中可以看出,原料在溶剂中的浓度对产物得率的影响非常小,不同溶剂用量情况下得率几乎没有变化。其它溶剂用量情况下,变化范围不超过0.49 %,因此可以判定原料在溶剂中的浓度对该反应的得率影响不大。
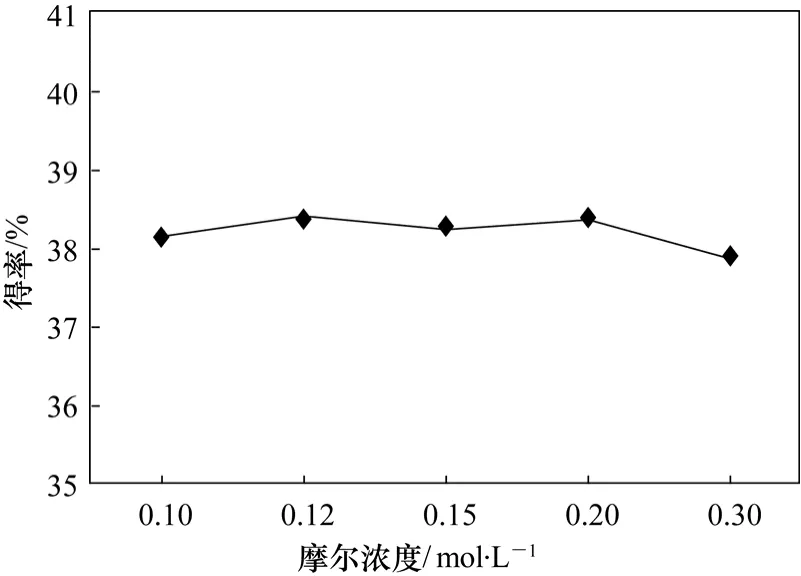
图4 原料在溶剂中的摩尔浓度对得率的影响
为探讨最高得率及最佳工艺条件,在此基础上,选择二乙基锌为进一步探索 9,10-环亚甲基假紫罗兰酮最高得率的催化剂,采用响应面法进行实验。
2.3 响应面法探讨 9,10-环亚甲基假紫罗兰酮的合成工艺
采用响应面法中的Box-Behnken Design(BBC)优化实验设计方法,以二乙基锌催化剂单因素试验为基础,选择三因素三水平实验设计对催化剂用量,冰浴时间和回流时间进行响应面优化。所选择实验因素水平如表4。

表4 实验因素水平及编码
根据Box-Behnken设计方案及实验实际结果拟合情况以及方差分析结果,选择对响应值显著的各项,可得二次回归方程,如式(2)。

根据回归分析结果,作出相应等高线图及曲面图,见图5、图6。
图5、图6中左起分别是冰浴时间与催化剂用量、回流时间与催化剂用量以及回流时间与冰浴时间对产物得率的交互影响的等高线图和曲面图。从图中可知 9,10-环亚甲基假紫罗兰酮的得率随着催化剂用量和冰浴时间、回流时间的延长出现先上升后下降的趋势,且冰浴时间较之回流时间对得率的影响要更为显著,交互作用明显,各因素并不呈现单一的线性关系,且所取范围存在极值点,可取得最大值。由此可知对产物得率影响的显著性为催化剂用量(X1)> 冰浴时间(X2)> 回流时间(X3)。
通过响应面分析工具可得到最大响应值,与之对应的 9,10-环亚甲基假紫罗兰酮的最佳合成工艺为:催化剂用量为 n (假性紫罗兰酮)∶n (二碘甲烷)∶n (二乙基锌) = 1∶1∶1.8,冰浴时间4.7 h,回流时间5.2 h,预测得率为78.9 %。
2.4 稳定性试验
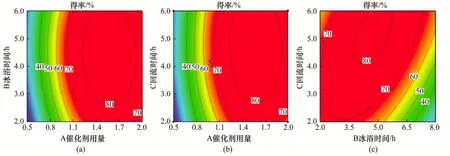
图5 响应面法优化产物得率的等高线图

图6 响应面法优化产物得率的曲面图
为验证响应面法对最佳合成工艺预测的可行性,采用模拟得到的最佳工艺,同时考虑到反应体系的不稳定性,分别进行了3次重复性实验,3次实验的得率分别为76.2 %、75.8 %、77.9 %,与理论值相差不大,因此,采用响应面法得到的最佳合成工艺是可以用来对真实实验就行模拟的,具有实用价值。
3 结 论
(1)以假性紫罗兰酮和二碘甲烷为原料,经Simmons-Smith反应合成 9,10-环亚甲基假紫罗兰酮,采用FT-IR、GC、GC-MS等手段对产物进行了表征,证实了产物结构。
(2)以单因素实验为基础,通过响应面法确定最佳工艺条件为催化剂用量n (假性紫罗兰酮) ∶n(二碘甲烷)∶n(二乙基锌)= 1∶1∶1.8,冰浴时间4.7 h,回流时间5.2 h,冰浴反应温度−5 ℃,反应溶剂选取二氯甲烷,且假紫罗兰酮在溶剂中的浓度为0.2 mol/L,该条件下产物 9,10-环亚甲基假紫罗兰酮得率为76.2 %。
[1]张承曾,汪清如. 日用调香术[M]. 北京:轻工业出版社,1989:104.
[2]Chapuis C, Brauehi R. Preparation of active flowery and woody-like odorant ketones via corey-chaykovsky oxiranylation. irones and analogues[J]. Helv. Chim. Acta,1993,76(5):2070-2088.
[3]陈学恒. 我国天然柠檬醛的利用及鸢尾的合成进展[J]. 现代化工,2002,22(7):8-12.
[4]黄绍华,温辉梁,刘崇波,等. 由山苍子油合成假性紫罗兰酮的相转移催化研究[J]. 天然产物研究与开发,1993,5(3):21-25.
[5]刘晓庚,陈学恒,桂衍胜,等. 鸢尾酮的合成路线研究[J]. 江西农业大学学报,1999,21(1):124-127.
[6]Schinz H,Ruzicka L,Seidel C F,et al. Synthesis de la,Q-2-irone[J].Helv. Chem. Acta,1947,30(2):1810-1814.
[7]Leo A Paquette,Wang Tingzhong, Emmanuel Pinard. Total synthesis of natural (+)-acetoxycrenulide[J]. J. Am. Chem. Soc.,1995,117(4):1455–1456.
[8]Torii S,Uneyame K,Matsunami S. Steroselective synthesis of(±)-irone[J]. J .Org. Chem.,1980,45:16-20.
[9]张玮,雷阿旺,赵志利. 固体碱催化合成假性紫罗兰酮研究[J]. 广州化工,2010,38(5):157-162.
[10]王保芢. 有机合成反应[M]. 北京:科学出版社,1985:388-389.

