晶粒度对铜点蚀行为的影响
李 珂,张 平,刘慧娟,周琼宇,钟庆东
(1.上海大学 上海市现代冶金与材料制备重点试验室,上海200072;2.四川省电力公司 遂宁公司,遂宁629000)
铜及其合金是一种重要的功能性材料。它们由于具有优良的导电性、导热性和良好的耐腐蚀性能,被广泛应用于电气、机械制造工业和电子行业等领域[1]。对铜及其合金的腐蚀机理和防护技术的研究一直是人们研究的热点问题[2]。
大量研究表明,在铜及其合金的使用过程中难以避免被温度、机械形变等外界环境所影响,这些都将改变铜的晶体状态[3-9]。这些晶体状态的改变不仅会影响铜的机械性能,而且还将影响铜的耐蚀性能。Shi[10-12]等研究了晶粒在纳米尺度下的铜在NaOH、氨等碱性环境中的腐蚀行为,Alain[13]等研究了形变对晶粒改变在0.5mol·L-1H2SO4环境中的腐蚀行为。上述研究结果均表明晶粒状态的改变会对铜表面氧化过程特别是初期的Cu2O形成产生明显的影响。一般情况下,铜及其合金表面能生产钝态或半钝态的保护薄膜,使多种腐蚀受到抑制,其腐蚀类型主要为均匀腐蚀[14-15]。但在工业应用中往往存在许多含SO42-,CO32-离子的硬质水,铜在这些环境中往往会发生点蚀这种破坏性极强而且程度难以预测的腐蚀[16]。
因此,本工作综合考虑到许多关于工业应用过程对铜晶体状态产生不可避免的影响及大量关于SO42-等离子对铜合金构件腐蚀的案例,系统研究了晶粒度对铜点蚀行为的影响。
1 试验
1.1 不同晶粒度铜试样制备
试验采用质量分数为99.95%的无氧高导电性紫铜。将其在氢气环境中退火,退火温度分别为200,600,1 000 ℃,保 温 时 间 为 2h。并采用DM2500M-莱卡金相显微镜对其晶粒度进行表征,结果见图1。
由图1可见,所制备的铜试样平均晶粒度分别为23,67,470μm。

图1 不同退火温度下铜试样表面的金相照片
1.2 电化学测试
将不同晶粒度的铜试样切割成10mm×10mm×10mm的块状试样,其工作面积为1cm2,其余表面用环氧树脂密封。试样表面用水磨砂纸逐级打磨至2 000号并用抛光剂抛光后,用去离子水和丙酮超声清洗。
试验所用溶液体系分别为0.1mol·L-1Na2SO4+0.01mol·L-1NaHCO3溶液、0.1mol·L-1NaOH 溶 液 和 0.1mol·L-1Na2SO4+0.1mol·L-1NaOH溶液。所有溶液皆采用分析纯试剂和去离子水配制而成。
电化学试验在CH1660C型电化学工作站上进行,采用三电极体系。参比电极为饱和甘汞电极(SCE),辅助电极为铂电极,文中电位均为相对SCE。极化曲线的电位扫描速率为5mV·s-1,电位扫描范围-300~1 200mV,再回扫到-200mV。电化学阻抗谱测量在开路电位下进行,其频率范围为100.0kHz~0.01Hz,测量信号的幅值为5mV。以上电化学测试均在室温25℃下进行。最后采用JSM-6700F型扫描电子显微镜(日本JEOL公司)对试样表面腐蚀后的形貌进行观察。
2 结果与讨论
2.1 铜在不同溶液中的点蚀特征
图2为晶粒度为23μm的铜试样在三种溶液中的极化曲线。图3为循环极化测试后所对应的电极表面形貌。由图2(a)可见,曲线表现为典型的活性溶解型点蚀的极化曲线,当电极电位正向扫描时,铜的腐蚀电位为-0.14V,在大于腐蚀电位的阳极区域,电流密度随着电位升高迅速增大,发生阳极溶解。同时,在回扫的过程中,相同电位下的回扫电流密度大于正扫电流密度。这种现象是因为阳极溶解造成点蚀时点蚀坑内由于自催化效应使得阴离子聚集,从而进一步促进金属离子的溶解,造成回扫电流密度大于正扫电流密度[11,16]。由图3(a)可见,电极表面具有细密的点蚀坑,点蚀坑较深且坑内无腐蚀产物堆积。
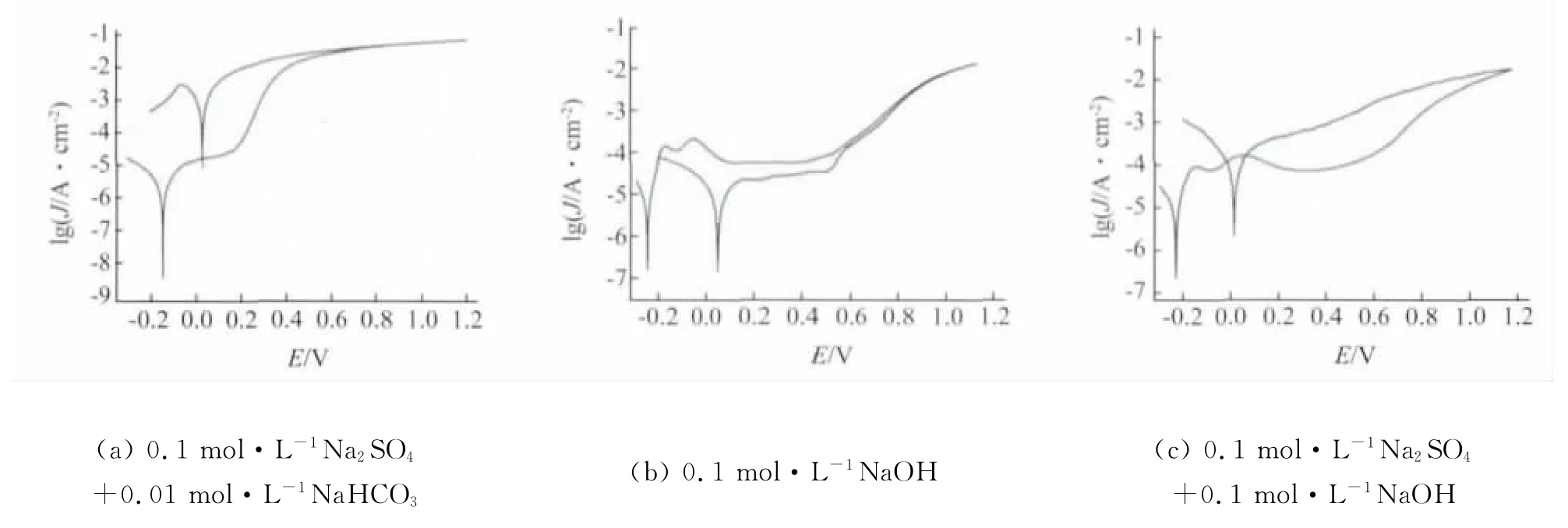
图2 晶粒度为23μm的试样在不同溶液中的极化曲线
图2 (b)为典型的可修复型钝化膜的极化曲线。在0.15~0.55V的电位区间内,电流密度维持相对稳定,表现出钝化区的特征,电位继续正扫后进入过钝区。在回扫过程中,相同电位下的回扫电流密度小于正扫电流密度,而且回扫电流密度在维钝区内相对稳定,表现出很强的自修复能力,使电位超过过钝区时对钝化膜层的破坏得以修复。从图3(b)中可以看出对应的电极表面未发生点蚀,仍然如测试前一样平整,但是电极表面色泽变暗,表明铜在0.1mol·L-1NaOH溶液中极化后电极表层覆盖着具有保护性的钝化膜。
图2(c)为典型的钝化膜破裂型点蚀的极化曲线。当电极电位正向扫描时,铜的腐蚀电位为-0.23V,在大于腐蚀电位的阳极区域,电流密度维持相对稳定,表现出明显的钝化特征。电位增大到0.6V后,电流密度迅速增大,进入膜破裂的过钝化区。电位回扫过程中,电流密度大于正扫电流密度。表明破坏的钝化膜层不能得到很好的修复。测试后观察发现细小腐蚀产物覆盖电极表面。从图3(c)中可以看出电极表面发生了点蚀,点蚀坑较大但是深度极浅,点蚀坑四周堆积了少量卷曲的腐蚀产物,并且产物与铜基体结合良好。而在其他部位则无腐蚀产物附着,表明在此溶液体系中,所发生的点蚀为表面钝化膜层局部破裂而引起的点蚀。通过图3(c)可进一步验证图2(c)所示表面覆盖着一层具有保护性的钝化膜层。

图3 晶粒极为23μm的试样在不同溶液中极化曲线测试后表面形貌
2.2 铜晶粒度对铜极化行为的影响
图4 为不同晶粒度铜试样在3种溶液中的极化曲线。如图4(a)所示,不同晶粒度铜试样在0.1mol·L-1Na2SO4+0.01mol·L-1NaHCO3溶液均表现出活性溶解型点蚀。正扫过程中,不同晶粒度试样的腐蚀电位和腐蚀电流密度基本一致。但是电位超过腐蚀电位后,随着电位增加,不同晶粒度试样的腐蚀电流密度不再一致。随着晶粒度的增大,曲线由回扫电流与正扫电流所形成的滞后环逐渐减小。该滞后环可以代表点蚀的敏感性,环面积越大,点蚀坑内的自催化效应越强,点蚀越容易发生,即晶粒度越小,点蚀敏感性越强,点蚀越容易发生。这主要是因为晶粒度越小,晶界越多,更多的微电池将在晶界和晶体间形成,同时晶界处往往具有更多的电化学反应高活性区,这将大大提高阳极溶解的反应动力学,在此体系中主要表现为点蚀敏感性增强。

图4 不同晶粒度铜电极在3种溶液中的极化曲线
由图4(b)可见,不同晶粒度铜试样表面钝化膜层在此溶液中均有良好的自修复能力。而且随着晶粒度增大,表面钝化膜层的钝化性能越好,所形成的钝化膜保护性能越强。由图4(c)可见,不同晶粒度铜试样均表现出钝化膜破裂型点蚀的曲线特征。随着铜试样晶粒度增大,回扫电流密度与正扫电流密度所形成的滞后环逐渐增大,表面对应的点蚀敏感性增强。从图2(b)中可知,钝化膜层破坏发生在钝化膜表面,与钝化膜的性质直接相关。因此,晶粒度对钝化膜破裂型点蚀的影响主要表现为对钝化膜形成过程的影响。以往的研究均表明[17-18],铜晶粒越小,越有利于在电极表面快速形成一层具有保护性能的钝化膜。因而在0.1mol·L-1Na2SO4+0.1mol·L-1NaOH 溶液体系中,晶粒度越小,钝化性能越好,其点蚀敏感性越小。
2.3 腐蚀后铜试样表面的电化学阻抗谱
图5为不同晶粒度铜电极在3种溶液体系中循环极化后的电化学阻抗谱。由图5(a)可见,铜电极晶粒度越小,活性溶解点蚀发生后电极界面阻抗值越小。表明晶粒度越小,其电极界面的点蚀发生越严重。图5反映了活性溶解型点蚀后界面状况,在1Hz和1kHz扫描频率下分别有两个时间常数,分别体现了电极反应和活性溶解点蚀坑所引起电极表面电流不均匀分布的时间常数[19]。从图中可以看出。图5(b)为铜电极在0.1mol·L-1Na2SO4+0.1mol·L-1NaOH 溶液中 所测 Nyquist图和Bode图。可以看出,晶粒度越小,阻抗值越大。从1Hz~1kHz的频率范围内出现近似水平部分,表明体系主要表现为电容性,这是由于基体表面所覆盖的钝化膜在中频区表现出半导体膜层特性[20]。图5(c)为铜电极发生膜破裂型点蚀后的界面状况。铜电极晶粒度越小,其阻抗值越大,表明电极表面所发生点蚀越不严重,而因为膜层的破坏,相角在中频区不再体现出钝化膜的半导体特征,因此只有一个有电极反应所引起的时间常数存在。
3 结论
(1)溶液体系中含有SO42-/HCO3-将导致铜发生活性溶解型点蚀;晶粒度减小,晶界数量增多将增加铜的活性溶解型点蚀敏感性,点蚀发生后界面阻抗随着晶粒减小而逐渐减小。
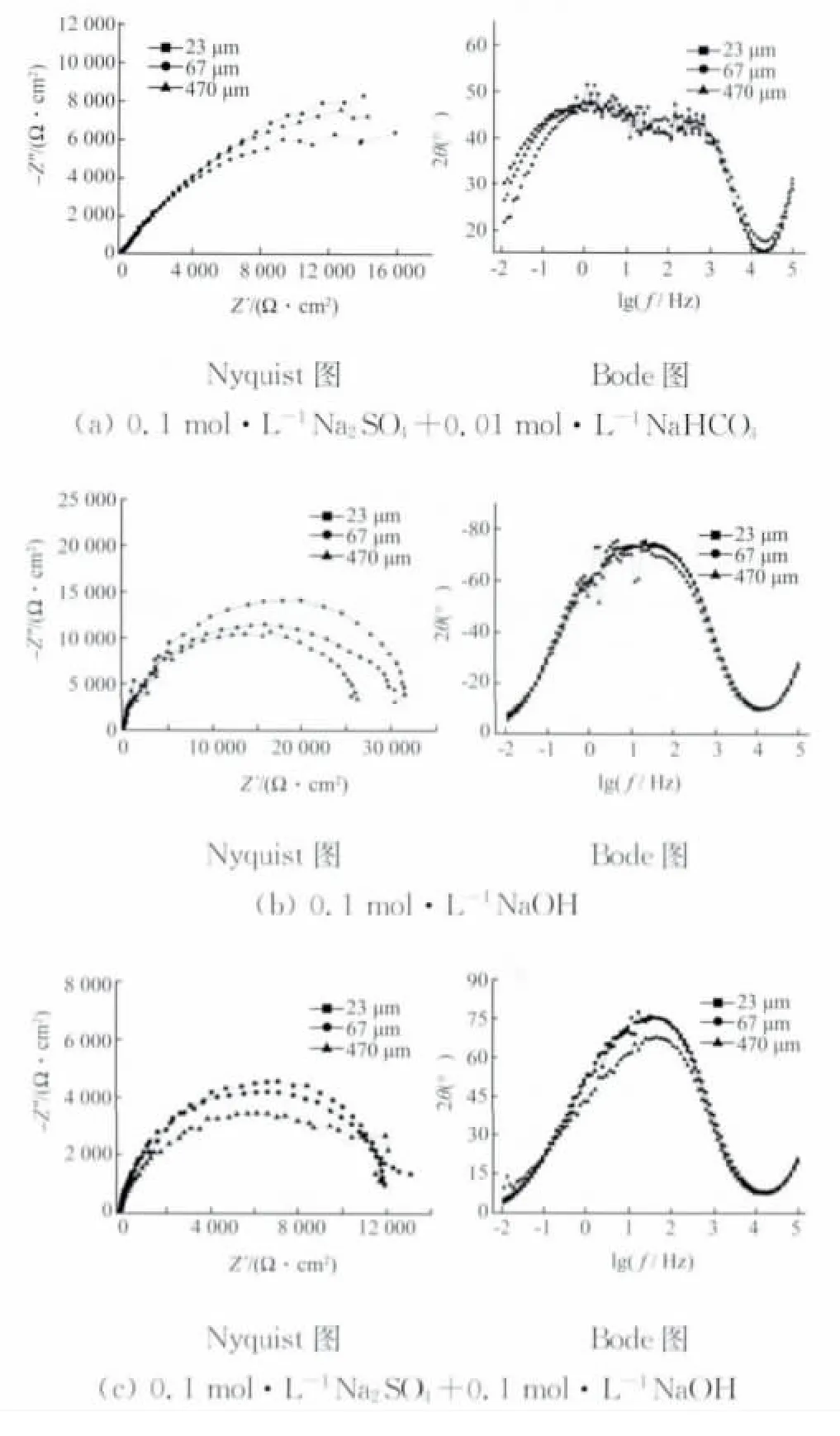
图5 不同晶粒度铜电极在3种不同溶液体系中循环极化后的电化学阻抗谱
(2)在含OH-的碱性环境中,铜具有良好的钝化性能,所形成的钝化膜层具有良好的自修复性能。晶粒度减小将促进铜在快速形成具有保护性的钝化膜层,膜层电化学阻抗增加。
(3)SO42-将导致铜在碱性环境中发生钝化膜破裂型点蚀;晶粒度减小,表面钝化膜层破裂发生点蚀的几率减小。
[1]刘平,田保红,赵冬梅.铜合金功能材料[M].北京:科学出版社,2004.
[2]雷惊雷,李凌杰,蔡生民,等.弱碱性介质中氯离子对铜电极腐蚀行为的影响[J].物理化学学报,2001,17(12):1107-1111.
[3]Yin S B,Li D Y.Effects of prior cold work on corrosion and corrosive wear of copper in HNO3and NaCl solutions[J].Materials Science and Engineering,2005,394(1/2):266-276.
[4]Li W,Li D Y.Variations of work function and corrosion behaviors of deformed copper surfaces[J].Applied Surface Science,2005,240(1/4):388-395.
[5]Guo W Y,Sun J,Wu J S.Effect of deformation on corrosion behavior of Ti-23Nb-0.7Ta-2Zr-O alloy[J].Materials Characterization,2009,60(3):173-177.
[6]Zhang X,Boelen B,Beentyes P,et al.Influence of uniaxial deformation on the corrosion behavior of precoated packaging steel[J].Progress in Organic Coatings,2007,60(4):335-342.
[7]Harandi S E,Idris M H,Jafari H.Effect of forging process on microstructure,mechanical and corrosion properties of biodegradable Mg-Ca alloy[J].Materials and Design,2011,32(5):2596-2603.
[8]Gao K W,Liu M Y,Zou F L,et al.Characterization of microstructure evolution after severe plastic deformation of pure copper with continuous columnar crystals[J].Materials Science and Engineering,2010,527(18/19):4750-4757.
[9]Chen J,Yan W,Li W,et al.Texture evolution and its simulation of cold drawing copper wires produced by continuous casting,Trans[J].Transactions of Nonferrous Metals Society of China,2011,21(1):152-158.
[10]Yu B,Woo P,Erb U.Corrosion behaviour of nanocrystalline copper foil in sodium hydroxide solution[J].Scripta Materialia,2007,56(5):353-356.
[11]Luo W,Xu Y M,Wang Q M,et al.Effect of grain size on corrosion of nanocrystalline copper in NaOH solution[J].Corrosion Science,2010,52(10):3509-3513.
[12]Shi P Z,Wang Q M,Xu Y M,et al.Corrosion behavior of bulk nanocrystalline copper in ammonia solution[J].Materials Letters,2011,65(5):857-859.
[13]Robin A,Aristides G,Martinez S,et al.Effect of cold-working process on corrosion behavior of copper[J].Materials and Design,2012,34:319-324.
[14]徐群杰,朱律均,齐航,等.Cu的腐蚀与缓蚀的光电化学研究[J].金属学报,2008,44(11):1360-1365.
[15]丁杰,林海潮,曹楚南.HSn70-1B铜管在碱性 NaCl溶液中的腐蚀行为[J].腐蚀科学与防护技术,2002,14(2):67-72.
[16]王长罡,董俊华,柯伟,等.HCO3- 和SO42- 对 Cu点蚀行为的影响[J].金属学报,2012,48(1):85-93.
[17]Wang L P,Zhang J Y,Gao Y,et al.Grain size effect in corrosion behavior of electrodeposited nanocrystalline Ni coatings in alkaline solution[J].Scripta Materialia,2006,55(7):657-660.
[18]Lu G J,Zangari G.Corrosion resistance of ternary Ni-P based alloys in sulfuric acid solutions[J].Electrochimica Acta,2002,47(18):2969-2979.
[19]Cruz R P V,Nishikata A,Tsuru T.AC impedance monitoring of pitting corrosion of stainless steel under a wet-dry cyclic condition in chloride-containing environment[J].Corrosion Science,1996,38(8):1397-1406.
[20]Wu H Y,Wang Yi,Zhong Q D,et al.The semiconductor property and corrosion resistance of passive film on electroplated Ni and Cu-Ni alloys[J].Journal of Electroanalytical Chemistry,2011,663(2):59-66.

