缩聚反应相对分子质量的控制与计算
张道洪 程新建 李廷成 张爱清
(中南民族大学化学与材料科学学院 湖北武汉 430074)
高分子化学作为高分子材料与工程及其相关专业的专业基础课程,其知识的掌握程度对后续课程的学习至关重要[1]。高分子化学聚合物反应从机理上可分为连锁聚合和逐步聚合,连锁聚合主要包括烯烃的聚合,其工业投资大,适用于大规模的国有企业投资和生产;而逐步聚合主要涉及涂料树脂、胶黏剂、不饱和聚酯树脂等工业化产品,投资规模小、见效快,适用于中小型民营企业投资和生产[2-3]。本文将对缩聚反应中相对分子质量的控制和计算进行分析讨论。
1 缩聚反应相对分子质量的控制理论
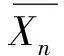
(1)
式中N0为体系中起始二元酸和二元醇的分子总数,N为t时刻聚酯分子数,p为t时刻官能团的反应程度。此公式的适用范围是2-体系、2-2体系等物质的量反应,反映的是两官能团等物质的量比时平均聚合度与反应程度的定量关系。因此,在某个反应阶段,只要测试(如通过红外光谱、核磁、化学滴定等分析手段)聚合体系的反应程度,就可以计算出聚合物的相对分子质量。在科研和工业上,难于让反应停留在某个反应时间,因为即使某时刻停止反应,倒出物料和降温的过程都需要时间,会导致部分聚合物的相对分子质量增加,相对分子质量分布变宽。因此,考虑官能团数之比来抑制反应程度和聚合物的相对分子质量是比较科学的,聚合反应进行到一定程度时,链端的官能团失去继续相互反应的能力,停止大分子链的增长。由此以二元酸(aAa)和二元醇(bBb)为例推导它们物质的量之比对聚合物相对分子质量的影响。
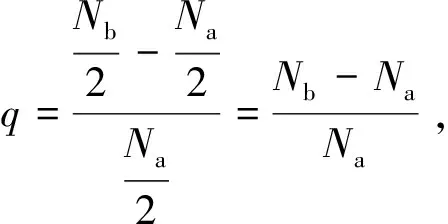
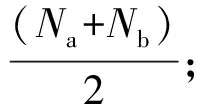
(2)
由式(2)可以看出,聚合物的相对分子质量最终取决于r或过量分率q和官能团的反应程度P。因此对于一个缩聚反应体系,只要确定r或q和反应程度P,就能计算出聚合物最终反应的理论平均聚合物,进而获得相对分子质量。对于具有不同2-2官能度体系来说,其r或q的计算至关重要,很多学生在计算过程中因理解不够而常常出现问题。下面用实例来进行分析。
2 缩聚反应相对分子质量的计算
对于2-2官能度体系的缩聚反应可以分为以下3类进行讨论[1]。
2.1 经典体系

2.2 端基封锁体系
对于端基封锁体系(aAa和bBb等物质的量体系,加入单官能团物质Cb′),单官能团物质Cb′一旦与增长的聚合物链反应,聚合物末端就被Cb′封住,不能再反应,因而使相对分子质量稳定(控制相对分子质量),因此单官能团物质称为黏度稳定剂或端基封锁剂。此体系与经典体系对比可看出,1mol的Cb′虽然只含有1mol的官能基团b,但所起的作用与1mol bBb(含2mol的官能基团b)相同。因此,在我们的教材中,q和r的表达式分别如下:
(3)
(4)
对于式(3)和式(4),很多学生对其中的“2”的理解不够透彻。实际上,我们根据过量分率q的定义,它是针对过量化合物的,对于这个体系,过量化合物是Cb′,它的表达式应为:

与式(4)一致。
2.3 综合体系
在综合体系(aRb体系,加入少量单官能团物质Cb′)中,基本只有一种aRb的体系,1mol的aRb实际上相当于经典体系的1mol aAa和1mol bBb的二聚体,同时由于加入了Cb′,又相当于端基封锁体系。因此这类体系实际上是前两种体系的综合,我们将它称为综合体系。
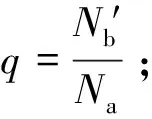
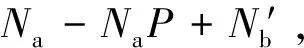
(5)
2.4 实例解析
下面通过实例来理解这3种体系的区别和相关性。
① 1mol的苯酐和1mol乙二醇进行缩聚反应,另加0.015mol的苯酐控制相对分子质量,问在乙二醇的反应程度达到0.999时的数均相对分子质量为多少?
对于这个例题,缩聚反应过程如图1所示:
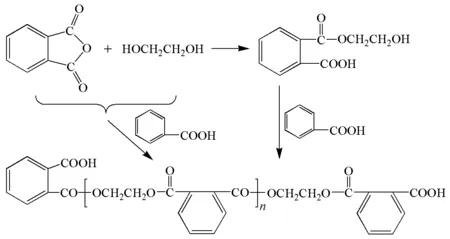
图1 缩聚反应示意图
此反应符合第一种经典反应体系,只要计算出r,代入式(2)即可获得平均聚合度,然后再乘以结构单元的平均相对分子质量。因此有:
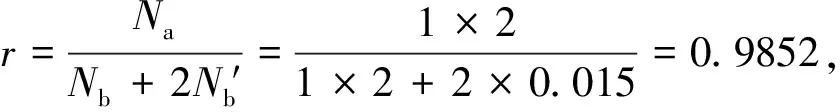
对比①和②可以看出,虽然过量的苯酐和苯甲酸均为0.015mol,但是过量的官能团不同,结果获得聚合物的相对分子质量是一样的,因此对于“端基封锁体系”的单官能团的Cb′物质来说,1mol的官能基团过量与bBb物质过量2mol官能基团的封端作用相同,这也证明了计算r或q时系数“2”的准确性。
③ 如果将②中的实例改为“1mol邻苯二甲酸乙二醇单酯进行缩聚反应,另加0.015mol的苯甲酸控制相对分子质量,问在乙二醇的反应程度达到0.999时的数均相对分子质量为多少?”。
此时的反应体系为综合体系,r的计算应为:
平均聚合度可用式(5)来计算:
此时的数均相对分子质量为:
此时的数均相对分子质量为:
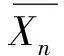
3 结论
参 考 文 献
[1] 潘祖仁.高分子化学.第4版.北京:化学工业出版社, 2010
[2] 黄美荣.大学化学,2001,16(2):35
[3] 陈远锋.化学工程与装备,2010(11):120

