阻塞性睡眠呼吸暂停综合征患者持续正压通气治疗后血清细胞因子的变化
李 蔚 江程澄 (重庆市中医院呼吸内科,重庆 400011)
阻塞性睡眠呼吸暂停综合征(OSAS)主要表现为口鼻腔气流停止,但是胸腹呼吸动作尚存在。该病可以累及多系统器官损害,是高血压、冠心病、心律失常、脑卒中等多种疾病的独立危险因素。本文拟探讨OSAS患者经持续正压通气(CPAP)治疗后血清因子的变化。
1 资料与方法
1.1 研究对象 我院2011年2月至2012年3月83例符合《睡眠呼吸暂停低通气综合征诊治指南》诊断的OSAS患者。根据呼吸睡眠暂停低通气指数(AHI)分为轻、中、重度组,AHI<5为轻度,15<AHI≤30为中度,AHI>30为重度,轻度组21例、中度组23例、重度组39例;其中男63例,女20例,平均年龄(46.64±8.22)岁,平均体质指数(BMI)(33.50±5.61)kg/m2。并选择同期我院体检中心体检的年龄、性别、体重指数相匹配的35例健康体检者为对照组。除外慢性肺部病变、冠心病、糖尿病、甲状腺疾病及脑血管疾病。排除烟酒史及饮咖啡和安眠药史。各组性别构成比、年龄和BMI差异无统计学意义(P>0.05)。见表1。
1.2 方法及内容 OSAS组应用美国伟康公司Alice5多导睡眠呼吸监测仪连续监测至少7 h,记录患者夜间脉搏血氧饱和度和心率、脑电图、眼电图、颌肌电图、双下肢肌电图、心电图、睡眠位置、胸腹起伏和鼻部气流情况。于晨起采集静脉血5 ml,离心15 min(3 000 r/min),分离血清,冷藏在-70℃冰箱中保存。并应用ELISA方法分批次测定肿瘤坏死因子(TNF)-α,白介素(IL)-8,人可溶性细胞间黏附分子1(sICAM-1)(试剂购自武汉博士德公司),核因子NF-κB(试剂购自基因美公司),操作时严格按照试剂盒说明进行。并于颈动脉分叉下1 cm处测颈动脉内膜中层厚度(IMT)。其中OSAS患者中度及重度组采用CPAP治疗,设定时间至少每晚8 h,压力选定以消除50% ~75%或以上的夜间睡眠呼吸暂停低通气次数,治疗3个月后,再次用相同方法进行睡眠监测,并比较治疗前后各指标的变化。
1.3 统计学方法 采用SPSS13.0软件,计量资料以±s表示;组间比较采用方差分析;多因素采用一般线性模型分析。
2 结果
2.1 治疗前各组观察指标比较 见表2。治疗前轻度组TNF-α、IL-8、IMT 明显高于对照组(P< 0.05);中度组 TNF-α、IL-8、IMT明显高于对照组、轻度组(P<0.05);重度组TNF-α、IL-8、IMT明显高于其他各组(P<0.05);治疗前中度组SICAM-1明显高于对照组和轻度组(P<0.05);重度组SICAM-1明显高于其他各组(P<0.05);治疗前轻、中度组NF-κB明显高于对照组(P<0.05);重度组NF-κB明显高于其他各组(P<0.05)。
表1 各组研究对象的一般情况比较(±s)
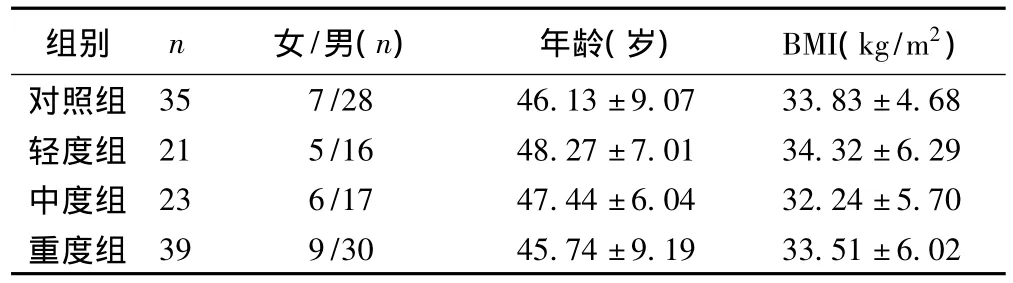
表1 各组研究对象的一般情况比较(±s)
组别 n 女/男(n) 年龄(岁) BMI(kg/m2)对照组35 7/28 46.13±9.07 33.83±4.68轻度组 21 5/16 48.27±7.01 34.32±6.29中度组 23 6/17 47.44±6.04 32.24±5.70重度组39 9/30 45.74±9.19 33.51±6.02
表2 各组治疗前 TNF-α、IL-8、sICAM-1、NF-κB 和 IMT 比较(±s)
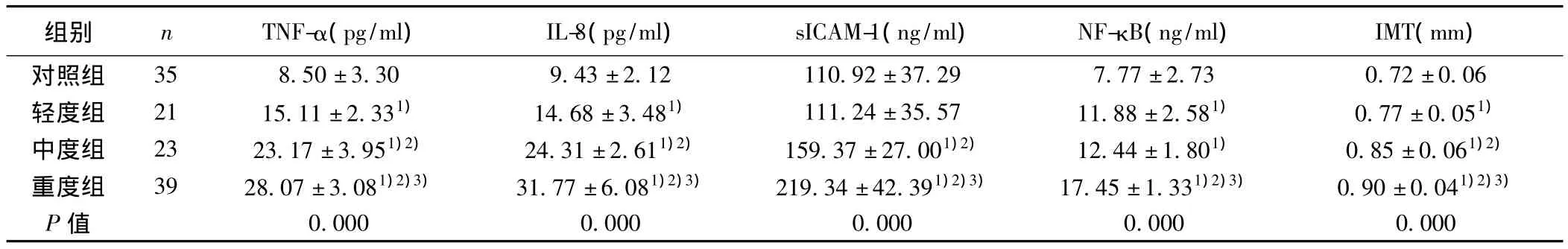
表2 各组治疗前 TNF-α、IL-8、sICAM-1、NF-κB 和 IMT 比较(±s)
与对照组比较:1)P<0.05;与轻度组比较:2)P<0.05;与中度组比较:3)P<0.05
组别 n TNF-α(pg/ml) IL-8(pg/ml) sICAM-1(ng/ml) NF-κB(ng/ml) IMT(mm)对照组 35 8.50±3.30 9.43±2.12 110.92±37.29 7.77±2.73 0.72±0.06轻度组 21 15.11±2.331) 14.68±3.481) 111.24±35.57 11.88±2.581) 0.77±0.051)中度组 23 23.17±3.951)2) 24.31±2.611)2) 159.37±27.001)2) 12.44±1.801) 0.85±0.061)2)重度组 39 28.07±3.081)2)3) 31.77±6.081)2)3) 219.34±42.391)2)3) 17.45±1.331)2)3) 0.90±0.041)2)3)P值0.000 0.000 0.000 0.000 0.000
2.2 CPAP治疗后中、重度组观察指标变化 分别以各观察指标为因变量,组别和治疗为处理因素进行方差分析,结果两组治疗后 TNF-α、IL-8、SICAM-1、NF-κB、IMT 均较治疗前明显降低(P<0.05)。见表3。
表3 CPAP 治疗前后中、重度组 TNF-α、IL-8、sICAM-1、NF-κB 和 IMT 比较(±s)
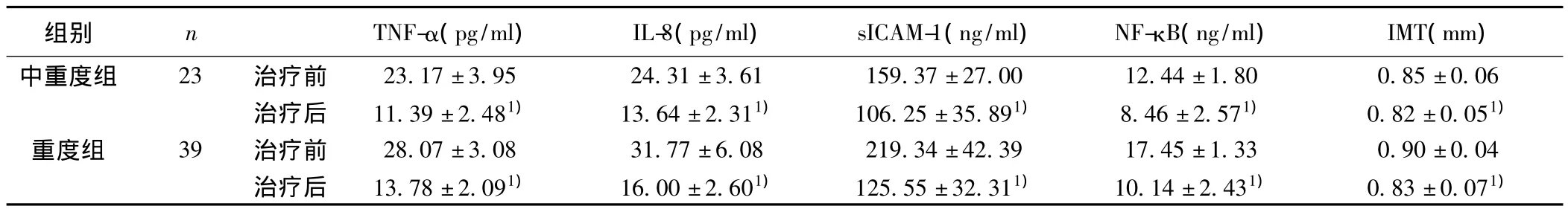
表3 CPAP 治疗前后中、重度组 TNF-α、IL-8、sICAM-1、NF-κB 和 IMT 比较(±s)
与治疗前比较:1)P<0.05
组别 n TNF-α(pg/ml) IL-8(pg/ml) sICAM-1(ng/ml) NF-κB(ng/ml) IMT(mm)中重度组 23 治疗前 23.17±3.95 24.31±3.61 159.37±27.00 12.44±1.80 0.85±0.06治疗后 11.39±2.481) 13.64±2.311) 106.25±35.891) 8.46±2.571) 0.82±0.051)重度组 39 治疗前 28.07±3.08 31.77±6.08 219.34±42.39 17.45±1.33 0.90±0.04治疗后 13.78±2.091) 16.00±2.601) 125.55±32.311) 10.14±2.431) 0.83±0.071)
3 讨论
OSAS是指夜间睡眠过程中呼吸暂停在10 s以上,而且反复发作,AHI≥5次/h,低通气是指呼吸较基础水平降低50%以上,同时血氧饱和度下降,伴有嗜睡等临床症状。打鼾是OSAS的特征性表现,鼾音量大,声响,且不规则,时有间断;OSAS患者表现为日间发生困倦或嗜睡感,患者可立即入睡;当呼吸暂停发生时,患者可能惊醒,突然坐起,大汗淋漓,甚至有濒死感;患者还可伴有夜间遗尿症、头痛、急躁、压抑、精神错乱、幻觉、极度敏感、敌视、智力和记忆力减退以及性功能障碍等,严重者可伴发心血管系统和其他重要生命器官的疾病表现〔1〕,OSAS可以大大增加心血管负性事件的发生率〔2,3〕,3项大型前瞻性群组研究表明,OSAS是全死因中的一个独立的危险因素〔4~6〕,如果不进行治疗,还会增加系统性炎症,血管内皮功能障碍,血小板活化和其他心血管负性事件的发生,比如心律失常,特别是心房颤动、冠状动脉疾病、无症状早期动脉粥样硬化、脑梗死〔7〕,一些研究表明OSAS的严重程度与IMT和血氧不足明显相关,其相关程度要高于阻塞事件的发生频率〔8,9〕。OSAS会导致身体内活性氧自由基(ROS)的增加,而过多的活性氧自由基又会促使发生氧化应激,这将进一步导致细胞结构,包括脂肪、细胞膜、蛋白质和DNA的损坏〔10〕,氧化应激还会导致免疫系统产生一连串的事件,如触发炎症,增加交感神经紧张,血管内皮功能障碍,代谢改变,和(或)增加血小板聚集等〔11,12〕。在某种程度上,这种间歇性低氧诱导一个重复缺氧/复氧循环过程,十分类似于缺血再灌注损伤,通过促进生产ROS,激活全身炎症,最终损害血管内皮功能。除了感应系统性炎症和氧化应激,间歇性低氧等离子体水平的存在增加了内皮素〔13〕,有研究显示即使轻度的OSAS也与减少内皮依赖性血管舒张有关〔14〕,而且内皮功能障碍程度与OSAS的严重程度也明显相关〔15,16〕,许多信号通路蛋白质,包括 TNF-α、白细胞介素 IL-1,IL-6,NF-κB 等均参与和诱导内皮功能障碍〔17,18〕,细胞内皮功能障碍可以选择性激活促炎的 NF-κB转录因子〔19〕,而 NF-κB可能会进一步刺激产生的促炎介质,例如细胞间黏附分子〔18〕,有报道显示,TNF-α水平与OSAS患者过多的日间睡眠时间明显正相关,而且IL-8水平也明显高于正常人〔20〕,以上研究结果与本文结果基本一致。CAPA一直作为治疗OSAS的首选方法〔21〕,可以改善睡眠结构,减少主观白天过度嗜睡和逆转其他已有的症状,还可以预防血氧不足,改善氧化损伤、减少氧化应激,抑制和改善已经发生的不各种不良后果〔22,23〕,一项随机对照试验研究表明,CPAP超过4个月可以大大减少患者颈动脉IMT以及严重的心血管事件的发生〔24〕。
1 Engleman HM,Douglas NJ.Sleepiness,cognitive function,and quality of life in obstructive sleep apnoea/hypopnoea syndrome〔J〕.Thorax,2004;59(7):618-22.
2 Marin JM,Carrizo SJ,Vicente E,et al.Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure:an observational study〔J〕.Lancet,2005;365(9464):1046-53.
3 Buchner NJ,Sanner BM,Borgel J,et al.Continuous positive airway pressure treatment of mild to moderate obstructive sleep apnea reduces cardiovascular risk〔J〕.Am J Respir Crit Care Med,2007;176(12):1274-80.
4 Young T,Finn L,Peppard PE,et al.Sleep disordered breathing and mortality:eighteen-year follow-up of the Wisconsin sleep cohort〔J〕.Sleep,2008;31(8):1071-8.
5 Marshall NS,Wong KK,Liu PY,et al.Sleep apnea as an independent risk factor for all-cause mortality:the Busselton Health Study〔J〕.Sleep,2008;31(8):1079-85.
6 Punjabi NM,Caffo BS,Goodwin JL,et al.Sleep-disordered breathing and mortality:a prospective cohort study〔J〕.PLoS Med,2009;6(8):e1000132.
7 Bradley TD,Floras JS.Obstructive sleep apnea and its cardiovascular consequences〔J〕.Lancet,2009;373(9657):82-93.
8 Suzuki T,Nakano H,Maekawa J,et al.Obstructive sleep apnea and carotid artery intima-media thickness〔J〕.Sleep,2004;27(1):129-33.
9 Schulz R,Seeger W,Fegbeutel C,et al.Changes in extracranial arteries in obstructive sleep apnoea〔J〕.Eur Respir J,2005;25(1):69-74.
10 Valko M,Leibfritz D,Moncol J,et al.Free radicals and antioxidants in normal physiological functions and human disease〔J〕.Int J Biochem Cell Biol,2007;39(1):44-84.
11 Greenberg H,Ye X,Wilson D,et al.Chronic intermittent hypoxia activates nuclear factor-kappa B in cardiovascular tissues in vivo〔J〕.Biochem Biophys Res Commun,2006;343(2):591-6.
12 Baldwin CM,Bootzin RR,Schwenke DC,et al.Antioxidant nutrient in-take and supplements as potential moderators of cognitive decline and cardiovascular disease in obstructive sleep apnea〔J〕.Sleep Med Rev,2005;9(6):459-76.
13 Kanagy NL,Walker BR,Nelin LD.Role of endothelin in intermittent hypoxia-induced hypertension〔J〕.Hypertension,2001;37(2 Part 2):511-5.
14 Duchna HW,Stoohs R,Guilleminault C,et al.Vascular endothelial dysfunction in patients with mild obstructive sleep apnea syndrome〔J〕.Wien Med Wochenschr,2006;156(21-22):596-604.
15 Trzepizur W,Gagnadoux F,Abraham P,et al.Microvascular endothelial function in obstructive sleep apnea:impact of continuous positive airway pressure and mandibular advancement〔J〕.Sleep Med,2009;10(7):746-52.
16 Priou P,Gagnadoux F,Tesse A,et al.Endothelial dysfunction and circulating microparticles from patients with obstructive sleep apnea〔J〕.Am J Pathol,2010;177(2):974-83.
17 Baguet JP,Barone-Rochette G,Pepin JL.Hypertension and obstructive sleep apnoea syndrome:current perspectives〔J〕.J Hum Hypertens,2009;23(7):431-43.
18 Kohler M,Stradling JR.Mechanisms of vascular damage in obstructive sleep apnea〔J〕.Nat Rev Cardiol,2010;7(2):677-85.
19 Ryan S,Taylor CT,McNicholas WT.Selective activation of inflammatory pathways by intermittent hypoxia in obstructive sleep apnea syndrome〔J〕.Circulation,2005;112(17):2660-7.
20 Ryan S,Taylor CT,McNicholas WT.Predictors of elevated nuclear factor-kappaB-dependent genes in obstructive sleep apnea syndrome〔J〕.Am J Respir Crit Care Med,2006;174(7):824-30.
21 Epstein LJ,Kristo D,Strollo PJ,et al.Clinical guideline for the evaluation,management and long-term care of obstructive sleep apnea in adults〔J〕.J Clin Sleep Med,2009;5(3):263-76.
22 Christou K,Kostikas K,Pastaka C,et al.Nasal continuous positive airway pressure treatment reduces systemic oxidative stress in patients with severe obstructive sleep apnea syndrome〔J〕.Sleep Med,2009;10(1):87-94.
23 Sharma SK,Agrawal S,Damodaran D,et al.CPAP for the metabolic syndrome in patients with obstructive sleep apnea〔J〕.N Engl J Med,2011;365(24):2277-86.
24 Drager LF,Bortolotto LA,Figueiredo AC,et al.Effects of continuous positive airway pressure on early signs of atherosclerosis in obstructive sleep apnea〔J〕.Am J Respir Crit Care Med,2007;176(7):706-12.

