神经危重症患者发生胃潴留相关危险因素及营养支持对预后的影响
金林梅, 孙 莉, 高 岚, 曹 杰
神经危重症患者多存在意识障碍、真性或假性球麻痹、肢体活动不灵、中枢性高热和并发感染等,影响患者进食,同时危重症患者机体处于高分解代谢状态,常常存在营养不良和营养风险,给予适当的营养支持尤为重要。目前有关学者们推荐,建议神经系统疾病伴有吞咽困难、意识障碍,有营养风险的危重症患者应尽早给予肠内营养支持,以降低危重症患者死亡和不良预后的发生率。但胃肠道的不耐受性,即胃肠动力障碍使肠内营养支持治疗在一定程度上受到限制。据文献[1]报道重症患者胃肠道不耐受性的发生率可达46%,尤其是经鼻胃管肠内营养期间发生胃肠不耐受的概率为56.3%[2]。因此能够实现早期肠内营养支持者不足50%[3],可耐受完全肠内营养患者不足20%[4,5]。为此本研究通过观察收住于我院神经内科重症监护病房(N-ICU)的危重症患者肠内营养支持治疗过程中胃潴留的发生情况,分析其相关危险因素及营养支持对预后的影响。
1 资料与方法
1.1 研究对象 选择自2012年7月 ~2013年2月在吉林大学白求恩第一临床医学院神经内科重症监护室住院患者,其中脑出血19例,脑梗死33例,颅内感染6例,癫痫持续状态5例,吉兰-巴雷综合征、脊髓病等其他疾病10例,共计73例。入选标准:诊断为神经系统疾病,Glasgow评分(Glasgow coma score,GCS)≤12分和/或 APACHE II评分 >16分;无法自主进食,需经鼻胃管实行肠内营养支持治疗;年龄在18岁以上。排除标准:年龄大于80岁;有消化系统器质性病变;严重心功能不全、肝肾功能障碍及内分泌疾病;住院时间少于1W。
1.2 实验分组 经鼻胃管行肠内营养的患者,总能量按20~25kCal/(kg·d)给予能量供应,4h抽吸1次胃腔残留量,根据残留量是否超过200ml,将患者分为胃潴留组和非胃潴留组,胃潴留组给予肠内、肠外联合营养支持,非胃潴留组给予全肠内营养支持。
1.3 观察内容 患者入院基本情况:包括患者的年龄、性别、现病史、既往史、GCS评分、血糖、感染等。现病史主要指患者的神经系统疾病诊断,既往史包括严重心功能不全、肝肾功能障碍及内分泌疾病,消化系统器质性病变,恶性肿瘤疾病等。患者的实验室检查:观察两组患者营养支持前后的前白蛋白、白蛋白、转铁蛋白、视黄醇结合蛋白和血红蛋白等血清蛋白指标的变化,及淋巴细胞、IgG、IgA、IgM、C3、C4等免疫指标变化。患者住院期间的诊疗:包括患者住院期间是否有机械通气、亚低温、镇静治疗,有无低血压等情况。
1.4 统计学处理 数据采用SPSS 19.0软件进行统计学处理,计数资料比较采用卡方检验,多因素分析采用logistic回归分析,计量资料采用 t检验,用±s表示,非正态分布的计量资料用秩和检验,P<0.05有统计学意义。
2 结果
2.1 入院时基本情况及相关化验比较 胃潴留组患者共25例,男14例,女11例;年龄为22~79岁,平均为 54.84±14.09岁。非胃潴留组患者共48例,男38例,女10例,年龄为25~80岁,平均为60.46±13.53岁。两组患者的年龄、性别比较,P>0.05差异均无统计学意义 (P值分别为 0.101、0.056),比较两组 GCS评分,P 值为 0.032,差异有统计学意义(见表1)。两组患者入院时的血糖、离子、感染、血清蛋白、免疫各指标水平比较,差异均无统计学意义 (P>0.05)。
2.2 胃潴留相关危险因素分析 目前临床观察到可能与发生胃潴留有关的危险因素包括性别、年龄、GCS评分分组、感染、离子紊乱、高血糖、是否使用机械通气、机械通气时间、亚低温、镇静治疗、低血压进行单因素分析,两组间比较无明显差异(P>0.05)。对各项行logistic回归分析,GCS评分分组(轻GCS 12~14分,中 GCS 9~11分,重 GCS≤8分)的 P 值为0.033(P <0.05,见表2),是发生胃潴留危险因素。
2.3 胃潴留与发病时间的关系 将发生胃潴留的患者距发病时间的分布,观察图1可知,距发病3w之内均可发生胃潴留,但在发病1w之内发生胃潴留的人数最多,达68%。
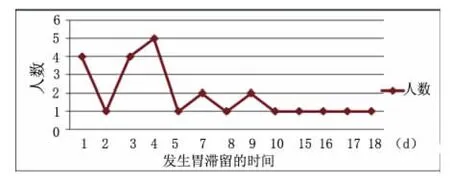
图1 发生胃潴留时间与人数
2.4 两组患者营养支持治疗后血清蛋白指标比较 两组患者经营养支持治疗1w后血红蛋白、白蛋白水平较营养支持前均显著降低(P<0.01);前白蛋白水平营养支持前后比较,均有所降低,但差异无统计学意义(P>0.05);视黄醇结合蛋白水平较营养支持治疗前升高,但无统计学意义(P>0.05);两组营养支持治疗1w后血清转铁蛋白水平均较治疗前有所下降,但胃潴留组患者的营养支持治疗1w前后比较差异有统计学意义(P<0.05),而非胃潴留组患者的前后差异无统计学意义(P>0.05)。两组间营养支持治疗1w、3w时的各血清白蛋白、前白蛋白、转铁蛋白、视黄醇结合蛋白和血红蛋白比较,均无明显差异(P>0.05)。
2.5 两组患者营养支持治疗后免疫指标水平比较 两组患者经营养支持治疗1w后较营养支持治疗前的免疫指标比较,淋巴细胞计数均减少,但差异无统计学意义(P>0.05);胃潴留组患者 IgG、IgA、IgM、C3、C4等指标前后比较均有所升高,但差异无统计学意义(P>0.05)。两组组间比较营养支持治疗1w时的各免疫指标,均无明显差异(P>0.05),但在营养支持治疗3w时,非胃潴留组的IgG(非胃潴留组16.16 ±4.71,胃潴留组9.55 ±1.66)、IgA(非胃潴留组 3.06 ± 0.43,胃潴留组1.85 ±0.42)水平高于胃潴留组,差异有统计学意义(P<0.05)。

表1 两组GCS评分比较
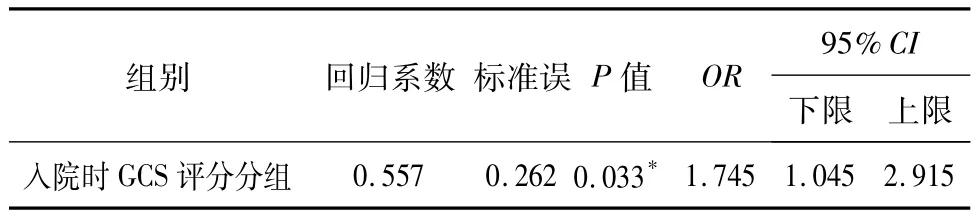
表2 GCS评分的回归分析
3 讨论
颅脑损伤后胃肠道动力障碍的发生机制尚不明确,目前有关研究认为颅脑损伤后经下丘脑-垂体-肾上腺轴、脑-肠肽、细胞因子和延髓迷走神经中枢途径[6]等对胃肠道的影响导致胃肠道蠕动减慢,发生胃潴留。
目前临床上客观判断肠内营养耐受性的方法多采用胃残留量(gastric residual volume,GRV)测定,但是GRV体积达到多少时应考虑存在肠内营养不耐受,并中止肠内营养的标准仍存有争议[7]。根据2006年由中华医学会重症医学分会推出的“危重患者营养支持指导意见”中指出:经鼻胃管营养的患者应密切观察胃腔残留量变化,为避免误吸的危险,通常需要每4h后抽吸1次胃腔残留量,潴留量<200ml时可维持原速度,潴留量<100ml时可增加输注速20m l/h;残留量≥200ml,则提示有胃潴留,应暂停输注或降低输注速度[8]。而在2011年“神经系统疾病肠内营养支持操作规范共识”中推荐,胃残留液>100ml时应用胃动力药物或暂停肠内营养[9]。我们在本次研究中采用胃残留量200ml为判定胃潴留的标准,进行试验分组。
3.1 神经危重症患者发生胃潴留的危险因素及时间 相关临床研究推测胃潴留的发生可能与患者的年龄、性别、GCS评分、感染、离子紊乱、高血糖,以及诊疗过程中是否使用机械通气、亚低温、镇静等治疗、有无低血压等因素有关[10,11]。我们的研究中对胃潴留组与非胃潴留组患者进行比较,发现患者的GCS评分越低发生胃潴留的可能性越大。张小鹏等[12]在严重脑损伤后急性上消化道病变的综述中指出当:颅脑损伤患者GCS评分<5分时,即出现胃排空明显延缓,胃内容物滞留及胃酸分泌增多等现象;Mutlu等在机械通气患者胃肠道并发症的预防和治疗的研究中总结:患者GCS评分越低,表明脑损伤越重,胃肠道相关并发症的发生率越高,GCS评分3~5分者胃潴留的发生率可达到46.43%,胃动力恢复慢,从而导致胃排空延迟出现胃潴留[13]。
本研究发现,神经危重症患者发病1w之内发生胃潴留的人数最多,之后胃潴留的发生率明显下降,这与患者发病时的应激反应关系密切。应激刺激交感神经兴奋,通过抑制胃肠神经丛的兴奋神经元而抑制胃动力,同时循环中释放增多的儿茶酚胺直接与胃平滑肌细胞膜上的α和β受体结合,抑制平滑肌细胞收缩,进而抑制胃肠道蠕动[6]。胃潴留在发病1w内发生率最高,与机体在急性期的应激反应最强烈有关。
3.2 肠内、肠外联合营养与全肠内营养后各营养指标比较 两组患者营养支持治疗1w后血清前白蛋白、白蛋白、血红蛋白较入院时比较均有降低,而视黄醇结合蛋白水平有所升高。这主要与其本身的半衰期时间长短差异有关,血清白蛋白的半衰期约为20d左右,故用于较短时间内的营养评价时敏感性差。转铁蛋白的半衰期8d,评价营养状况比白蛋白灵敏,但不能迅速反映营养治疗的效果。血清前白蛋白半衰期为1.9d,视黄醇蛋白的半衰期仅为12h,对饮食治疗反应迅速。此外我们的结果中半衰期短的血清前白蛋白不升反降,考虑因重症患者因意识障碍、卧床等原因并发的感染有关。在急性感染,尤其是细菌感染时血清前白蛋白做为一种非特异宿主防御物质在血清中浓度会迅速降低[14]。
比较两组患者营养支持治疗1w、3w时的各血清蛋白指标,发现两组患者的营养支持疗效无差异,即发生胃潴留的患者经肠内营养与肠外营养联合治疗也可提供机体代谢所需的蛋白质等营养,且与全肠内营养相比无明显差异。这符合黎介寿等[15]提出的重症患者采用全营养支持,首选肠内营养,必要时肠内与肠外营养联合应用的观点。
3.3 全肠内营养较肠内、肠外联合营养可提高危重症患者免疫功能 营养支持治疗1w时两组患者免疫指标比较无明显差异,而在营养支持治疗3w后非胃潴留的 IgG、IgA高于胃潴留组。郑天衡等[16],陆静珏等[17]相关研究结果一致,他们研究得出早期肠内营养支持可改善急性期卒中患者机体的免疫功能,降低感染并发症的发生率的结果。肠内营养与肠外营养的动物模型研究证实,肠外营养组的小肠上皮内淋巴细胞数减少和细菌易位增多的主要影响因素是缺乏肠道喂养,而不是肠外营养本身[18]。说明肠内营养可改善神经危重症患者的免疫功能。
3.4 治疗
对于发生胃潴留的危重症神经疾病患者,首先积极治疗原发病,缓解急性应激状态,如降低颅内压、纠正休克、控制感染、维持正常血氧水平及保持水电解质平衡等综合措施,其次给予对症治疗。目前改善胃肠动力的药物有拟胆碱类药物、5-羟色胺受体激动剂和拮抗剂、多巴胺受体拮杭剂、胃动素受体激动剂、头孢菌素等[19]。此外,中药及针刺穴位治疗,可促进胃肠动力,缓解胃潴留[20]。对于药物不能缓解的胃潴留患者,可以考虑留置鼻空肠置管营养管。
虽然通过胃残留量测定来判断肠内营养是否耐受存在诸多缺陷,但由于目前尚无被普遍接受的更可靠的指标,胃残留量测定仍是临床上广泛使用的评价手段。注重胃残留量的变化趋势,动态观察胃残留量,及时发现胃潴留,调整营养支持治疗方案,对神经危重症患者神经功能恢复及减少并发症、改善预后均有重要意义。
[1]吴宗键.肠外与肠内联合营养支持是营养支持治疗的发展方向[J].上海医药,2010,31(6):252-253.
[2]Montejo JC.Enteral nutrition-related gastrointestinal complications in critically ill patients:amulticenter study.The Nutritional and Metabolic Working Group of the Spanish Society of Intensive Care Medicine and Coronary Units[J].Crit Care Med,1999,27(8):1447-1453.
[3]Heyland DK,Schroter-Noppe D,Drover JW,etal.Nutrition support in the critical care setting:current practice in Canadian ICUs-opportunities for improvement[J].JParenter Enteral Nutr,2003,27(1):74-83.
[4]Rohm KD,Schollhorn T,Boldt J,etal.Nutrition support and treatment ofmortality disorders in critically ill patients:results of a survey on German intensive care units[J].Eur JAnaesth,2008,25(1):58-66.
[5]Elke G,Schadler D,Engel C,etal.Current practice in nutritional support and its association with mortality in septic patients Results from a national,prospective,multicenter study[J].Crit Care Med,2008,36(6):1762-1767.
[6]杭春华,史继新.创伤性脑损伤后胃肠功能障碍[J].江苏医药杂志,2003,29(11):851-853.
[7]周 华,许 媛.危重症病人营养支持指南解读[J].中国实用外科杂志,2008,28(11):925-928.
[8]中华医学会重症医学分会.危重病人营养支持指导意见(2006)[J].中国实用外科杂志,2006,26(10):721-732.
[9]中华医学会肠外肠内营养学分会神经疾病营养支持学组.神经系统疾病肠内营养支持操作规范共识[J].中华神经科杂志,2011,44(11):787-791.
[10]刘竹青,袁 军,刘 冬,等.神经内科危重症肠内营养支持期间胃动力障碍的临床观察和策略[J].中国药物与临床,2012,12(3):387-388.
[11]王 军,鲍月红,于志伟,等.神经外科重症患者胃潴留的动态观察及与血糖、昏迷程度的相关分析[J].中国医药导刊,2010,12(9):1505-1507.
[12]张小鹏.严重脑损伤后急性上消化道病变[J].国外医学神经病学神经外科学分册,1992,19(1):38-39.
[13]Mutlu GM,Mutlu EA,Factor P.Prevention and treatment of gastrointestinal complications in patients on mechanical ventilation[J].Am JRespir Med,2003,2(5):395-411.
[14]郭 旭.血清前白蛋白测定的临床价值[J].淮海医药,2006,24(5):446-448.
[15]黎介寿.临床营养支持策略的变迁[J].中国普外基础与临床杂志,2009,16(12):953-955.
[16]郑天衡,王少石,陈真理,等.早期肠内营养支持对急性期卒中患者免疫功能的影响[J].中国脑血管病杂志,2006,3(8):356-360.
[17]陆静珏,韩 英,陆志成.早期肠内营养支持对重型脑卒中患者营养状况和免疫功能的影响[J].山东医药,2009,49(51):89-91.
[18]Wildhaber BE,Yang H,Spencer AU,etal.Lack of enteral nutrition-effects on the intestinal immune system[J].JSurg Res,2005,123(1):8-16.
[19]王志刚,刘凤林,秦新裕.胃瘫治疗的进展[J].国外医学消化系疾病分册,2002,22(1):8-11.
[20]陈德昌,景炳文,杨兴易,等.大黄对胃肠功能衰竭的治疗作用[J].解放军医学杂志,1996,21(1):24.

