参浮化痰丸质量标准的研究
王 萍, 付 玲, 聂继红*, 卜淑卫
(1.新疆医科大学附属中医医院,新疆 乌鲁木齐830000;2.新疆医科大学药学院,新疆 乌鲁木齐830054)
参浮化痰丸处方来源于新疆医科大学附属中医医院长期临床实践的经验方,由党参、浮小麦、陈皮、防风、黄芩、制半夏等多味药材组成,其主要功效为益气固表,健脾燥湿,止咳化痰。用于慢性阻塞性肺疾病稳定期的治疗,临床疗效较好。为方便患者使用,本课题将其研究开发成浓缩丸剂。在完成制备工艺的基础上,为有效控制该制剂质量,保证临床疗效,本研究对其进行了薄层色谱鉴别研究,建立了其中陈皮、防风、黄芩的定性鉴别方法;采用高效液相色谱法,对制剂中的主要有效成分—橙皮苷、5-O-甲基维斯阿米醇苷及升麻素苷进行定量分析,建立了参浮化痰丸的质量标准,为全面有效控制产品质量提供实验依据。
1 仪器与试药
1.1 仪器 Waters 2695高效液相色谱仪 (Waters 2996二极管阵列检测器,美国 Waters公司);AL204电子天平 [梅特勒-托利多仪器 (上海)有限公司];AG135电子天平 [梅特勒-托利多仪器(上海)有限公司];Direct-QTM超纯水仪 (Millipore)。
1.2 试药
对照品:陈皮对照药材 (批号:120969-200808,供TLC法鉴别用);防风对照药材 (批号:120947-201108,供TLC法鉴别用);黄芩对照药材 (批号:120955-201008,供TLC法鉴别用);橙皮苷对照品 (批号:110721-201014,供定量测定用);5-O-甲基维斯阿米醇苷对照品 (批号:111523-201007,供定量测定用);升麻素苷对照品(批号:111522-201008,供定量测定用)均由中国药品生物制品检定所提供。
参浮化痰丸 (批号分别为20110712、20110713、20110714,由新疆医科大学附属中医医院提供)。
水为超纯水;乙腈、甲醇为色谱纯试剂;薄层层析用硅胶G(青岛海洋化工有限公司);实验中所用其他试剂均为分析纯。
2 方法与结果
2.1 陈皮的薄层色谱鉴别[1-5]取本品适量,研细,取样品粉末3 g,加甲醇40 mL,加热回流1 h,滤过后,滤液蒸干,残渣加水30 mL使溶解,用三氯甲烷振摇提取3次,每次20 mL,弃去三氯甲烷液;再用乙酸乙酯振摇提取4次,每次20 mL,合并乙酸乙酯液,蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液。另取橙皮苷对照品,加甲醇制成饱和溶液,作为对照品溶液。另取陈皮对照药材,同法制得对照药材溶液。按处方比例称取缺陈皮的其他药材,按制备工艺制备阴性样品,照上述方法制得缺陈皮的阴性对照溶液。照《中国药典》2010年版一部附录VI B薄层色谱法项下试验,吸取供试品溶液5μL,对照品溶液2μL,对照药材溶液及阴性对照溶液各10μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-甲醇-水 (100∶17∶13)作为展开剂,展开至约6 cm时,取出,晾干,再以甲苯-乙酸乙酯-甲酸-水 (20∶10∶1∶1)的上层溶液为展开剂,展开至约10 cm,取出后晾干,喷以2%三氯化铝乙醇溶液,晾干后置紫外光灯 (365 nm)下检视。结果供试品色谱中,在与对照药材及对照品色谱相应的位置上,显相同颜色的斑点。而阴性无干扰。见图1。

图1 陈皮薄层色谱图Fig.1 TLC chromatogram of Citri reticulatae Pericarpium
2.2 防风的薄层色谱鉴别[1,6-8]取本品粉末3 g,加甲醇30 mL,超声处理30 min后,滤过,滤液蒸干后,加水20 mL,振摇使残渣溶解,用乙酸乙酯振摇提取2次,每次20 mL,合并乙酸乙酯提取液后再用水饱和的正丁醇振摇提取2次,每次20 mL,合并正丁醇提取液,蒸干后,加甲醇1 mL使残渣溶解,得到供试品溶液。另取5-O-甲基维斯阿米醇苷对照品适量,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。另取防风对照药材,同上述方法,制成对照药材溶液。按处方比例称取缺防风的其他药材,按制备工艺制备阴性样品,同法制备缺防风的阴性对照溶液。按《中国药典》2010年版一部附录VI B项下,分别吸取供试品溶液、对照药材溶液、对照品溶液及阴性对照溶液各10μL,点于同一硅胶G薄层板上,以三氯甲烷-甲醇 (4∶1)为展开剂,展开,取出,晾干后置紫外灯 (365 nm)下检视。结果供试品色谱中,在与对照药材及对照品色谱相应的位置上,显相同颜色的斑点,且阴性无干扰。见图2。

图2 防风薄层色谱图Fig.2 TLC chromatogram of Saposhnikoviae Radix
2.3 黄芩的薄层色谱鉴别[1,9-10]取本品 15 g,研细,加甲醇40 mL,加热回流1 h后,滤过,滤液蒸干后,加水15 mL使残渣溶解,用稀盐酸调节溶液pH值至2后,再用乙酸乙酯振摇提取2次,每次20 mL,合并提取液,蒸干后的残渣加甲醇0.5 mL使溶解,作为供试品溶液;另取黄芩对照药材,照上述方法制备得到对照药材溶液;另取黄芩苷对照品,加乙醇制得每1 mL含1 mg的溶液,作为对照品溶液;按处方比例称取缺黄芩的其余药材,按已得到的制备工艺制备阴性样品,照上述方法制成缺黄芩的阴性对照溶液。照薄层色谱法(《中国药典》2010年版一部附录VI B),吸取供试品溶液、对照品溶液、对照药材溶液及阴性对照溶液各10μL,分别点于同一硅胶 G薄层板上,以乙酸乙酯-丁酮-甲酸-水(5∶3∶1∶1)为展开剂,展开后取出,晾干。结果在供试品色谱中,在与对照药材及对照品色谱相应的位置上,显相同颜色的斑点,而阴性对照无干扰。结果见图3。
2.4 橙皮苷、5-O-甲基维斯阿米醇苷的HPLC法测定[11-12]
2.4.1 色谱条件 SYMMETRY C18色谱柱 (4.6 mm×150 mm,5μm),流动相为乙腈-0.1%磷酸(17∶83),橙皮苷、5-O-甲基维斯阿米醇苷的检测波长分别为283 nm和254 nm,柱温为30℃,体积流量为1.0 mL/min,进样量为10μL。
2.4.2 橙皮苷和5-O-甲基维斯阿米醇苷对照品溶液的制备 精密称取橙皮苷对照品37.50 mg,5-O-甲基维斯阿米醇苷对照品24.78 mg,置同一50 mL量瓶中,加甲醇使溶解后,稀释至刻度,摇匀,作为贮备液 (其中橙皮苷质量浓度为0.750 0 mg/mL,5-O-甲基维斯阿米醇苷质量浓度为0.495 6 mg/mL)。

图3 黄芩薄层色谱图Fig.3 TLC chromatogram of Scutellariae Radix
2.4.3 供试品溶液的制备 将样品研细,精密称取约1 g,置于锥形瓶中,加入甲醇10 mL,密塞,振摇,称质量,加热回流1 h,冷却后称质量并补足减失的质量,滤过后,滤液再用0.45μm的微孔滤膜过滤,取续滤液,进样量10μL,经高效液相色谱法测定,峰面积积分值经2.4.6项下线性回归方程计算得出醇提液中橙皮苷和5-O-甲基维斯阿米醇苷的质量浓度,进一步计算得出样品中橙皮苷和5-O-甲基维斯阿米醇苷的质量浓度,即可。
2.4.4 阴性对照样品溶液的制备 按处方比例精密称取缺陈皮、防风的其余药材,按上述制备工艺制备得到阴性样品,按供试品溶液制备方法制备阴性对照样品溶液。
2.4.5 专属性试验 精密吸取上述对照品溶液、供试品溶液与阴性对照溶液各10μL,分别注入液相色谱仪,得到的色谱图见图4。结果表明:在供试品色谱中,呈现与对照品色谱主峰保留时间一致的色谱峰,且阴性对照色谱图中在待测成分保留时间处无杂质峰出现。表明本方法有良好的专属性。
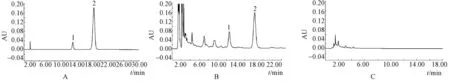
图4 橙皮苷、5-O-甲基维斯阿米醇苷高效液相色谱图Fig.4 HPLC chromatogram s of hesperidin and 4'-O-β-D-glucosyl-5-O-methylvisamm inol
2.4.6 线性关系考察 分别精密吸取2.4.2项下橙皮苷、5-O-甲基维斯阿米醇苷对照品贮备液各1、2、3、4 mL,置5 mL的量瓶中,加甲醇至刻度,摇匀后,滤过,分别制成质量浓度为150.0、300.0、450.0、600.0μg/mL的系列橙皮苷标准溶液及质量浓度为 99.1、198.2、297.4、396.5 μg/mL的5-O-甲基维斯阿米醇苷标准系列溶液。用上述4个标准溶液及贮备液,按上述色谱条件分别进样分析,进样量为10μL。以对照品的质量浓度为横坐标,峰面积积分值为纵坐标,得到橙皮苷、5-O-甲基维斯阿米醇苷的回归方程分别为:橙皮苷A=17 823.12 C-114 545.55(相关系数 r=0.999 9);5-O-甲基维斯阿米醇苷A=24 227.05 C-4 589.67,相关系数r=0.999 9。结果表明:在150.0~750.0μg/mL范围内,橙皮苷峰面积值(A)与质量浓度 (C)有良好的线性关系;而5-O-甲基维斯阿米醇苷在99.1~495.6μg/mL范围内,峰面积值 (A)与质量浓度 (C)的线性关系良好。
2.4.7 精密度试验 精密吸取对照品溶液10μL,重复进样6次,结果橙皮苷和5-O-甲基维斯阿米醇苷峰面积的 RSD分别为0.38%(n=6)、0.66%(n=6)。表明仪器精密度良好。
取同一对照品溶液,连续测定5 d,测定峰面积值,结果橙皮苷和5-O-甲基维斯阿米醇苷峰面积的日间精密度 RSD分别为0.80% (n=6)、1.12%(n=6)。
2.4.8 稳定性试验 取同一供试品溶液,分别于0、6、12、24、48 h进样,结果橙皮苷和5-O-甲基维斯阿米醇苷峰面积的RSD分别为0.70%(n=6)、1.75%(n=6)。表明供试品溶液在48 h内稳定性良好。
2.4.9 重复性试验 精密称取同一批样品,照供试品溶液制备方法平行制得6份供试品溶液,分别测定橙皮苷和5-O-甲基维斯阿米醇苷的量,结果其RSD分别为0.76%(n=6)、1.82%(n=6),表明本试验方法重复性良好。
2.4.10 加样回收率试验 精密称取已测定的同批样品6份,分别精密加入橙皮苷和5-O-甲基维斯阿米醇苷对照品适量,按上述供试品溶液制备方法制备,按照确定的色谱条件测定,分别计算回收率,结果见表1、2。
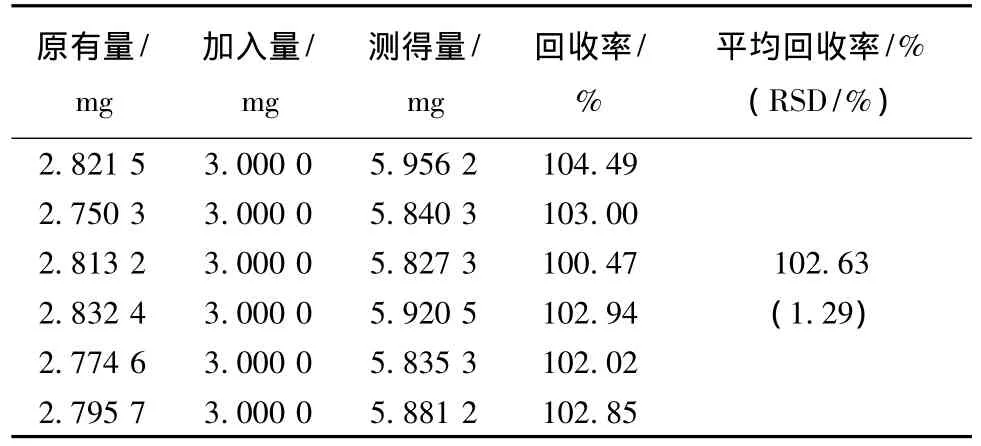
表1 橙皮苷加样回收率试验结果 (n=6)Tab.1 Results of recovery tests of hesperidin(n=6)

表2 5-O-甲基维斯阿米醇苷加样回收率试验结果 (n=6)Tab.2 Results of recovery tests of 4'-O-β'-D-glucosyl-5-O-methylvisam m inol(n=6)
2.5 升麻素苷的 HPLC 法测定[1,13]
2.5.1 色谱条件 SYMMETRY C18色谱柱 (4.6 mm×150 mm,5μm),流动相为甲醇-水 (33∶67),检测波长254 nm,体积流量1.0 mL/min,柱温30℃,进样量10μL。
2.5.2 对照品溶液的制备 精密称取升麻素苷对照品3.86 mg,置100 mL量瓶中,加适量甲醇使溶解后,加甲醇至刻度,摇匀,得到质量浓度为0.038 6 mg/mL升麻素苷贮备液。
2.5.3 供试品溶液的制备 取样品适量,研细,从中精密称取样品粉末约1 g,加甲醇20 mL,密塞,振摇后称定质量,超声40 min,冷却,称定质量,用甲醇补足减失的质量,滤过,滤液用0.45 μm的微孔滤膜过滤后,取续滤液,进样量10μL,经高效液相色谱法测定,峰面积积分值经2.5.6项下线性回归方程计算得出醇提液中升麻素苷的质量浓度,进一步计算得出样品中升麻素苷的量,即可。
2.5.4 阴性对照样品溶液的制备 按处方比例精密称取缺防风的其余药材后,按制备工艺制备,得到阴性样品,按上述供试品溶液制备方法制得阴性对照样品溶液。
2.5.5 专属性试验 分别精密吸取上述供试品溶液、对照品溶液、阴性对照溶液各10μL,注入液相色谱仪,测定,即得,结果见图5。结果表明:供试品色谱中呈现与对照品色谱主峰保留时间一致的色谱峰,而且在阴性对照色谱图中,在与待测成分相同的保留时间处,无杂质峰出现。表明本方法专属性良好。
2.5.6 线性关系考察 精密吸取升麻素苷对照品贮备液各1、2、3、4 mL,置5 mL的量瓶中,加甲醇至刻度,摇匀,滤过,得到质量浓度为7.72、15.44、23.16、30.88μg/mL的升麻素苷标准系列溶液。按上述色谱条件,用上述4个标准溶液及贮备液,分别进样分析,进样量为10μL。以峰面积积分值为纵坐标,对照品的质量浓度为横坐标,得到升麻素苷的回归方程为A=23 100.74 C+4 387.08,相关系数r=0.999 9。表明在7.7~38.6 μg/mL范围内,升麻素苷峰面积值 (A)与质量浓度 (C)呈良好的线性关系。
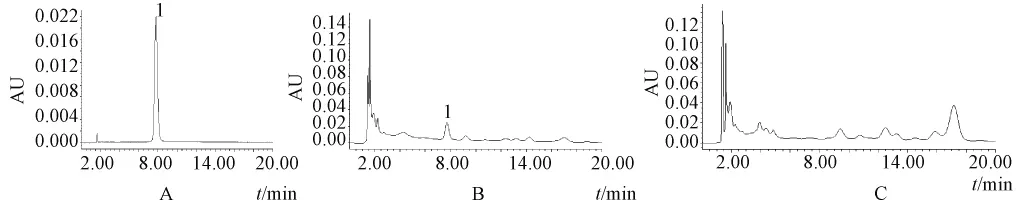
图5 升麻素苷高效液相色谱图Fig.5 HPLC chromatogram s of prim-O-glucosylcim ifugin
2.5.7 精密度试验 精密吸取升麻素苷对照品溶液10μL,重复进样6次,测定峰面积值,结果其RSD为0.40%,表明仪器有良好的精密度。
取同一对照品溶液,连续测定5 d,结果其峰面积的日间精密度RSD为0.47%。
2.5.8 稳定性试验 取同一供试品溶液,于0、6、12、24、48 h分别进样分析,结果其峰面积的RSD为1.59%。结果表明,在48 h内供试品溶液有良好的稳定性。
2.5.9 重复性试验 精密称取同一批样品,照供试品溶液制备方法,平行制得6份供试品溶液后,分别测定升麻素苷的量,计算,结果其 RSD为1.52%,表明本方法有良好的重复性。
2.5.10 加样回收率试验 取已测定的同批样品,精密称取6份,按照表3精密加入升麻素苷对照品适量,照供试品溶液制备方法制备,得到测试溶液,按确定的色谱条件进样分析,计算,得到其回收率见表3。
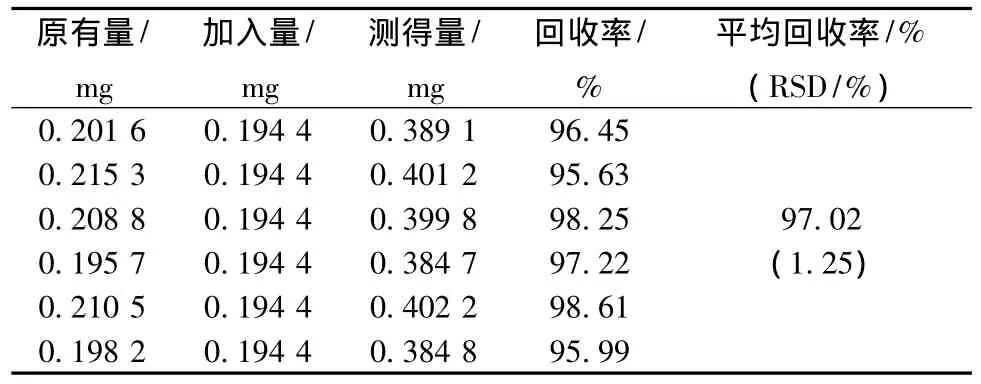
表3 升麻素苷加样回收率试验结果 (n=6)Tab.3 Results of recovery tests of prim-O-glucosyl-cim ifuqin(n=6)
2.6 样品测定结果 取不同批号的样品,按前述供试品溶液制备法制备,按照确定的色谱条件测定,计算结果见表4。
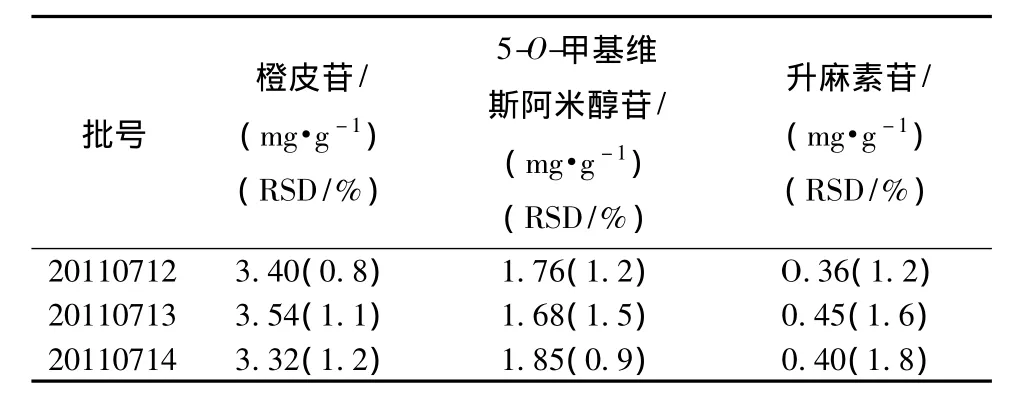
表4 样品测定结果 (n=3)Tab.4 Determination results(n=3)
3 讨论
在参考2010年版《中国药典》 (一部)及大量文献的基础上,本试验对全方药味分别进行了TLC法定性鉴别试验研究,分别采用多种不同的供试品处理方法及展开剂进行试验,结果参浮化痰丸中主要成分陈皮、黄芩、防风薄层色谱斑点清晰,分离效果较好,具有重现性好、专属性强、简便、快速等特点,可作为该制剂的定性鉴别依据。而方中其余药材如党参、浮小麦、制半夏等,因未能得到理想的TLC图谱,因此未能列入质量标准。
在陈皮的薄层色谱鉴别研究中,曾参照2010年版《中国药典》 (一部)[1]及文献[2-5]项下方法,采用石油醚回流提取或甲醇超声处理等多种供试品处理方法,并以三氯甲烷-甲醇-水(32∶17∶5)的下层溶液或乙酸乙酯-甲醇-水 (6∶1∶3)的上层溶液等为展开剂,结果均未得到理想的色谱图;后又多次进行展开剂距离的调整,结果得到了比较理想的薄层色谱图。因此将其列入了质量标准。
在采用HPLC法测定橙皮苷时,曾分别采用了甲醇-醋酸-水 (35 ∶4 ∶61)[1]、乙腈-水-冰醋酸(22 ∶77 ∶1)[2]、乙腈-0.15% 醋酸 (20 ∶80)[3]、甲醇-冰醋酸溶液 (37∶63)[4]多种流动相进行研究,均未能得到理想的色谱图,而当采用乙腈-0.1%磷酸 (17∶83)作为流动相时,得到的色谱图峰形较好,分离度较理想。
在研究过程中曾试图采用甲醇-水(40∶60)[1]、甲醇-水 (38∶62)[13]等流动相,对升麻素苷及5-O-甲基维斯阿米醇苷同时进行测定,但由于升麻素苷出峰时间较晚,因此在本研究中无法采用同一流动相同时测定5-O-甲基维斯阿米醇苷和升麻素苷。而当采用乙腈-0.1%磷酸 (17∶83)作为流动相时,得到的5-O-甲基维斯阿米醇苷峰形较好,分离度较理想。因此意外发现5-O-甲基维斯阿米醇苷和橙皮苷可以采用同一流动相在不同波长处同时测定,而且经方法学考察各项指标均符合定量测定的要求。
在采用HPLC法测定升麻素苷时,分别采用了甲醇-水 (40 ∶60)[1]、甲醇 -0.04 mol/L 乙酸钠(30 ∶70)[6]、甲醇-水 (38 ∶62)[13]、乙腈-水-醋酸 (13∶88∶0.03)[14]作为流动相进行分离,结果得到的升麻素苷峰均未能与杂质峰有效分离。因此考虑调整流动相的比例,在结合峰形、分离度及出峰时间等多种因素的情况下,最终在流动相为甲醇-水 (33∶67)时,升麻素苷峰与杂质峰有效分离。经方法学考察各项指标均符合定量测定的要求。
橙皮苷、5-O-甲基维斯阿米醇苷定量测定项下,在供试品溶液的制备过程中,为了保证样品中橙皮苷、5-O-甲基维斯阿米醇苷充分提取,分别对不同种类的提取溶剂 (乙醇、甲醇)、不同质量分数的提取溶剂 (50%甲醇、60%甲醇、70%甲醇、80%甲醇、90%甲醇)、溶剂加入倍量 (5倍、10倍、20倍、30倍、40倍、50倍)、提取方法 (不同超声处理时间、不同回流时间)进行考察。结果本品用10倍量甲醇,回流提取1 h,提取效果较好。
在研究供试品溶液的提取方法时,为了使样品中升麻素苷充分提取,分别对乙醇、甲醇作为提取溶剂、不同质量分数的甲醇提取溶剂 (50%甲醇、60%甲醇、70%甲醇、80%甲醇、90%甲醇)、甲醇不同加入量 (10倍、20倍、30倍、40倍、50倍)、样品提取方法 (不同超声处理时间、不同回流时间)进行了研究,结果表明,本品用20倍量甲醇超声40 min处理时,升麻素苷提取效果较好。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[2]林以宁,赵浩如,杨晓琴.健脾药糕的质量标准研究[J].中国药房,2005,16(1):57-58.
[3]郑志宏,苏彦斌,张凤荣.安神温胆丸质量标准的研究[J].中成药,2009,31(8):1219-1223.
[4]金 阳.健脾颗粒质量标准研究[J].中成药,2007,29(9):1403-1405.
[5]孙冬梅.二陈汤复方颗粒质量标准的研究[J].中国实验方剂学杂志,2007,13(10):9-10.
[6]黄杰芳,李惠霞,邓慧敏.辛夷鼻炎丸的质量标准研究[J].中草药,2009,40(8):1245-1247.
[7]徐韧柳,葛智鑫.感冒清热颗粒质量标准研究[J].中成药,2006,28(5):664-668.
[8]肖永庆,杨 滨,姚三桃,等.防风质量标准的研究[J].中国中药杂志,2001,26(3):185-187.
[9]刘征辉,叶挺祥,赵洪芝,等.黄连羊肝片质量标准研究[J].中成药,2009,31(8):附3-附6.
[10]龚苏晓,张铁军,许 浚,等.儿童清肺糖浆质量标准研究[J].时珍国医国药,2008,19(2):467-469.
[11]林 清,吴雪梅,马晓鹂,等.HPLC法测定健脾颗粒中橙皮苷的含量[J].中国药房,2009,20(9):698-699.
[12]陆静娴,祝 明,陈 勇.HPLC同时测定藿香清胃颗粒中升麻素苷、5-O-甲基维斯阿米醇苷、栀子苷含量[J].中成药,2009,31(11):1701-1704.
[13]毛彦杰,岳 敏,谷学新,等.五虎散质量标准的研究[J].中草药,2004,35(12):1354-1356.
[14]刘焕蓉,王 虹,秦雪梅,等.HPLC法测定玉屏风不同配伍中 4种黄酮成分[J].中草药,2011,42(6):1122-1124.

