芬戈莫德治疗复发缓解型多发性硬化的系统评价
姜明静 曹立颖 刘宁
多发性硬化(multiple sclerosis,MS)是人群中最常见的中枢神经系统脱髓鞘疾病,全世界共有数百万人受累[1]。临床通常将其分为4种类型:复发缓解 型 MS(relapsing-remitting multiple sclerosis,RRMS)、继发进展型 MS(SPMS)、原发进展型MS(PPMS)、进展复发型 MS(PRMS)。MS患者中80%~85%在开始发病时表现为RRMS[2]。
减少RRMS复发几率是治疗RRMS的重要环节,这将大大降低由于反复多次发作所致的病死率和病残率。临床常用于治疗MS的免疫调节剂主要包括干扰素β(INF-β)[3]、醋酸格拉默[4]、达克珠单抗(daclizumab)[5]等,但这些治疗药需经皮下、肌肉或静脉等途径给药,故亟需开发更为方便的口服治疗药。
芬戈莫德(fingolimod)通过降低进入中枢神经系统内的自身侵袭性淋巴细胞数量而发挥疗效,芬戈莫德不仅具有新型的作用机制——属1-磷酸鞘氨醇(sphingosine-1-phosphate)受体调节剂[6],且是迄今获美国FDA批准用于治疗RRMS的第一个口服药物[7]。本研究试图通过系统评价相关试验,探讨芬戈莫德治疗RRMS的临床效果。
1 材料和方法
1.1 材料 Cochrane Library(2012年第3期)、EMBASE(1974-2012-07)和 PubMed(1966-2012-07)、中国生物医学数据库 (CBM,1978-2012-07)、中国期刊全文数据库 (CNKI,1979-2012-07)和维普数据库(VIP,1989-2012-07)中芬戈莫德治疗RRMS的所有随机对照试验(randomized controlled trials,RCT)相关文献。
(1)纳入标准:①文献类型为随机对照试验;②观察对象:患者符合 McDonald标准(2005)[8]或Poser等[9]制定的RRMS诊断标准;③分组和干预措施:试验组口服芬戈莫德1.25mg/d或0.5mg/d,对照组采用肌肉注射β1a-干扰素、安慰剂等其他治疗;④结局测量指标:年复发率(annualized re-lapse rate,ARR);扩展性病残状态量表(expanded disability status scale,EDSS)评分[10]:测量总分0~10分,分值越高表明神经功能缺损程度越重;治疗期间未复发的MS患者人数;经磁共振成像(MRI)确认的新发或扩大的损害数;安全性评价:治疗期间总的不良反应事件、严重不良反应事件、因不良反应中止治疗的患者数。(2)排除标准:非随机对照试验;数据不全或无原始数据。
1.2 方法 计算机检索 Cochrane Library、EMBASE和PubMed、中国生物医学数据库(CBM)、中国期刊全文数据库(CNKI)和维普数据库(VIP),手工检索相关杂志和会议论文等。英文检索词包括randomized controlled trial、fingolimod、“multiple sclerosis,relapsing-remitting”[Mesh]等;中文检索词包括芬戈莫德、复发缓解型多发性硬化、随机对照试验等。根据不同数据库特点采取相应主题词检索与自由词检索结合方式进行检索。文献检索无语种限制。
由两名评价员独立完成文献筛选、资料提取和方法学质量评价并交叉核对,如遇分歧通过讨论或根据第三位研究人员的意见协商解决。采用Cochrane协作网推荐的“风险评估工具”进行偏倚风险评估,其中RCT偏倚风险评估内容如下:(1)随机方法是否正确;(2)是否做到隐蔽分组、方法是否正确;(3)是否采用盲法;(4)有无失访或退出,如有失访或退出时,原因是否描述清楚,是否采用意向性分析法;(5)选择性报告研究结果;(6)是否存在其他潜在偏倚。每条标准依研究具体情况按“是”、“否”、“不清楚”进行评价,其中“是”表示低度偏倚风险,“否”表示高度偏倚风险,“不清楚”表示中度偏倚风险。
1.3 统计学处理 采用Cochrane协作网提供的RevMan 5.1软件进行 Meta分析,计数资料用相对危险度(OR)作为疗效效应量,计量资料采用均方差(MD)、加权均方差(WMD)作为疗效效应量,二者均以95%CI表示,检验水准P=0.05。首先分析纳入研究的人群、治疗方法等影响临床异质性因素,对各研究进行亚组分析或敏感性分析;然后采用χ2检验分析亚组内的统计学异质性,若亚组间无统计学异质性(P>0.1,I2≤50%)采用固定效应模型进行 Meta分析[11];若存在临床异质性(P≤0.1,I2>50%),首先分析存在临床异质性的原因,确定能否采用随机效应模型进行Meta分析[12]。若研究间存在明显的临床异质性,则不进行合并,只对其进行描述性分析。
2 结果
2.1 文献检索结果 初检出1588篇文献,经阅读文题及摘要,排除重复及非临床试验文献,初筛纳入10篇,进一步阅读全文,排除干预措施、测量指标等不符合纳入标准或符合排除标准的研究。最终纳入3篇英文文献,实验设计均为多中心RCT[13-15],其中1篇为芬戈莫德(剂量1.25mg/d和0.5mg/d)与β1a-干扰素对比[13],2篇为芬戈莫德(剂量分别为1.25mg/d[14-15]、0.5mg/d[15]和5 mg/d[14],其中5mg组因不良反应多、致死率高而未纳入分析)与安慰剂对比,全部样本总计2749人。各纳入研究文献的基本情况见表1。
2.2 文献质量 本系统评价依据Cochrane Handbook 5.1风险偏倚评估工具对纳入研究进行风险偏倚评估,纳入研究存在一定程度的偏倚风险。纳入试验中随机分组方法在3个研究中都有详尽报道,并对盲法及隐蔽分组方法进行了具体描述。因此纳入试验存在选择性偏倚、实施偏倚等的低度可能性。纳入研究风险评估结果详见表2。
2.3 结局测量指标
2.3.1 年复发率(ARR)的评价:纳入3个芬戈莫德与安慰剂和β1a-干扰素治疗RRMS比较的研究[13-15],分析其 ARR的情况。因为3个研究亚组间存在临床异质性,故不进行合并,具体见表3。3个研究中,芬戈莫德组ARR均低于对照组。
2.3.2 EDSS评分变化的评价:芬戈莫德与其他治疗(β1a-干扰素、安慰剂)相比,2个试验[13,15]报道了EDSS评分在治疗前后的变化情况,其中2个研究[13,15]中的芬戈莫德1.25mg组之间有临床异质性(P<0.0001,I2=94%),采用随机效应模型合并后Meta分析结果显示芬戈莫德1.25mg组与对照组相比,治疗后的EDSS评分差异无统计学意义〔MD=-0.29,95%CI(-0.62~0.04)〕。芬戈莫德0.5mg组两研究间无统计学异质性(P=0.63,I2=0%),采用固定效应模型合并后结果显示芬戈莫德0.5mg组与对照组相比,治疗后的EDSS评分明显降低〔MD=-0.11,95%CI(-0.19~-0.03)〕。
2.3.3 治疗期间未复发的 MS患者人数的评价:芬戈莫德与对照组相比,3个研究中的芬戈莫德1.25mg组之间存在临床异质性(P=0.002,I2=84%),采用随机效应模型合并后Meta分析结果显示芬戈莫德1.25mg组未复发患者人数多于对照组相比,〔OR=2.88,95%CI(1.59~5.22)〕。芬戈莫德0.5mg组的各研究间无统计学异质性(P=0.17,I2=48%),采用固定效应模型合并后 Meta分析结果显示芬戈莫德0.5mg组与对照组相比,治疗期间未复发的MS患者人数增加〔OR=2.45,95%CI(1.82~3.29)〕。上述结果表明芬戈莫德1.25mg组和0.5mg组与β1a-干扰素、安慰剂等治疗相比,未复发的MS人数均明显增多。
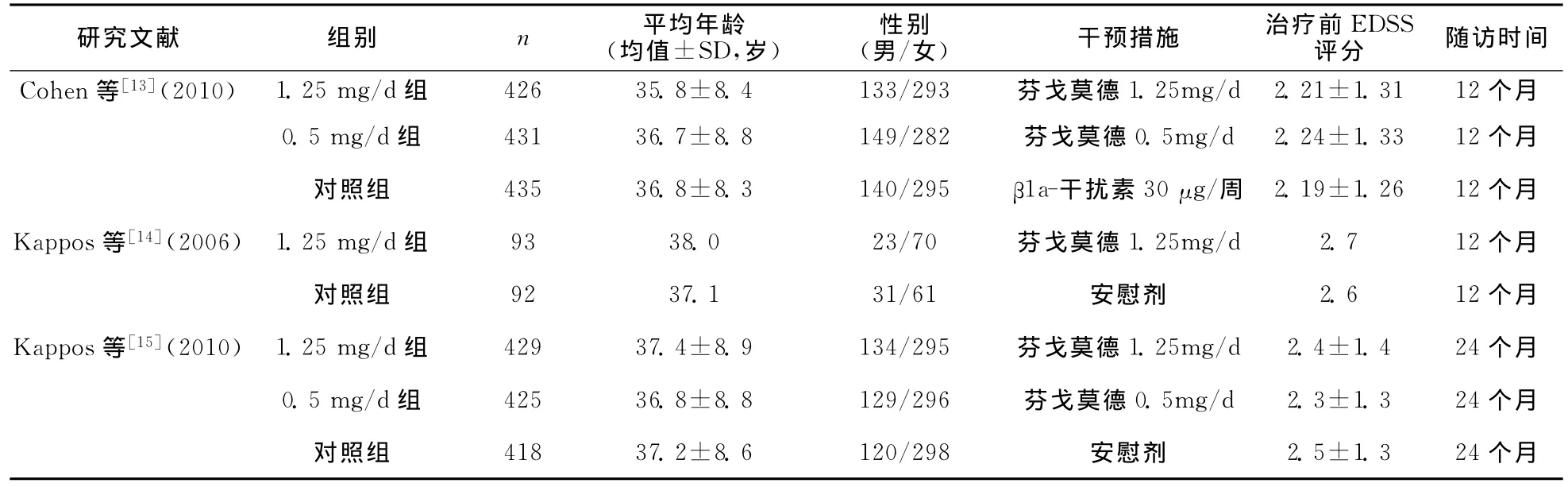
表1 纳入试验的基本情况

表2 纳入研究方法学质量评估
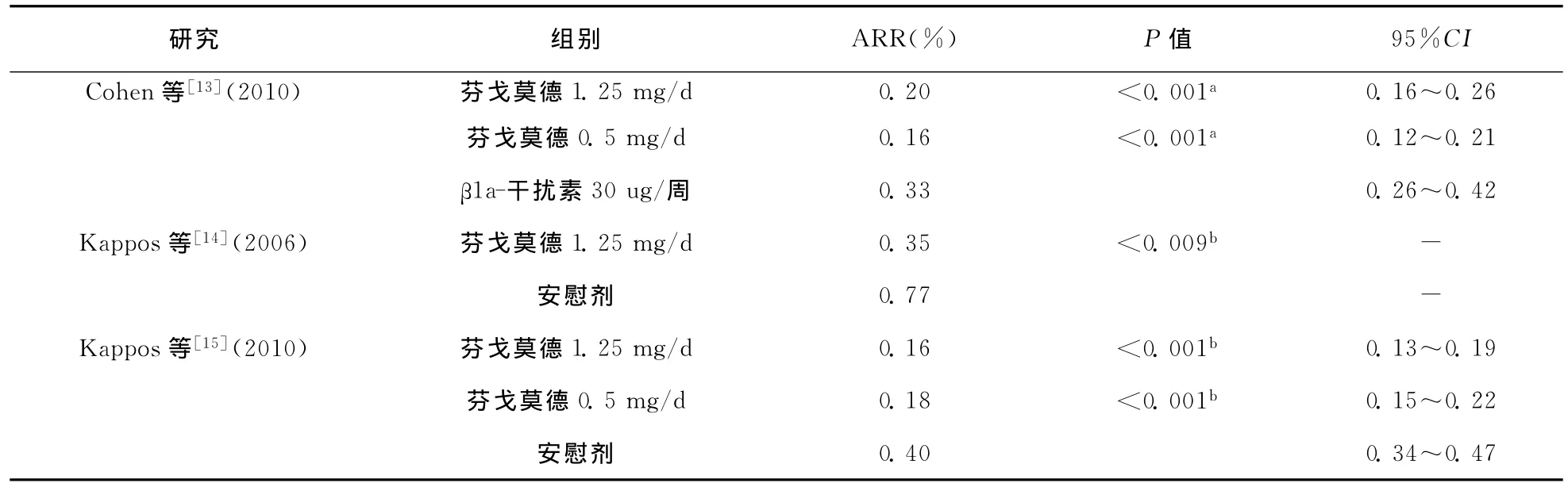
表3 年复发率的比较
2.3.4 经MRI确认的新发或扩大的损害数的评价:纳入的3个研究[13-15]中,不同研究中1.25mg组和0.5mg组均间存在临床异质性〔其中,芬戈莫德1.25mg组与对照组比较,损害数无明显差异(P<0.00001,I2=96%);0.5mg组与对照组比较,损害数无明显差异 (P<0.00001,I2=98%)〕,采用随机效应模型,Meta分析结果提示芬戈莫德1.25mg组和0.5mg组与对照组比较,经MRI确认的新发或扩大的损害数差异均无统计学意义〔分别为OR=-3.91,95%CI(-8.34~0.51);OR=-4.06,95%CI(-10.33~2.21)〕。
2.3.5 安全性评价:在总的不良反应事件发生率方面,纳入的3个研究中,不同研究中1.25mg组和0.5mg组均存在临床异质性(其中,芬戈莫德1.25mg组与对照组相比P=0.53,I2=96%;0.5 mg组与对照组相比P=0.02,I2=83%),采用随机效应模型,Meta分析结果提示芬戈莫德1.25 mg组和0.5mg组与对照组比较,芬戈莫德组总的不良反应事件发生率差异均无统计学意义〔分别为OR=1.04,95%CI(0.74~1.47);OR=0.85,95%CI(0.36~2.00)〕。
在总的严重不良反应事件发生率方面,纳入的3个研究中,不同研究中1.25mg组和0.5mg组均存在临床异质性(其中,芬戈莫德1.25mg组与对照组相比P=0.05,I2=66%;0.5mg组与对照组相比P=0.14,I2=53%),采用随机效应模型,Meta分析结果提示芬戈莫德1.25mg组和0.5 mg组与对照组比较,在总的严重不良反应事件发生率与对照组相比差异均无统计学意义〔分别为OR=1.29,95%CI(0.71~2.34);OR=0.91,95%CI(0.55~1.51)〕。
在因不良反应而中止治疗的患者数方面,纳入的3个研究中,不同研究中1.25mg组和0.5mg组均无统计学异质性(其中芬戈莫德1.25mg组P=0.44,I2=0%;0.5mg 组P=0.29,I2=12%),采用固定效应模型合并后Meta分析结果显示,芬戈莫德1.25mg组和0.5mg组因不良反应而中止治疗的患者与对照组相比差异无统计学意义〔其中,1.25mg组OR=2.21,95%CI(1.57~3.12);0.5mg组OR=1.17,95%CI(0.78~1.74)〕,但0.5mg组因不良反应而中止治疗的患者数较少,提示芬戈莫德0.5mg组安全性相对较好。
3 讨论
本研究基于国内外随机对照试验对芬戈莫德治疗RRMS的有效性和安全性进行Meta分析。为了避免各研究间异质性的影响,对纳入的试验根据研究情况采用了亚组分析的方法,分别对芬戈莫德1.25mg和0.5mg组进行了亚组分析。总体结果显示,芬戈莫德1.25mg组和0.5mg组治疗RRMS的疗效较优于β1a-干扰素、安慰剂治疗对照等,安全性方面与对照组相比无明显差异。
在有效性方面,芬戈莫德1.25mg和0.5mg组ARR均低于β1a-干扰素及安慰剂治疗等对照组;芬戈莫德组治疗期间未复发的MS患者人数多于对照组〔其中,1.25mg组OR=2.88,95%CI(1.59~5.22);0.5mg 组OR=2.45,95%CI(1.82~3.29)〕。而且芬戈莫德0.5mg/d组比1.25mg/d组ARR更低、EDSS评分改善更显著〔MD=-0.11,95%CI(-0.19~-0.03)〕,表明芬戈莫德组MS患者与安慰剂组比较疾病进展风险降低、治疗期间未复发的MS患者人数明显增加〔OR=2.45,95%CI(1.82~3.29)〕。在安全性方面,总的不良反应事件、总的严重不良反应事件、因不良反应而中止治疗的患者数等安全性事件发生率上,芬戈莫德1.25mg组和0.5mg组与对照组相比均无明显差异〔分别为1.25mg组OR=1.04,95%CI(0.74~1.47);0.5mg 组OR=0.85,95%CI(0.36~2.00)〕、总的严重不良反应事件〔分别为 1.25mg组OR=1.29,95%CI(0.71~2.34);0.5mg 组OR=0.91,95%CI(0.55~1.51)〕、因不良反应而中止治疗的患者数〔其中,1.25mg 组OR=2.21,95%CI(1.57~3.12);0.5mg 组OR=1.17,95%CI(0.78~1.74)〕等安全性指标,芬戈莫德1.25mg组和0.5 mg组与对照组相比均无明显差异,但0.5mg组因不良反应而中止治疗的患者数较少。Meta分析结果显示芬戈莫德有效且安全性较好的剂量与FDA批准的芬戈莫德剂量相符,即0.5mg 1次/d口服。
芬戈莫德为鞘氨醇-1-磷酸盐受体调节剂[6],为前体药物,在体内经鞘氨醇激酶作用形成芬戈莫德磷酸化物之后才呈现出生物学活性。芬戈莫德与鞘氨醇-1-磷酸盐受体的结合在治疗RRMS有效的作用机制中最为重要。芬戈莫德经磷酸化后可转变为鞘氨醇-1-磷酸盐Ⅰ型受体拮抗剂,导致受体分子内陷。该药为亲脂性药物,可稳定地透过血-脑脊液屏障,进入中枢神经系统后发生磷酸化,通过与神经细胞上的鞘氨醇-1-磷酸盐受体相互作用,可阻止淋巴结释放淋巴细胞[6],抑制炎性细胞因子的合成,减少其渗透进入中枢神经系统而引起炎性反应和神经损害,促进轴突增生[16]。此外,存在于中枢神经系统中的鞘氨醇-1-磷酸盐受体具有调节神经发生和神经功能的生理效应。而芬戈莫德能够透过血-脑脊液屏障并在中枢神经系统的白质中蓄积,因此芬戈莫德还具有神经保护和神经再生功能[17]。
芬戈莫德不仅具有新型的作用机制,且是迄今全球范围内获准治疗RRMS的第一个口服药物。芬戈莫德用药为1次/d,药物-药物和药物-食物相互作用少见,用药时不需考虑进食及进食时间的影响。其治疗RRMS患者降低复发风险、延长至再次复发时间和延缓病残进展的疗效都显著优于安慰剂,而总不良反应发生率与β1a-干扰素相似,表明口服芬戈莫德有效、安全而且简便。
虽然本研究共纳入3个试验,全部为多中心研究,样本量较大,但各研究样本存在一定的异质性,由于入选的试验用药剂量和随访时间尚未统一,可能存在不同程度的偏倚和混杂因素,且多数研究未报道其远期疗效,尚需要大量的高质量试验并结合长期的临床实践进行观察。
综上所述,芬戈莫德0.5mg/d治疗RRMS具有一定优势,芬戈莫德口服治疗RRMS患者具有一定安全性和有效性,同时用药方案亦十分简便,有望成为RRMS治疗的首选一线用药。本系统评价得出的结论需要更多高质量的随机对照试验进一步验证。今后的临床研究应严格按照CONSORT声明2010版[18]对RCT进行全面、客观报告,提高报告质量。
[1]Anderson DW,Ellenberg JH,Leventhal CM,et al.Revised estimate of the prevalence of multiple sclerosis in the United States[J].Ann Neurol,1992,31(3):333-336.
[2]Noseworthy JH,Lucchinetti C,Rodriguez M,et al.Multiple sclerosis[J].N Engl J Med,2000,343(13):938-952.
[3]Wiesemann E,Deb M,Hemmer B,et al.Early identification of interferon-beta responders by ex vivo testing in patients with multiple sclerosis[J].Clin Immunol,2008,128(3):306-313.
[4]Vollmer T,Panitch H,Bar-Or A,et al.Glatiramer acetate after induction therapy with mitoxantrone in relapsing multiple sclerosis[J].Mult Scler,2008,14(5):663-670.
[5]Rose JW,Watt HE,White AT,et al.Treatment of multiple sclerosis with an anti-interleukin-2receptor monoclonal antibody[J].Ann Neurol,2004,56(6):864-867.
[6]Kenji Chiba,Hirotoshi Kataoka,Noriyasu Seki,et al.Fingolimod(FTY720),the sphingsine 1-phosphate receptor modulator,as a new therapeutic drug in multiple sclerosis[J].InflamRegen,2011,31(2):167-174.
[7]Scott LJ.Fingolimod:a review of its use in the management of relapsing-remitting multiple sclerosis[J].CNS Drugs,2011,25:673-698.
[8]Polman CH,Reingold SC,Edan G,et al.Diagnostic criteria for multiple sclerosis:2005revisions to the“McDonald Criteria”[J].Ann Neurol,2005,58(6):840-846.
[9]Poser CM,Paty DW,Scheinberg L,et al.New diagnostic criteria for multiple sclerosis:guidelines for research protocols[J].Ann Neurol,1983,13(3):227-231.
[10]Kurtzke JF.Rating neurologic impairment in multiple sclerosis:an expanded disability status scale(EDSS)[J].Neurology,1983,33(11):1444-1452.
[11]Mak A,Cheung MW,Fu EH,et al.Meta-analysis in medicine:an introduction[J].Int J Rheum Dis,2010,13(2):101-104.
[12]Higgins JP,Thompson SG,Decks JJ,et a1.Measuring inconsistency in meta-analyses[J].BMJ,2003,327(7414):557-560.
[13]Cohen JA,Barkhof F,Comi G,et al.Oral fingolimod or intramuscular interferon for relapsing multiple sclerosis[J].N Engl J Med,2010,362(5):402-415.
[14]Kappos L,Antel J,Comi G,et al.Oral fingolimod(FTY720)for relapsing multiple sclerosis[J].N Engl J Med,2006,355(11):1124-1140.
[15]Kappos L,Radue EW,O'Connor P,et al.A placebo-controlled trial of oral fingolimod in relapsing multiple sclerosis[J].N Engl J Med,2010,362(5):387-401.
[16]Chun J,Hartung HP.Mechanism of action of oral fingolimod(FTY720)in multiple sclerosis[J].Clin Neuropharmacol,2010,33:91-101.
[17]Gonzalez-Cabrera PJ,Cahalan SM,Nguyen N,et al.S1P(1)receptor modulation with cyclical recovery from lymphopeniaameliorates mouse model of multiple sclerosis[J].Mol Pharmacol,2012,81:166-174.
[18]Schulz KF,Altman DG,Moher D,et al.CONSORT 2010 statement:updated guidelines for reporting parallel group randomised trials[J].Int J Surg,2011,9(8):672-677.

