丙泊酚对肝缺血再灌注大鼠肺损伤及PI3K/Akt通路的影响*
高伟忠, 但 伶, 田泽丹, 张 殷, 黄 燕
(重庆医科大学附属第二医院麻醉科,重庆400010)
肝脏缺血再灌注(ischemia reperfusion)损伤是肝脏外科常见的病理生理过程,在中央型肝肿瘤及肝移植手术中常采取结扎肝蒂的方法来阻断肝血流以减少术中出血,研究发现当血供恢复后不仅可引起肝脏原发功能低下,还因为炎性因子和凋亡因子的释放、钙超载及自由基的产生等引起再灌注损伤,导致远隔器官如脑、肺、心脏等的功能受损[1]。
丙泊酚(propofol)是一种常用的静脉麻醉药,研究发现其能通过灭活氧自由基、抗脂质过氧化及抗炎在缺血再灌注损伤中发挥保护作用[2];研究还发现丙泊酚在肝缺血再灌注所致的心脑损伤中可通过磷脂酰肌醇3-激酶/蛋白激酶B(phosphatidylinositol 3-kinase/protein kinase B,PI3K/Akt)信号通路发挥保护作用[3-4]。丙泊酚能否通过PI3K/Akt信号通路在肝缺血再灌注所致的肺损伤中发挥保护作用,尚未见报道。本实验拟建立大鼠肝缺血再灌注肺损伤模型,通过观察丙泊酚对大鼠全肝缺血再灌注肺损伤PI3K/Akt信号通路活化的影响,来探讨丙泊酚在全肝缺血再灌注肺损伤中的作用机制。
材料和方法
1 动物与试剂
清洁级SD大鼠66只,雌雄不限,体重250~280 g,由重庆医科大学动物饲养中心提供。兔抗鼠Akt多克隆抗体、兔抗鼠p-Akt多克隆抗体、兔抗鼠Bcl-2多克隆抗体和兔抗鼠 β-actin单克隆抗体(Bioworld),Annexin V-FITC细胞凋亡检测试剂盒(碧云天生物技术研究所),FACS Calibur流式细胞仪(BD),1% 丙泊酚注射液 (Astra Zeneca),PI3K阻断剂wortmannin(Proteintech)。
2 实验分组和模型制备
大鼠随机分成4组,假手术组(S组,n=6)、肝缺血再灌注组(IR组,n=24)、丙泊酚组(P组,n=24)和丙泊酚+PI3K阻断剂wortmannin组(P+W组,n=12),IR 组和 P 组按再灌注 1 h、3 h、6 h、12 h分为4个亚组,P+W 组按再灌注3 h、6 h分为2个亚组。参照 Pringle's等[5]建立全肝缺血再灌注模型,术前大鼠禁食12 h,自由饮水,10%水合氯醛4 mL/kg行腹腔注射麻醉,S组仅解剖肝门,不结扎;IR组采用结扎肝蒂全肝缺血30 min,再灌注的方法建立大鼠肝缺血再灌注模型;P组缺血前10 min经尾静脉缓慢注射负荷剂量的丙泊酚20 mg·kg-1,再以20 mg·kg-1·h-1的速度尾静脉泵注直至处死,余同IR组;P+W组缺血前经尾静脉注射 PI3K阻断剂Wortmannin 15 μg·kg-1[6],余同 P 组。
3 标本采集
S组于分离肝门后1 h时、IR组和 P组于再灌注 1 h、3 h、6 h、12 h 时、P+W 组于再灌注 3 h、6 h时处死大鼠,开胸迅速取右肺组织行细胞凋亡检测;左肺取部分肺组织置于-80℃冰箱低温保存,用Western blotting检测蛋白变化,剩余肺组织用10%多聚甲醛固定,HE染色,光镜下观察病理变化。
4 指标测定
4.1 Western blotting测定各组肺组织总 Akt(t-Akt)、磷酸化 Akt(p-Akt)和 Bcl-2蛋白的表达从-80℃冰箱中取出肺组织,用液氮研磨至粉末,加蛋白裂解液裂解30 min后,4℃ 15 000 r/min离心15 min,取上清液,Bradford比色法测定蛋白质浓度,分装于-80℃ 冰箱保存备用。以20 μg蛋白上样量进行聚丙烯酰胺凝胶电泳(SDS-PAGE),半干法电转至PVDF膜,5% 的脱脂奶粉室温封闭1 h,Ⅰ抗(兔抗鼠 anti-t-Akt、anti-p-Akt和 anti-Bcl-2多克隆抗体1∶1 500)过夜,Ⅱ抗(HRP 标记山羊抗兔抗体1∶20 000)37℃ 反应1 h,并以兔抗鼠β-actin(1∶500)单克隆抗体同上操作,作为上样对照。加入ECL(Pierce)化学发光试剂,Bio-Rad凝胶成像仪显影成像,Bio-Rad图像分析系统进行蛋白条带的灰度值测定,以反映 t-Akt、p-Akt和 Bcl-2蛋白的表达 。
4.2 Annexin V-FITC/PI荧光双染色法检测肺细胞凋亡 新鲜肺组织用冷磷酸盐缓冲液(PBS)清洗后,剪碎,300目铜网过滤制成细胞悬液,调整各管的细胞数约为1×109/L,再取肺细胞(2~5)×105个,以PBS液清洗,500 r/min离心1 min,沉淀肺细胞,弃去上清液,加入结合缓冲液195 μL,悬浮肺细胞,加入Annexin V 5 μL,混匀后避光放置 10 min,然后 PBS液清洗,500 r/min离心 1 min,沉淀肺细胞,以 190 μL结合缓冲液重悬细胞,加入10 μL碘化丙啶(PI),混匀后上机,行流式细胞术检测,用CellQuest Pro软件分析细胞凋亡率[7]。以Annexin V为横轴,PI为纵轴:其中左上象限为机械性损伤细胞,右上象限为晚期凋亡细胞或坏死细胞,左下象限为正常细胞,右下象限为早期凋亡细胞。
4.3 HE染色观察肺组织病理学变化 肺组织用10% 多聚甲醛固定、石蜡包埋切片后行HE染色,光镜下观察肺组织病理变化。
5 统计学处理
采用SPSS 18.0软件分析,计量资料以均数±标准差(mean±SD)表示,多组间比较采用单因素方差分析,以P<0.05为差异有统计学意义。
结 果
1 肺组织t-Akt、p-Akt及Bcl-2蛋白表达
与S组比较,IR组、P组和P+W组肺组织中p-Akt和Bcl-2蛋白的表达水平升高(P<0.05);与 IR组比较,P组p-Akt和Bcl-2蛋白表达水平升高(P<0.05),P+W 组 p-Akt和 Bcl-2蛋白表达水平差异无统计学意义(P>0.05);与 P组比较,P+W 组 p-Akt和Bcl-2蛋白表达水平下降(P<0.05);各组中t-Akt蛋白表达差异无统计学意义(P>0.05),见图1~3和表1。
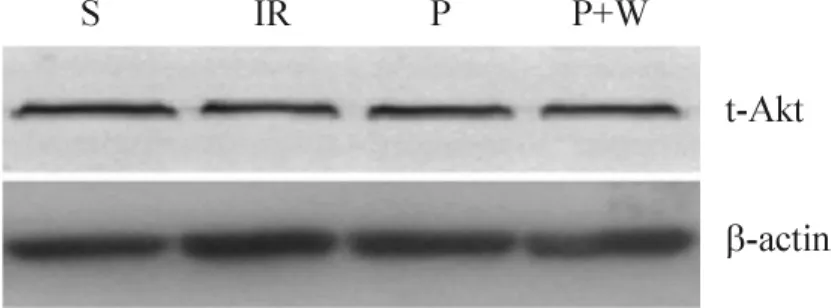
Figure 1.Expression of t-Akt protein in lung tissues 3 h after hepatic ischemia reperfusion in each group detected by Western blotting.图1 肝缺血再灌注3 h肺组织t-Akt的表达

Figure 2.Expression of p-Akt protein in lung tissues 1,3,6 and 12 h after hepatic ischemia reperfusion in each group detected by Western blotting.图2 肝缺血再灌注1、3、6和12 h肺组织p-Akt的表达

Figure 3.Expression of Bcl-2 protein in lung tissues 1,3,6 and 12 h after hepatic ischemia reperfusion in each group detected by Western blotting.图3 肝缺血再灌注1、3、6和12 h肺组织Bcl-2的表达

表1 不同时点t-Akt、p-Akt和Bcl-2蛋白的表达水平Table 1.Expression of t-Akt,p-Akt and Bcl-2 proteins in lung tissues at different time points(mean±SD.n=6)
2 肺组织细胞凋亡情况
与S组比较,IR组、P组和P+W组肺细胞凋亡率升高(P<0.05),再灌注3 h时肺细胞凋亡率最高;与 IR组比较,P组肺细胞凋亡率降低(P<0.05),P+W组肺细胞凋亡率差异无统计学意义(P>0.05);与 P组比较,P+W 组肺细胞凋亡率升高(P<0.05),见图4和表2。

Figure 4.Representative results of lung cell apoptotic rate in all groups.A:S group;B:IR group;C:P group;D:P+W group.图4 各组肺细胞凋亡情况比较

表2 不同时点肺细胞凋亡率的比较Table 2.Apoptotic rates of lung cells induced by hepatic ischemia reperfusion at different time points(mean±SD.n=6)
3 肺组织病理学改变
S组肺组织结构正常;IR组肺间质水肿,肺泡壁破坏,肺泡内可见炎性细胞浸润伴出血,尤以再灌注6 h时明显,P组肺组织损伤较IR组轻,肺泡壁增宽,肺泡腔出血较少,偶见炎症细胞;而P+W组肺组织损伤较P组重,和IR组无明显差别,见图5。

Figure 5.The lung tissue pathological changes(HE staining,×200).A:S group;B:IR group;C:P group;D:P+W group.图5 各组肺组织病理学变化
讨 论
本研究参照 Pringle's法,通过结扎大鼠肝蒂的方法来建立肝缺血再灌注肺损伤模型,大鼠肝缺血再灌注后光镜下见肺组织结构破坏严重,肺泡内炎症细胞浸润,肺泡腔出血,检测肺细胞凋亡率升高,提示大鼠肝缺血再灌注肺损伤模型制备成功。根据预实验再灌注3 h时肺细胞凋亡率最高,6 h时肺组织病理学损伤最重,故P+W组取再灌注3 h和6 h时检测相关指标。
细胞凋亡是由基因调控的程序性、主动性细胞死亡,表现为凋亡基因的表达和相关信号转导通路的激活,PI3K/Akt信号通路是近年来研究的一条重要的抗凋亡信号通路,PI3K是一种胞内磷脂酰肌醇激酶,当受到来自G蛋白偶联受体或酪氨酸激酶的信号后,PI3K的p110亚基与 p85亚基结合而活化Akt,激活的 Akt能够向细胞质和细胞核内转运,并与相应部位的底物蛋白发生作用,使底物蛋白特定部位的丝、苏氨酸磷酸化形成 p-Akt,p-Akt通过对下游因子bcl-2、bad及 bax等的调节在细胞内发挥抗凋亡、促进细胞生存的调控作用[8-9]。其中,bcl-2是抗凋亡家族中最重要的抗凋亡基因,研究发现其编码的Bcl-2蛋白通过阻止线粒体通透性转换孔的开放、对抗脂质过氧化及减轻细胞内钙超载等发挥抗损伤和抑制细胞凋亡的作用[3,10];研究还发现Bcl-2蛋白能通过阻止线粒体内细胞色素 C的释放、抑制caspase-3的激活来抑制细胞凋亡[11]。
本研究中P组较IR组p-Akt和Bcl-2蛋白表达水平增高,肺细胞凋亡率降低,肺组织病理学损伤减轻,说明丙泊酚对大鼠肝缺血再灌注诱发的肺损伤有抑制作用,这与 Wang等[4]的研究结果丙泊酚能通过PI3K/Akt信号通路抑制组织缺血再灌注后细胞凋亡,从而保护组织器官相一致;P+W组在使用特异性阻断剂 wortmannin阻断 PI3K/Akt信号通路后,p-Akt和Bcl-2蛋白表达水平明显下降,肺细胞凋亡率增高,肺组织病理学损伤加重,说明P+W组丙泊酚的保护作用减弱;进而说明丙泊酚减轻大鼠肝缺血再灌注诱发的肺损伤与 PI3K/Akt信号通路激活,上调 p-Akt和Bcl-2蛋白表达,下调肺细胞凋亡有关,而使用PI3K特异性阻断剂阻断PI3K/Akt信号通路则丙泊酚的保护作用被抑制。
丙泊酚作为烷基酚类的短效静脉麻醉药因具有麻醉诱导起效快、苏醒迅速且功能恢复完善的特点而广泛应用于临床,我们前期的研究发现丙泊酚可以抑制 AIF和 p38 MAPK信号通路的激活,下调NF-κB和iNOS的表达,从而减少炎症因子的释放,减轻炎症反应保护组织器官[12-13];研究还发现丙泊酚能通过灭活氧自由基和减轻钙超载的作用减轻缺血再灌注对机体的损伤[2,14-15]。最新研究认为丙泊酚的药理机制是通过激活 GABA(γ-氨基丁酸)受体,产生镇静催眠作用,大剂量时使 GABA受体脱敏感,从而抑制中枢神经系统,发挥镇静催眠效应,作为GABA受体之一的GABAB受体属于G蛋白偶联受体家族,当GABAB受体受到刺激激活后,可通过G蛋白偶联受体信号活化 PI3K,从而激活 PI3K/Akt信号通路,产生生物学效应[16-18]。
综上所述,我们得出丙泊酚可以减轻大鼠肝缺血再灌注诱发的肺损伤,该作用与PI3K/Akt信号通路的激活进而下调细胞凋亡有关,通过对丙泊酚作用机制的深入研究,可能为临床应用提供新的理论依据。
[1] Miranda LE,Capellini VK,Reis GS,et al.Effects of partial liver ischemia followed by global liver reperfusion on the remote tissue expression of nitric oxide synthase:lungs and kidneys[J].Transplant Proc,2010,42(5):1557-1562.
[2] Yuzbasioglu MF,Aykas A,Kurutas EB,et al.Protective effects of propofol against ischemia reperfusion injury in rat kidneys[J].Ren Fail,2010,32(5):578-583.
[3] 芦 滨,赵建力,牛栓成,等.异丙酚对肝缺血再灌注大鼠心肌损伤的影响及PI3K/Akt信号通路在其中的作用[J].中华麻醉学杂志,2010,30(10):1250-1253.
[4] Wang HY,Wang GL,Yu YH,et al.The role of phosphpinositide-3-kinase/Akt pathway in propofol-induced postconditioning against focal cerebral ischemia-reperfusion injury in rats[J].Brain Res,2009,1297:177-184.
[5] Maehara S,Adachi E,Shimada M,et al.Clinical usefulness of biliary scope for Pringle's maneuver in laparoscopic hepatectomy[J].J Am Coll Surg,2007,205(6):816-818.
[6] Wang Y,Ahmad N,Wang B,et al.Chronic preconditioning:a novel approach for cardiac protection [J].Am J Physiol Heart Circ Physiol,2007,292(5):H2300-H2304.
[7] 陆远强,黄卫东,顾琳慧,等.高渗氯化钠溶液复苏抑制失血性休克大鼠肺细胞凋亡的初步研究[J].中华危重症医学杂志:电子版,2008,1(2):79-83.
[8] Wang B,Shravah J,Luo H,et al.Propofol protects against hydrogen peroxide-induced injury in cardiac H9c2 cells via Akt activation and Bcl-2 up-regulation[J].Biochem Biophys Res Commun,2009,389(1):105-111.
[9] Song JQ,Teng X,Cai Y,et al.Activation of Akt/GSK-3β signaling pathway is involved in intermedin1-53protection against myocardial apoptosis induced by ischemia/reperfusion[J].Apoptosis,2009,14(11):1299-1306.
[10] 祝海洲,詹自力,何卫阳,等.地塞米松和川芎嗪对肾缺血再灌注时c-Fos、Bcl-2、ICAM-1蛋白表达的影响[J].中国病理生理杂志,2004,20(5):893-895.
[11] Park SE,Park C,Kim SH,et al.Korean red ginseng extract induces apoptosis and decreases telomerase activity in human leukemia cells[J].J Ethnopharmacol,2009,121(2):304-312.
[12] 邓必高,但 伶,曹慧灵.异丙酚对大鼠内毒素脑损伤AIF表达和细胞凋亡的影响[J].中国病理生理杂志,2012,28(4):746-750.
[13] 曹慧灵,但 伶,邓必高.异丙酚抑制脂多糖致大鼠脑损伤时p38 MAPK的活化[J].中国病理生理杂志,2011,27(8):1639-1642.
[14] Jin YC,Kim W,Ha YM,et al.Propofol limits rat myocardial ischemia and reperfusion injury with an associated reduction in apoptotic cell death in vivo[J].Vasc Pharmacol,2009,50(1-2):71-77.
[15] 杨 舜,裴 淩.异丙酚和氯胺酮减轻大鼠肾缺血再灌注损伤[J].中国病理生理杂志,2010,26(1):177-180.
[16] Stewart DS,Savechenkov PY,Dostalova Z,et al.p-(4-Azipentyl)propofol:a potent photoreactive general anesthetic derivative of propofol[J].J Med Chem,2011,54(23):8124-8135.
[17] Leon I,Cocinero EJ,Millán J,et al.Exploring microsolvation of the anesthetic propofol[J].Phys Chem Chen Phys,2012,14(13):4398-4409.
[18] Yang B,Wang BF,Lai MJ,et al.Differential involvement of GABAAand GABABreceptors in propofol self-administration in rats[J].Acta Pharmacol Sin,2011,32(12):1460-1465.

