三七不同药用部位聚炔类成分的GC-MS分析研究
周建良, 陆静娴, 谭春梅, 郑 成, 陈碧莲
(浙江省食品药品检验研究院,浙江杭州310004)
三七为五加科植物三七Panax notoginseng(Burk.)F.H.Chen的干燥根,主产于云南、广西及四川等地,是我国特有的名贵中药材,具有散瘀止血、消肿止痛之功效。三七含有多种化学成分,主要有效成分之一是皂苷类成分。此外,三七还含有其他药用成分,如三七素、黄酮、挥发油、氨基酸、植物甾醇等[1-2]。近年来,有文献报道三七的脂溶性成分对结肠癌细胞株及部分革兰氏阳性菌有强烈的抑制活性,经分离纯化并鉴定了两个聚乙炔醇类化合物,人参炔醇 (panaxynol)和人参环氧炔醇 (panaxydol)[1]。人参炔醇可抑制血管紧张素II诱导的血管收缩,降低自发性高血压大鼠平均脉动压,同时还具有抗炎及抗血小板凝聚活性;另人参炔醇具有抗癌、抑菌、镇静、镇痛、降压、抗炎和神经细胞保护等多种作用[3-5]。
目前,三七水溶性皂苷类和氨基酸成分的分析研究较多[6-11],但少有对聚炔类成分分析的研究报道[12],鉴于该类成分的特殊活性,本研究采用气质联用 (GC-MS)方法对12批三七药材及不同药用部位中的聚炔类成分进行分析和测定。
1 仪器与试药
1.1 仪器 Agilent 7000 GC/MS Triple Quad气质联用仪 (气相系统为7890A GC System)。
1.2 试药 环己烷为分析纯;对照品正十八烷(octadecane)购自中国食品药品检定研究院;三七药材及不同药用部位购自亳州、文山药材市场,经浙江省食品药品检验研究院郭增喜主任中药师鉴定均属于五加科植物三七Panax notoginseng(Burk.)F.H.Chen,样品来源见表1。
2 方法与结果
2.1 样品制备 取三七药材 (或不同药用部位)粉末约1 g,精密称定,精密加入环己烷25 mL,正十八烷内标溶液 (40.25μg/mL,溶剂环己烷)1.0 mL,85℃加热回流30 min,滤过,取续滤液进行GC-MS分析。
2.2 GC-MS分析条件 HP-5MS毛细管柱(30 m×0.25mm×0.25μm);初始柱温60℃,保持3 min,再以10℃/min的速率升至250℃,保持8 min;载气为氦气;体积流量1.2 mL/min;进样口温度250℃;分流模式为不分流。MS条件:离子源为EI;电离电压70 eV;质谱质量扫描范围为50~600 amu;溶剂延迟5 min。

表1 三七药材及药用部位样品来源Tab.1 Sam p les collection of Panax notoginseng
2.3 三七聚炔类成分结构解析 在上述GC-MS色谱分离条件下,对三七药材不同药用部位 (主根、花、剪口、筋条、茎叶、须根)进行分析。将GCMS所得的质谱信息经NIST08数据库检索对照分析,鉴定了3个聚炔类成分,保留时间15.1 min的色谱峰为 methyl 5,7-hexadecadiynoate,19.7 min为人参炔醇,21.1 min为人参环氧炔醇,保留时间17.3 min的色谱峰为内标峰正十八烷,见表2。代表性色谱图见图1。
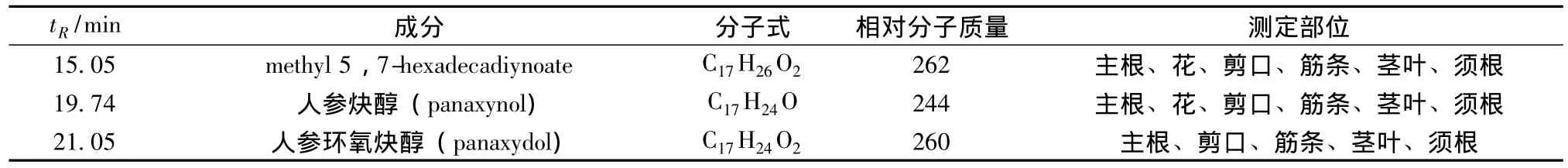
表2 三七药材中鉴定的聚炔类成分Tab.2 Polyacetylenes identified from different parts of Panax notoginseng
2.4 三七聚炔类成分相对定量分析 由于缺乏聚炔类成分的对照品,采用定量加入内标溶液,比较样品峰面积与内标峰面积比值的大小表征样品中methyl 5,7-hexadecadiynoate、人参炔醇和人参环氧炔醇量的相对高低。定量分析时,采用丰度高且具有特征性的碎片离子作为定量离子,其中人参炔醇和人参环氧炔醇为m/z91.1,methyl 5,7-hexadecadiynoate为m/z205.2,内标峰正十八烷为m/z 71.1,内标出峰位置处未出现干扰峰,见图2。在精密度试验中,对同一份样品重复进样分析6次,内标峰面积的RSD为2.1%(n=6),表明精密度良好。
三七主根、花、剪口、筋条、茎叶和须根等三七不同药用部位中聚炔类成分的相对含有量结果见图3[相对含有量=样品峰面积/内标峰面积/称样量 (折算至每克的含有量)]。结果表明methyl 5,7-hexadecadiynoate、人参炔醇和人参环氧炔醇在三七不同药用部位中有较大差异。
3 讨论
本实验从三七环己烷提取物中鉴定了3个聚炔类成分,其中人参炔醇和人参环氧炔醇为主要的聚炔类成分。由于三七聚炔类成分不稳定,加上对照品缺乏,本实验采用内标校正的相对含有量测定法对该类成分进行了定量测定,其结果在同一操作下具有可比性。
测定结果表明,3个聚炔类成分的总含有量在三七筋条、3年生主根、花、剪口中较高,在茎叶中较低;主根中,三七3年生的总含有量最高,而头数越多,含有量越低;三七花中的人参炔醇含有量很高,但人参环氧炔醇几乎未能检测到。
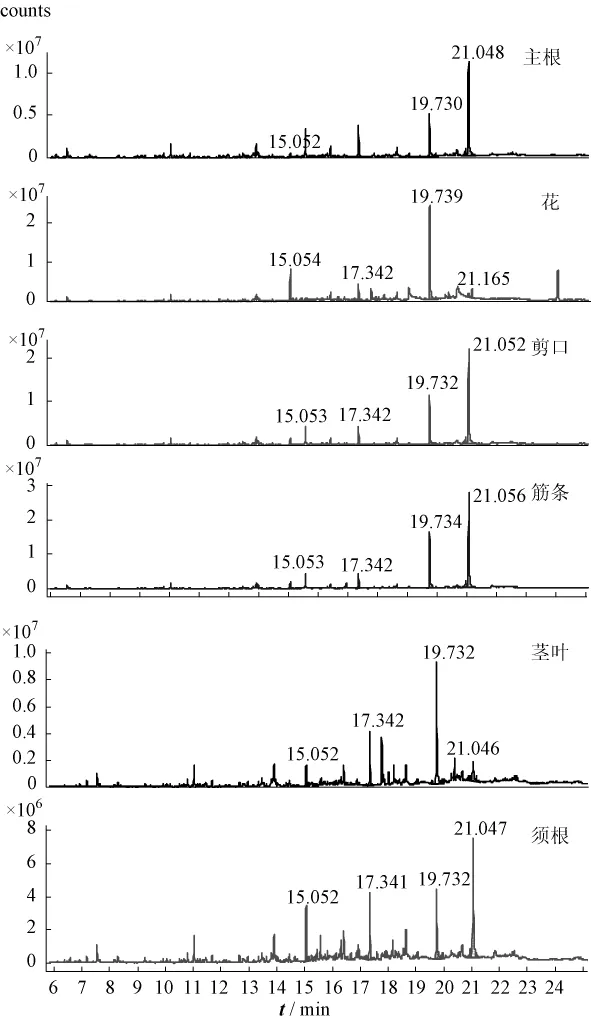
图1 三七药材不同药用部位的GC-MS总离子流代表性图谱Fig.1 Representative GC-M S total ion chromatograms(TICs)of different parts of Panax notoginseng
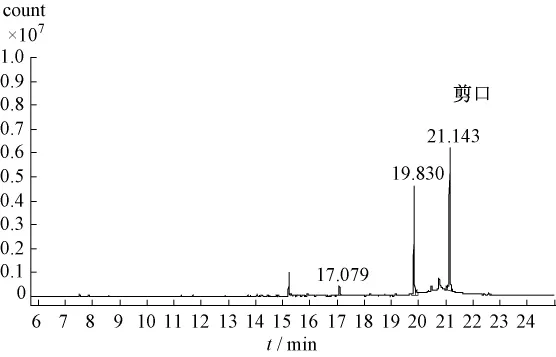
图2 不加内标的样品GC-MS总离子流代表性图谱 (文山剪口)Fig.2 Representative GC-MS TIC of Panax notoginseng sample w ithout internal standard(W ensan Jiankou)
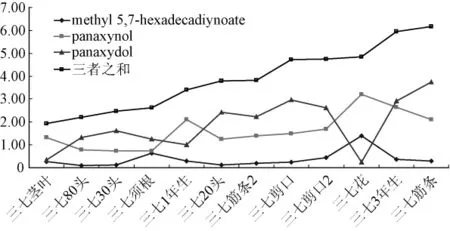
图3 三七不同药用部位聚炔类成分的相对含有量及其总和Fig.3 Relative amount of polyacetylenes from different parts of Panax notoginseng
[1]林 琦,赵 霞,刘 鹏,等.三七脂溶性化学成分的研究 [J].中草药,2002,33(6):490-492.
[2]刘 刚,鲍建材,郑友兰,等.三七的化学成分研究进展[J].人参研究,2004(2):10-18.
[3]段贤春,汪永忠,周 安,等.三七中人参炔醇的提取、分离和鉴定 [J].安徽中医学院学报,2008,27(2):50-52.
[4]聂宝明,陆 阳,陈泽乃.天然聚乙炔醇类研究进展[J].中草药,2002,33(11):1050-1053.
[5]段贤春,汪永忠,居 靖,等.人参炔醇研究进展 [J].安徽医药,2008,12(1):1-3.
[6]乔春玲,官金梅,丁艳芬,等.不同产地三七皂苷的HPLC指纹图谱与含量的比较研究 [J].现代中药研究与实践,2011,25(5):25-27.
[7]万晓青,夏伯侯,楼招欢,等.三七不同炮制品中皂苷类成分的含量比较 [J].中华中医药杂志,2011,26(4):841-843.
[8]黄天卫,张文斌,孙玉琴,等.不同轮作年限三七总皂苷含量分析[J].现代中药研究与实践,2011,25(3):3-4.
[9]李汶罡,赵修华,祖元刚.水溶性三七总皂苷制备与表征[J].植物研究,2011,31(4):503-507.
[10]陈中坚,孙玉琴,董婷霞,等.不同产地三七的氨基酸含量比较 [J].中药材,2003,26(2):86-88.
[11]李 聪,张 红,马 衡,等.三七中氨基酸的分析[J].氨基酸杂志,1992(4):45.
[12]居 靖,朱满洲,章俊如,等.超临界CO2萃取三七脂溶性成分及其GC-MS分析 [J].中国医院药学杂志,2007,27(8):1076-1078.

