透骨草提取物对人肝癌SMMC-7721细胞p53和PUMA蛋白表达的影响*
姜春雨,曾常茜
(1.吉林省图们市石岘镇中心卫生院药剂科,吉林 延边 133101; 2.大连大学医学院·辽宁省生物有机重点实验室,辽宁 大连 116622)
对于大多数肝癌患者,化学治疗仍为主要的治疗手段。然而目前临床应用的抗肝癌药物在杀伤肝癌细胞的同时,对某些正常的细胞也有一定程度的损害[1-2]。因此,寻找对肝癌疗效好且毒副作用小的药物成为目前的重要课题。透骨草 Phryma leptostachya L.var.asiatica Hara为透骨草科植物的干燥全草入药,具有清热解表、活血消肿作用[3]。本研究中观察了透骨草提取物对人肝癌SMMC-7721细胞形态的影响,并通过检测透骨草提取物对SMMC-7721细胞p53和p53上调凋亡调控因子(PUMA)蛋白表达的影响,进一步探讨透骨草提取物诱导SMMC-7721细胞凋亡的分子机制,旨在为透骨草抗肝癌作用的研究提供实验室依据。
1 材料与方法
1.1 仪器与试药
人肝癌SMMC-7721细胞,由吉林省肿瘤研究所提供;鼠抗人p53抗体和鼠抗人PUMA抗体(编号为4976)购自Cell Signaling Technology公司,通用型SP试剂盒(批号为812251A)、DAB显色试剂盒(批号为K107715A)购自福州迈新生物技术公司。RPMI 1640(批号为307964)、小牛血清和胰蛋白酶为美国Gibco公司产品;MTT和DMSO为Sigma公司产品;药物采自辽宁金州大黑山,经王心毓先生鉴定为透骨草科植物。BB16UV型CO2培养箱,德国Heraeus公司;CKX41型倒置显微镜(日本Olympus公司)。
1.2 方法
透骨草提取物制备方法:采取加热回流提取法。取干燥透骨草50 g,加8倍量75%乙醇,提取2 h,过滤,滤液水浴浓缩成干膏。
细胞培养:SMMC-7721细胞使用RPMI 1640培养基培养,应用时加入青霉素100 U/mL、链霉素100 mg/L和含10%灭活的小牛血清,置37℃及5%CO2培养箱中培养。
倒置显微镜观察检测SMMC-7721细胞形态:选取处于对数生长期且生长良好的SMMC-7721细胞,将其接种于6孔细胞培养板中,每孔2.0 mL,37℃ 5%CO2孵育12 h。弃去孔中培养液,磷酸盐缓冲液(PBS)洗涤2次。试验组加入终质量浓度为40.91 μg/mL 的透骨草提取物(IC50)2.0 mL,对照组加入等体积的RPMI-1640细胞培养液,继续孵育24 h,观察倒置显微镜下活细胞形态变化情况。
免疫组化方法检测SMMC-7721细胞p53和PUMA蛋白的表达:按试剂盒说明进行操作。将对数生长期的SMMC-7721细胞以1.0×105个/mL细胞加入培养瓶,37℃ 5%CO2培养24 h,待细胞贴壁后,加入终浓度为40.91 μg/mL的透骨草提取物,另设RPMI 1640培养液作为对照。继续培养96 h,弃去培养液,PBS洗涤2次,消化并收集细胞,用PBS稀释SMMC-7721细胞为1.0×106个 /mL。SMMC -7721细胞涂片,丙酮固定 20 s,PBS冲洗2 min×3次,滴加内源性过氧化物酶阻断剂,室温孵育15 min,PBS冲洗3 min;滴加正常非免疫动物血清,室温孵育15 min,弃血清,分别滴加鼠抗人鼠抗人p53抗体、鼠抗人PUMA抗体,37℃孵育2 h,PBS冲洗2 min×3次。滴加生物素标记二抗,室温孵育15 min,PBS冲洗2 min×3次,滴加链霉菌抗生物素-过氧化物酶溶液,室温孵育10 min,PBS冲洗2 min×3次。加DAB底物混合液,镜下观察显色,自来水终止显色。苏木素复染,封片,置显微镜下观察。在显微镜下随机计数200个细胞,细胞核或细胞浆出现棕色判断为阳性细胞,无棕色染色者为阴性细胞,计算阳性细胞占所有细胞的比例。
1.3 统计学处理
2 结果
2.1 对SMMC-7721细胞形态的影响
倒置显微镜下观察可见,对照组SMMC-7721细胞贴壁生长,密集排列、形态呈梭形或多边形,胞体透亮折光性好。40.91 μg/mL透骨草提取物作用于 SMMC-7721细胞24 h后,细胞胞体积明显缩小,形态不规则,轮廓不清晰,细胞皱缩变形,细胞脱壁增加。
2.2 对SMMC-7721细胞p53和PUMA蛋白表达的影响
免疫组化方法观察结果显示,未用透骨草提取物处理的对照组SMMC-7721细胞p53蛋白低表达,细胞核着棕黄色的细胞量少,经40.91 μg/mL透骨草提取物处理后的 SMMC-7721细胞p53蛋白表达明显增高,细胞核着棕黄色的细胞量多,经统计学处理差异显著(P<0.01);未用透骨草提取物处理的对照组SMMC-7721细胞PUMA蛋白低表达,细胞浆着棕黄色的细胞量少,经40.91 μg/mL透骨草提取物处理后的 SMMC-7721细胞PUMA蛋白表达明显增高,细胞浆着棕黄色的细胞量多,经统计学处理差异显著(P<0.01)。见表1。
表1 免疫组化法检测SMMC-7721细胞p53和PUMA蛋白表达结果(±s,n=3)
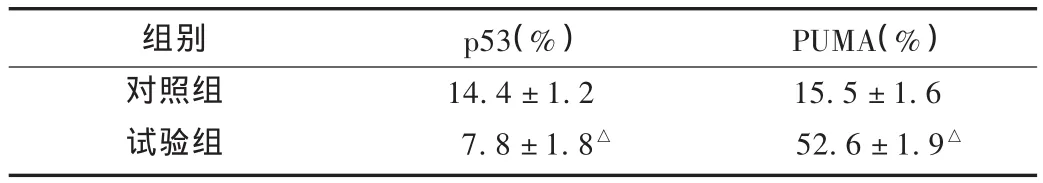
表1 免疫组化法检测SMMC-7721细胞p53和PUMA蛋白表达结果(±s,n=3)
注:与对照组比较,△P <0.01。
组别对照组试验组p53(%)14.4±1.2 7.8±1.8△PUMA(%)15.5±1.6 52.6 ±1.9△
3 讨论
笔者的前期研究发现,透骨草提取物对人卵巢癌SKOV3细胞、人乳腺癌 MCF-7细胞、人宫颈癌胞 Hela细胞、人肝癌HepG-2细胞、人肺癌A549细胞增殖有显著的抑制作用[4]。本研究中用倒置显微镜下观察发现,40.91 μg/mL 透 骨草提取物作用后的SMMC-7721细胞与对照组相比,细胞胞体积明显缩小,形态不规则,细胞皱缩变形,细胞脱壁增加,从形态学上证明透骨草提取物可诱导SMMC-7721细胞凋亡。
p53基因是重要的肿瘤抑制基因,能影响多种细胞内信号转导通路,抑制细胞增殖活化、诱导细胞凋亡、抑制某些信号转导以及抑制血管新生等[5]。本研究中通过免疫组化方法检测发现40.91 μg/mL透骨草提取物处理的SMMC-7721细胞24 h后,p53蛋白表达显著增加,表明透骨草提取物可能通过上调p53蛋白表达诱导SMMC-7721细胞凋亡。
p53基因的抗肿瘤作用有赖于其激活下游靶基因,并诱导细胞凋亡或细胞周期阻滞。PUMA是Bcl-2蛋白家族中促凋亡成员之一,因其含有一个BH3结构域,亦称为BH3仅有蛋白,是细胞凋亡的重要启动子。研究发现,PUMA是p53诱导细胞凋亡或细胞周期阻滞的靶基因[6-7],p53的结合位点位于PUMA的上游启动序列中,感应到凋亡刺激信号后,p53会结合其位于上游启动序列中的结合位点,从而诱发PUMA转录及其蛋白表达[8]。为了进一步探究透骨草提取诱导SMMC-7721细胞凋亡是否与p53下游因子PUMA的表达相关,本研究中通过免疫组化方法检测发现,40.91 μg/mL透骨草提取物处理的 SMMC-7721细胞24 h后,PUMA蛋白表达显著增加,表明透骨草提取物可能通过上调PUMA蛋白表达诱导SMMC-7721细胞凋亡。鉴于PUMA对p53的依赖性,推测透骨草提取物诱导SMMC-7721细胞凋亡的机制可能与上调p53,进而上调PUMA蛋白表达有关。P53/PUMA通路诱导细胞凋亡是由多个信号转导蛋白参与的复杂过程,相关分子机制有待进一步更深入的研究。
[1]Trotti A,Colevas AD,Setser A,et al.CTCAE v3.0:development of a comprehensive grading system for the adverse effects of cancer treatment[J].Semin Radiat Oncol,2003,13(3):176 - 181.
[2]Jemal A,Siegel R,Ward E,et al.Cancer statistics,CA:a cancer[J].J Clin,2008,58(2):71 - 96.
[3]高 松.辽南地区药用植物图鉴[M].北京:科学出版社,2008:196.
[4]曾常茜,高 松,沈 阳,等.透骨草提取物对肿瘤细胞体外增殖的影响[J].辽宁中医杂志,2009,36(11):1 952-1 954.
[5]Wang JL,Jiao SC,Hu Y,et al.Effect of Recombinant Human Adenovirus p53 Combined with Cisplatin on the Expression of Human Lung Adenocarcinoma A549 Cell Gene[J].Acta Acad Med Sin,2010,32(4):383 - 388.
[6]Liu XH,Zhang XF,Wang YL.Inhibitive effect of 3 -bromopyruvic acid on human breast cancer MCF-7 cells involves cell cycle arrest and apoptotic induction[J].Chinese Medical Journal,2009,122(14):1 681 - 1 685.
[7]Peng QP,Liang HJ,Zhou Q,et al.Expression of hexokinase- Ⅱgene in human colon cancer cells and the therapeutic significance of inhibition thereof[J].Zhonghua Yixue Zazhi,2007,87(15):1 058 -1 062.
[8]Yu J,Yue W,Wu B,et al.PUMA Sensitizes Lung Cancer Cells to Chemotherapeutic Agents and Irradiation[J].Clin Cancer Res,2006,12(9):2 928 -2 936.

