羧甲基化壳聚糖季铵盐与牛血清白蛋白的相互作用研究
李小芳,冯小强*,杨 声,王廷璞
1天水师范学院 生化学院,天水 741001;2定西师范高等专科学校,定西 743000
血清白蛋白可以与许多内源和外源性化合物结合,药物要通过血浆的储运,才能到达受体部位产生药效。因此,研究药物分子与蛋白质间的相互作用具有重要的理论及实际意义[1,2]。壳聚糖作为一种天然的聚阳离子多糖,具有多种独特的生物活性和功能,如活化淋巴细胞、增强机体免疫力、抗菌抑菌[3,4]、止血[5]、降低血酯和胆固醇以及抗肿瘤[6]等生物活性。在前期工作中,笔者利用壳聚糖分子结构的特性,制备了羧甲基化壳聚糖季铵盐(CMCQA),发现 CMCQA 对常见细菌 St.aureus、E.coli和真菌A.niger具有很好的抑制作用,且对E.coli和St.aureus的最小抑菌浓度值较壳聚糖降低了 5倍[7],CMCQA有望在医学领域有更为广泛的应用。有关CMCQA与BSA之间相互作用的研究,目前尚未见报道。本实验采用光谱法研究了CMCQA与BSA的作用机理,该研究为生命科学研究提供有用的信息。
1 实验部分
1.1 材料与仪器
CMCQA(制备方法参见文献[7],羧甲基取代度为0.62,季铵盐取代度为0.54);BSA(北京奥博星生物技术责任有限公司),配成浓度为10-5mol/L的溶液,在4℃下保存备用;0.05 mol/L的 Tris-HCl(pH=7.2)缓冲溶液,用 0.01 mol/L NaCl溶液配制。RF-5301PC型荧光分光光度计(日本岛津公司)。
1.2 CMCQA与BSA的作用
在10 mL容量瓶中均加入BSA溶液2.0 mL,然后加入不同浓度的CMCQA溶液,以Tris-HCl定容,作用1 h。以280 nm为激发波长,设定激发和发射狭缝宽度均为3 nm,记录280~700 nm范围内的荧光发射光谱。样品池为1 cm ×1 cm石英吸收池。
2 结果与讨论
2.1 荧光光谱
BSA是内源性荧光物质,其分子中的色氨酸、酪氨酸残基均能发射荧光。在大多数情况下,认为蛋白质的荧光主要来自色氨酸残基的贡献,而且含色氨酸残基的蛋白质的天然荧光及其变化直接反映了蛋白质中色氨酸残基本身及其周围环境的变化[8]。从图1结果可以看出,随着CMCQA浓度的增加,BSA的内源荧光强度有规律地降低,说明CMCQA对BSA的荧光具有猝灭作用,CMCQA与BSA之间发生了相互作用。

图1 CMCQA对BSA作用的荧光光谱图Fig.1 Fluorescence spectra of BSA interacted with different concentrations of CMCQA
2.2 对BSA荧光猝灭方式的确定
表1为不同温度下CMCQA对BSA荧光猝灭的Stern-Volmer方程与猝灭常数。CMCQA对BSA的猝灭常数均远远大于200 L/mol,各类猝灭剂对生物大分子的kq最大值为2.0×1010L·mol-1·s-1[9],可以初步判断CMCQA对BSA的荧光猝灭属于生成复合物的静态猝灭。另外,动态与静态猝灭也可依据不同温度下的猝灭常数得以区别。对动态猝灭,温度升高将有利于荧光体和荧光猝灭剂分子之间的有效碰撞,并可以促进电子的转移过程,Ksv随温度的升高而增大;若是静态猝灭,温度升高,产物的稳定性降低,静态猝灭常数Ksv减小[10]。在该研究体系中,CMCQA对BSA的荧光猝灭常数随温度的升高而减小,进一步表明CMCQA对BSA的荧光猝灭作用不是由扩散和碰撞引起的动态猝灭,而是生成复合物的静态猝灭[11]。

表1 不同温度下CMCQA对BSA荧光猝灭的Stern-Volmer方程与猝灭常数Table 1 Stern-Volmer equations and quenching constants of BSA fluorescence quenching with CMCQA at different temperatures
2.3 结合常数和结合位点数
在CMCQA对BSA的荧光静态猝灭过程中,假设生物大分子BSA有n个相同且独立的结合位点,可与猝灭剂 CMCQA(称为 Q)结合常数为 kA,则BSA与猝灭剂Q的配合反应可表示为:

当Q的浓度远远大于BSA浓度时,荧光体系的荧光强度和Q的浓度满足以下关系:
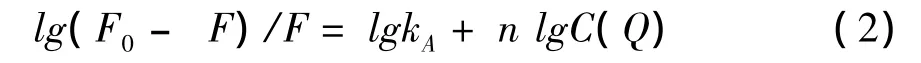
根据方程(2),lg(F0– F)/F~lgC(Q)曲线拟合可得到方程、平衡常数和结合位点数见表2所示。在室温下,CMCQA与BSA的的结合常数KA为2.45×104L/mol,CMCQA与BSA的结合位点数等于1.04,考虑实验误差,认为一个CMCQA分子能与一个BSA分子结合形成配合物。结合常数随温度升高而减小,是因为当温度升高,有利于结合产物的解离,使得平衡常数减小。

表2 不同温度下CMCQA对BSA荧光猝灭对数方程及其参数Table 2 Logarithm equations and parameters of BSA fluorescence quenching with CMCQA at room temperatures
2.4 作用力类型的判定
以不同温度下lnKA对1/T作图,得到直线y=7.33+823.16 x(r=0.98833),根据直线的斜率可以求出ΔH为-6.844 kJ/mol。同样,根据热力学公式[12],求得CMCQA与BSA反应的有关热力学参数(见表3)。因此,可认为CMCQA与BSA之间主要是通过静电引力相互作用。反应的ΔH <0,表明反应为放热反应,升高温度将不利于向生成复合物的方向进行,所以升高温度致使静态猝灭结合常数减小,生成复合物的稳定性下降,进一步说明CMC-QA对BSA的猝灭是形成复合物导致静态猝灭的过程。

表3 CMCQA与BSA结合的热力学参数Table 3 Themodynamic parameters of the interaction between CMCQA and BSA
3 结论
CMCQA与BSA之间通过静电引力相互作用,对BSA的猝灭过程为静态猝灭。在室温下,CMCQA与BSA的结合常数KA和结合位点数n分别为2.45×104L/mol和1.04。说明CMCQA对白蛋白的构象和分子能级都有明显作用,很可能CMCQA是一类具有明显的抗菌、抗病毒等活性的药物。
1 Xu Y(徐岩),Huang HG(黄汉国),Shen HX(沈含熙).Fluorescence quenching behavior of human serum albumin by quinolone antibacterials.Chin J Anal Chem(分析化学),1998,26:1494-1497.
2 Feng XZ(冯喜增),Jin RX(金瑞样),Qu Y(曲芸),et al.Studies on the ions'effect on the binding interaction between HP and BSA.Chem J Chin Univ(高等学校化学学报),1996,17:866-869.
3 Li B,Wang X,Chen RX,et al.Antibacterial activity of chitosan solution against Xanthomonas pathogenic bacteria isolated from Euphorbia pulcherrima.Carbohydr Polym,2008,72:287-292.
4 Chung YC,Chen CY.Antibacterial characteristics and activity of acid-soluble chitosan,Bioresour Technol,2008,99:2806-2814.
5 Xie W,Xu P,Liu Q.Antioxidant activity of water-soluble chitosan derivatives.Bioorg Med Chem Lett,2001,11:1699-1701.
6 Suzuki K,Mikami T,Okawa Y,et al.Antitumor effect of hexa-N-acetylchitohexaose and chitohexaose.Carbohydr Polym,1986,151:403-408.
7 Li XF(李小芳),Feng XQ(冯小强),Yang S(杨声),et al.Preparation and antibacterial activity of water-soluble o-carboxymethyl chitosan quaternary ammonium salt,Food Sci(食品科学),2011,32(9):79-81.
8 Liu Y(刘媛),Xie MX(谢孟峡),Kang J(康娟).Influence of total saponins of Panax notoginseng on the conformation of BSA.Acta Chim Sin(化学学报),2003,61:1305-1310.
9 Xie MX(谢孟峡),Xu XY(徐晓云),Wang YD(王英典),et al.Spectroscopic investigation of the interaction between 2,3-dihydro-4',5,7-trihydroxyflavone and human serum albumin.Acta Chim Sin(化学学报),2005,63:2055-2062.
10 Chen GZ(陈国珍),Huang XZ(黄贤智),Zheng ZX(郑朱梓),et al.Fluorescence Analytical Method(荧光分析方法).Beijing:Science Press,1990.122.
11 Li GZ(李桂芝),Liu YM(刘永明),Guo XY(虢新运),et al.Study on the interaction between bovine serum albumins and topotecan hydrochloride or irinotecan hydrochloride,Acta Chim Sin(化学学报),2006,64:679-685.
12 Shao S(邵爽),Ma BY(马博英),Wang XJ(王学杰),et al.Study on the interaction between cefodizime sodium and bovine serum albumin.Acta Physico-chimica Sin(物理化学学报),2005,21:792-795.

