机械活化铁氧化物气基还原热力学再探*
布林朝克 张邦文 赵瑞超 张 胤 许 嘉
(1.内蒙古科技大学稀土学院;2.内蒙古科技大学分析与测试中心)
笔者此前已就机械活化铁氧化物气基还原的热力学进行过研究,并在文献[1]中对研究结果进行了报道。但在随后进行其他相关研究[2-3]时发现,由于采用了引自某教科书的不准确的铁氧化物气基还原反应标准摩尔吉布斯自由能变化表达式,导致文献[1]中有些结果和结论是错误的。为此,本研究利用自行导出的铁氧化物气基还原反应标准摩尔吉布斯自由能变化的准确表达式[3],对机械活化铁氧化物气基还原的热力学重新进行探讨。
1 铁氧化物气基还原反应标准摩尔吉布斯自由能变化的准确表达式[3]
根据铁氧化物的气基还原反应、分解反应以及还原气体(CO或H2)的燃烧反应三者间的联系,可以导出铁氧化物气基还原反应标准摩尔吉布斯自由 能变化的准确表达式如表1、表2所示。

表1 铁氧化物CO还原反应标准摩尔吉布斯自由能变化的准确表达式

表2 铁氧化物H 2还原反应标准摩尔吉布斯自由能变化的准确表达式
表1、表2中的还原反应式可用如下通式表示:
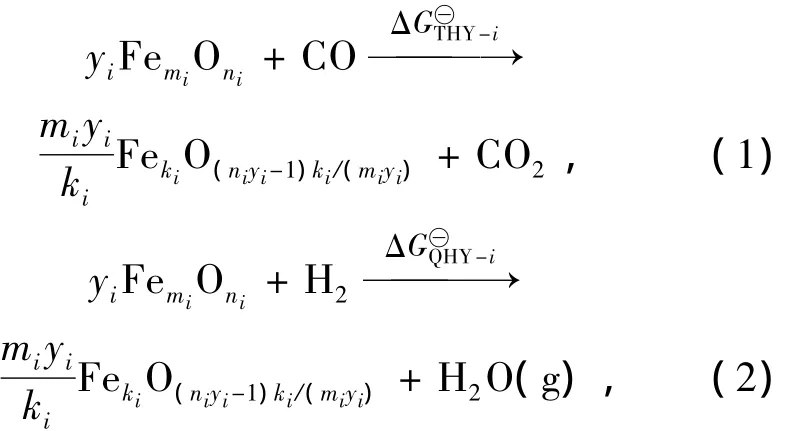
2 机械活化铁氧化物的气基还原热力学平衡式
机械活化是利用压缩、剪切、摩擦、研磨、延伸、冲击、弯曲等手段对固态物质施加机械力而诱发其物理化学性质发生变化的过程[4]。机械力作用下,一方面固态物质的颗粒和晶粒不断细化,活性表面和晶界面积增多,另一方面固态物质的晶格发生扭曲和位错,乃至形成热力学亚稳态的无定形相,从而使机械能部分地转化为固态物质的储能而使其活化[5]。可见,储能可作为活化程度的量度,用以揭示机械活化对铁氧化物还原热力学的影响规律。
铁氧化物的机械活化过程可描述为
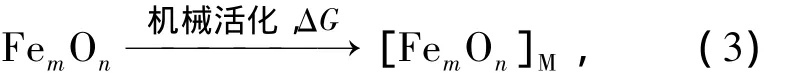
式中,[FemOn]M表示机械活化铁氧化物,ΔG为机械活化过程中1 mol铁氧化物的吉布斯自由能变化。因为由机械力引起的熵变 ΔS≈0[5],故 ΔG≈ΔH,即可用ΔG近似代替储能ΔH。

用XTHY-i和XQHY-i分别表示储能铁氧化物还原反应平衡时CO和H2的压力分数(即还原所需最低CO或 H2压力分数),并以压力代替逸度,经推导[1],可得
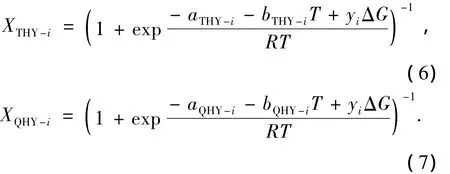
式(6)、式(7)即为储能铁氧化物的CO还原和H2还原热力学平衡式,它们揭示了机械活化铁氧化物气基直接还原所需最低CO或H2压力分数与铁氧化物储能和还原温度间的关系。
由式(6)、式(7)可以得出[1]:
(1)温度一定时,机械活化铁氧化物气基还原所需最低CO或H2压力分数随储能的增加而减小。
(2)机械活化铁氧化物的CO还原和H2还原分别存在一个“临界CO压力分数”

和一个“临界H2压力分数”

当 XTHY-i<或 XQHY-i<时,所需还原温度随储能的增加而升高,反之则所需还原温度随储能的增加而降低。
将表1 中的bTHY-i数据和表2中的bQHY-i数据分别代入式(8)和式(9),可得和的具体值如表3所示。应该指出,文献[1]中由于引用了不准确的铁氧化物气基还原反应标准摩尔吉布斯自由能变化表达式,因而得出的和值与此完全不同,是错误的。
表3 和 的具体值

表3 和 的具体值
i X c T HY-i X c QHY-i 1 0.000 049 0.000 001 2 0.587 058 0.030 424 3 0.007 835 0.000 174 4 0.889 854 0.151 331
3 机械活化铁氧化物气基还原的热力学平衡图和叉形图
为了更直观地展示机械活化铁氧化物气基还原的热力学特征,将表1和表2中的有关数据代入式(6)、式(7),经计算,画出储能分别为 0、5、10 kJ/mol时各铁氧化物气基还原的热力学平衡图如图1~图6所示,同时,还画出了储能为0时Fe2O3气基还原体系的叉形图以及储能分别为0、5、10 kJ/mol时Fe3O4气基还原体系的叉形图如图7~图10所示(由于图7中XTHY-1的值在图示温度范围内小于3.41×10-4,故相应平衡曲线在图中表现为似乎与横坐标重合)。

图1 储能Fe2 O3的CO还原平衡曲线

图2 储能Fe2 O3的H 2还原平衡曲线

图3 储能Fe3 O4的CO还原平衡曲线

图4 储能Fe3 O4的H 2还原平衡曲线
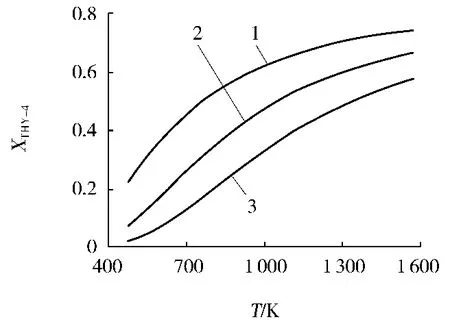
图5 储能FeO的CO还原平衡曲线1—储能0;2—储能5 kJ/mol;3—储能10 kJ/mol

图6 储能FeO的H 2还原平衡曲线
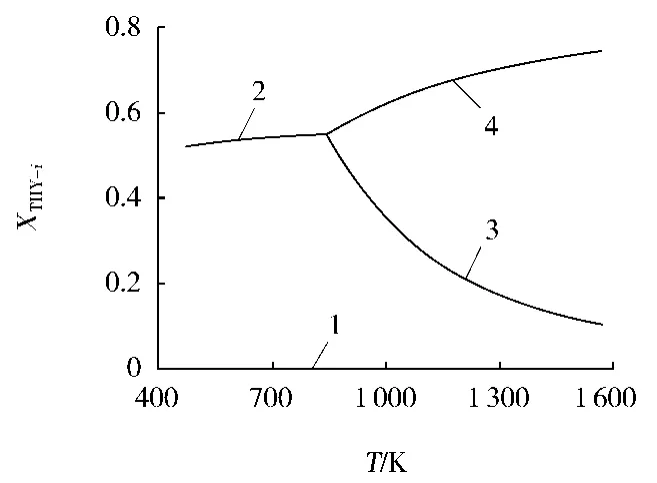
图7 零储能Fe2 O3的CO还原体系叉形图
1— XTHY-1;2—XTHY-2;3—XTHY-3;4—XTHY-4
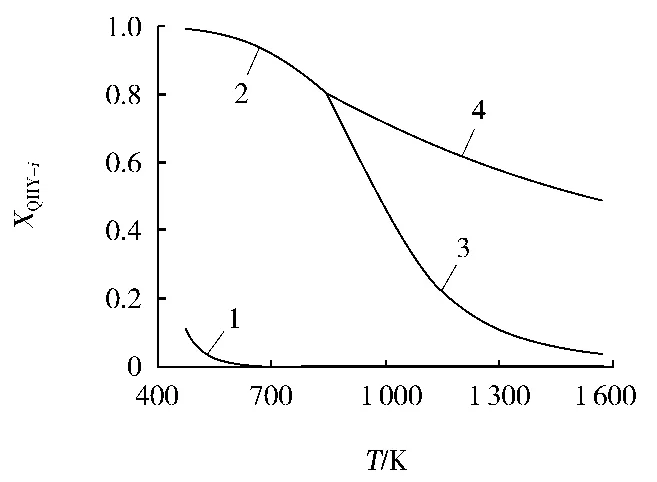
图8 零储能Fe2O3的H 2还原体系叉形图
1— XQHY-1;2—XQHY-2;3—XQHY-3;4—XQHY-4
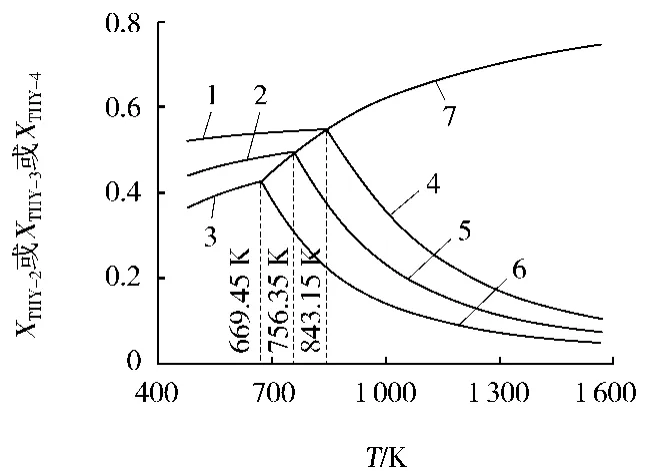
图9 不同储能Fe3 O4的CO还原体系叉形图

图10 不同储能Fe3 O4的H 2还原体系叉形图
将图1~图6与文献[1]中的储能铁氧化物气基还原热力学平衡图比较可知,两者在曲线形状和还原气体压力分数的变化范围上都有较大差异,特别是储能Fe2O3气基还原热力学平衡图,本研究得出的是递减曲线,而文献[1]中得出的是递增曲线。应以本研究所得结果为准。
3.1 储能对铁氧化物气基还原所需最低气体压力分数的影响
由图1~图6可以看出,各种铁氧化物的还原平衡曲线均随着铁氧化物储能的增加而下移,从而直观地印证了第2节中的第1条结论:在一定温度下,机械活化铁氧化物气基还原所需最低CO或H2压力分数随储能的增加而减小。
3.2 储能对铁氧化物气基还原所需还原温度的影响
将图1~图6与表3进行对比分析,可总结出在一定的还原气体压力分数下,铁氧化物的还原温度随储能的变化规律如表4所示。
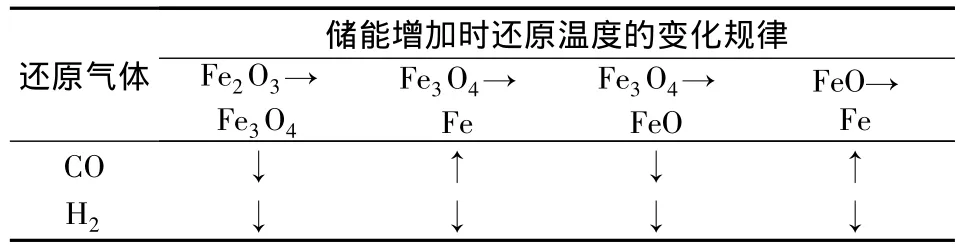
表4 一定还原气体压力分数下储能增加时铁氧化物还原温度的变化规律
表4中Fe2O3在一定还原气体压力分数下的还原温度随储能的增加而降低,这恰好与文献[1]中的结论相反。
3.3 Fe2O3的储能对还原叉形图的影响
图7、图8显示,即使不储能,Fe2O3还原所需最低CO或H2压力分数也比Fe3O4和FeO的低得多。因此,Fe2O3的储能对还原叉形曲线不产生显著影响。
3.4 Fe3O4的储能对还原叉形图的影响
如图9、图10 所示,843.15 K(570 ℃,对应的平衡CO和H2压力分数分别为0.551 4和0.804 3)为零储能Fe3O4还原方式的转折温度:T<570℃时,还原方式为Fe3O4→Fe;T>570℃时,还原方式为Fe3O4→FeO。
在还原方式的转折温度下,储能Fe3O4的两个气基还原反应的标准摩尔吉布斯自由能变化应相等,即

或


式(12)表明,无论是CO还原还是H2还原,Fe3O4的还原转折温度都具有相同的表达式,即还原方式的转折温度是Fe3O4的固有性质,与还原气体种类无关。显然,当 ΔG=0时==843.15 K=570 ℃。
在文献[1]中,由于引用的铁氧化物气基还原反应标准摩尔吉布斯自由能变化表达式不准确,因而得出了以下错误结论:和具有不同的表达式;当ΔG=0时≈573℃,≈569℃。
将式(12)分别代入式(6)、式(7),并将 XTHY-i和 XQHY-i换用与和对应的和表示,可得
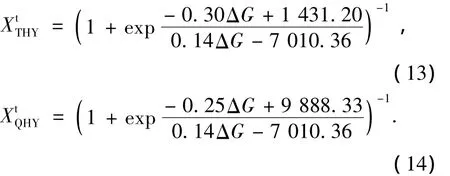
式(11)、式(12)表明,与储能Fe3O4的还原方式转折温度对应的还原平衡CO压力分数和H2压力分数具有不同的表达式,这正体现了CO和H2两种还原剂还原能力的差别。
由式(11)、式(12)可导出


由式(12)及式(15)和式(16)给出的规律在图9和图10中清晰可见:随着Fe3O4储能的增加,CO还原叉形曲线向低温、低CO压力分数方向移动,H2还原叉形曲线则向低温、高H2压力分数方向移动。这在本质上是CO和H2两种还原剂对Fe3O4的还原能力存在差异的体现。
3.5 Fe3O4的储能对FeO还原起始温度的影响
仔细观察表2和表3,可以发现反应THY-2、THY-3、THY-4之间以及反应QHY -2、QHY -3、QHY-4之间存在如下关系:

因此,当Fe3O4储能时,有

在还原方式的转折温度下,储能Fe3O4的两个还原反应的标准摩尔吉布斯自由能变化相等,此时由式(19)、式(20)可得
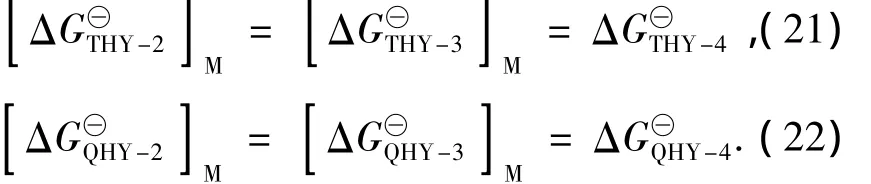
式(21)、式(22)表明,在储能Fe3O4还原方式的转折温度下,FeO的两个还原反应及储能Fe3O4的两个还原反应的标准摩尔吉布斯自由能变化均相等,故无论Fe3O4的储能状态如何,FeO的还原平衡曲线必始于储能Fe3O4还原方式的转折点,图9、图10直观地反映了这一点。因此,对于Fe3O4气基还原体系,Fe3O4还原方式的转折温度即为FeO还原的起始温度:若Fe3O4未储能,则该温度即为传统的570℃;若使Fe3O4储能,则该温度将降低,传统的570℃温度界限将被打破,正如图9、图10所示。显然,若以FeO为起始反应物,则应无起始温度的限制。
4 结论
制,但在Fe3O4气基还原体系中,FeO具有与Fe3O4还原方式的转折温度一致的还原起始温度。若使Fe3O4储能,其还原方式的转折温度将下降,Fe3O4和FeO的气基还原反应的传统570℃温度界限将被打破。
(1)笔者在文献[1]中给出的以下4方面结果是错误的,应以本研究所得结果为准:①机械活化铁氧化物气基还原时“临界CO压力分数”和“临界H2压力分数”的值;②机械活化铁氧化物气基还原的热力学平衡图;③Fe2O3在一定还原气体压力分数下的还原温度随机械力储能的增加而上升;④机械活化Fe3O4还原方式的转折温度在以CO为还原气体和以H2为还原气体时具有不同的表达式。
(2)Fe3O4的机械力储能增加时,其CO还原叉形曲线向低温、低CO压力分数方向移动,而H2还原叉形曲线则向低温、高H2压力分数方向移动。
(3)FeO本身的气基还原不受起始温度的限
[1] 布林朝克,张邦文,赵瑞超,等.机械活化铁氧化物的气基还原热力学[J].金属矿山,2013(2):63-67.
[2] 布林朝克,张邦文,赵瑞超,等.通过热力学多因素耦合控制氧化铁碳热还原顺序[J].金属矿山,2013(4):82-85.
[3] 布林朝克,郭 婷,张邦文,等.Fe2O3逐级还原顺序起源分析[J].金属矿山,2013(6):53-57.
[4] Suryanarayana C.Mechanical alloying and milling[J].Progress in Materials Science,2001,46:1-184.
[5] Tromans D,Meech J A.Enhanced dissolution of minerals:stored energy,amorphism and mechanical activation[J].Miner Eng,2001,14(11):1359-1377.

