乙酰溴法测定棉籽壳中木质素的含量
王建庆, 曹佃元, 张 玉
(1. 东华大学 生态纺织教育部重点实验室, 上海 201620; 2. 东华大学 国家染整工程技术研究中心, 上海 201620)
乙酰溴法测定棉籽壳中木质素的含量
王建庆1,2, 曹佃元2, 张 玉2
(1. 东华大学 生态纺织教育部重点实验室, 上海 201620; 2. 东华大学 国家染整工程技术研究中心, 上海 201620)
利用木质素乙酰化衍生物在280 nm处具有强烈吸收的特征,建立了一种用紫外分光光度法测定棉籽壳中木质素含量的新方法。研究了木质素乙酰化反应过程中乙酰溴体积分数、反应温度、时间和高氯酸质量浓度的影响规律,得到的优化反应条件为:乙酰溴体积分数30%、反应温度70 ℃、时间60 min、高氯酸质量浓度0.69 mol/L。在此条件下,乙酰溴法测得的棉籽壳木质素含量为19.59%。与Klasson法相比,该测量方法具有简单迅速,重演性和精密度好的优点。
棉籽壳; 木质素; 乙酰溴; 乙酰化反应
棉籽壳是印染前处理加工中较难去除的杂质之一,其化学组成是木质素、单宁、纤维素、半纤维素以及其他多糖类,还有少量的蛋白质、油脂和矿物质,以木质素为主[1]。研究表明,木质素是高度取代的苯丙烷单元以碳碳键和醚键联结而成的三维网状天然高分子聚合物,是由松柏醇、芥子醇和对香豆醇为先体衍生而成的复杂化合物,存在较多的酚羟基等活性基团。棉籽壳具有分层结构,其中木质素呈多层形态分布,与半纤维素共同构成纤维素网状骨架之间的黏合剂和填充剂[2-5]。鲜有有关棉籽壳木质素含量测定的报道,研究木质素的含量及溶解规律对去除棉籽壳有现实的指导意义。
测定木质素含量的方法较多,最常用的测定方法是Klasson法,其基本方法是将样品置于质量分数为72%的硫酸中,使其中的多糖类物质发生水解溶除,留下的残渣为酸不溶木质素,经过滤除去糖类化合物,对剩余残渣进行水洗、干燥和称量得到木质素的含量[6]。Klasson法分析时间长,耗费样品多,测定误差较大,且具有一定局限性[7]。对于草本植物材料如棉籽壳中的木质素而言,其组成、结构、含量及物理化学性能均不同于木材,因此,探索方便适用的测定方法对棉籽壳的研究利用具有重要意义。
乙酰溴法也是测定木质素含量的一种重要方法,具有所需样品量少,测定过程简单易行、迅速准确的特点。其基本原理是将样品置于乙酰溴-冰醋酸的混合溶液中,木质素中的酚羟基发生乙酰化,形成的乙酰化木质素溶液在280 nm处有最大紫外吸收峰,通过测量该处的紫外吸收值可以定量判断木质素的含量。测定过程中加入高氯酸可提高木质素乙酰化的速度[8-10]。本文在Klasson法测定棉籽壳木质素含量的基础上,提出棉籽壳木质素含量的乙酰溴法测定方法,以期对棉籽壳结构和性能的研究提供方便。
1 材料与方法
1.1 材料、试剂与仪器
材料与试剂:棉籽壳(河北咏亮粮油制品有限公司)。木质素(Sigma-Alorich Co.Ltd);木糖(Sigma-Alorich Co.Ltd);乙酰溴(Sigma-Alorich Co.Ltd);高氯酸(国药集团化学试剂有限公司);冰醋酸(上海凌峰化学试剂有限公司),所用试剂均为分析纯。
仪器:U-2910型紫外可见分光光度计(Hitachi High Technologies Co.);H.H.S 21-4型电热恒温水浴锅(上海医疗器械五厂);FA1004型电子天平(上海精科天平);101A-2E型电热鼓风干燥箱(上海实验仪器厂)。
1.2 木质素乙酰化反应
准确称取5.0 mg标准木质素,置于25 mL具塞试管中,加入5 mL体积分数为10%~40%乙酰溴的冰醋酸溶液和质量浓度为0~0.91 mol/L的高氯酸,盖好试管塞,在40~90 ℃恒温水浴下反应15~180 min,然后,将反应液移入装有10 mL 2 mol/L氢氧化钠和10 mL冰醋酸溶液的容量瓶中终止反应,充分混匀,用冰醋酸稀释至50 mL,以冰醋酸为空白溶液,测定并比较不同反应条件下产物在280 nm 处的紫外吸收值。
标准工作曲线:取一定量的木质素标准品,配制成质量浓度分别为0.008、0.012、0.016、0.020、0.024和0.028 g/L的标准液,按前述条件进行乙酰化反应,测定溶液在280 nm处的紫外吸收值,得到标准工作曲线如图1所示。其线性方程为Y=-0.215 04+42.242 86X,线性相关系数R=0.996 73,线性范围为0.008~0.002 8 g/L。

图1 木质素乙酰化溶液的紫外吸收标准工作曲线Fig.1 UV absorption standard work curve of acetylated lignin solution
1.3 棉籽壳木质素含量测定
1.3.1 试样准备
将市售棉籽壳研磨粉粹成颗粒细度为0.245 μm以下的粉末状,于105 ℃干燥2 h,取出后置于干燥器中冷却,备用。
1.3.2 Klasson法
参照GB/T 2677.8—1994《造纸原料酸不溶木素含量的测定》,准确称取1 g(称量精度0.000 1 g)经1.3.1处理的棉籽壳试样,用体积比为2∶1的苯醇混合液进行抽提处理,移入100 mL的具塞锥形瓶中,加入15 mL质量分数为72%的硫酸,盖好瓶塞,充分混匀,然后将锥形瓶置于18~20 ℃水浴中,保温2 h,并不时摇荡锥形瓶,到达规定时间后,将该混合液移至容量为1 000 mL的三角烧瓶中,加水至560 mL,使硫酸稀释至质量分数为3%,沸腾条件下回流水解4 h,静置沉淀,用恒重的砂芯漏斗抽除过滤,将盛有残渣的坩埚放到烘箱中105 ℃烘至恒重,于干燥器中冷却至室温并称量,得酸不溶木质素质量,按下式计算木质素含量:
式中:m1为烘干后酸不溶木质素质量,g;m2为绝干棉籽壳试样质量,g。
1.3.3 乙酰溴-分光光度法
称取5.0 mg按1.3.1方法制备的棉籽壳,按1.2的步骤进行乙酰化处理并测定乙酰化溶液在280 nm处的紫外吸收值,根据标准工作曲线,计算棉籽壳中木质素的含量。
2 结果与讨论
2.1 棉籽壳乙酰化条件的确定
乙酰溴法测定木质素含量的准确性与乙酰化反应的程度密切相关,因此,通过优化试验条件使木质素充分乙酰化和溶解是十分必要的。影响木质素乙酰化的主要因素有乙酰溴浓度、反应温度和反应时间,试验结果表明,加入高氯酸有助于乙酰化反应。
2.1.1 乙酰溴体积分数的影响
乙酰溴在冰醋酸介质中的体积分数对木质素的乙酰化反应有很大影响。图2示出乙酰溴体积分数对木质素乙酰化反应的影响。当冰醋酸介质中乙酰溴的体积分数在30%以下时,随着乙酰溴体积分数的增加,木质素的乙酰化程度逐渐增大,超过30%后,试样的紫外吸收值不再发生变化。说明乙酰溴体积分数为30%是乙酰化的最佳值。

注:反应温度70 ℃,时间30 min,高氯酸浓度0.47 mol/L。图2 乙酰溴体积分数对木质素乙酰化反应的影响Fig.2 Effect of acetyl bromide volume fraction on lignin acetylation
2.1.2 反应温度的影响
图3示出反应温度对木质素乙酰化的影响。由图可知,在70 ℃以下时,温度升高有利于反应的进行,当反应温度达到 70 ℃,试样的紫外吸收值接近最大值,超过80 ℃后,试样的紫外吸收出现下降,其原因可能是因为反应体系的温度接近或超出乙酰溴的沸点,造成乙酰溴组分的挥发从而影响木质素乙酰化反应所致。所以,反应温度控制在70 ℃为宜。
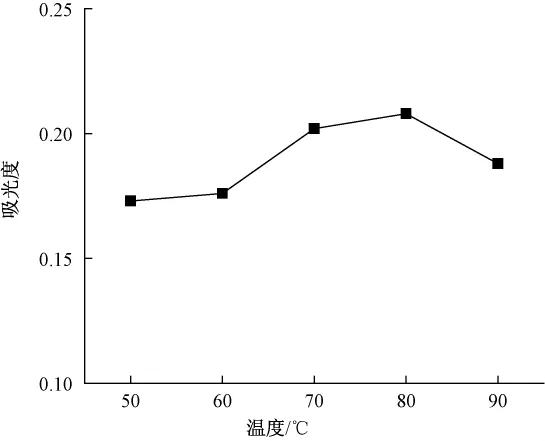
注:乙酰溴体积分数30%,时间30 min,高氯酸0.47 mol/L。图3 温度对木质素乙酰化反应的影响Fig.3 Effect of reaction temperature on lignin acetylation
2.1.3 反应时间的影响
图4示出反应时间对木质素乙酰化反应的影响。在反应温度为70 ℃、反应时间为60~180 min时,木质素乙酰化产物的紫外吸收比较稳定,但超过180 min后,其紫外吸收值随着时间的延长急剧增大。有研究表明,提高温度可能使木聚糖的降解加速,从而对测定带来干扰[11]。因此,在反应温度为70 ℃的条件下,反应时间选用60 min比较合适。

注:乙酰溴体积分数30%,温度70 ℃,高氯酸浓度0.47 mol/L。图4 反应时间对木质素乙酰化反应的影响Fig.4 Effect of reaction time on lignin acetylation
2.1.4 高氯酸对木质素乙酰化反应的影响
高氯酸是较强的含氯氧化剂,可使木质素发生氧化降解,在酸性条件下还可使木质素发生氯化,促进木质素溶解从而加速乙酰化反应。
图5示出木质素乙酰化产物的紫外吸收情况。由图可知,反应体系加入高氯酸后,反应产物的紫外吸收明显增强,表明高氯酸有助于木质素的乙酰化反应。图6进一步证明了高氯酸浓度对反应的影响。木质素乙酰化产物的紫外吸收值随高氯酸浓度增大而增加,高氯酸浓度为0.69 mol/L时,紫外吸收值为最大,对木质素乙酰化的增效作用达到最大,继续增加高氯酸的浓度,溶液紫外吸收值无显著变化。因此,高氯酸浓度以0.69 mol/L为宜。

注:乙酰溴体积分数30%,温度70 ℃,时间30 min。图5 木质素乙酰化溶液的吸收曲线Fig.5 UV absorption of acetylated lignin solution
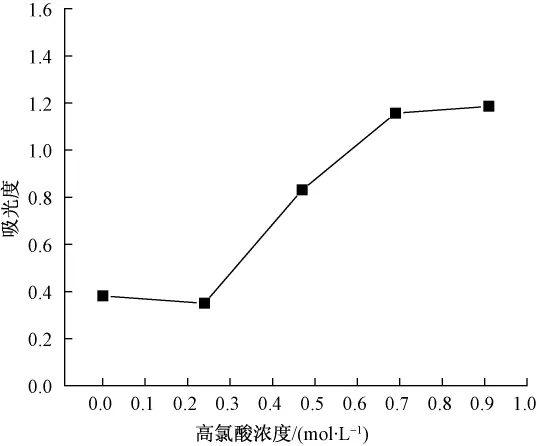
注:乙酰溴体积分数30%,温度70 ℃,时间30 min。图6 高氯酸浓度对木质素乙酰化反应的影响Fig.6 Effect of perchloric acid concentration on lignin acetylation
木质素乙酰化产物稳定性的试验结果表明,在室温条件下,反应结束后的木质素乙酰化衍生物溶液经6 000 s后,仍可保持稳定的紫外吸收性能,如图7所示,证明反应产物的稳定性足以满足测定要求。

图7 木质素乙酰衍生物溶液的稳定性Fig.7 Stability of acetylated lignin solution
综上所述,木质素含量测定的优化条件为:乙酰溴体积分数30%,反应温度70 ℃,反应时间60 min,高氯酸0.69 mol/L。
2.2 乙酰溴法与Klasson法的比较
根据得到的最佳处理条件对棉籽壳进行乙酰化处理,测定结果与Klasson法的数据见表1。

表1 乙酰溴法与Klasson法测定结果的比较Tab.1 Comparison of determination results between Klasson method and acetyl bromide method %
比较表1数据可知,乙酰溴法测得棉籽壳中木质素含量低于Klasson法,这与文献[7]报道的对木材中木质素含量的测定结果有较大的差异,产生差异的原因可能在于木材与棉籽壳的结构和组成不同有关。Klasson法更适用于纯度较高的木质纤维中木质素的测定,相对于结构和组成复杂得多的棉籽壳而言,其复杂的分层结构和组成,可能阻碍棉籽壳中多糖类物质的彻底降解,导致酸性降解后的残留产物不仅限于木质素一种成分,从而导致该方法的测定结果大于棉籽壳中木质素实际值的情况。
乙酰溴法与木质素中的酚羟基间存在定量的反应关系,加入高氯酸可以促进棉籽壳的溶解,有利于乙酰化反应的顺利进行,因而乙酰溴法测定所得木质素含量数据更为可靠。该方法采用紫外分光光度法测定,过程简单、快速,与以质量为依据的Klasson法相比,其重演性和精确度高,测量标准相对偏差低,因而可靠性更高。
3 结 语
1)木质素乙酰化的优化反应条件为:乙酰溴体积分数30%,反应温度70 ℃,反应时间60 min,加入高氯酸有利于乙酰化反应,加入浓度以0.69 mol/L为宜。为避免体系中多糖类物质的干扰,应严格控制反应条件。
2)用乙酰溴法测得棉籽壳中木质素的含量为19.59%。本文方法具有简便、快速、重演性和精密度高,样品耗费量少等优点。
鉴于目前尚无棉籽壳中木质素检测方法的现状,本文提出的方法旨在探索乙酰溴法测定的可行性,对于实际应用来说,许多工作尚待深入进行。
FZXB
[1] 赵酒泉. 去除棉籽壳的研究[J]. 印染, 1994, 20(3): 9-11. ZHAO Jiuquan. A study on the removal of cotton seed coat fragments[J]. Dyeing & Finishing,1994, 20(3): 9-11.
[2] 郑庆康. 木质素的生物降解[J]. 四川纺织科技,1998(1): 38-39. ZHENG Qingkang. The biodegradation of lignin[J]. Sichuan Textile Technology,1998(1): 38-39.
[3] 高洁, 汤烈贵. 纤维素科学[M]. 北京:科学出版社, 1996:230-231. GAO Jie, TANG Liegui. Cellulose Science [M]. Beijing: Science Press, 1996:230-231.
[4] 阎贺静, 华兆哲, 堵国成,等. 降解棉籽壳用精练酶的选择[J]. 印染,2009, 35(12): 6-8. YAN Hejing, HUA Zhaozhe, DU Guocheng, et al. Selection of scouring enzyme for cotton shell removal[J]. Dyeing & Finishing, 2009, 35(12): 6-8.
[5] 王国新. 棉籽壳制备木糖的水解过程研究[D]. 天津:天津大学,2009. WANG Guoxin. Studies on the hydrolysis process of cotton seed hulls for xylose production[D]. Tianjin: Tianjin University,2009.
[6] 李靖, 程舟, 杨晓伶,等. 紫外分光光度法测定微量人参木质素的含量[J]. 中药材, 2006 (3): 239-241. LI Jing, CHENG Zhou, YANG Xiaoling, et al. Determination of lignin content in tinyPanaxginsengby UV spectrophotometry[J]. Journal of Chinese Medicinal, 2006(3): 239-241.
[7] IIYAMA K, WALLIS A F A. An improved acetyl bromide procedure for determining lignin in woods and wood pulps[J]. Wood science and technology, 1988, 22(3): 271-280.
[8] 苏同福, 高玉珍, 刘霞,等. 木质素的测定方法研究进展[J]. 河南农业大学学报, 2007, (3): 356-362. SU Tongfu, GAO Yuzhen, LIU Xia, et al. Review of determination of lignin[J]. Journal of Henan Agricultural University,2007, (3): 356-362.
[9] VAN J D Zyl. Notes on the spectrophotometric determination of lignin in wood samples[J]. Wood science and technology, 1978, 12(4): 251-259.
[10] RONALD Hatfield, ROMUALDO S,FUKUSHMA. Can lignin be accurately measured[J]. Crop science, 2005, 45(3): 832-839.
[11] HATFIELD R D,GRABBER J,RALPH J, et al. Using the acetyl bromide assay to determine lignin concentrations in herbaceous plants: some cautionary notes[J]. J Agric Food Chem, 1999,47(2): 628-632.
Acetyl bromide test method for determining amount of lignin in cottonseed coat
WANG Jianqing1,2, CAO Dianyuan2, ZHANG Yu2
(1.KeyLaboratoryofScience&TechnologyofEco-Textile,MinistryofEducation,DonghuaUniversity,Shanghai201620,China; 2.NationalEngineeringResearchCenterforDyeing&FinishingofTextiles,DonghuaUniversity,Shanghai201620,China)
A new method to determine the amount of lignin in cottonseed coat was established with ultraviolet spectrophotometry, which is based on the strong absorption characteristic of the acetylate derivatives of lignin at 280 nm. The influence of acetyl bromide volume fraction, reaction temperature and time, and perchloric acid mass concentration on lignin acetylation reaction was investigated. And the optimized process conditions were obtained as follows: acetyl bromide volume fraction 30%, reaction temperature 70 ℃, reaction time 60 min, and perchloric acid mass concentration 0.69 mol/L. Compared with Klasson method, the acetyl bromide test method has such advantages as simpliness, rapidness, good reproducibility and precision.
cottonseed coat; lignin; acetyl bromide; acetylation reaction
0253- 9721(2013)09- 0012- 05
2012-10-09
2013-03-06
国家十二五科技支撑计划项目(2011BAE07B08)
王建庆(1956—),男,研究员。主要研究纺织品新型染整技术。E-mail:jqwang@dhu.edu.cn。
TS 192.1
A

