赤铁矿对模拟污水中重金属铬(Ⅵ)离子的吸附及固定化
石书柳,吴丽梅,廖立兵
(中国地质大学(北京)材料科学与工程学院,北京 100083)
铬是动物和人体必需的微量元素之一,成年人体内铬的含量约为5~6 mg,对维持人体正常的生理功能有着重要的作用,但大量的铬进入环境对人体、植物和动物都会产生很大的危害。铬主要来源于金属冶炼、印染纺织、皮革鞣制、木材加工和电镀电解等工业排放的“三废”中[1-2]。环境中的铬主要以三价铬(Ⅲ)阳离子和六价铬(Ⅵ)铬酸根阴离子形式存在。相比铬(Ⅲ),铬(Ⅵ) 具有更强的致癌和致突变能力,其毒性是铬(Ⅲ)的100 多倍;同时,铬(Ⅵ) 具有很强的氧化能力和迁移能力,对生态环境和人类健康构成严重威胁[3]。
含铬废水的处理方法有离子交换法、化学还原法、电解法、生物法和吸附法等。与其它方法相比,吸附法具有设备简单、操作容易、回收铬方法简单和可再生利用等优点而被广泛采用。目前研究较多的吸附吸附剂主要有天然矿物质、农林废弃物、聚合物、树脂、微生物絮凝剂以及炭(碳)质吸附剂等。Tewari等[4]利用天然膨润土对含铬废水进行处理,在pH值为2、温度为50℃的条件下,最大吸附量可达5.9 mg/g。赤铁矿是一种重要的铁氧化物,是土壤中广泛存在的稳定矿物之一,由于具有较大表面积、较多表面活性官能团以及较强的电荷可变性,使其对土壤的物理化学特性,尤其是对营养元素和污染物质、重金属离子的吸持、迁移、有效性和毒性均有着极其重要的作用[5]。金属氧化物尤其是铁锰氧化物与重金属离子的相互作用一直是土壤化学和环境化学研究的重点,国内外学者对其进行了广泛的研究,方继敏等[6]研究了赤铁矿对五氯苯酚的吸附特性及机理研究,王强等[7]研究了赤铁矿对铬(Ⅲ)的吸附动力学及等温吸附特征。然而,对于赤铁矿对铬(Ⅵ)的吸附作用却鲜有报道。本文作者通过不同添加量、不同吸附时间、不同初始浓度、不同pH值条件下赤铁矿对铬(Ⅵ) 吸附性能的分析以及赤铁矿吸附铬(Ⅵ) 前后和焙烧后XRD、SEM 分析深入探讨了赤铁矿对铬(Ⅵ)的吸附机理。
1 实验部分
1.1 材料
实验中使用的重铬酸钾由北京化工厂购得,分析纯。K2Cr2O7储备溶液是称取2.826 g的K2Cr2O7在100 mL 去离子水中搅拌溶解,然后定容到1 L,制得储备液中铬(Ⅵ)的最后浓度是1 g/L。赤铁矿由天津市福晨化学试剂厂提供,分析纯,实际Fe2O3含量(以Fe 计)为69.8%~70.1%。
1.2 吸附与解吸实验
(1)吸附实验 移取100 mL 一定浓度含铬(Ⅵ)模拟废水置于100 mL的具塞锥形瓶中,加入一定量赤铁矿,调节不同的pH值,变化反应温度,在恒温振荡器内振荡一定时间后,取出75 mL 左右水样于离心管中,10 000 r/min 下离心10 min,得上清液用孔径为22 nm 滤纸过滤后进行测试,下层沉淀保留并干燥。在探究不同条件对吸附量的影响实验中,添加量变量依次为1.00 g/L、2.00 g/L、4.00 g/L、6.00 g/L、8.00 g/L、10.00 g/L;时间变量依次为3 min、5 min、10 min、15 min、20 min、30 min、45 min、60 min、90 min、120 min、150 min、180 min;浓度变量依次为10 mg/L、20 mg/L、50 mg/L、100 mg/L、200 mg/L、500 mg/L、1000 mg/L;pH值变量依次为1、3、5、7、9、11、13。测得浓度分别用式(1)和式(2)计算其去除率η和吸附容量q。

式中,c0为铬(Ⅵ) 离子初始浓度,mg/L;ce为平衡时铬(Ⅵ) 离子初始浓度,mg/L;V为溶液体积,L;m为赤铁矿的添加量,g。
(2)解吸实验 20℃下,称取100 g 赤铁矿粉末加入到2 L 浓度为2.0 g/L的铬(Ⅵ)溶液中,每2 h 搅拌10 min,至12 h 吸附饱和,测定此时溶液浓度,对吸附后的赤铁矿进行离心并用去离子水洗涤2~3 遍,60℃下烘干后,平均分成5 份,分别在600℃、800℃、1000℃、1200℃焙烧4 h,并保留一份不作处理,完成焙烧后,称取不同温度下焙烧及未处理的赤铁矿各1 g 加入到200 mL 用NaOH 调节pH值为11的蒸馏水中进行解吸,并测得其解吸曲线,计算解吸量和解吸率。
1.3 分析测试
采用X 射线衍射(XRD)了解烧结样品的物相组成(结晶的种类和形态),日本理学Dmax 12 kW 型衍射仪,管电压为40 kV,管电流为100 mA,Cu 靶(λCuKα=1.5418 Å,1Å=0.1 nm),连续扫描模式,起始角=10°,终止角=80°,步宽=0.02。采用日本岛津公司SSX-550 型号的扫描电子显微镜对材料的微观形貌进行观察。SEM 表征是为了观察吸附材料的微观形貌,察看其孔道结构是否联通、分布是否均匀以及气孔大小尺寸等。
2 结果与讨论
2.1 赤铁矿添加量对去除铬(Ⅵ)离子的影响

图1 赤铁矿添加量对去除铬(Ⅵ)离子的影响
铬(Ⅵ)离子浓度为20 mg/L、pH值为5±0.5、293 K±1 K 下恒温振荡120 min,考察赤铁矿添加量分别为1.00 g/L、2.00 g/L、4.00 g/L、6.00 g/L、8.00 g/L、10.00 g/L时对模拟废液中铬(Ⅵ)去除效果的影响,结果见图1。由图1 可知,随赤铁矿添加量的增大,铬(Ⅵ)去除率不断增大,达到一定量后去除率就不再发生明显变化。去除效果随着去除剂量的增加而增加可以归因于去除剂表面积增加,从而为吸附反应提供了更多的反应活性点[8]。当赤铁矿的添加量小于6.00 g/L时,随赤铁矿用量的增大,铬(Ⅵ)去除率变化较大;当赤铁矿用量大于6.00 g/L时,铬(Ⅵ)去除量基本趋于稳定,不再随赤铁矿的加入而变化。因此,赤铁矿的最佳添加量为6.00 g/L。
2.2 时间对赤铁矿去除铬(Ⅵ)离子性能的影响
铬(Ⅵ)离子浓度为20 mg/L、赤铁矿添加量为6 g/L、pH值为5±0.5、293 K±1 K 下恒温振荡,考察吸附时间对模拟废液中铬(Ⅵ)在赤铁矿上去除效果的影响,结果见图2。由图2 可知,赤铁矿对铬(Ⅵ)的吸附速率最初迅速增加,在60 min时,单位吸附量可达0.71 mg/g,之后增长趋缓,120 min时又有小幅的增长。可见,以6.00 g/L的赤铁矿处理20 mg/L的铬(Ⅵ)溶液,达到吸附平衡用时约120 min,最大吸附量可达0.77 mg/g。
描述吸附反应动力学的方程有多种,本实验将分别采用准一级吸附动力学方程和准二级吸附动力学方程对吸附时间数据进行处理。

图2 接触时间对赤铁矿吸附铬(Ⅵ)的影响
准一级吸附动力学的线性方程如式(3),准二级动力学方程如式(4)[9]。
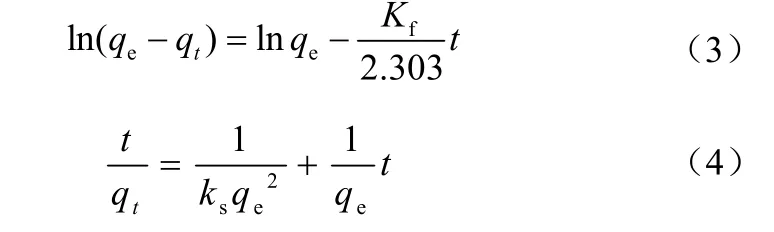
式中,qe和qt分别为平衡时和t(min)时间铬(Ⅵ)在赤铁矿上的吸附量,mg/g;Kf为准一级动力学常数,min−1;Ks为准二级动力学常数,g/(mg·min)。
如图3所示,(a)、(b)分别为准一级动力学模拟曲线和准二级动力学模拟曲线。分别根据图中各曲线的斜率与截距可计算得出准一级动力学常数Kf、准二级动力学常数Ks及不同模型中达到平衡时的理论吸附量qe(cal),并将所得数据与初始浓度c0,曲线的决定系数R2值以及平衡时的实际吸附量qe(exp)展示于表1 中。对比表中数据可知,准二级动力学模拟曲线的决定系数R2值为0.9983,优于准一级动力学模拟曲线的R2值,并且通过准二级动力学方程计算得到平衡时的理论吸附量比通过准一级动力学方程计算得到吸附量更接近实际的吸附量。由此可见,准二级动力学模型能够很好地描述铬(Ⅵ)在赤铁矿上的吸附动力学行为。这说明准二级动力学模型包含吸附的所有过程,如外部液膜扩散、表面吸附和颗粒内部扩散等[10],能够更为真实地反映铬(Ⅵ)离子在赤铁矿上的吸附机理。

图3 赤铁矿吸附铬(Ⅵ)离子的动力学模型

表1 准一级吸附模型和准二级吸附模型公式数据
2.3 铬(Ⅵ)离子浓度对对赤铁矿吸附性能的影响
赤铁矿添加量为6 g/L、pH值为5±0.5、293 K±1 K 下恒温振荡120 min,考察铬(Ⅵ)离子初始浓度分别为10 mg/L、20 mg/L、50 mg/L、100 mg/L、200 mg/L、500 mg/L、1000 mg/L时,赤铁矿对模拟废液中铬(Ⅵ)去除效果的影响,结果如图4所示。由图可知,随着铬(Ⅵ)离子初始浓度的增加,铬(Ⅵ)离子在赤铁矿上的吸附量也随之增大;当铬(Ⅵ)离子初始浓度低于200 mg/L时,吸附量随浓度增长迅速,增幅很大;当铬(Ⅵ)离子初始浓度高于200 mg/L时,吸附量增长趋缓,增幅逐渐减小,当铬(Ⅵ)离子浓度达到1000 mg/L时,赤铁矿对铬(Ⅵ)离子的吸附达到饱和,此时吸附量达到最大值为4.80 mg/g。为深入对铬(Ⅵ) 离子在赤铁矿上的吸附行为的研究,特采用最常用的Langmuir 吸附等温方程和Freundlich 吸附等温方程对图4 中平衡数据作进一步探讨。
固体在溶液中的吸附是个复杂的过程,涉及固体与溶质、固体与溶剂、溶质与溶剂等相互之间的作用。平衡等温吸附模型描述的是吸附剂与被吸附物之间的相互作用,通过实验结果与吸附模型的拟合度,可以帮助解释吸附过程中的吸附机制及吸附剂表面的异向性[11]。
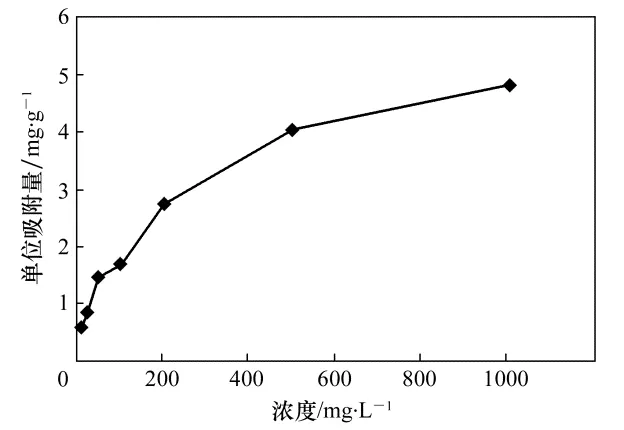
图4 初始浓度对赤铁矿吸附铬(Ⅵ)离子的影响
Langmuir 模型假设吸附剂表面各向同性,吸附过程是均质的单层吸附,其吸附等温方程的基本形式如式(5),线性化后为式(6)[12-13]。

式中,qe为吸附平衡时单位吸附量,mg/g;ce为吸附平衡时溶液的铬(Ⅵ)离子浓度,mg/L;qmax为单层饱和最大吸附容量,mg/g;b为吸附平衡常数。
Freundlich 模型是经验模型,广泛应用于单层非均匀性吸附体系,其吸附等温方程的基本形式如式(7),线性化后为式(8)[14-15]。
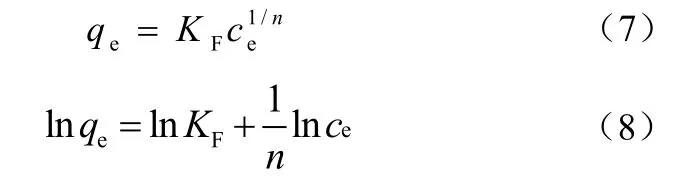
式中,qe为吸附平衡时单位吸附量,mg/g;ce为吸附平衡时溶液的铬(Ⅵ)离子浓度,mg/L;KF为反映吸附容量的吸附常数;n的值与吸附强度有关。
如图5所示,图中(a)、(b)分别为Langmuir等温吸附模型和Freundlich等温吸附模型的模拟曲线。由回归方程的截距与斜率计算得的两种模型的相关参数列于表2。分析表中数据可知,通过Langmuir等温吸附模型拟合所得的决定系数R2为0.9237,低于通过Freundlich等温吸附模型拟合所得的值。另外,由Langmuir等温方程计算得的最大吸附量qmax为2.79 mg/L,与实际吸附量4.80 mg/g有较大出入,可见,Freundlich等温吸附模型更适合用来拟合铬(Ⅵ)离子在赤铁矿上的吸附。根据Freundlich 理论[16],KF和n为与材料吸附容量和吸附性能有关的参数,KF越大,吸附效果越好;1/n越小,表示材料越容易吸附。一般认为,1/n介于0.1~0.5,则容易吸附。而1/n>2的物质,则难以吸附。由Freundlich等温方程计算得1/n为0.4215,介于0.1~0.5 之间,可见铬(Ⅵ)离子在赤铁矿上的吸附是比较容易进行的。
2.4 pH值对赤铁矿去除铬(Ⅵ)离子性能的影响
铬(Ⅵ)离子浓度为20 mg/L、赤铁矿添加量为6 g/L、293 K±1 K 下恒温振荡120 min,考察当pH值分别为1.0、3.0、5.0、7.0、9.0、11.0、13.0时,赤铁矿对模拟废液中铬(Ⅵ)去除效果的影响,结果如图6所示。可以看出,赤铁矿对铬(Ⅵ)离子的吸附量明显与溶液的pH值相关,整体随pH值得升高而降低,当pH值小于3时,吸附量随pH值的升高显著降低;当pH值由3 升高到9时,吸附量持续下降,但下降趋势趋于平缓;当pH值大于11时,吸附量随pH值升高再次大幅降低。由此得出结论,赤铁矿对模拟废液中铬(Ⅵ)离子的吸附在强酸性环境中效果最好,在中碱性环境中较差。这与路则栋等[17]和李会东等[18]分别利用羟基氧化铁改性硅藻土和生物法吸附水中铬(Ⅵ)离子的实验结果相符。
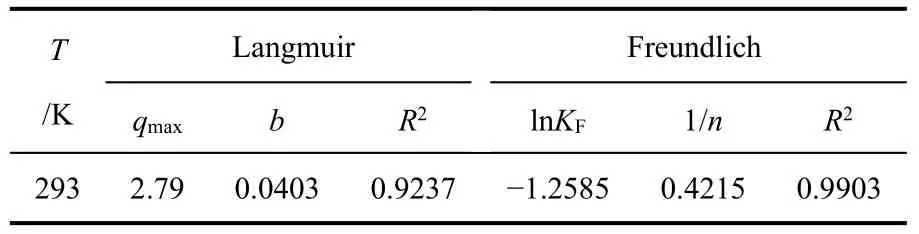
表2 Langmuir和Freundlich等温吸附公式数据

图5 铬(Ⅵ)离子在赤铁矿上吸附的两种等温吸附模型
对固液吸附来说,溶液的pH值是影响该过程的一个重要因素,因为pH值不仅可影响吸附质表面的理化性质,同时也影响溶液中被吸附物的存在状态。一方面,氧化铁在水溶液中由于表面羟基化作用而使其具有活性较大的表面,在一定介质条件下可能从介质中缔合一个质子使氧化铁表面带上正电荷,或表面配位水合基离解出一个质子而使表面带负电荷,称为表面离子化或电离化,从而导致氧化铁表面可变电荷的出现,表达式如式(9)、式(10)[19]。

图6 pH值对赤铁矿吸附铬(Ⅵ)离子的影响
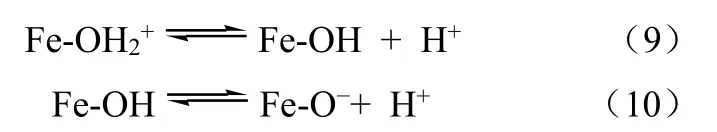
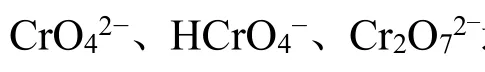
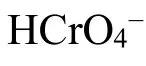
2.5 不同焙烧温度对铬(Ⅵ) 解吸量的影响
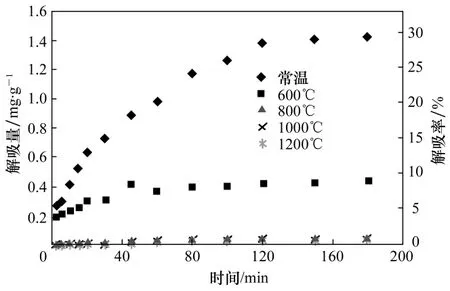
图7 不同焙烧温度对铬(Ⅵ)离子解吸曲线的影响
图7为不同焙烧温度对铬(Ⅵ)离子解吸曲线的影响。由图7 可以看出,吸附铬(Ⅵ)离子后经焙烧后的赤铁矿较经常温干燥的赤铁矿的铬(Ⅵ)离子的解吸量有明显的降低。经常温干燥的赤铁矿解吸平衡时间约为120 min,最大解吸量为1.41 mg/g,此时解吸率为29.4%;600℃焙烧后的赤铁矿解析平衡时间缩短,约为60 min,最大解析量明显降低,为0.43 mg/g,解吸率亦降至8.9%;当焙烧温度提高800℃及以上时,铬(Ⅵ)离子的解吸量及解吸率已接近于零。由此有得出结论,焙烧温度对吸附后赤铁矿的铬(Ⅵ)离子的解吸效果有明显影响,焙烧温度越高铬(Ⅵ)离子越不易解吸。鉴于此现象有两种可能原因:一方面,由于K2Cr2O7的沸点为500℃,高温有利于K2Cr2O7的挥发;另一方面,高温焙烧可改变赤铁矿表面形貌,孔道收缩而更加致密,从而可将已吸附的铬(Ⅵ)包覆在其中,减小铬(Ⅵ)离子的解吸。
2.6 XRD
赤铁矿吸附铬(Ⅵ)离子前后及1000℃焙烧后的XRD 图谱如图8所示。对比赤铁矿吸附铬(Ⅵ)离子前后图谱不难发现,赤铁矿的主要衍射峰并未发生偏移,亦没有新的衍射峰产生,可见铬(Ⅵ)离子并未进入赤铁矿晶体内部,也未发生反应生成新的物相,铬(Ⅵ)离子在赤铁矿上的吸附应以表面吸附为主。对比赤铁矿焙烧前后图谱可知,赤铁矿的主要衍射峰未偏移也无新的衍射产生,可推知,即使高温下赤铁矿也不与K2Cr2O7发生反应生成新的物相,也并不改变赤铁矿的晶体结构。
2.7 SEM
对比赤铁矿焙烧前后SEM 形貌图可以发现,焙烧前赤铁矿颗粒表面粗糙,颗粒粒径较大,经焙烧后,赤铁矿颗粒粒径有所减小并且更均一,表面更光滑致密。由此可推知,高温对赤铁矿表面形貌及结构有明显影响。焙烧前赤铁矿的粗糙表面可增大表面积从而使其比表面积提高,有利于对铬(Ⅵ)离子的吸附;焙烧后赤铁矿,表面收缩、致密化可将一部分吸附在表面的铬(Ⅵ)离子包覆在其中,从而使铬(Ⅵ)离子不易解吸。

图8 赤铁矿吸附铬(Ⅵ)离子前后及焙烧后的XRD 图谱
3 结论
20℃下赤铁矿对铬(Ⅵ)离子的最佳添加量为6 g/L,最大吸附量为4.80 mg/g,且很好地遵循拟二级动力学模型、Freundlich等温吸附模型。在等温吸附研究中,随着铬(Ⅵ)离子浓度的增加,吸附量先增加后趋于平缓,直至吸附饱和,吸附量达到最大。在研究酸碱度的影响实验中,随pH值的增加,吸附量减小,最佳pH值环境为强酸性;焙烧温度对吸附后赤铁矿的铬(Ⅵ)离子的解吸效果有明显影响,焙烧温度越高铬(Ⅵ)离子越不易解吸。综合XRD和SEM 测试分析,赤铁矿对铬(Ⅵ)离子的吸附主要为表面吸附,高温焙烧可影响赤铁矿的表面形貌。
[1]公绪金,李伟光,张妍妍,等.活性炭吸附水中六价铬机理及影响因素[J].山东建筑大学学报,2001,26(4):396-402.
[2]程昌敬,刘东,张嫦.羧甲基化壳聚糖修饰磁性硅粒子去除Cr(Ⅵ)离子[J].化工进展,2012,31(1):227-232.
[3]王家宏,常娥,丁绍兰,等.吸附法去除水中六价铬的研究进展[J].环境科学与技术,2012,35(2):67-72.
[4]Tewari N,Guha B K,Vasudevan P.Adsorption study of hexavalent chromium by bentonite clay[J].Asian Journal of Chemistry,2005,17(4):2184-2190.
[5]王强,屈亚非,肖广全,等.α-Fe2O3对Cr(Ⅲ)的等温吸附特征研究[J].土壤学报,2010,47(1):159-162.
[6]方继敏,李山虎,龚文琪,等.赤铁矿对五氯苯酚的吸附特性及机理研究[J].武汉理工大学学报,2008,30(9):57-60.
[7]王强.赤铁矿对Cr(Ⅲ)的吸附动力学研究[J].西南大学学报:自然科学版,2010,32(3):50-53.
[8]谭秋荀,张可方,赵焱,等.活性氧化铝对六价铬的吸附研究[J].环境科学与技术,2012,35(6):130-133.
[9]王小雨,吕国诚,王乾乾,等.累托石对水中扑尔敏的吸附性能[J].化工进展,2012,31(4):938-942.
[10]Chang M Y,Juang R S.Adsorption of tannic acid,humic acid,and dyes from water using the composite of chitosan and activated clay[J].J.Colloid and Interface Sci.,2004,278(1):18-25.
[11]Gil A,Assis F C C,Albeniz S,et al.Removal of dyes from wastewaters by adsorption on pillared clays[J].Chemical Engineering Journal,2011,168(3):1032-1040.
[12]王艳,唐晓武,刘晶晶,等.黄土对锰离子的吸附特性及机理研[J].岩土工程学报,2011,34(12):2292-2298.
[13]张培,张小平,兰永辉,等.活性炭纤维吸附处理模拟焦化废水尾水[J].化工进展,2012,31(12):2786-2790.
[14]吴代赦,杜俊逸,李萍.水溶液中氟的吸附平衡模型研究进展[J].南昌大学学报:工科版,2010,32(2):103-112.
[15]阿依努尔·达吾提,迪丽努尔·塔力甫,阿布力克木·阿布力孜,等.羊骨基活性炭对溶液中Pb(Ⅱ)的吸附性能[J].2010,29(12):2390-2394.
[16]张巧丽,高乃云,乐林生,等.氧化铁/活性炭复合吸附材料去除水中砷的研究[J].同济大学学报:自然科学版,2006,34(12):1647-1661.
[17]路则栋,张庆乐,田名刚,等.羟基氧化铁改性硅藻土对六价铬的吸附性能[J].地下水,2012,34(6):180-183.
[18]李会东,周建红,张大为,等.水体中六价铬生物吸附与解吸附条件与特性[J].湖南科技大学学报:自然科学版,2010,25(2):122-124.
[19]王强,卜锦春,魏世强,等.赤铁矿对砷的吸附解吸及氧化特征[J].环境科学学报,2008,28(8):1612-1617.
[20]Li Y,Gao B,Wu T,et al.Hexavalent chromium removal from aqueous solution by adsorption on aluminum magnesium mixed hydroxide[J].Water Research,2009,43(12):3067-3075.
[21]Leyva-Ramos R,Jacobo-Azuara A,Diaz-Flores P E,et al.Adsorption of chromium(Ⅵ) from an aqueous solution on a surfactant-modified zeolite[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2008,330(1):35-41.

