曝气量对生物流化床处理丙烯酸丁酯废水的影响
徐洁,宋玉栋,周岳溪* ,黄震,,梁冬梅,何绪文
1.吉林农业大学资源与环境学院,吉林 长春 130118
2.中国环境科学研究院水污染控制技术研究中心,北京 100012
3.中国矿业大学(北京)化学与环境工程学院,北京 100083
丙烯酸丁酯[1-2]是一种重要的化工原料,在胶粘剂、弹性体、合成纤维、建筑材料、高吸水性树脂、紫外/电子束(UV/EB)固化、絮凝剂、助剂、洗涤剂等众多领域展现出优异的应用前景,近年来发展迅速,生产规模不断扩大。丙烯酸丁酯生产过程中会产生大量废水,废水中含有丙烯酸盐[3]、对甲基苯磺酸盐等有毒有机物,化学需氧量高达60 ~70 g/L[4],属于高浓度有机废水。目前国内外针对该废水的处理方法主要有湿式催化氧化法[5]、焚烧法[6]和生物法[7-8]等。其中湿式催化氧化法和焚烧法存在着能耗大、成本高,在处理高含盐废水时容易发生设备堵塞和腐蚀等问题,而以厌氧生物法[8-10]为主的生物处理技术[11-12]存在处理负荷低,停留时间长,耐冲击负荷较差等问题[10,13-14]。
范志庆等[4]的研究表明,采用好氧流化床可实现丙烯酸丁酯废水的高负荷处理,废水中的丙烯酸和对甲基苯磺酸能得到完全氧化。郑盛之等[9,15]的研究表明,采用厌氧接触法和微氧生物流化床,可使废水中的丙烯酸高效转化为乙酸和丙酸,从而降低废水毒性,有利于后续的产甲烷处理。另一方面,已有研究表明[16-17],磺酸盐类物质在好氧条件下较易降解,在厌氧条件下较难降解,当废水中碳源或硫源缺乏时才能缓慢降解。因此,研究反应器内供氧条件对废水中特征污染物丙烯酸和对甲基苯磺酸降解的影响,对于新型处理工艺的开发和工艺条件的优化均具有重要意义。笔者采用生物流化床反应器考察了曝气量对丙烯酸丁酯废水处理效果的影响。
1 材料与方法
1.1 生物流化床处理装置
生物流化床工艺流程如图1 所示,反应器为有机玻璃制成,有效容积12 L(长21.5 cm ×宽21.5 cm×高61 cm),采用聚氨酯微生物载体(10 mm ×10 mm×10 mm),填充量约50%。该载体是一种比表面积大、过水通气性好、传质效率高的泡沫型载体,在高浓度含酚废水和染料废水的处理方面取得了较好的效果[15-16]。反应器内部设有加热棒,温度控制在(25 ±1)℃。模拟废水由蠕动泵提升进入流化床。反应器底部设有砂芯曝气头,通过转子流量计控制曝气量。曝气头布置在反应器一侧的底部,其曝气气流的推流作用使反应器内液体带动生物载体循环流动,实现流化。
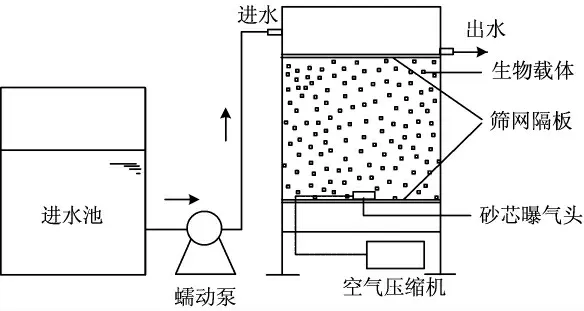
图1 生物流化床Fig.1 Reactor of biological fluidized bed
1.2 驯化污泥
接种污泥取自处理养猪废水的UASB 反应器,其VSS/SS 为0.65,生物载体经挂膜和驯化后加入反应器。在室温条件下,先用人工挤压的方式将接种污泥吸入生物载体,在曝气条件下,用1 000 mg/L丙烯酸和200 mg/L 对甲基苯磺酸组成的自配废水进行驯化,将驯化后的生物载体加入到反应器中连续运行。
1.3 进水组成
丙烯酸丁酯生产废水中,主要污染物为丙烯酸钠和对甲基苯磺酸钠,其CODCr占80%以上,丙烯酸钠和对甲基苯磺酸钠的浓度比约为5∶1(按丙烯酸和对甲基苯磺酸质量计算)。按照CODCr∶N∶P =200∶5∶1 用自来水配制模拟丙烯酸丁酯废水。其中丙烯酸和对甲基苯磺酸作为碳源,氯化铵和磷酸二氢钾分别提供微生物生长所需的N 和P。同时,进水pH 用NaOH 调节到7.0 左右。
1.4 测试项目
1.4.1 常规指标的测定
溶解性有机碳(DOC)采用岛津TOC-VCPH总有机碳分析仪测定;DO 采用SG6 溶解氧测定仪(梅特勒- 托利多仪器有限公司)测定;ORP、pH 采用PE20 实验室pH 计(梅特勒- 托利多仪器有限公司)测定;混合液悬浮固体浓度(MLSS)、混合液挥发性悬浮固体浓度(MLVSS)采用重量法测定。
1.4.2 特征污染物的测定
使用Dionex ICS–1000 离子色谱仪(戴安中国有限公司)测定丙烯酸、乙酸、丙酸和对甲基苯磺酸浓度,其中阴离子色谱柱为IonPac AS11-HC,抑制器为ASRS-300 4 mm,淋洗液采用5 mmol/L 的NaOH,流速和抑制电流分别设为1 mL/min 和13 mA。测定对甲基苯磺酸则采用120 mmol/L 的NaOH 淋洗液,抑制电流为297 mA。
2 结果与讨论
2.1 曝气量对反应器内氧化还原条件的影响
反应器启动成功后,维持反应器HRT 为8 h,进水丙烯酸浓度为1 000 mg/L,对甲基苯磺酸浓度为200 mg/L。先后控制曝气量为高、中、低三个阶段,各阶段运行时间、曝气量及反应器内DO 浓度与ORP 状况如表1 和图2 所示。可以看出,在高曝气量条件下(320 L/h),反应器内溶解氧在0.5 mg/L以上,处于好氧状态。在中、低曝气量条件下(160和40 L/h),反应器内溶解氧浓度相近,均为0.5 mg/L 以下,处于微好氧状态,其中低曝气量下反应器内ORP 更低,为-272 ~-245 mV。

表1 不同曝气阶段的运行条件Table 1 Process parameters at different aeration rate

图2 不同曝气量条件下反应器内的DO 浓度及ORPFig.2 DO and ORP of reactor at different aeration rate
2.2 曝气量对丙烯酸处理效果的影响
不同曝气量条件下,反应器对丙烯酸的去除效果如图3 所示。由图3 可知,高曝气量(320 L/h)条件下,反应器对丙烯酸去除效果很好,出水丙烯酸平均浓度1 mg/L 左右,丙烯酸去除率达到99%以上。中等曝气量(160 L/h)条件下,去除效果较前一阶段差,出水丙烯酸平均浓度为30.2 mg/L,丙烯酸平均去除率为97.0%。低曝气量(40 L/h)条件下,出水丙烯酸平均浓度为13.5 mg/L,丙烯酸平均去除率为98.6%。综上所述,在高、中、低三个曝气量条件下,无论反应器处于好氧或微好氧状态,丙烯酸均可得到较好的去除,在DO 浓度为0.36 ~0.93 mg/L,ORP 为-272 ~-106 mV 的条件下,各阶段丙烯酸的平均去除率均可达97%以上。
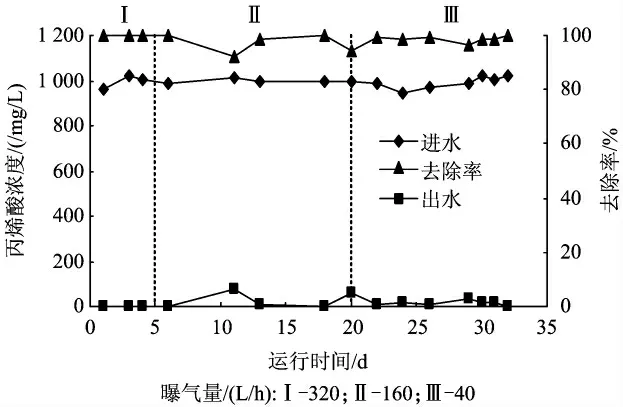
图3 不同曝气量条件下丙烯酸的去除效果Fig.3 Removal efficiency of acrylic acid at different aeration rate
2.3 曝气量对对甲基苯磺酸处理效果的影响
不同曝气量条件下,反应器对对甲基苯磺酸的去除效果如图4 所示。由图4 可知,高曝气量(320 L/h)条件有利于对甲基苯磺酸的去除,出水对甲基苯磺酸平均浓度为26.5 mg/L,平均去除率达87%,这与十二烷基磺酸钠等其他磺酸盐类的降解特性相似[17-21]。当曝气量降至160 L/h 时,对甲基苯磺酸去除效果显著下降,出水对甲基苯磺酸平均浓度为150 mg/L,平均去除率仅24.5%。进一步降低曝气量至40 L/h,出水对甲基苯磺酸平均浓度升至159 mg/L,对甲基苯磺酸平均去除率为20.6%。综上所述,对甲基苯磺酸在好氧条件下(DO 浓度为0.70 ~0.93 mg/L,ORP 为-128 ~-106 mV)去除效果较好,微好氧条件下(DO 浓度为0.36 ~0.53 mg/L,ORP 为-272 ~-179 mV)去除效果显著下降。

图4 不同曝气量下对甲基苯磺酸的去除效果Fig.4 Removal efficiency of Para-toluene sulphonic acid at different aeration rate
2.4 曝气量对乙酸和丙酸生成量的影响
相关研究表明,微好氧或厌氧条件下丙烯酸降解中间产物为乙酸和丙酸[4,9,15]。不同曝气量条件下,反应器内乙酸和丙酸的生成量如图5 所示。
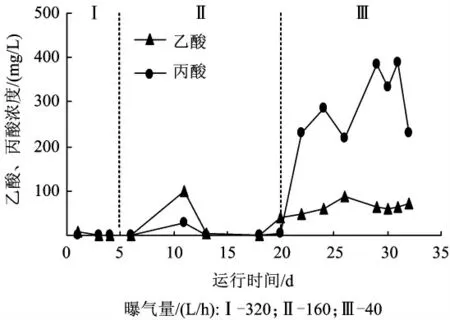
图5 不同曝气量条件下乙酸、丙酸的生成量Fig.5 Generation of acetic acid and propionic acid at different aeration rate
由图5 可知,在高曝气量(320 L/h)条件下,反应器内处于好氧状态,乙酸、丙酸的生成量很少,出水中未检出丙酸,乙酸平均浓度仅9.42 mg/L。中等曝气量(160 L/h)条件下,反应器内有少量丙酸生成,乙酸生成量略有增加,出水乙酸平均浓度为28.5 mg/L,丙酸平均浓度为6.4 mg/L,乙酸生成量高于丙酸。低曝气量(40 L/h)下,乙酸、丙酸生成量显著增加,出水乙酸平均浓度为65.3 mg/L,丙酸平均浓度为296.0 mg/L,丙酸生成量高于乙酸。与丙烯酸去除量相比,平均每去除1.0 mol 丙烯酸,生成0.08 mol 乙酸和0.29 mol 丙酸。李莎等[15]的微氧流化床中(进水丙烯酸浓度为6 000 ~9 000 mg/L),平均每1.00 mol 丙烯酸降解生成0.22 mol 乙酸和0.36 mol 丙酸。郑盛之等[9]的厌氧接触反应器中,平均每去除1.00 mol 丙烯酸可以生成0.25 mol 乙酸和0.425 mol 丙酸。与此相比,本研究中的乙酸和丙酸生成量较低,可能与进水丙烯酸浓度较低,生成的乙酸、丙酸快速降解有关。综上所述,微好氧条件较好氧条件更利于乙酸和丙酸的生成,且当ORP为-245 mV 以下生成量较大。
2.5 曝气量对溶解性有机碳去除效果的影响
不同曝气量条件下,反应器对废水中溶解性有机碳(DOC)的去除效果如图6 所示。由图6 可知,高曝气量(320 L/h)条件下,反应器对DOC 去除效果较好,出水中DOC 平均浓度为63.4 mg/L,平均去除率为89.9%。当曝气量降为160 和40 L/h 时,出水中DOC 平均浓度分别上升为179 和345 mg/L,平均去除率分别降为72.4%和46.1%。可见,随着曝气量的降低,DOC 去除率逐渐下降,出水中DOC 浓度逐渐升高。
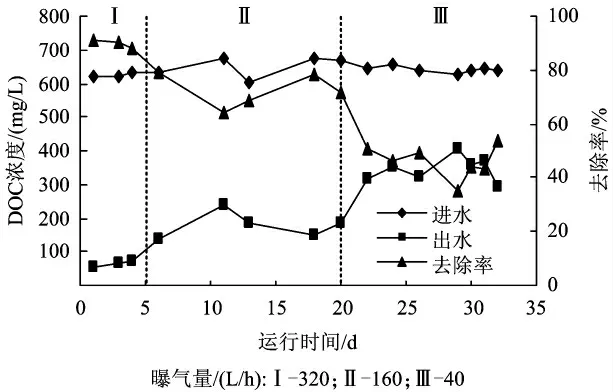
图6 不同曝气量条件下DOC 的去除效果Fig.6 Removal efficiency of DOC at different aeration rate
3 结论
(1)在进水丙烯酸浓度为1 000 mg/L,对甲基苯磺酸浓度为200 mg/L,pH 为7.0,HRT 为8 h,25 ℃的高曝气量(320 L/h)条件下,反应器处于好氧状态;在中、低曝气量(160 和40 L/h)条件下,反应器处于微好氧状态。
(2)当ORP 为-272 ~-106 mV,DO 浓度为0.36 ~0.93 mg/L 时,曝气量变化对丙烯酸去除影响不大,丙烯酸平均去除率在97%以上;丙烯酸既可在好氧(ORP 为-128 ~-106 mV,DO 浓度为0.70 ~0.93 mg/L)条件下完全氧化,也可在微好氧(ORP 为-272 ~-245 mV,DO 浓度为0.39 ~0.46 mg/L)条件下部分转化为中间降解产物乙酸和丙酸,且丙酸生成量大于乙酸。
(3)好氧条件有利于对甲基苯磺酸的去除,平均去除率达87%,微好氧条件下对甲基苯磺酸去除率降为20%~24%。
(4)好氧条件有利于废水DOC 的去除,平均去除率由好氧条件下的89.9% 降为微好氧条件下的46.1%。
[1]邵艳秋,张桂芬.丙烯酸丁酯合成方法的改进[J].沈阳化工,2000,29(2):70-71.
[2]王振山,刘鸿雁,王景峰,等.萃取法处理丙烯酸丁酯废水的技术开发[J].吉林化工学院学报,2004,21(1):24-25.
[3]JANSSEN P H. Isolation of Clostridium propionicum strain 19acry3 and further characteristics of the species[J].Archives of Microbiology,1991,155(6):566-571.
[4]范志庆,宋玉栋,周岳溪,等.三相生物流化床处理高浓度丙烯酸丁酯生产废水[J].环境科学,2011,32(5):1382-1387.
[5]袁霞光,冷冰,余启炎. 丙烯酸废水湿式氧化催化剂的研究[J].石油化工,2005,34(7):684-687.
[6]李国屏. 丙烯酸及其酯的废水处理[J]. 上海化工,1994,19(1):29-31.
[7]徐俊.高浓度丙烯酸及酯类废水处理方法的探讨[J].丙烯酸化工与应用,2006,19(2):14-18.
[8]SCHONBERG J C,BHATTACHARYA S K,MADURA R L,et al. Evalution of anaerobic treatment of selected petrochemical wastes[J]. Journal of Hazardous Materials,1997,54(1/2):47-63.
[9]郑盛之,宋玉栋,周岳溪,等.厌氧接触式反应器预处理高浓度丙烯酸废水[J].环境工程学报,2011,5(3):26-29.
[10]DEMIRER G,SPEECE R.Anaerobic biotransformation of acrylic acid in UASB reactors:significance of process staging,physical homogenization of microorganism and microbial acclimation[J].Environmental Technology,1997,18(11):1111-1121.
[11]SPEECE R E. Anaerobic biotechnology for industrial wastewater[J]. Environmental Science & Technology,1983,17 (9):416-427.
[12]黄海远,张志军. 丙烯酸酯废水的生化处理[J]. 丙烯酸化工与应用,2004,17(4):17-21.
[13]张忠祥,钱易.废水生物处理新技术[M]. 北京:清华大学出版社,2004.
[14]DEMIRER G N,SPEECE R E. Anaerobic biotransformation of four 3-carbon compounds (acrolein,acrylic acid,ally lalcohol and n-propanol)in UASB reactors[J]. Water Research,1998,32(3):747-759.
[15]李莎,郑盛之,宋玉栋,等. 多级微氧生物流化床预处理高浓度丙烯酸废水[J].环境科学,2012,33(9):3167-3171.
[16]赵婧,蒋进元,丁林,等. 核黄素对偶氮染料生物降解的影响[J].环境科学研究,2009,22(10):1193-1197.
[17]黄满红,李咏梅,顾国维.直链烷基苯磺酸钠在厌氧-缺氧-好氧污水处理系统中的迁移转化规律[J]. 环境科学,2007,28(7):1502-1506.
[18]TEMMINK H,KLAPWIJK B. Fate of linear alkylbenzene sulfonate (LAS)in activated sludge plants[J].Water Research,2004,38(4):903-912.
[19]ARVIND K M,PRADEEP K. Fate of linear alkylbenzene sulfonates in the environment:a review[J]. International Biodeterioration & Biodegradation,2009,63(8):981-987.
[20]GARCIA M T,CAMPOS E,RIBOSA I,et al.Anaerobic digestion of linear alkyl benzene sulfonates:biodegradation kinetics and metabolite analysis [J]. Chemosphere,2005,60 (11 ):1636-1643.
[21]CONSTANTINA P,KATERINA S,MICHAEL K,et al. On the complete aerobic microbial mineralization of linear alkylbenzene sulfonate[J].Desalination,2007,215(1/2/3):198-208. ▷

