美创AMAX-200血凝分析仪性能的初步评价
张鸿伟,刘 斌(.昆明市第一人民医院检验科 6500;.楚雄医药高等专科学校检验系医学检验专业007级5班,云南楚雄 675005)
本院检验科急诊化验室引进AMAX-200凝血分析仪使用已两年,并且为24h运转,为了更好地了解该仪器的性能,根据《医学实验室质量与能力认可准则》的要求,设备在常规使用中应显示出能够达到规定的性能标准,亦需进行性能评估[1]。根据国际血液学标准委员会(ICSH)和美国国家临床实验室标准委员会(CLSI)的有关文件要求[2-3],并参考了部分文献资料[4-6],作者用新鲜血浆和质控血浆从精密度、准确度、携带污染率、抗干扰能力(以影响度作为评价指标)等方面对美创AMAX-200凝血分析仪磁珠凝固法检测的常规凝血项目进行性能初步评估,现将结果报道如下。
1 材料与方法
1.1 仪器 德国美创AMAX-200血凝分析仪,仪器操作和维护保养遵循仪器使用说明书。
1.2 试剂 (1)凝血酶原时间(PT):天津美创太平洋科技有限公司生产,批号T-812,ISI值为1.04。(2)凝血酶时间(TT):上海太阳生物技术有限公司生产,批号:122041。(3)活化部分凝血活酶时间(APTT):德国美创(北京美创公司)生产,批号:TE09835。(4)纤维蛋白原 (Fib):德国美创(北京美创公司)生产,批号:TOC031。
1.3 混合血浆的准备
1.3.1 样本采集方法 抗凝全血标本用真空负压采血管采集2.7mL静脉血,枸橼酸钠(109mmol/L)抗凝剂0.3mL抗凝,抗凝比例为1∶9,充分混匀。
1.3.2 正常混合血浆的制备 收集健康体检人员血浆20份,男女各半,采血后半小时内3 000r/min离心10min后每管收集1.5mL至干净容器内,总共约30mL充分混匀,分装后密封放置于-80℃冰箱保存待用。
1.3.3 异常混合血浆的制备 收集肝移植患者及肝病患者异常血浆20份,男女各半,采血后半小时内3 000r/min离心10 min后每管收集1.5mL至干净容器内,总共约30mL充分混匀,分装后密封放置于-80℃冰箱保存待用。
1.4 干扰物的准备
1.4.1 溶血物的准备 用血常规管采集静脉血3mL,1 500 r/min离心5min,弃去上层血浆,留下红细胞层,加入蒸馏水后充分混匀,待红细胞完全破坏后上机测血红蛋白浓度,待用。
1.4.2 高脂血的准备 收集临床上乳靡血清3mL,上机测量三酰甘油(TG,5.64mmol/L),放干净容器内,充分混匀密封后放置于-80℃冰箱保存待用。
1.4.3 高胆红素血准备 收集临床上黄疸血清3mL,上机测量总胆红素(TBil,3 198μmol/L),放在干净容器内,充分混匀密封后放置于-80℃冰箱保存待用。
1.5 方法
1.5.1 精密度试验 根据CLSI的EP5-A2文件相关要求[3],在美创AMAX-200血凝仪上分别测定正常和异常水平混合血浆的PT、APTT、TT和FIB,以了解仪器的重复性。(1)批内精密度:收集的冷冻正常混合血浆和异常血浆,用同一批号的试剂3h内连续重复测定正常和异常混合血浆各20次。(2)日间精密度:用购买的质控血浆每日检测一次,连续进行30d检测。
1.5.2 准确度试验 AMAX-200仪器经正常维护保养后,使用厂家配套的定值标准血浆检测3次,将所得数据取均值与定值标准血浆靶值计算偏倚。
1.5.3 携带污染率试验 取高值和低值两个不同浓度的混合血浆,先对高值标本重复测定3次(H1、H2、H3)后,紧接着对低值标本重复测定3次(L1、L2、L3),计算携带污染率。计算公式:污染率(%)=|L1-L3|/|H3-L3|×100%。
1.5.4 抗干扰能力试验 即血凝仪在有异常样品或干扰物存在情况下的抗干扰能力。干扰因素包括溶血(Hb 6g/L)、高脂血(TG 5.64mmol/L)、高胆红素血(TBil 3 198μmol/L)等干扰性试验,按一定比例加入正常混合血浆,分别在AMAX-200血凝仪上测定PT、FIB、TT、APTT各2次,取平均值。以未加干扰物的混合血浆测定值为标准,计算出影响度,以影响度作为评价指标。影响度(%)=(加干扰物混合血浆测定值-未加干扰物混合血浆测定值)/未加干扰物混合血浆测定值×100%。
1.5.5 精密度及准确度的判定 依据按NCCLS提出的PT、APTT、FIB总允许误差(TEa)的要求。
2 结 果
2.1 精密度试验 PT、APTT、TT和Fib各项目批内及批间变异系数均在规定的允许范围之内,由此可见仪器重复性较好,见表1。
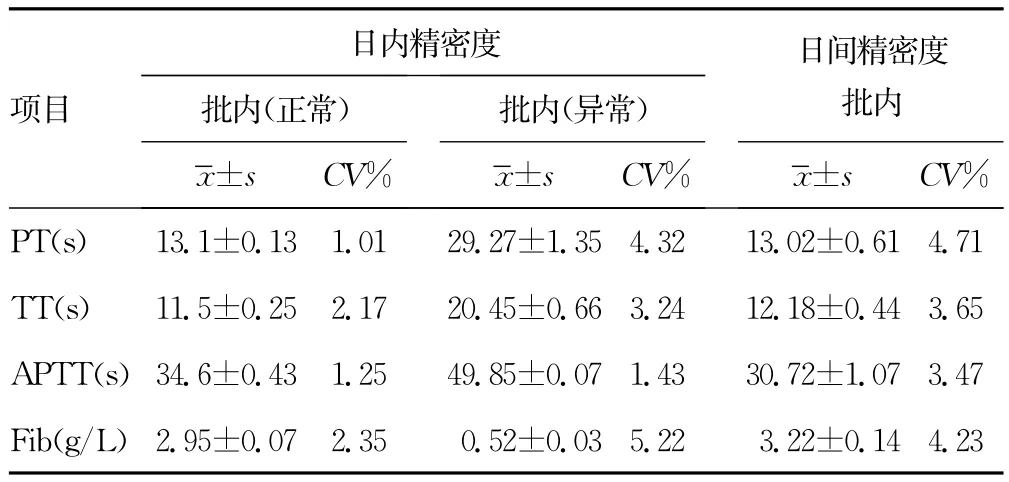
表1 AMAX-200凝血分析仪日内(n=20)及日间精密度(n=30)测定结果
2.2 准确度试验 PT、APTT、TT、Fib各项目测定结果的偏倚%小于4%,见表2。
2.3 携带污染率试验 PT、APTT、TT的携带污染率均不超过5%,见表3。

表2 德国美创AMAX-200密封血凝仪准确度测定结果
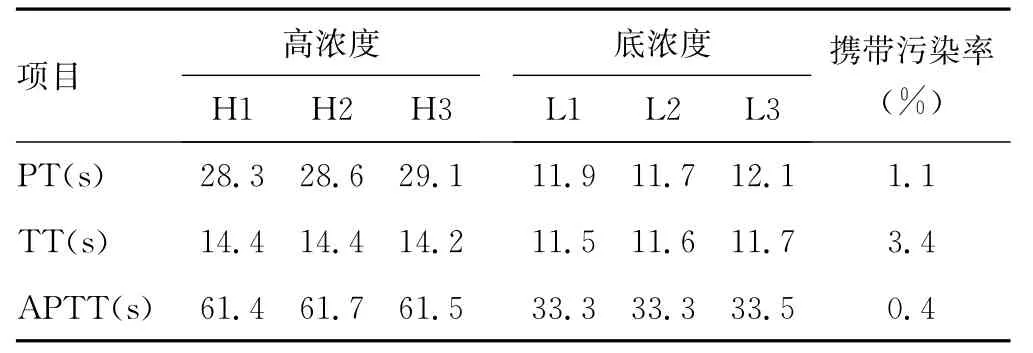
表3 PT、APTT、TT携带污染率测定结果
2.4 抗干扰能力试验 加入干扰物的混合血浆测定值结果、各浓度干扰物对血凝影响度,见表4。

表4 各浓度干扰物对血凝影响度
3 讨 论
本试验研究表明,在AMAX-200血凝分析仪上测定PT、APTT、TT和Fib的正常水平批内及批间变异系数均小于5.00%,异常水平仅有Fib大于5.00%,原因为数值太小,在检测下限附近。满足实验室检测要求,可见该全自动凝血分析仪具有良好的重复性和稳定性。本台仪器的精密度(CV)与文献资料报道的机械凝固法其他仪器的CV基本一致 ,但部分项目的CV偏高值得注意;与有关文献资料报道的光学凝固法其他仪器的CV未见明显差异[5-6]。准确性试验结果表明,PT、APTT、TT和Fib测定结果的偏倚率均在4%以内,与有关文献资料报告的偏倚相符[8-9],符合美国CLIA′88相关文件的要求,从而保证了测定值的准确性。携带污染率试验结果可见,PT、TT、APTT三项的携带污染率在0.4%~1.1%,均不超过5.0%,表明仪器测定标本后自洁系统良好。干扰性试验表明,该仪器抗黄疸能力强,在加入总胆红素浓度0~3 198μmol/L时PT、Fib、TT、APTT影响度均在美国CLIA′88规定的允许偏差范围(PT、APTT允许偏差范围为±15%,FIB允许偏差范围为±20%)内,但PT影响度增大(大于7%);加入TG含量0~5.642mmol/L时,PT相比较其他项目影响度偏大(影响度为9.93%)。而溶血标本PT、Fib、APTT在血红蛋白含量达4.8g/L时受干扰较小(影响度小于5%),但在血红蛋白含量大于4.8g/L时 ,FIB干扰较大(影响度为-10.69%~-11.64%)。故在实际工作中应尽量避免溶血,如发生溶血应重新采集再行测定。
综上所述,AMAX-200血凝分析仪在本院检验科使用两年后仍然保持结果准确可靠和性能稳定的特点,可继续适用于检验科的正常使用。
[1] 国家合格评定国家认可委员会.CNAS-CL02:2008医学实验室质量和能力认可准则[S].北京:中国合格评定国家认可委员会,2008.
[2] 熊立凡,李树仁.I临床检验基础[M].3版.北京:人民卫生出版社,2004:73-101.
[3] CLSI.EP5-A2evaluation of precision performance of quantitative measurement methods;approved Guide--line-second edition[S].Wayne,PA:NCCLS,2004.
[4] 冯仁丰.临床检验质量管理技术基础[M].上海:上海科技文献出版社,2007:89.
[5] 黄福达,杨志钊,梁培松,等.应用NCCLS EP5-A2文件评价CA7000全自动血凝仪的精密度[J].检验医学与临床,2010,7(16):1710-1712.
[6] 王茜.CA-1500全自动血凝分析仪的分析性能评价[J].实用医院临床杂志,2012,9(5):82-85.
[7] 谢田刚,王海燕,王胜江.Destiny Max全自动血凝分析仪性能评价[J].医疗卫生装备,2012,33(6):107-109.
[8] 许小英,于海涛,周存敏,等.某型号全自动血凝分析仪的性能评价[J].国际检验医学杂志,2012,33(11):1361-1362,1369.
[9] 朱小东,谢志雄,许永志,等.STAGO Compact全自动凝血分析仪性能评价[J].医疗装备,2010,23(9):19-20.

