紫杉醇联合奈达铂或顺铂周方案同步放化疗治疗Ⅲ期非小细胞肺癌的临床研究
钟世寿 杜 驰
(内江市第二人民医院肿瘤中心,四川 内江 641003)
紫杉醇联合奈达铂或顺铂周方案同步放化疗治疗Ⅲ期非小细胞肺癌的临床研究
钟世寿 杜 驰
(内江市第二人民医院肿瘤中心,四川 内江 641003)
目的 观察每周小剂量紫杉醇联合奈达铂或顺铂同步放化疗治疗局部晚期非小细胞肺癌(NSCLC)的疗效及不良反应。方法 58例不能手术Ⅲ期非小细胞肺癌患者(Ⅲa期22例,Ⅲb期36例),随机分为观察组29例:接受紫杉醇45mg/m2d1+奈达铂25 mg/m2d1化疗,每周一次。对照组29例:接受紫杉醇45mg/m2d1+顺铂25 mg/m2d1化疗,每周一次。两组同期行肺部三维适形放疗(GTV:6600cGy/30f/6+w、CTV:6000 cGy /30F/6+w、PTV:5400 cGy /30F/6+w)。结果 同步放化疗后评价疗效:观察组:CR1例;PR17例,总有效率(CR+PR)66.7%。对照组:CR0例;PR15例,总有效率(CR+PR)71.4%。χ2=0.02,P>0.05,两组比较差异无统计学意义。白细胞减少;贫血;肝功损害;放射性肺炎及放射性食道炎发生率两组比较差异亦无统计学意义(P>0.05)。肾功损害,恶心;呕吐及体质量下降>10%,发生率观察组明显低于对照组,两组比较差异均有统计学意义(P<0.05)。结论 紫杉醇联合奈达铂与紫杉醇联合顺铂同步放化疗治疗局部晚期非小细胞肺癌疗效确切,但紫杉醇联合奈达铂比紫杉醇联合顺铂患者耐受性更好。
紫杉醇;奈达铂;顺铂;同步放化疗;局部晚期非小细胞肺癌
非小细胞肺癌(non-small cell lung cancer,NSCLC)占全部肺癌的75%~80%,局部晚期不能手术切除的非小细胞肺癌患者约30%~40%,5年生存率仅为5%~6%,大多数死于局部未控和远处转移[1]。单纯放疗5年生存率仅为0%~10%,中位生存期仅15个月[2]。吴一龙等[3]总结不可切除的局部晚期NSCLC取得两点治疗共识,一是同时化放疗优于序贯化放疗模式,二是标准治疗模式为含铂放案化疗与放疗。目前,临床上多采用紫杉醇联合顺铂同步放化疗,但由于顺铂胃肠道不良反应严重,多数患者无法耐受而终止治疗。奈达铂为第二代铂类抗癌药物[4,5],肾毒性、消化道反应等不良反应明显轻于顺铂,因此我科将顺铂改为奈达铂,联合紫杉醇同步放化疗治疗不能手术的IIIa或IIIb期非小细胞肺癌患者,总结报道如下。
1 资料与方法
1.1 临床资料
58例患者均经病理或细胞学确诊为NSCLC,根据2002年UICC肺癌TNM分期为Ⅲa期22例,Ⅲb期36例。(纵膈淋巴结的判断以CT为准,最小径≥1cm为阳性)。其中男性39例;女性19例,年龄31~73岁,平均57岁。病理类型为鳞癌32例;腺癌21例;其他5例。两组性别;年龄;临床分期及病理类型方面无统计学意义(P>0.05)。所有患者KPS评分>70分;预计生存期超过3个月;有客观可测量病灶;因医学原因不能手术;既往未接受过放化疗。58例患者均无心;肝;肾及造血功能障碍;血常规检查正常。
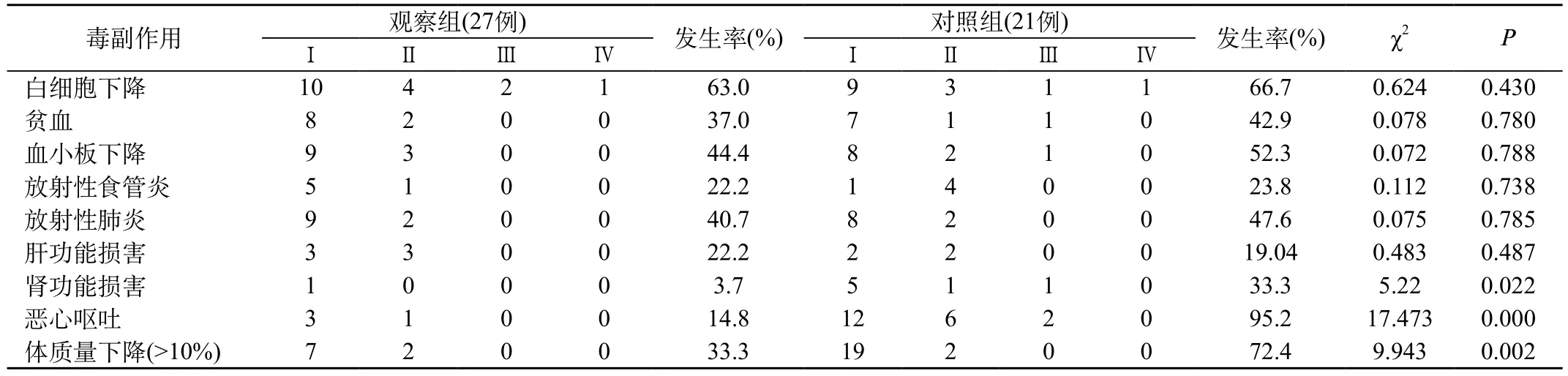
表1 两组患者同步放化疗不良反应情况
1.2 治疗方案
观察组29例:接受紫杉醇45mg/m2(ivgtt,d1)+奈达铂25mg/m2(ivgtt,d1)化疗,每周一次共6周。对照组29例:接受紫杉醇45mg/m2(ivgtt,d1)+ 顺铂25mg/m2(ivgtt,d1)化疗,每周一次共6周。两组同期行肺部三维适形放疗。(GTV:6600Cgy/30f/6+w、CTV:6000 Cgy/30f/ 6+w、PTV:5400 Cgy/30f/6+w)。
1.3 疗效及不良反应评价
近期疗效于治疗完成1月后评价。依据2003年WHO实体瘤疗效评价标准分为完全缓解(CR),部分缓解(PR),稳定(SD),进展(PD)。化疗毒副反应按WHO分级标准[6],急性放射性反应评价采用RTOG/EROTC标准[7]。
1.4 统计学方法
采用χ2检验比较两组治疗后近期疗效和不良反应,所有统计处理应用SPSS13.0软件包完成。
2 结 果
2.1 两组患者治疗情况
预期每组患者接受174次化疗,每例患者接受6次化疗。观察组29例共完成171次化疗,共27例完成预期化疗。对照组29例共完成165次化疗,29例共21例完成预期化疗。观察组和对照组平均化疗次数分别为5.89次和5.69次,P<0.01,差异有统计学意义。
2.2 近期疗效
同步放化疗后评价疗效:观察组:CR1例;PR17例,总有效率(CR+PR)66.7%。对照组:CR0例;PR19例,总有效率(CR+PR)71.4%。χ2=0.075,P=0.785,两组比较差异无统计学意义。
2.3 不良反应
观察组和对照组白细胞减少发生率分别为63.0%和66.7%,P>0.05,差异无统计学意义;贫血发生率分别为25.3%和25.6%;血小板减少发生率分别为29.3%和27.6%;差异均无统计学意义。肝功能损害;放射性食管炎及放射性肺炎发生率两组差异亦无统计学意义。肾功能损害发生率观察组低于对照组,差异有统计学意义。恶心呕吐发生率观察组低于对照组,差异亦有统计学意义。见表1。
3 讨 论
肺癌是我国最常见的恶性肿瘤之一,70%以上的患者在确诊时就失去手术机会,有文献证明局部晚期NSCLC患者的淋巴结、骨髓、血液中检出微小转移阳性率为31%~100%,发生微小转移者的局部复发率、远处转移发生率显著增高,局部病灶未控或复发、远处转移是局部晚期NSCLC治疗失败和生产率低的重要原因之一。理论上单纯化疗能控制远处微小转移灶,放疗能控制局部病灶。但有学者报告单纯化疗后有80%的患者死于局部复发,单纯根治性放疗后有70%~80%的患者死于远处转移,1年生产率为52.3%,3年生产率仅20%。因而人们逐渐认识到放射治疗结合化疗有望提高局部晚期NSCLC患者局部控制率和生产率。Ready和Vokes[8]认为目前治疗局部晚期NSCLC的最好方法是化疗加放疗的综合治疗,有相互协同、相互补充、相互加强作用。因此美国国立癌症研究所及2003年ASCO会议提出同步放化疗是治疗失去手术指针的局部晚期NSCLC的标准方案[9]。目前,临床上多采用紫杉醇联合顺铂同步放化疗,但由于顺铂胃肠道不良反应严重,多数患者无法耐受而终止治疗。奈达铂为第二代铂类抗癌药物。作用机制为与水结合产生多种离子型物质,与碱基结合,通过抑制DNA复制而发挥抗肿瘤作用,已证实结合的碱基位点与順铂相同,其水溶性比顺铂高10倍。与顺铂无交叉耐药。
本研究用奈达铂代替顺铂与紫杉醇联合治疗初治的无法手术的Ⅲ期非小细胞肺癌,有效率达到81.8%,与顺铂疗效相近,但却大大增强了患者的耐受性。首先能够配合完成的同步放化疗的患者比例增高,;其次胃肠道不良反应轻于顺铂,也相应让患者保持了体质量,提高了生活质量;最后肾毒性低于顺铂,也增加了药物的安全性。综上,奈达铂与紫杉醇结合同步放化疗,对无法手术的Ⅲ期非小细胞肺癌患者的疗效确切,不良反应轻。值得临床推广使用。
[1] Non-small cell lung cancer collaborative group.Chemotherapy in non-small cell lung cancer:a Meta analysis using update on individual patients from 52 radomized clinical trials [J].Br Med J, 1995,311(7010):899-909.
[2] 殷蔚伯,谷铣之.肿瘤放射治疗学[M].3版.北京:中国协和医科大学出版社,2002:623-642.
[3] 吴一龙,瘳美琳,蒋国樑,等.局部晚期非小细胞肺癌诊断治疗之共识[J].中华肿瘤杂志,2002,24(6):576-578.
[4] Cai YP,Xu S,Lin SJ,et al.Comparison of outcomes of Taxol Cisplatin and Taxol Nedaplatin chemotherapy regimens for advanced non-samll cell lung cancer [J].Zhonghua Zhong Liu Za Zhi,2010,1(32):74.
[5] 喻志冲,王贺芳,田大龙.长春瑞滨加奈达铂同步三维适形放疗治疗晚期非小细胞肺癌[J]. 中国临床医学,2009,3(16):359.
[6] 孙燕.内科肿瘤学[M].北京:人民卫生出版社,2001:994-996.
[7] 申文江,王绿华.放疗损伤[M].北京:中国医药科技出版社,2001: 256-260.
[8] Ready NE,Vokes EE.Induction or consolidation systemic therapy in the multimodality treatment of unresectable locally advanced non-small cell lung cancer[J].Lung Cancer,2003,42(1):65-69.
[9] ARA AV,Merrins K,Craigw W,et al.Cancer Medicine 6[M].ASCO, 2003.
The Research of Paclitaxel Weekly Combined with Nedaplatin or Cisplatin Concurrent with Radiotherapy and Chemotherapy for Advanced Ⅲ Non-small Cell Lung Cancer
ZHONG Shi-shou, DU Chi
(Cancer Center, Najiang Second People's Hospital, Neijiang 641003, China)
Objective To observe efficacy and adverse reactions of the low-doses of paclitaxel weekly combined with nedaplatin or cisplatin concurrent with radiotherapy and chemotherapy for locally advanced non-small cell lung cancer (NSCLC). Methods 58 patients with inoperable stage III non-small cell lung cancer (22 cases with IIIa and stage 36 cases with IIIb) were randomly divided into observation group and control group. In observation group of 29 cases: paclitaxel 45mg/m2d1+ nedaplatin 25 mg/m2d1 once a week, while in control group of 29 cases: paclitaxel 45mg/m2d1 + cisplatin 25 mg/m2d1. All pationts in two groups accepted three-dimensional conformal radiotherapy (GTV: 6600cGy/30f/6+w, CTV: 6000 cGy/30F/6+w, PTV: 5400 cGy/30F/6+ w). Results In observation group CR 1cases, PR 17cases, the total response rate (CR+PR) was 66.7%, and in the control group: CR 0 cases; PR 15 cases, the total response rate (CR+PR) was 71.4% (P>0.05), the difference was not statistically significant between two groups. There was no significant difference in two groups patients with leukopenia, anemia, liver damage, radiation pneumonitis and radiation esophagitis, respectively; but renal damage, nausea, vomiting and weight loss (>10%) rate were significantly lower than the control group, with statistically significant (P<0.05). Conclusion The effective between two regimens is the same for locally advanced non-small cell lung cancer, but paclitaxel combined with nedaplatin is better tolerated than paclitaxel plus cisplatin when synchronous radiotherapy .
Paclitaxel; Nedaplatin; Cisplatin; Concurrent chemoradiotherapy; Locally advanced non-small cell lung cancer
R734.2
B
1671-8194(2013)20-0054-02

