原子吸收法测定电解质各组分的分析方法研究
石玉英,闫月娥,王益梅
(攀枝花钢企欣宇化工有限公司,四川攀枝花 617000)
1 前言
镁电解技术是海绵钛生产过程中实现物料循环利用必不可少的重要环节,而电解质成分是影响电解效率的关键因素。因此,准确测定电解质混合物中各组分的含量对于合理调配电解质混合物的组成、提高电解效率有着重要的意义。目前检测电解质中各组分元素大部分厂家都用化学滴定方法进行,此方法一方面滴定终点不容易判断,另一方面需要时间较长(完成一个样大约需要2小时)。为提高电解质组分的检测精度及检测效率,我们曾多次试验用ICP对电解质组分进行检测,但在试验中发现电解质中Ca、Mg、Na三种元素由于其外层电子排布的影响,这三种元素非常易电离元素。尤其是钠[1],若用ICP来测量,结果不可避免的会偏低,因为ICP火焰温度高,样品一喷入火焰中,立即电离,即便加入电离抑制剂也作用不大,这时检测器很容易漏检,结果肯定偏低。若用原子吸收法测量,其采用空气—乙炔火焰,温度低,再加上有适量的SrCl2、CsCl做电离抑制剂,适当的调节酸度和波长选择等一系列条件协调控制就能达到快速准确测定的目的。
2 试验部分
2.1 试验原理
将试液喷入火焰中,使钙、镁、钠原子化,在火焰中形成的基态原子对特征谱线产生选择性吸收,将测得的样品的吸光度和校准溶液的吸光度进行比较,确定样品中被检测元素的浓度[2]。
2.2 试验方法
取0.2000 g(精确到0.0001 g)的样品放入一个100 ml的烧杯中,用30 ml的蒸馏水溶解,用定量滤纸过滤上述溶液,用蒸馏水清洗滤纸上的滤渣和烧杯壁几次,并将滤液转移到一个200 ml的容量瓶中,用纯水定容并揺匀。从定容好的样品溶液中取10 ml转移到100 ml的容量瓶中,定容,用原子吸收测定。
3 结果与讨论
3.1 仪器分析参数的设定
我们用北京普析通用有限责任公司生产的原子吸收光谱仪TAS-990 Super进行试验,初步设定仪器的运行参数见表1。
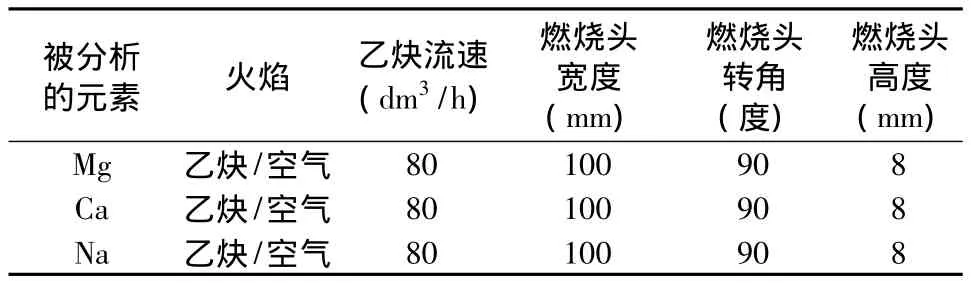
表1 各检测元素的分析条件及参数
3.2 待测元素的浓度范围
按照生产工艺要求多极镁电解槽运行最佳电解质组分为电解质中CaCl2、MgCl2、NaCl含量分别在 24.0% ~26.0%、15.5% ~18.5%、53.5% ~62.5%。
3.3 干扰元素的消除
干扰元素主要包括其它元素对待测元素的干扰及待测元素之间的干扰[3]。
3.3.1 背景干扰的消除
根据多极镁电解槽生产工艺,我们知道电解质中存在0.2% ~0.3%的Al及微量硫酸盐、硅酸盐,在用原子吸收测定电解质中Ca、Mg含量时,Al及硫酸盐、硅酸盐的存在对Ca、Mg的测定有很大影响。这是由于Al及硫酸盐、硅酸盐形成稳定的钙盐而干扰钙的测定,加入5.0 ml的1.0%SrCl2作为稀释剂可以与Al及硫酸盐、硅酸盐形成更稳定的化合物,释放出 Ca、Mg,从而消除干扰[4]。碱金属钠的电离电位小于6eV,在空气—乙炔火焰中容易电离,导致吸光度降低,在分析溶液中加入2.0 ml的0.1%CsCl电离抑制剂,大大增加火焰中的自由电子浓度,使平衡向有利形成基态原子的方向移动,增大基态原子浓度。在试验中我们分别用SrCl2溶液及CsCl溶液做稀释剂及抑制剂跟不加稀释剂及抑制剂进行对比,分别测量5次,具体情况见表2。
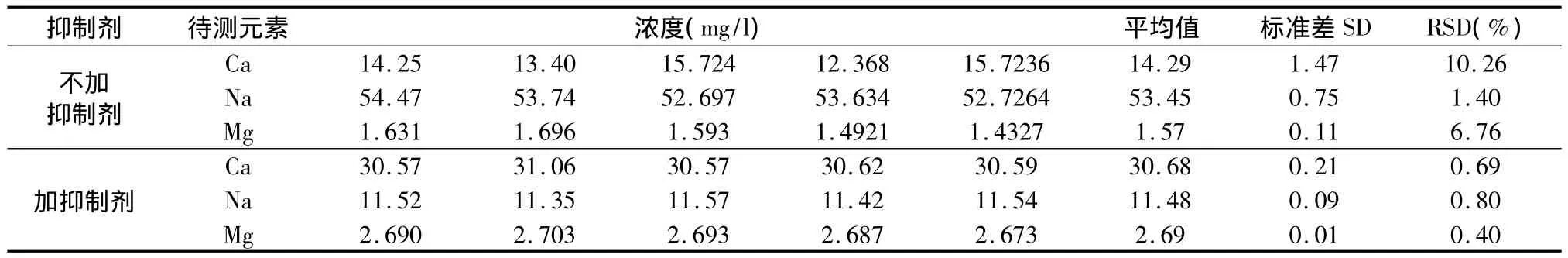
表2 水和SrCl2溶液定容对应检测浓度
从表3可以看出,加入抑制剂后检测数据明显稳定,因此选用SrCl2溶液作为稀释剂可以消除Al及硫酸盐、硅酸盐对钙、镁测定的干扰,加CsCl电离抑制剂可以消除背景对钠离子检测的干扰。
3.3.2 待测元素之间干扰的消除
分别对不同含量Na和Ca、Mg混合标准溶液及加入SrCl2后的标准溶液进行测定,考核电解质样品中Ca、Mg、Na共存时各元素间的干扰及测定Ca、Mg时加入SrCl2对Na的测定的干扰,测定结果显示,Ca、Mg、Na之间基本没有干扰。但加入SrCl2后对Na的测定有影响,使Na的测定值偏低,因此进行电解质样品分析时需配置Na和Ca、Mg两套混合标准系列测定。
3.4 标准曲线和波长的选择
按照生产工艺要求镁电解电解质中CaCl2、MgCl2、NaCl含量分别在 24.0% ~26.0%、15.5% ~18.5%、53.5% ~62.5%,选择合适的标准曲线的浓度梯度,对应的回归方程及相关系数和标线见表3。
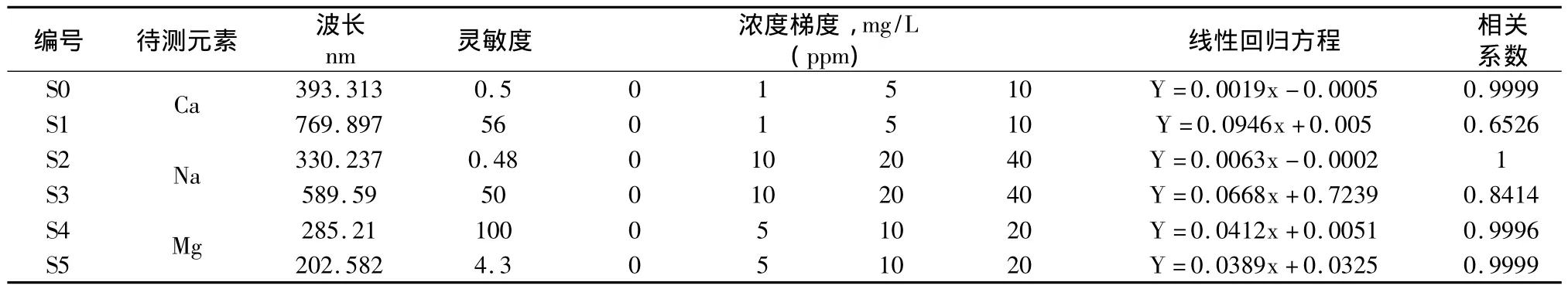
表3 电解质中各成分对应标准曲线的浓度梯度表
分析波长一般选择灵敏度相对较高的主灵敏线,但从表3可以看出主灵敏线由于对应的吸收光强太强,背景干扰严重,导致标线不稳,因此选择灵敏度相对较低的次灵敏线作为分析线较为合理,即Ca选393.313 nm、Na选330.237 nm、Mg选202.582 nm作为本方法的分析线。
3.5 验证分析方法的精密度
对同一样品进行10次平行试验,求得相对标准偏差,计算变异系数,验证该方法的精密度,具体数据见表4。
由表4数据表明,分析项目的相对标准偏差小于5%,证明该分析方法准确性高,精密度好。
3.6 回收率实验
采用标准加入法测定各个方法的回收率[5]。在5个用该方法己测定的试样溶液中,分别加入已知量的Ca、Na、Mg标样,再用该方法进行测定。根据原含量、加入量和测定量计算回收率,结果见表5。由表5可知,该方法的回收率在96.1%~104.4%之间,回收率较好,表明所采用的分析方法准确有效。
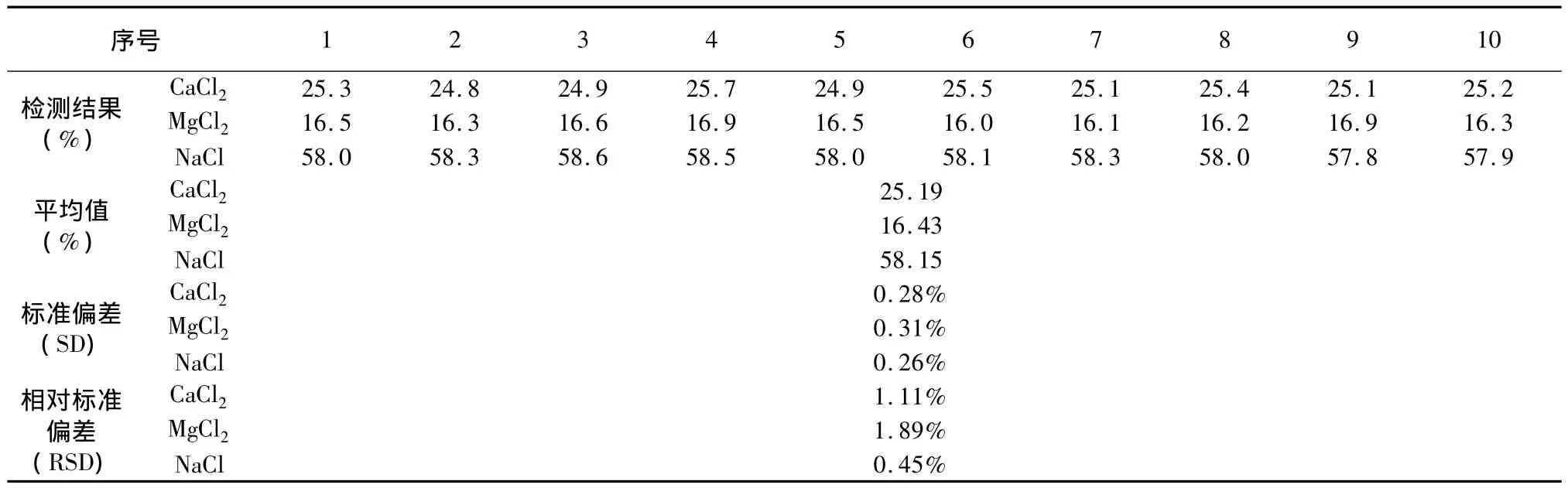
表4 精密度实验

表5 电解质中Ca、Na、Mg含量测定方法回收率实验数据表
4 结论
原子吸收法测定镁电解电解质组分的测定条件为:用5 ml的1.0%的SrCl2溶液作为稀释剂,加2 ml的0.1%的CsCl电离抑制剂可以消除背景对检测元素的干扰,测定波长分别为 Ca 393.313 nm、Na 330.237nm、Mg 202.582 nm,相对标准偏差CaCl2为1.11%、NaCl为0.45%、MgCl2为1.89%,加标回收率为96.1%~104.4%。该方法具有操作简便、快速、测量范围大、准确性高、精密度好等优点,可以满足镁电解电解质组分含量的测定要求。
[1] 武汉大学.分析化学[M].第3版.北京:高等教育出版社,1995.
[2] 郭德济.光谱分析法[M].重庆:重庆大学出版社,1999.
[3] 林世光.冶金化学分析[M].北京:冶金工业出版社,1981.
[4] 李树信.原子吸收光谱分析中的干扰及消除方法[M].北京:北京大学出版社,1987.
[5] Zhang G Y,Wang Y H,Wang J J.Continuous determination of Cu,Cr,Co,Ni,Pb and Cd in geochemical exploration samples by HG-AAS[J].Guangpuxue Yu Guangpu Fenxi,22(3):487-490.

