聚4-氨基丁酸修饰碳纳米管掺杂碳糊电极的制备及其对多巴胺的测定*
郑新宇,周学酬,郑舒燕,苏 妍,郑丽辉,林瑞余*
(1.福建农林大学生命科学学院,福州350002;2.福建农林大学植物保护学院,福州350002;3.福建省职业病与化学中毒预防控制中心,福州350002)
多巴胺(Dopamine,DA)是哺乳动物中枢神经系统中的一种非常重要的信息传递物质[1]。脑组织内多巴胺神经能与多种病症,如帕金森病、亨丁顿舞蹈症和多动症等息息相关[2-4]。目前,测量DA浓度的方法有滴定法[5]、分光光度法[6]、液相色谱法[7]等。与这些检测方法相比,电化学方法具有简便、快捷、灵敏度高、成本低廉等优点,目前已成为一种重要的分析手段。但由于DA在固体电极上的过电位较大,因此用未修饰的固体电极对DA进行直接测定,灵敏度一般较低。经过化学修饰的电极,能降低过电位并增加DA的传质速率,可提高测定DA的灵敏度,因此在DA的测定中越来越受到重视[8-9]。目前常见的电极修饰有聚合膜、Nafion膜和碳纳米管等[10-13]。其中氨基酸聚合膜广泛用于制备化学修饰电极,如半胱氨酸、赖氨酸、甘氨酸、组氨酸、谷氨酸、精氨酸、脯氨酸、丝氨酸、色氨酸、异白氨酸、天冬氨酸等[14]。氨基酸聚合膜修饰电极具有稳定性好、使用寿命长等特点,被大量应用于实际样品中多巴胺的分析测定[8-9,15-16],提高了检测的灵敏度。目前未见4-氨基丁酸(4-ABA)聚合膜修饰电极用于多巴胺测定的相关报道。本文采用在碳糊中掺入碳纳米管制备碳纳米管掺杂碳糊电极(CNTPE),并在电极表面修饰 4-ABA,制成 P-4-ABA/CNTPE,并对DA进行测定,结果显示DA峰电流大大增加,电位差减小。制备的电极具有简单,不易脱落,稳定性好及抗干扰能力强等特点。
1 实验部分
1.1 实验仪器及试剂
CHI660D电化学工作站(上海辰华仪器公司)。
采用三电极系统:自制的P-4-ABA/CNTPE为工作电极,Ag/AgCl为参比电极,铂丝为辅助电极。PHS-3C型精密酸度计(上海大普仪器厂)用于测量溶液的pH值。
光谱纯石墨粉、碳纳米管、液体石蜡、4-ABA购自上海国药,盐酸多巴胺(DA)、抗坏血酸(AA)和尿酸(UA)购自中国生物药品制品检验所,盐酸多巴胺注射液购于广州白云山明兴制药有限公司。其余常用试剂均为分析纯以上试剂,实验用水为二次蒸馏水。
1.2 修饰电极的制备
称取适量的石墨粉,然后加入适量的液体石蜡与适量的碳纳米管混合,研磨均匀(时间5 min),将此碳糊压入电极管的顶端凹槽(直径3 mm,深2 mm),填充紧密,压实,然后在称量纸上打磨光滑。用二次蒸馏水冲洗电极头,常温下晾干备用。得到CNTPE。将制备好的 CNTPE置于含有0.02 mol/L 4-ABA 的0.02 mol/L 磷酸缓冲液(pH 5.0)中,在-0.5~2.0 V电位范围内循环扫描6圈(扫描速度200 mV/s),取出用水冲洗干净,即得 P-4-ABA/CNTPE。上述所有实验均在室温下进行。
1.3 多巴胺测定方法
取含一定量DA标准液的BR缓冲液(pH 2.0)5 mL于电解池内,采用三电极体系在0.2 V~1.2 V电位范围内进行 CV扫描。DA在 P-4-ABA/CNTPE上于0.710 V处出现了明显的氧化峰,在0.604 V处出现还原峰,基于氧化峰峰型好,峰电流大于还原峰,本实验则采用记录氧化峰峰电流与DA浓度的关系进行检测。
2 结果与讨论
2.1 碳糊电极制备
2.1.1 碳纳米管的影响
试验中固定石墨粉与液体石蜡的质量分别为0.2 g 和 0.1 g,然后分别掺入 0、0.01 g、0.02 g、0.03 g、0.04 g、0.05 g、0.06 g 的碳纳米管,研究碳纳米管加入量变化时DA响应电流的变化情况,结果表明,随着碳纳米管加入量的增加,P-4-ABA/CNTPE对DA的响应电流出现先增加后减少的趋势。由于碳纳米管具有很大的表面积,掺入碳糊电极可增大电极的电化学反应面积,使多巴胺在电极上的反应电流增大。但碳纳米管用量过大,会吸附更多的液体石蜡,反而不利于增大电极的电化学反应面积,而导致DA的响应电流减小。当碳纳米管量为0.04 g(质量分数为16.67%)时,P-4-ABA/CNTPE 对 DA 的响应电流最大(如图1)。因此本试验选择碳纳米管的量占石墨粉与碳纳米管总量16.67%。
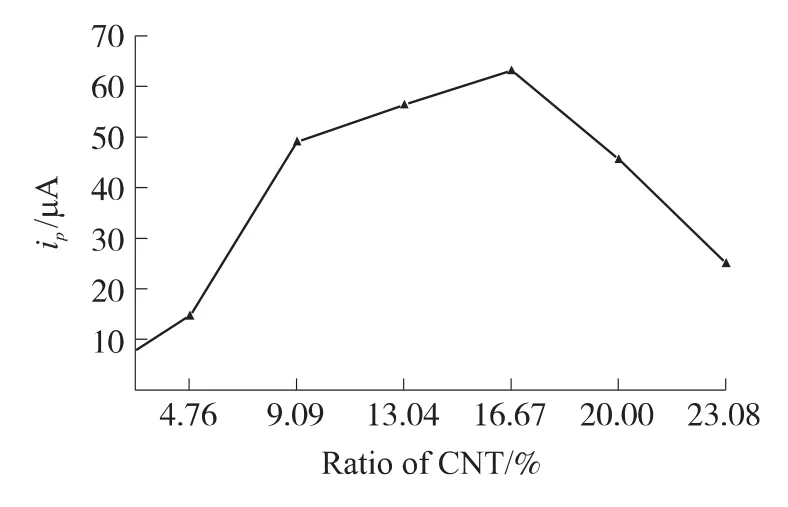
图1 碳纳米管比例对DA氧化峰电流的影响
2.1.2 粘合剂的影响
液体石蜡作为CNTPE的粘合剂,为了考察粘合剂的影响。固定碳纳米管的量占石墨粉与碳纳米管总量16.67%的前提下,逐步改变液体石蜡与石墨粉和碳纳米管总量的比例。试验表明,随着液体石蜡含量的提高,峰电流逐渐减小(如图2),但石蜡比例偏小会导致电极强度变差,碳糊容易脱落。当液体石蜡与石墨粉和碳纳米管总量的比例为1∶3时,峰电流较大,机械强度也较好。所以本试验选择粘合剂与固体粉末的比例为1∶3。

图2 粘合剂比例对DA氧化峰电流的影响
2.2 电聚合条件的影响
2.2.1 聚合底液pH的影响
试验选定磷酸盐缓冲溶液(PP)作聚合底液,分别试验了pH值为5.0~8.0的磷酸盐缓冲溶液进行电聚合,并将聚合后的P-4-ABA/CNTPE对2.0×10-5mol/L DA进行CV扫描。试验结果得出:不同酸度底液聚合得到的电极对DA峰电流和峰电位均有影响:随着底液pH值的不断增大,响应电流不断减小,氧化峰电位不断负移,还原峰电位不断正移。故实验选定pH为5.0的PP缓冲溶液作聚合底液。
2.2.2 聚合底液4-ABA浓度的影响
在选定的pH为5.0的磷酸盐缓冲溶液中进行电聚合,逐步提高底液 4-ABA的浓度,分别为:0.005 mol/L、0.01 mol/L、0.02 mol/L、0.04 mol/L和0.06 mol/L。然后将聚合后的 P-4-ABA/CNTPE电极对2.0×10-5mol/L DA进行CV扫描。结果发现4-ABA的浓度对聚合后电极的性能有较大的影响,结果如图3所示。当4-ABA的浓度过大时,所得P-4-ABA/CNTPE电极对DA的响应峰电流较小,测量重现性较差,这可能是高浓度聚合得到的膜比较致密,表面积下降造成的。但若其浓度过低,修饰电极对DA的响应电流也很小,这可能是电极表面的聚合物膜覆盖程度低所致[17]。故实验选定浓度为0.02 mol/L的4-ABA磷酸缓冲溶液为聚合底液。

图3 修饰剂浓度对DA氧化峰电流的影响
2.3 4-ABA在碳纳米管掺杂碳糊电极上的电聚合
图4所示为4-ABA在碳糊电极上的电聚合曲线。在扫描第一圈时,氧化峰电流较小,峰形不明显,这可能是因为开始时碳纳米管碳糊电极导电性较差引起的。到了第二圈后,峰电流变大,峰形也变好了,这说明聚合一圈后,4-ABA在电极表面再聚合变得更容易。因为聚4-ABA是导电聚合物,第一圈扫描后碳纳米管碳糊电极表面修饰了部分聚4-ABA,使电极导电性增强,有利于后续4-ABA的电聚合。

图4 4-ABA在修饰电极上的电聚合循环伏安图扫速:200 mV/s;圈数:6;电位范围:-0.5 V ~2.0 V。
2.4 DA在不同电极上的循环伏安曲线
分别以 CPE(1)、P-4-ABA-CPE(2)、CNTPE(3)、P-4-ABA/CNTPE(4)为工作电极,在 DA 浓度为4.0×10-5mol/L 的 B-R 缓冲液(pH 2.0)中于 0.2 V~1.2 V进行循环伏安扫描(扫速为200 mV/s)。结果如图5所示。在CPE(1)电极上,DA出现了一对极其微弱的氧化还原峰,峰电流很低;峰型较差,ΔE1=445 mV。对于掺入碳纳米管的CNTPE(3)而言,其氧化峰电流是CPE(1)的1.5倍,还原峰则是CPE(1)的1.8倍,且氧化峰和还原峰均正移,峰电位差减为376 mV,说明碳纳米管的掺入,增大了电极表面积。P-4-ABA-CPE(2)电极是 CPE(1)电极经4-ABA修饰处理得到的,其氧化峰和还原峰电流较CPE(1)电极而言均增大,与此同时ΔE2也减少为131 mV。把 CNTPE(3)修饰 4-ABA得到的电极P-4-ABA/CNTPE(4)对DA进行测定,电极响应电流为变为原来的2.4倍,电位差变为106 mV。比较上述四种电极对DA的循环伏安曲线,可以发现P-4-ABA/CNTPE(4)电极对DA的响应电流最大,峰形最佳,峰电位差最小。本实验采用该电极作为工作电极,建立检测DA的方法。

图5 DA在各种电极上的循环伏安图扫速:200 mV/s。
2.5 扫描速率的影响
在扫速 10 mV/s~600 mV/s下对含 1.0×10-4mol/L的DA在0.02 mol/L、pH 2.0的 BR 缓冲溶液中进行线性伏安扫描(如图6),随着扫速v的增加,DA的氧化峰峰电位逐渐正移,还原峰峰电位逐渐负移。其氧化峰电流和还原峰电流与扫速的平方根呈线性关系,线性方程分别为 ip=2.515 8 V1/2-1.057 6,R2=0.994 8,ip=2.502 5 V1/2-2.548 6,R2=0.992 7。由此可见,DA在P-4-ABA/CNTPE上的电化学反应是受扩散控制的[18]。

图6 DA在修饰电极上的线性扫描伏安图
2.6 富集时间的选择
浓度为4.0×10-5mol/L 的 DA,在 pH 2.0 的 BR缓冲介质中,以修饰电极为工作电极,分别静置富集2 s、5 s、10 s、20 s、30 s,结果表明,静置时间为 10 s时,峰电流即达最大。因此试验选择静置10 s后,再进行CV扫描。
2.7 修饰电极的重现性
对4.0×10-5mol/L的DA进行10次重复测定,峰电流的相对标准偏差RSD为4.13%。这表明该P-4-ABA/CNTPE对DA的测定具有良好的重现性。同样研究了该修饰电极的稳定性,将该修饰电极放置10 d后,再对相同浓度的DA进行测量,峰电流值仅下降5.23%,表明该P-4-ABA/CNTPE具有较好的稳定性。
2.8 DA在修饰电极上的线性范围和检测限
在最优实验条件下,利用循环伏安法(CV)对DA进行测定。发现DA氧化峰电流与其浓度在8.0×10-5~5.3×10-7mol/L 内呈线性关系,回归方程为 ip=0.087 3C+0.451 6(ip为峰电流/μA,C 为浓度/μmol/L,R2=0.9941),检测限为2.0×10-7mol/L。
2.9 干扰实验
按试验方法对4.0×10-5mol/L的DA溶液进行测定,当相对误差<5%时,100倍的柠檬酸,10倍的酒石酸,50倍的葡萄糖,400倍的氯化钠、氯化钾和200倍的氯化钙不干扰测定。
对2.0×10-5mol/L 的 DA 和 2.0×10-3mol/L 的AA、2.0×10-5mol/L的UA存在的混合液中进行CV 扫描。试验结果如图7所示,AA、DA和UA的电位分别为0.405、0.710、0.835V,100 倍的 AA 以及同等浓度的UA的存在并不干扰DA的测定。三者可以明显分离开,说明P-4-ABA/GCE电极对DA具良好的选择性,可在AA和UA存在的溶液中对DA进行测定。

图7 AA,DA和UA在修饰电极上的循环伏安图
2.10 样品的测定及加标回收率实验
量取1 mL盐酸多巴胺注射液(标示浓度为10 g/L,2 mL/支)先用蒸馏水稀释100倍,后量取1 mL该稀释液于100 mL棕色容量瓶中,用pH 2.0的BR缓冲溶液定容,采用标准加入法进行定量测定。结果见表1。将一男性志愿者的尿样,用pH 2.0的BR缓冲溶液稀释200倍后,采用P-4-ABA/CNTPE进行测定,结果见表2。从表1、表2可以看出,两种实际样品的回收率分别在87.50% ~104.26%和92.30% ~97.04%之间,说明该方法可用于实际样品的测定。
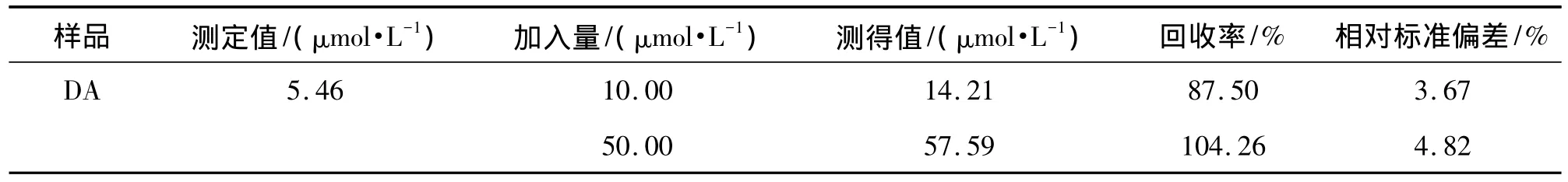
表1 盐酸多巴胺注射液测定结果(n=5)

表2 实际尿样测定结果(n=5)
3 结论
本文制备的P-4-ABA/CNTPE修饰电极,对DA具有良好的电催化作用,可较大程度提高DA检测的灵敏度。P-4-ABA/CNTPE制作简单、成本低廉、稳定性好,在用于盐酸多巴胺注射液和人体实际尿样的测定时,结果令人满意。
[1]Wightman R M,May L J,Michael A C.Detection of Dopamine Dynamics in the Brain[J].Anal Chem,1988,60:769A-779A.
[2]Neubold C,KalcberK,Diewald W,etal.Voltammetric Determination of Nitrate with a Modified Carbon Paste Electrode[J].Electroanalysis,1994(6):227-236.
[3]Gerhardt G A,Gezanagy O G,Moghaddam B,et al.Nafion-Coated Electrode with High Selectivity for CNS Electrochemistry[J].Brain Research,1984,290:390-395.
[4]Rice M E,OkeA,BradberryC W,etal.Simultaneous Voltammetric and Chemical Monitoring of Dopamine Release in Situ[J].Brain Reseach,1985,340:151-155.
[5]Salem F B.Spectrophotometric and Titrimetric Determination of Catecholamines[J].Talanta,1987,34(9):810-812
[6]Maminski M,Olejniczak M,Chudy M,et al.Spectrophotometric Determination of Dopamine in Microliter Scale Using Microfluidic System Based on Polymeric Technology[J].Analytica Acta,2005,540(1):153~157
[7]Guan C L,Ouyuang J,Li Q L,et al.Simultaneous Determination of Catecholamines by Ion Chromatography with Direct Condutivity[J].Talanta,2000,50(6):1197-1203
[8]Zhang W,Yuan R,Chai Y Q.A Simple Strategy Based on Lanthanum-Multiwalled Carbon Nanotube Nanocomposites for Simultaneous Determination of Ascorbic Acid,Dopamine,Uric Acid and Nitrite[J].Sens Actuat B 166-167(2012)601-607.
[9]Chitravathi S,Kumara Swamy B E,Mamatha G P,et al.Simultaneous Electrochemical Determination of Dopamine and Ascorbic Acid Using Poly(L-Serine)Modified Carbon Paste Electrode[J].Journal of Molecular Liquids,2011,160:193-199.
[10]刘蓉,钟桐生,雷存喜.多巴胺电化学传感器的研究进展[J].化学传感器,2011,31(3):10-15.
[11]王存嫦,阳明辉,鲁亚霜,等.一种新的多层碳纳米管复合膜修饰的葡萄糖生物传感器制备[J].传感技术学报,2003,20(1):18-21.
[12]张晓敏,任春生,应敏,等.四氨基钴酞菁(CoTAPc)在金电极上成膜过程的研究[J].传感技术学报,2004,2:306-313.
[13]许红岩,王丽莉,王彦怀,等.没食子酸在Nafion/单壁碳纳米管/聚(3-甲基噻吩)复合膜修饰电极上的电化学行为及测定[J].传感技术学报,2008,21(7):1113-1118.
[14]王春燕,李云辉,田坚.氨基酸化学修饰电极的制备及其应用[J].长春理工大学学报(自然科学版),2011,34(1):150-153.
[15]杨怀成,陆喜良,魏万之.聚L-丝氨酸/碳纳米管复合导电薄膜的制备及在多巴胺的电化学测定中的应用[J].化学试剂,2010,32(10):907-909.
[16]孙登明,由文颖.聚L-谷氨酸修饰电极的制备及对多巴胺的测定[J].分析科学学报,2005,21(5):530-532.
[17]廖文利,李忠彬,李念兵.抗坏血酸在聚L-谷氨酸修饰玻碳电极上的电化学行为研究[J].重庆文理学院学报(自然科学版),2010,29(5):57-60.
[18]李启隆,胡劲波.离子注入修饰电极及其在药物分析中的应用[J].化学通报,2000,63(3):32-36.

