LC-MS/MS 法同时测定口炎清颗粒中8种成分
张子建, 孙冬晓, 王 婧, 董立华, 郭盼盼, 王春英*
(1.河北省中医院口腔科,河北 石家庄050011;河北医科大学药学院药物分析教研室,河北 石家庄050017;河北医科大学第一医院药剂科,河北石家庄 050031)
LC-MS/MS 法同时测定口炎清颗粒中8种成分
张子建1, 孙冬晓2, 王 婧3, 董立华2, 郭盼盼2, 王春英2*
(1.河北省中医院口腔科,河北 石家庄050011;河北医科大学药学院药物分析教研室,河北 石家庄050017;河北医科大学第一医院药剂科,河北石家庄 050031)
目的 建立用液相色谱-串联质谱法同时测定口炎清颗粒 (天冬、麦冬、玄参、山银花、甘草)中8种成分的方法。方法 采用C18色谱柱,以甲醇-水为流动相,梯度洗脱。采用混合线性离子肼,电喷雾离子源,多反应离子检测和负离子模式进行扫描,对口炎清颗粒中哈巴苷、甘草苷、绿原酸、肉桂酸、甘草酸、甘草次酸、鲁斯可皂苷元、菝契皂苷元等8种化学成分进行同时检测。结果 所有被测物的线性关系良好 (r>0.999);方法回收率为100.5%~107.6%,RSD为1.3%~3.2%。结论 此方法准确,快速,重复性好,有望为口炎清颗粒的质量控制提供依据。
口炎清颗粒;液相色谱-串联质谱;质量控制
口炎清颗粒是由天冬,麦冬,玄参,山银花和甘草五味中药组成的复方制剂,具有滋阴清热,解毒消肿之功效,用于治疗阴虚火旺所致的口腔疾病[1-3]。目前,对于该制剂的质量控制主要是以绿原酸为指标成分的高效液相色谱法[1,4-5]。虽有文献对口炎清颗粒的指纹图谱进行了研究,并对一些色谱峰进行了归属研究,但缺乏定量数据,并且由于采用的是高效液相色谱法,分析周期长达2 h[6]。液质联用 (LC-MS/MS)技术具有专属性好,灵敏度高和快速高效的特点,已逐渐成为中药成分定量分析的有效方法[7-8]。本研究采用混合线性离子肼,电喷雾离子源,多反应离子检测和负离子模式进行扫描,同时测定口炎清颗粒中哈巴苷、甘草苷、绿原酸、肉桂酸、甘草酸、甘草次酸、鲁斯可皂苷元和菝契皂苷元8种成分,为口炎清颗粒的质量控制提供参考。
1 仪器与试药
3200 Q-Trap型串联三重四级杆质谱仪,Analyst 1.4.2分析软件 (美国AB公司);Agilent 1200液相色谱仪,包括G1311A型四元梯度洗脱泵,G1329A型自动进样器和G1322A型在线脱气仪(美国 Agilent公司)。口炎清颗粒 (规格:10 g/袋,批号为 C1A028,D2A012,C2A020,厂家为广州白云山和记黄埔中药有限公司)。菝契皂苷元、鲁斯可皂苷元、哈巴苷和甘草酸对照品 (南京泽朗医药科技有限公司),肉桂酸和绿原酸对照品 (中国食品药品检定研究院),甘草苷和甘草次酸对照品 (上海宝曼生物科技有限公司),所有对照品纯度均大于98%。甲醇 (色谱纯,Fisher公司),甲酸及其他试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件 Diamonsil C18色谱柱(4.6 mm ×150 mm,5 μm);流动相为甲醇 (A)-水 (B),梯度洗脱 (A∶B为0~4 min,20∶80~60∶40;4~6 min,60 ∶40~95 ∶5;6~14 min,95 ∶5;14~14.1 min,95∶5~20∶80);柱温 35℃;体积流量0.8 mL/min;进样量5 μL。
2.2 质谱条件 电喷雾离子源;多反应离子监测,采用负离子模式扫描,源喷射电压-4 500/5 500 V;温度650℃;气帘气 25 psi(1 psi=6.895 kPa);雾化气60 psi,辅助气 65 psi。8种被测成分的化学结构、二级谱图、监测离子对、出峰时间、解簇电压和碰撞电压见图1。
2.3 溶液的制备
2.3.1 对照品溶液的制备 分别精密称取8种对照品适量,各置10 mL量瓶中,加甲醇溶解并定容,摇匀,即得对照品贮备液。精密量取各贮备液适量,置10 mL量瓶中,加50%甲醇定容,摇匀,得各化合物的混合对照品溶液。对照品溶液的色谱图见图2。
2.3.2 供试品溶液的制备 精密称取颗粒剂细粉约2.5 g,加入50%甲醇50 mL,称定质量,超声处理1 h,冷至室温,用50%甲醇补足减失的质量,摇匀,12 000 r/min离心10 min,取上清液即得。供试品溶液的色谱图见图2。
2.4 线性关系与定量限 精密量取混合对照品溶液适量,用50%甲醇定量稀释制得系列质量浓度梯度的混合对照品溶液,进样测定,记录色谱图。以对照品质量浓度C为横坐标,峰面积A为纵坐标,进行线性回归,得回归方程,结果见表1。

表1 口炎清颗粒中8种被测成分的回归方程,相关系数,线性范围及最低定量限Tab.1 Regression equation,correlation coefficient and quantitation limits of the 8 components in Kouyanqing Granules
2.5 精密度试验 取供试品溶液,连续进样6次,记录色谱图,计算哈巴苷、绿原酸、甘草苷、肉桂酸、甘草酸、甘草次酸、鲁斯可皂苷元和菝契皂苷元峰面积的 RSD分别为2.5%、1.4%、0.9%、3.1%、1.5%、1.8%、2.1%、3.2%。表明该方法具有较好的精密度。
2.6 稳定性试验 将供试品溶液于室温下放置0、2、4、6、8和12 h,分别进样,记录峰面积,计算哈巴苷、绿原酸、甘草苷、肉桂酸、甘草酸、甘草次酸、鲁斯可皂苷元和菝契皂苷元峰面积的RSD 分 别 为 2.7%、2.1%、1.2%、2.4%、1.6%、1.4%、1.7%、2.5%,表明供试品溶液室温放置12 h内稳定。
2.7 重复性试验 精密称取同一批号的供试品细粉6份,按2.3.2项下的方法制备供试品溶液,进样测定,计算哈巴苷、绿原酸、甘草苷、肉桂酸、甘草酸、甘草次酸、鲁斯可皂苷元和菝契皂苷元含有量的RSD分别为1.6%、2.4%、1.8%、3.1%、0.8%、1.7%、2.5%、2.9%,表明该方法的重复性良好。

图1 口炎清颗粒中8种被测成分的化学结构、二级质谱图、监测离子对、出峰时间、解簇电压和碰撞电压Fig.1 Chemical structures,the product ion spectra,MS/MS fragment ions,declustering potential(DP)and collision energy(CE)of the 8 components in Kouyanqing Granules
2.9 加样回收率试验 精密称取同一批号已知含有量的供试品细粉6份,每份1.25 g,分别精密加入各被测组分以50%甲醇为溶解的混合对照品贮备液10 mL,及50%甲醇40 mL,按2.3.2项下的方法操作,进样测定,计算各成分的平均回收率,结果见表2。
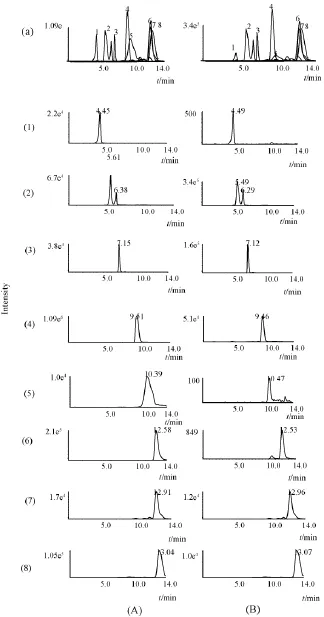
图2 对照品溶液 (A)和供试品溶液 (B)的总离子流色谱图 (a)和提取离子色谱图Fig.2 Total ionschromatograms(a)and extract ions chromatograms of standard solution(A)and sample solution(B)
2.10 样品测定 取口炎清颗粒3批,分别按2.3.2项下的方法处理,进样测定,计算各化合物的质量分数,结果见表3。
3 讨论
3.1 测定成分的选择 口炎清颗粒由五味中药组成,《中国药典》及其他文献报道只选择了山银花中的绿原酸为定量指标成分。本试验从每味中药中选择1~3个主要化学成分为测定指标,具体如下:天冬中的菝契皂苷元[9];麦冬中的鲁斯可皂苷元[10];山银花中绿原酸[11];玄参中的哈巴苷和肉桂酸[12];甘草中的甘草苷、甘草酸和甘草次酸[3]。由于此方法能够兼顾到制剂组方中的每一味药,故能较全面的控制该制剂的质量。

表2 口炎清颗粒中8种被测成分的回收率 (n=6)Tab.2 Recoveries of 8 components in Kouyanqing Granules(n=6)

表3 样品测定结果 (n=3)Tab.3 Results of sample analysis(n=3)
3.2 绿原酸的定量 在对绿原酸进行检测时,无论是选择m/z353.1→191.0,还是其他离子对,在其对照品和样品色谱图上均出现两个色谱峰。据文献报道[14],因为绿原酸的分子结构中存在双键结构,其在水溶液以顺反两种异构体的形式存在,并且互相转化,直至达到平衡。因此在定量时应按两色谱峰之和计算。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:465
[2]曾宪涛.他克莫司软膏加口炎清颗粒治疗糜烂型OLP的疗效评价[J].临床口腔医学杂志,2011,27(7):432-433.
[3]于 飞.地塞米松磷酸钠联合口炎清颗粒治疗口腔糜烂型扁平苔藓[J].中国实验方剂学杂志,2010,16(18):206,209.
[4]梅 林,袁 英,胡承波.高效液相色谱法测定口炎清颗粒中绿原酸含量[J].中国药业,2007,16(5):15.
[5]罗 杰,杨东升,欧阳慧芳,等.口炎清颗粒(无糖型)中绿原酸的含量测定[J].中国中药杂志,2003,28(8):780-781.
[6]关倩怡,黄 琳,彭 维,等.口炎清颗粒指纹图谱研究[J].中山大学学报:自然科学版,2011,50(1):115-118.
[7]Qiao Shi,Shi Rui,Liu Man,et al.Simultaneous quantification of flavonoids and phenolic acids inHerba Scutellariae barbataeand its confused plants by high performance liquid chromatography-tandem mass spectrometry[J].Food Chem,2011,129(3):1297-1304.
[8]班丽娜,徐远金.HPLC/MS同时测定双黄连口服液中的4种有效成分[J].中成药,2012,34(2):265-268.
[9]徐从立,陈海生,谭兴起,等.中药天冬的化学成分研究[J].天然产物研究与开发,2005,17(2)128-130.
[10]黄宝美,姚程炜,边清泉,等.非水毛细管电泳法同时测定麦冬中薯蓣皂苷元和鲁斯可皂苷元的含量[J].药学学报,2011,46(4):443-446.
[11]柴兴云,李 萍,唐力英.山银花化学成分研究[J].中国中药杂志,2004,29(9):865-866.
[12]师 怡,许 晖,阙慧卿,等.玄参化学成分的药理作用和分析方法[J].海峡药学,2006,18(4):58-60.
[13]吴昭晖,罗佳波,游文玮.甘草药材HPLC指纹图谱研究[J].中草药,2005,36(12):1868-1872.
[14]Clifford M N,Kirkpatrick J,Kuhnert N,et al.LC-MSnanalysis of the cis isomers of chlorogenic acids[J].Food Chem,2008,106(1):379-385.
Simultaneous determination of eight components in Kouyanqing Granules by LC-MS/MS
ZHANG Zi-jian1, SUN Dong-xiao2, WANG Jing3, DONG Li-hua2, GUO Pan-pan2, WANG Chun-ying2*
(1.Department of Stomatology,Hebei Provincial TCM Hospital,Shijiazhuang 050011,China;2.Department of Pharmaceutical Analysis,School of Pharmacy,Hebei Medical University,Shijiazhuang 050017,China;3.Department of Pharmacy,The First Hospital,Hebei Medical University,Shijiazhuang 050031,China)
AIMTo establish a LC-MS/MS method for simultaneously determining eight components in Kouyanqing Granules(Asparagi Radix,Ophiopogonis Radix,Scrophulariae Radix,Lonicerae Flos,Glycyrrhizae Radix et Rhizoma).METHODSA C18column was used with the mobile phase of methanol-water(containing 0.5 mmol/L ammonium acetate and 0.1%formic acid)in gradient elution mode.Analytes(harpagide,liquiritin,chlorogenic acid,cinnamic acid,glycyrrhizic acid,glycyrrhetinic acid,ruscogenin and sarsasapogenin)were detected using a hybrid quadrupole linear ion trap mass spectrometer that was equipped with an electrospray ionization source operating in the negative and multiple-reaction monitoring(MRM)modes.RESULTSAll the components showed good linearity(r>0.999).Their recoveries were 100.5% -107.6%with RSDs of 1.3%-3.2%.CONCLUSIONThe developed method is accurate,sensitive,rapid and suitable for the quality control of Kouyanqing Granules.
Kouyanqing Granules;LC-MS/MS;quality control
R927.2
A
1001-1528(2013)05-0952-05
10.3969/j.issn.1001-1528.2013.05.020
2012-12-26
河北省自然基金-石药集团医药联合研究基金资助项目 (C2011206170);河北省教育厅自然科学指令性课题 (2009147)
张子建 (1972—),男,主治医师,医学硕士,从事口腔医学研究。Tel:(0311)66792669,E-mail:zjzh3@163.com
*通信作者:王春英 (1972—),女,博士,副教授,主要从事中药质量控制和体内过程研究。Tel:(0311)86265625,E-mail:wangcy730301@163.com

