丹黄凝胶剂成型工艺研究
陈新民, 陈丽华, 彭稳稳, 李俊松*, 李 文
(1.南京中医药大学江苏省中药炮制重点实验室,江苏南京210029;2.江西中医学院现代中药制剂教育部重点实验室,江西南昌330004;3.南京市中医院,江苏南京 210001)
丹黄凝胶剂成型工艺研究
陈新民1, 陈丽华2, 彭稳稳1, 李俊松1*, 李 文3*
(1.南京中医药大学江苏省中药炮制重点实验室,江苏南京210029;2.江西中医学院现代中药制剂教育部重点实验室,江西南昌330004;3.南京市中医院,江苏南京 210001)
目的 研究丹黄凝胶剂的成型工艺。方法 以透皮性能作为主要评价指标,采用体外经皮渗透试验对凝胶剂基质、促渗剂和载药量进行考察。结果 以1.0%卡波姆-940为凝胶基质,2%氮酮为促渗剂,载药量为4.5%制备丹黄凝胶剂的工艺可行。结论 丹黄凝胶剂制备工艺简便,质地均匀细腻,稳定性良好。
丹黄凝胶剂;成型工艺;体外透皮;卡波姆-940
丹黄凝胶方为临床经验方,由大黄、黄柏、黄芩、丹参等八味中药组成,含有醌类、生物碱类和黄酮类等多种成分,临床上用于治疗痤疮。凝胶剂是由一些高聚物或共聚物吸收大量水分后形成的溶胀交联状态的半固体,具有良好的生物相容性,对药物的释放具有缓释、控释作用等优点,把传统的中药提取物加入凝胶基质,可增强黏附性,提高局部药物浓度,使疗效得以提高[1]。本实验以透皮性能作为主要评价指标,采用体外经皮渗透法考察了丹黄凝胶剂的成型工艺,并通过正交试验优化了丹黄凝胶剂的处方,确定了丹黄凝胶剂的制备工艺。
1 仪器与试药
1.1 仪器与材料 Agilent1100型高效液相色谱仪,HP1100型二极管阵列检测器,Agilent色谱工作站 (Agilent科技有限公司);AG285型电子天平(瑞士梅特勒-托利多公司);KQ-500超声清洗仪器 (昆山市超声仪器有限公司);YB-P6智能透皮实验仪 (天津药典标准仪器厂);改良Franz扩散池 (自制);TGL-16B型台式离心机 (上海安亭科学仪器厂);Phs-3C型pH计 (上海康仪仪器有限公司);NDJ-1型旋转黏度计 (上海天平仪器厂);ELECTRONIC BALANCE电子天平 (慈溪市天东衡器厂)。
1.2 试剂与药品 药用级Carbomer 940(北京国人逸康科技有限公司);PEG 400(上海凌峰化学试剂有限公司);Azone(国药集团化学试剂有限公司);甘油 (国药集团化学试剂有限公司);丙二醇 (成都市科龙化工试剂厂);三乙醇胺 (上海凌峰化学试剂有限公司);CMC-Na(国药集团化学试剂有限公司);药用级HPMC-E4M(上海卡乐康包衣技术有限公司);EDTA(重庆化学试剂总厂);NaHCO3(上海化学试剂有限公司);三乙胺(国药集团化学试剂有限公司);大黄酚 (0796-20005)和盐酸小檗碱 (110713-200208)对照品均由中国药品生物制品检验所提供;甲醇、乙腈为色谱纯,水为蒸馏水,其余试剂均为分析纯。雄性SD大鼠,体质量200~220 g,由南京中医药大学实验动物中心提供。
2 方法与结果
2.1 体外试验含量测定方法建立
2.1.1 色谱条件及方法学考察 Kromasil 100-5 C18色谱柱 (250 mm×4.6 mm,5 μm,江苏汉邦科技有限公司);流动相为乙腈 (A)-0.5%三乙胺(B)溶液 (磷酸调节pH至3.5),按表1中的规定进行梯度洗脱;体积流量1.0 mL/min;柱温30℃;进样量20 μL;检测波长254 nm(大黄酚)、265 nm(小檗碱),参比波长360 nm。在此色谱条件下,大黄酚和小檗碱的峰能完全分开,且样品中其他成分对测定没有干扰。大黄酚在0.345~44.20 μg/mL与峰面积呈良好的线性关系,线性回归方程为A=39.537C-12.059,r=0.999 8;盐酸小檗碱在0.449~57.50 μg/mL与峰面积呈良好的线性关系,线性回归方程为A=51.014C-30.005,r=0.999 9;其精密度RSD分别为1.09%和0.56%;稳定性RSD值分别为1.23%和0.92%;重复性RSD分别为2.55%、0.90%;平均回收率分别为100.57%、100.03%,RSD值分别为1.58%、2.09%。
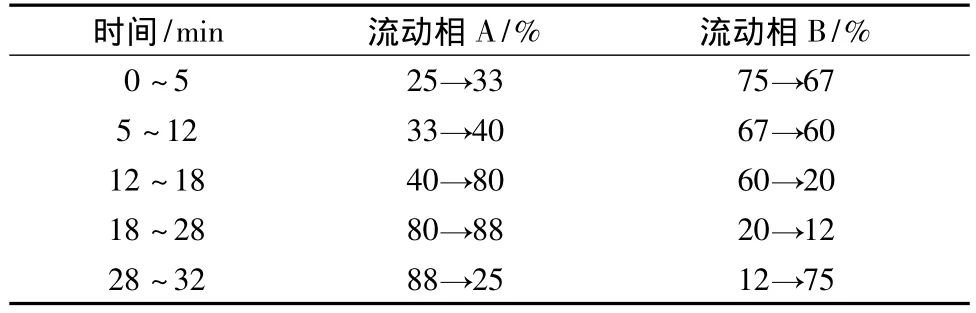
表1 梯度洗脱顺序Tab.1 Gradient elution of mobile phase
2.1.2 体外透皮测定[2]固定YB-P6型透皮扩散试验仪,在接受室中加入搅拌子和预温37℃的接受液。将新鲜制备好的离体鼠皮从生理盐水中取出,固定于改良的Franz扩散池上,使皮肤角质层面向上,将供试凝胶样品均匀涂布于鼠皮上 (注意排除气泡),接受池加入5 mL接收液[3](含30%丙二醇和20%乙醇的生理盐水溶液),外夹层以 (3±1)℃的循环水浴保温,磁力搅拌子以300 r/min的速度搅拌,分别于2、4、6、8、12、24 h取出接受液0.5 mL(同时立即补充接受液0.5 mL)。所取样品用0.45 μm微孔滤膜滤过,取续滤液20 μL进样测定含量,并计算一定时间内的单位面积累积渗透量。
2.2 丹黄凝胶成型工艺研究
2.2.1 提取物溶剂系统的选择[4]取丹黄凝胶提取物9份,每份约0.10 g,置于10 mL量瓶中,分别加入不同比例组合的混合溶剂适量,超声20 min,放至室温后用相应的溶剂定容,摇匀,离心,滤过,沉淀物于50℃真空干燥箱中烘干恒重,计算丹黄凝胶提取物的溶解量。另吸取滤液2.5 mL置10 mL量瓶中,用甲醇稀释,超声放冷后并定容,取样过0.45 μm的微孔滤膜,弃去初滤液,取续滤液进样测定。
丹黄凝胶提取物溶解量的计算方法:

丙二醇、乙醇及水不同比例组成的混合溶剂对提取物及指标成分大黄酚和小檗碱的溶解情况研究结果如表2。

表2 溶剂系统考察结果Tab.2 Results for dissolvability of extract,chrysophanol and berberine in different reagents
结果表明,提取物及指标成分大黄酚和小檗碱的溶解量均随着丙二醇和乙醇用量的增大而增大,其中溶剂组成为30%丙二醇、30%乙醇、40%水的混合溶剂对提取物及提取物中指标成分均有较好的溶解性。因此,将此比例组成的混合溶剂作为凝胶中提取物的溶剂系统。
2.2.2 凝胶基质选择[5]称取凝胶材料适量于烧杯中,加入10%的甘油搅拌均匀使其全部润湿,按比例加入适量的水,完全溶胀,得空白凝胶。另按比例称取提取物 (3%含药凝胶),加入含30%丙二醇和30%乙醇的水溶液适量,水浴上加热溶解。将提取物溶液加入到空白凝胶中,搅拌使其分布均匀后,加入三乙醇胺调节pH值,搅拌均匀,即得含药凝胶。
以成型性、涂展性为指标,将制备得到的凝胶置白色透明玻璃容器中并密封,于室温下放置0 d、15 d后进行考察。结果见表3。

表3 凝胶基质成型性考察结果Tab.3 Results for proeessing technology of the type and amount of gel matrix
通过0 d、15 d外观性状考察,以0.5%卡波姆、1.0%卡波姆、1.5%卡波姆为基质,所得的含药凝胶易涂展,黏稠度大,成型性好且稳定,以下实验选择1.0%卡波姆进行进一步研究。
2.2.3 促渗剂的选择[6-7]取卡波姆-940用适量,加入10%的甘油搅拌使其浸润,加适量水搅拌后放置过夜,使其充分溶胀。取丹黄凝胶提取物加入丙二醇研匀,再加入乙醇和适量蒸馏水,水浴上加热使其完全溶解,待冷后加入不同比例的Azone,搅拌均匀,缓慢加入上述空白凝胶基质中,在充分搅拌的同时加入三乙醇胺调节pH值,使其成凝胶状,再加入蒸馏水至足量,搅匀,即得丹黄凝胶。
按2.1.2项下对含有不同比例Azone的丹黄凝胶剂进行体外透皮渗透试验,取接受液测定含量,计算24 h内单位面积的累计渗透量[8-9],并绘制累计渗透量曲线图,见图1、2。
(1)促渗动力学方程拟合
根据24 h内各取样点接受液中指标成分大黄酚和小檗碱的累计渗透量,分别采用零级动力学方程、一级动力学方程及Higuchi方程等多种数学模型对不同质量分数Azone下的平均累计渗透量M与时间t的关系进行拟合,结果以Higuchi方程的拟合优度最高,月桂醇氮酮 (Azone)的加入大大提高了大黄酚和小檗碱透皮的速率,随着氮酮浓度的升高,促渗作用先增大后减小。当氮酮质量分数为2%时,对指标成分大黄酚和小檗碱的促渗效果均达到最大,见表4、5。

图1 Azone质量分数对大黄酚透皮渗透的影响Fig.1 Effect of Azone concentration on penetrating of chrysophanol in Danhuang Gel
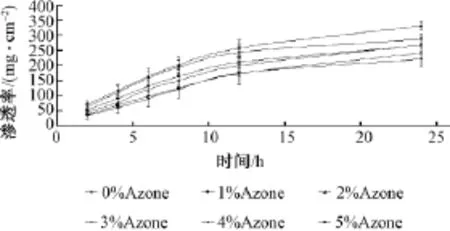
图2 Azone质量分数对小檗碱透皮渗透的影响Fig.2 Effect of Azone concentration on penetrating of berberine in Danhuang Gel
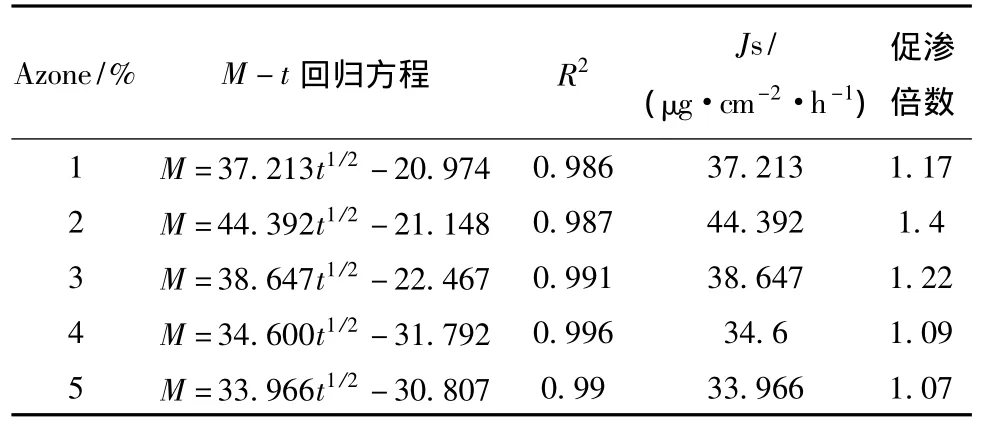
表4 大黄酚的透皮渗透动力学方程Tab.4 Model parameters for penetrating of chrysophanol in Danhuang Gel
(2)不同质量分数促渗剂相似因子分析
对含有不同质量分数氮酮的丹黄凝胶中大黄酚和小檗碱在各时间点的平均累积渗透百分率进行相似因子分析[10-11],结果表明,氮酮质量分数对凝胶中指标成分大黄酚和小檗碱的透皮渗透有显著的影响。与空白对照比较,含1%和2%氮酮的凝胶中大黄酚的体外透皮渗透有显著差异;小檗碱中只有在2%氮酮时与空白对照有显著性差异。由于2%氮酮对大黄酚和小檗碱均达最大促渗效果,因此选择2%氮酮作为丹黄凝胶剂的促渗剂。
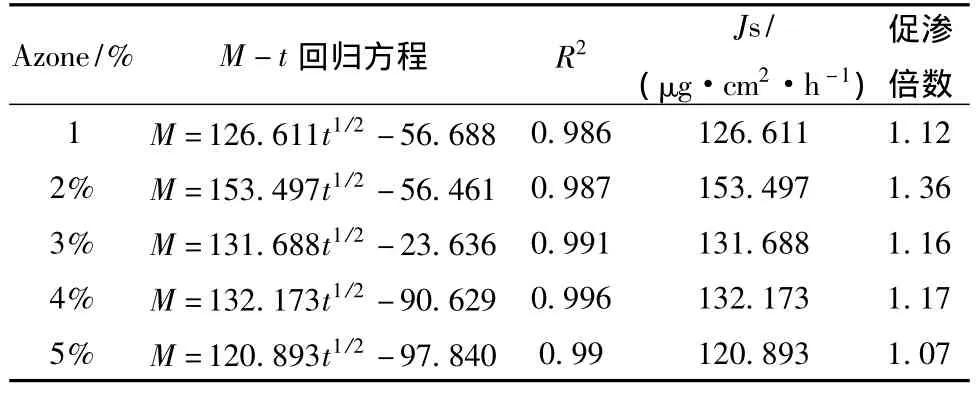
表5 小檗碱的透皮渗透动力学方程Tab.5 Model parameters for penetrating of berberine in Danhuang Gel
2.2.4 pH调节剂的选择 按照上述凝胶制备方法,最后分别加入0.5%、1.0%、1.5%、2.0%和2.5%的三乙醇胺,搅拌均匀,得不同三乙醇胺用量的丹黄凝胶。分别用10 mL烧杯取丹黄凝胶约1.0 g,加少量蒸馏水,搅拌后转移至10 mL量瓶中,加蒸馏水适量,超声波20 min,放冷后定容,离心后滤过,取滤液测定pH值,结果1.5%的三乙醇胺调节pH值使成凝胶状。
2.3 凝胶的制备 取卡波姆-940适量,加入用量为10%的甘油使其湿润,搅拌均匀并调成糊状,加蒸馏水适量,搅拌,浸泡,放置24 h使其充分溶胀,搅拌均匀,得空白凝胶,备用。依处方比例称取丹黄提取物适量,加入丙二醇后研匀,再加入乙醇和适量蒸馏水,于水浴上加热使药物充分溶解,将用量为2.0%的月桂氮卓酮加至上述溶液中,搅拌均匀,得药物的混合溶液,然后缓慢加至上述备用的空白凝胶基质中,搅拌,使药物均匀分散在凝胶基质中,最后在充分搅拌的同时加入用量为1.5%的三乙醇胺调节pH值使成凝胶状,加蒸馏水至1 000 g,搅拌均匀,既得丹黄凝胶剂。
3 讨论
凝胶剂工艺研究主要考察其透皮性能的优劣,为了保证与体内过程有良好的相关性,体外实验使用的接受液应与生理成分接近且要有较好的接收透皮药物的能力,形成漏槽条件。预试验发现常用的生理盐水和磷酸缓冲溶液对指标成分大黄酚和小檗碱不能形成漏槽条件,根据提取物溶解性研究结果,考察了以含30%丙二醇的生理盐水溶液(A)、含40%乙醇的生理盐水溶液 (B)、含30%丙二醇和20%乙醇的生理盐水溶液 (C)及含30%PEG的生理盐水溶液 (D)作为接受液,大黄酚的渗透量依次是C>B>D>A,小檗碱的渗透量依次是C>D>B>A,因此选择含有30%丙二醇(PG)和20%乙醇的生理盐水溶液作为透皮渗透试验的接受液。
对于大多数药物而言,皮肤是药物难以透过的一道生理屏障,对于脂溶液性差或太强的药物均需要加入适量的透皮促渗剂。油/水分配系数测定试验发现提取物中大黄酚和小檗碱的脂溶性都比较小,因此本实验采用透皮促渗试验考察了促渗剂氮酮及用量,结果用量为2%的氮酮促渗效果最为明显。同时还以临床用药量为基础,考察了基质的载药量,发现基质载药量会影响大黄酚和小檗碱的透皮速率,但药物的透皮速率并不是随着基质载药量的增大而无限增加,可能是因为除了与基质载药量有关外,透皮速率还与透皮有效面积有关,即一定面积的皮肤载药量是有限的。
[1]熊 欣,刘淑芝,顼佳音,等.新型载体经皮凝胶剂的研究进展[J].中国实验方剂学杂志,2011,17(22):244-249.
[2]李 燕.雷公藤甲素外用凝胶的研制[D].重庆:重庆医科大学,2008:23.
[3]魏 敏,周莉玲,黄春青,等.以主药溶解性能筛选体外经皮渗透试验中的接收液[J].中药材,2005,28(4):332-334.
[4]杨文展,郑俊民,郝劲松.毗哇酮凝胶剂的研制[J].中国医药工业杂志,1998,29(4):161-163.
[5]夏洪德.双黄冰凝胶剂的制备[J].中国医院药学杂志,1999,17(6):341-342.
[6]代 龙.风湿镇痛凝胶体外透皮实验[J].中成药,2000,22(5):324-325.
[7]王 森,朱卫丰,欧水平,等.促透剂对良肤乳膏中丹皮酚、白鲜碱、梣酮和甘草次酸的体外透皮吸收及皮肤滞留量的影响[J].中国中药杂志,2009,34(14):1778-1782.
[8]郑俊民.经皮给药新剂型[M].北京:人民卫生出版社,2006:282-284.
[9]荆蕴杰,方 亮,郭汉文.促进剂对复方脚癣灵搽剂中小檗碱和黄芩苷体外经皮吸收及其皮内滞留量的影响[J].沈阳药科大学学报,2008,25(9):679-683.
[10]Yuksel N,Kanik A,baykara T.Comparsion ofin introdissolution profiles by ANOVA-based mode-depent and independent methods[J].Int Pharm,2000,209:57-67.
[11]Gohel M C,Panchal M K.Novel use of similarity factorsf2and Sd for the development of diltiavem HCL modified-release talets using a 3(2)factorial design[J].Drug Dev Ind Pharm,2002,28(1):77-80.
Molding proeess of Danhuang Gel
CHEN Xin-min1, CHEN Li-hua2, PENG Wen-wen1, LI Jun-song1*, LI Wen3*
(1.Nanjing University of Traditional Chinese Medicine,Jiangsu Provincial Key Laboratory of Chinese Medicine Processing,Nanjing 210029,China;2.Key Laboratory of Modern Preparation of Treditional Chinese Medicine,Ministry of Education,Jiangxi University of Treditional Chinese Medicine,Nanchang 330004,China;3.Nanjing Municipal Hospital of TCM,Nanjing,210001,China)
Danhuang Gel;widding process;transdermal penetrationin vtiro;Carbomer-940
R944
A
1001-1528(2013)05-0944-05
10.3969/j.issn.1001-1528.2013.05.018
2012-05-06
江苏省中医药局科技项目 (LB09081)
陈新民 (1985—),男,硕士,从事中药制剂研究。Tel:(025)86798281,E-mail:chenxinmin411@163.com
*通信作者:李俊松 (1964—),男,博士,研究员,硕士生导师,从事中药制剂与炮制研究。Tel:(025)86798281,E-mail:lijunsong1964@163.com李 文,主任中药师,从事中药制剂与新药研究。Tel:(025)52275118,E-mail:njzyyliwen@sohu.com

