下转换发光粉体材料NaGd (WO4)2:Eu3+的制备及荧光性能研究
顾婉娜,刘连利,王莉丽,崔 岩
(渤海大学科技实验中心,辽宁 锦州 121013)
稀土荧光材料传统的制备方法为高温固相法,因水热法有着制备条件容易控制,易于获得较好形貌和结晶性的粉体颗粒的优点,近年来关于水热法制备稀土荧光材料的报道较多[1-3]。钨酸盐由于发光光谱稳定,W-O共价键构成的多面体中氧离子受到邻近高价态钨的极化作用,有可能使得激活离子浓度淬灭效应较弱,可掺杂的激活离子浓度较高而受到关注[4,5]。李志强等[6]用水热法合成了由纳米棒组成的直径为100 nm的NaGd (WO4)2:Eu3+绒球发光粉;廖定生等人[7]采用水热法合成了粒径为 1 μm的 La(WO3)3荧光粉体颗粒,无论合成了哪种形貌的荧光粉体,都显示了很强的荧光性能。本文采用水热法合成不同Eu3+掺杂浓度的NaGd (WO4)2:Eu3+荧光粉体,并研究了其荧光性能。
1 实验部分
1.1 试剂与仪器
1.1.1 试剂
氧化钆(Gd2O3,含量≥99.5%);氧化铕(Eu2O3,含量≥99.0%);钨酸钠(Na2WO4·2H2O,含量≥99.5%);硝酸(HNO3,含量≥98.0%);实验用水为去离子水。
1.1.2 主要仪器
AB-104-N型电子天平(Mettler Toledo-Group公司);DF-101S恒温加热磁力搅拌器(巩义市予华仪器有限责任公司);20 mL水热反应釜(上海隆拓仪器设备有限公司);DGG-9053AD型电热恒温鼓风干燥箱(上海森信实验仪器有限公司)。
1.2 实验方法
将一定质量的 Gd2O3和 Eu2O3分别与过量的HNO3在恒温水浴中进行反应,加热浓缩至全部结晶,制得硝酸盐,用去离子水溶解分别定容至 100 mL,待用。配制 0.2 mol/L (Na2WO4·2H2O)待用。将制备好的 1 mL Gd(NO3)3、2 mL Na2WO4,Eu3+的掺杂浓度为 1%、2%、5%、10%、15%、20%,分别加入到20 mL反应釜中,用稀硝酸、氢氧化钠调节pH=5,用玻璃棒搅拌均匀,去离子水填充至填充度约为70%,将反应釜密封,200 ℃恒温加热24 h后,自然降至室温。将反应釜中溶液转移置烧杯中静置,待烧杯中粉体沉淀后,去除上部清夜,用蒸馏水洗涤粉体三次,每次静置3 h。将洗好的粉体放入烘箱中加热至80 ℃干燥12 h,得到NaGd(WO4)2样品粉末。
1.3 样品表征
X射线衍射仪(D/tax检测器,日本理学Rigaku Utimal Ⅴ);扫描电子显微镜(S4800,日本日立公司);荧光光光谱仪(FLUOROMAX-4-NIR,Horiba公司)对NaGd (WO4)2:Eu3+纳米粉及纳米膜进行了表征。
2 结果与讨论
2.1 样品的XRD分析
200 ℃水热法制备的无掺杂与掺杂10% Eu3+的NaGd(WO4)2粉末的X射线粉末衍射图,如图1所示。由图可见无掺杂与Eu3+掺杂量为10%的XRD谱图与JSPDS标准卡片 25-0829的图谱中Na0.5Gd0.5WO4晶体数据基本一致,基本无其它杂峰,Eu3+掺杂对NaGd(WO4)2的晶体结构基本上没有影响,但 Eu3+掺杂量为10%与未掺杂的XRD 谱比较,衍射峰强度有所降低,这说明 Eu3+浓度的增加会降低了基质材料的结晶度[8]。

图1 NaGd(WO4)2:x %Eu3+纳米粉的XRD谱图Fig. 1 XRD patterns of NaGd(WO4)2:x %Eu3+ samples(1)x=0 (2)x=10%
2.2 样品的SEM分析
Eu3+掺杂量为 10%的 NaGd(WO4)2:Eu3+纳米粉体的SEM图见图2,在电镜下观察不同Eu3+掺杂量的样品形貌没有太大的差别。实验制备的NaGd(WO4)2:Eu3+晶体微观形貌为上下对称的八面体,锥形,尺寸大小不均一,在100 nm到1μm之间,表面附着着一些小颗粒。
2.3 荧光分析
612 nm监测下的NaGd(WO4)2:Eu3+粉体的激发光谱图见图3,激发谱中 355~380 nm 范围内有几个弱得激发峰,对应的是 Eu3+4f→4f 跃迁吸收;在394 nm处的锐峰对应于Eu3+离子7F0→5L6能级跃迁的吸收;464 nm处的激发峰对应于Eu3+7F0→5D2能级跃迁的吸收;534 nm处的激发峰对应于Eu3+离子7F0→5D1能级跃迁的吸收。其中394 nm处的激发峰强度最大,说明制备的粉末样品可被紫光有效激发。在394 nm处激发测得样品的发射光谱图,如图4所示。

图2 NaGd(WO4)2:xEu3+纳米粉的SEM图像Fig. 2 SEM image of NaGd(WO4)2:xEu3+(x=10%)samples
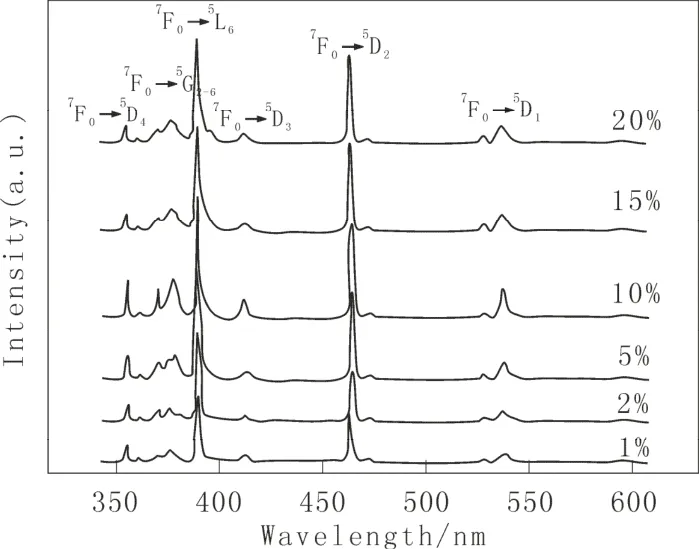
图3 NaGd(WO4)2:Eu3+纳米粉激发荧光谱图(发射波长为612 nm)Fig. 3The excitation spectra of NaGd(WO4)2:Eu3+samples measured by monitoring the 612 nm emission
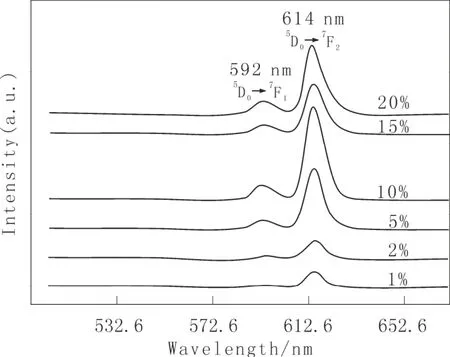
图4 NaGd(WO4)2:Eu3+粉体发射荧光谱图(激发波长为39 4 nm)Fig. 4 The emission spectra of NaGd(WO4)2:Eu3+powders upon excitation at 39 nm
样品的发射光谱中有两个峰,最强峰在614 nm附近,为5D0→7F2电偶极跃迁,5D0→7F2电偶极跃迁应在616 nm附近,出现这种现象的原因可能由于纳米材料中Eu3+受到较强的晶场作用,其5D0和7F2能级间的距离变宽,导致5D0→7F2发射出现蓝移现象[9]。
在 394 nm激发下发射光谱强度与铕离子掺杂浓度有关,Eu3+的掺杂浓度低于 10%时,发光强度随着Eu3+的掺杂浓度增加而加强,在Eu3+的掺杂量为10%时达到最大值;Eu3+的掺杂浓度由10%增加到20%时,粉体荧光强度开始降低,这是由于相邻Eu3+离子之间的交叉弛豫,导致能量非辐射传递增加造成的。同样,在590 nm处的5D0→7F1能级跃迁发光也随着 Eu3+浓度增加而增大,Eu3+的掺杂浓度高于10%发光强度又降低,可以判断 WO42-和Eu3+之间有明显的能量传递[1]。发光强度由强至弱的顺序为Eu3+掺杂量:10%>20%>5%>15%>2%>1%。
3 结 论
本文采用水热法制备了NaGd(WO4)2:Eu3+粉体材料,制备的NaGd(WO4)2:Eu3+晶体的微观形貌为八面体棱形,尺寸大小为几百纳米,在394 nm监测下的荧光光谱中,主要有592 nm附近的5D0→7F1磁偶极跃迁和614 nm附近的5D0→7F2电偶极跃迁。Eu3+掺杂量为10%时荧光强度最大。
[1]易 敏,等. 水热法合成白光Ca1-xWO4:xEu3+荧光粉的表征[J]. 广西师范学院学报:自然科学版, 2010,27(1):45–48.
[2]钱先华,等. NaY(WO4)2:Eu3+红色荧光粉的水热法制备及其发光性能研究[J]. 聊城大学学报(自然科学版),2011, 24(1):74–77.
[3]马瑞利,等. Yb3+, Er3+共掺MWO4(M=Cd, Ba)纳米晶体的制备及发光性能[J]. 陕西师范大学学报(自然科学版),2010,38(1):65-69.
[4]时朝璞,等.水热法制备近红外发光 NaLa(WO4)2:Ln(Ln=Er, Nd)球形粒子的研究[J].中国稀土学报,2007,25(5):545–548.
[5]左周,等. NaGd(WO4)2:Yb3+, Tm3+纳米粉的制备与上转换发光性能[J]. 中国稀土学报, 2012,30(1):73–77.
[6]李志强,等.水热法制备NaGd(WO4)2: Eu3+发光材料[J]. 河北大学学报(自然科学版), 2012,32(2):129–133.
[7]廖金生,等. LED用La2(WO4)3:Eu3+红色荧光粉合成及光谱性能[J].光子学报, 2011,40(5):658–661.
[8]李志强,等.水热法制备YAG:Ce纳米荧光粉[J]. 河北大学学报:自然科学版, 2009,29(2):133-136.
[9]刘晃清, 等.二氧化锆纳米材料中Eu3+的发光特性[J]. 物理学报,2004, 53(1):282-285.

