新生儿败血症患儿母亲围生期感染因素及其临床症状和体征分析
王 迎,邓 颖
新生儿败血症是新生儿期常见感染性疾病,病情凶险,进展迅速,即便感染未波及神经系统,仍将增加脑白质损伤和终身残疾的机会[1]。据世界卫生组织报道,世界范围内新生儿感染所导致的新生儿死亡人数达160 万,其中新生儿败血症是主要死亡原因之一[2],预防和有效控制感染是新生儿重症监护病房(NICU)工作的重要挑战[3]。因此,探讨新生儿败血症易感因素、感染早期临床特征及护理干预措施,可尽早识别感染征象,加强防治措施,降低感染后并发症,改善预后。本研究采用病例对照研究,回顾性分析我院NICU 120例新生儿败血症患儿母亲围生期感染因素、患儿临床症状及体征,以明确感染高危因素及感染早期最具代表性临床症状、体征,提高对该病的诊疗水平。
1 资料与方法
1.1 临床资料 选择2007年1月—2012年1月首都医科大学附属北京妇产医院NICU住院患儿240例为研究对象。新生儿均在入院12 h内及抗生素使用前行血培养,根据是否合并败血症分为败血症组120例和非败血症组120例,败血症组纳入标准参照2003年《新生儿败血症诊疗方案》的诊断标准[4]:具有临床表现且符合下列任一条:血培养或无菌体腔内培养出致病菌;如果血培养标本培养出条件致病菌,则必须与另次(份)血、或无菌体腔内、或导管头内培养出同种细菌。非败血症组血培养结果未见致病菌,临床无感染征象。两组患儿性别、分娩方式、胎龄、出生体质量比较,差异均无统计学意义(P>0.05);两组患儿Apgar评分比较,差异有统计学意义(P<0.05,见表1)。
1.2 研究方法 采用病例对照研究,搜集资料内容包括败血症组及非败血症组母亲围生期感染因素、新生儿临床症状及体征。母亲围生期感染因素包括孕期或产时发热(体温>37.5 ℃)、白细胞计数(WBC<4.0×109/L或>10.0×109/L)及中性粒细胞分数异常(≥77%)、C反应蛋白(CRP)升高(>3 mg/L)、产道特殊细菌定植(包括B族溶血性链球菌、李斯特菌、真菌、大肠埃希菌、假丝酵母菌、葡萄球菌、滴虫)、绒毛膜羊膜炎或子宫内膜炎、胎膜早破>18 h、有无胎儿宫内窘迫(胎心≤100次/min或≥160次/min)、羊水胎粪污染;入院后观察患儿的临床症状及体征,包括精神反应差(食欲欠佳、哭声减弱、嗜睡、精神萎靡)、高血糖(全血血糖>7.0 mmol/L)、循环不良(手足较凉、肤色苍白或紫绀)、病理性黄疸(足月儿血清胆红素>221 μmol/L、早产儿血清胆红素>255 μmol/L、持续时间超过生后2~4周或进行性加重)、发热(体温>37.3 ℃)、消化系统症状包括喂养不耐受,呼吸系统症状包括呼吸窘迫(进行性呼吸困难、三凹征、青紫、呼吸衰竭),心血管系统症状包括心动过速(足月儿心率170~190次/min、早产儿心率200~220次/min),中枢神经系统症状包括易激惹,休克早期症状(皮肤花斑、肢端冷、毛细血管再充盈时间>3 s)。并收集两组患儿预后资料。
1.3 统计学方法 采用SPSS 17.0统计软件进行统计学分析。计数资料比较采用χ2检验;败血症发生的危险因素分析采用多因素Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 两组母亲围生期感染因素分析 败血症组与非败血症组母亲孕期或产时发热、WBC及中性粒细胞分数升高、CRP升高、产道特殊细菌定植、绒毛膜羊膜炎或子宫内膜炎、胎膜早破>18 h、羊水胎粪污染检出率比较,差异均有统计学意义(P<0.05,见表2)。以单因素分析差异有统计学意义的因素为自变量进行多因素Logistic回归分析,结果显示,孕母孕期或产时发热、WBC及中性粒细胞分数升高、CRP升高、产道特殊细菌定植、绒毛膜羊膜炎或子宫内膜炎、胎膜早破>18 h、羊水胎粪污染与败血症的发生有回归关系(P<0.05,见表3)。
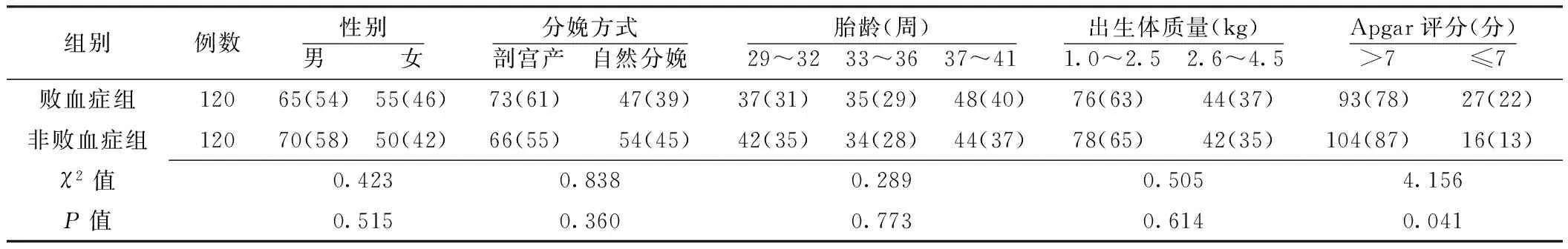
表1 两组患儿一般资料比较 〔n(%)〕

表2 败血症组与非败血症组母亲围生期感染因素的单因素分析〔n(%)〕
注:WBC=白细胞计数,CRP=C反应蛋白
2.2 两组患儿临床症状及体征分析 败血症组与非败血症组患儿精神反应差、高血糖、循环不良、发热、喂养不耐受、呼吸窘迫、心动过速、易激惹、休克早期症状检出率比较,差异均有统计学意义(P<0.05,见表4)。以单因素分析差异有统计学意义的因素为自变量进行多因素Logistic回归分析,结果显示,精神反应差、高血糖、循环不良、病理性黄疸、呼吸窘迫、心动过速与败血症的发生有回归关系(P<0.05,见表5)。
2.3 两组患儿预后及并发症或合并症 败血症组痊愈92例,基本痊愈26例,成活率98%,放弃治疗1例,死亡1例(临床诊断感染性休克);并发症或合并症:新生儿呼吸窘迫综合征(NRDS)43例,新生儿窒息27例,新生儿贫血13例,动脉导管未闭5例,脑室内出血(IVH)4例,肺出血3例,支气管肺发育不良2例,弥散性血管内凝血(DIC)1例,早产儿视网膜病(ROP)1例;112例门诊随访生长发育及神经发育基本正常,8例失访。非败血症组:痊愈118例,基本痊愈2例,成活率100%;并发症或合并症:NRDS 25例,新生儿窒息16例,新生儿贫血11例,动脉导管未闭2例,IVH 1例,ROP 1例;113例门诊随访生长发育及神经发育基本正常,7例失访。
表3 新生儿败血症患儿母亲围生期感染因素的Logistic回归分析
Table3 Multi-factor Logistic regression analysis of mothers′ perinatal infection factors in sepsis group

变量βSEWaldχ2值P值OR值95%CI孕期或产时发热2.6720.54424.1120.00014.469(4.980,42.036)WBC及中性粒细胞分数升高2.8110.54326.7490.00016.622(5.729,48.226)CRP升高3.3910.59932.0220.00029.698(9.176,96.119)产道特殊细菌定植3.0840.58427.8720.00021.850(6.953,68.662)绒毛膜羊膜炎或子宫内膜炎3.2820.73120.1700.00026.632(6.358,111.552)胎膜早破>18h2.0320.44620.7580.000 7.600 (3.184,18.298)羊水胎粪污染2.8960.50033.5390.00018.110(6.795,48.266)

表4 败血症组与非败血症组患儿临床症状及体征的单因素分析 〔n(%)〕
表5 新生儿败血症临床症状及体征Logistic回归分析
Table5 Multi-factor Logistic regression analysis of clinical symptoms and signs in sepsis group

变量βSEWaldχ2值P值OR值95%CI精神反应差 1.2930.38011.6070.0013.645(1.732,7.671)高血糖 1.9610.48616.2610.0007.104(2.739,18.422)循环不良 1.2300.416 8.760 0.0033.421(1.515,7.725)病理性黄疸 1.8480.43717.8460.0006.334(2.692,14.951)呼吸窘迫-1.7280.639 7.317 0.0070.178(0.051,0.621)心动过速 1.7390.703 6.113 0.0135.690(1.434,22.581)
3 讨论
3.1 新生儿败血症危险因素分析 本研究发现败血症组母亲围生期高危因素包括孕期或产时发热、WBC及中性粒细胞分数升高、CRP升高、产道特殊细菌定植、绒毛膜羊膜炎或子宫内膜炎、胎膜早破>18 h、羊水胎粪污染。国内外许多相关研究均提示绒毛膜羊膜炎、胎膜早破>18 h、产道特殊细菌定植(细菌性阴道炎)、羊水胎粪污染、血象异常均是败血症高危因素[5]。Popowski等[6]指出胎膜早破的孕妇产前或产时WBC和CRP升高与绒毛膜羊膜炎、新生儿感染密切联系,故临床尤需关注对有胎膜早破病史的新生儿感染症状的防控。李正红等[7]临床研究认为母亲围生期感染极易导致新生儿感染以致败血症的发生,应将母亲围生期因素与患儿临床表现相结合,密切监测病情变化。以上文献与本研究均提示:患儿入院时需认真评估母亲围生期感染高危因素,加强感染防范意识,进行全面监测,密切观察病情,及时发现感染相关临床表现,采取救治措施。
3.2 败血症患儿症状及体征分析 本研究探讨了感染早期最具代表性的临床症状及体征,发现败血症组感染早期征象以精神反应差、高血糖、循环不良、病理性黄疸、呼吸窘迫、心动过速为最突出表现,主要原因是新生儿皮肤-黏膜及血-脑脊液屏障功能薄弱,机体体液及细胞免疫未发育成熟,致病菌进入机体大量繁殖并释放毒素,造成血行感染,产生全身炎性反应综合征(SIRS),可致多脏器功能异常,表现为反应异常包括精神反应差、嗜睡;呼吸窘迫致机体缺血缺氧、糖代谢紊乱、血糖升高;同时,细菌释放的毒素作用于心肌细胞后可引起心肌细胞能量代谢异常,细胞膜通透性增高,毒素及细菌本身成分可在体内形成循环免疫复合物引起心血管内皮细胞的广泛受损,呈现心功能不全表现及循环不良状态。有研究显示黄疸可以是新生儿败血症突出的或惟一的表现,表现为黄疸迅速加重或退而复现或持续不退[8]及无法解释的黄疸。据童笑梅[1]研究报道,SIRS可发生意识改变如精神反应差,心率≥180次/min;出现呼吸窘迫,表现为呼吸>60次/min伴有喘息、三凹征或低血氧饱和度;血糖不耐受(>10 mmol/L)、喂养不耐受诸多表现。Camacho-Gonzalez等[9]的研究显示,新生儿败血症早期临床表现以反应异常最具诊断价值,敏感度高,因此密切观察临床表现是早期发现新生儿败血症最基本方法,对于存在感染高危因素的新生儿应进行感染相关症状或体征的监测,如出现精神反应异常,应预见可疑感染,及早进行感染指标监测,必要时根据经验应用广谱抗生素,以预防败血症发生[10]。感染早期征象多不典型且多种多样,有时很轻微,有时可表现为呼吸暂停、喂养不耐受,是由于呼吸、消化功能尚未完全成熟,易被忽视,一旦出现这些临床症状,也应预见可能是疾病早期或病情进展,提高警惕,密切关注患儿感染相关临床症状有无加重或新的症状出现,及时筛查感染指标,提高治疗效果。
依据本研究及其他相关研究可以看出,合理并综合利用临床资料,大样本量深入探讨新生儿败血症早期感染临床症状,作为临床客观评价指标,制定相关量表,有助于完善新生儿败血症有效临床干预措施,切实提高疾病治疗水平。本研究由于样本量较少,故结论仅有一定参考价值,今后需要大样本、前瞻性研究进一步分析。
综上所述,新生儿败血症早期症状多样化,医务人员需全面评估母亲围生期高危因素,提高警惕,加强感染性疾病的防控措施及临床观察,及时治疗并实施护理干预,降低败血症发生的风险。
1 童笑梅.新生儿血行感染[J].中国新生儿科杂志,2009,24(5):257-260.
2 Al-Shamahy HA,Sabrah AA,Al-Robasi AB,et al.Types of Bacteria associated with Neonatal Sepsis in Al-Thawra University Hospital,Sana′a,Yemen,and Their Antimicrobial Profile[J].Sultan Qaboos Univ Med J,2012,12 (1):48-54.
3 Prashant A,Vishwanath P,Kulkarni P,et al.Comparative assessment of cytokines and other inflammatory markers for the early diagnosis of neonatal sepsis-a case control study[J].PLoS One,2013,8(7):e68426.
4 中华医学会儿科学分会新生儿学组,《中华医学会中华儿科杂志》 编辑委员会.新生儿败血症诊疗方案[J].中华儿科杂志,2003,41(12):897-899.
5 姜毅.新生儿败血症诊疗进展[J].中国新生儿科杂志,2010,25(2):69-72.
6 Popowski T,Goffinel F,Maillard F,et al.Maternal markers for delecting early-onest neonatal infection and chorioamnionitis in cases of premature rupture of membranes at or after 34 weeks of gestation:a two-center prospective study[J]. BMC Pregnancy Childbirth,2011,7(11):26.
7 李正红,王丹华.新生儿早发型败血症的临床特点[J].中华围产医学杂志,2011,14(7):420-424.
8 邵肖梅,叶鸿瑁,丘小汕.实用新生儿学[M].4版.北京:人民卫生出版社,2011:340-343.
9 Camacho-Gonzalez A,Spearman PW,Stoll BJ,et al.Neonatal infectious diseases evaluation of neonatal sepsis[J].Pediatr Clin North,2013,60(2):367-389.
10 周慧萍,曹莉,蒋玲,等.104 例新生儿败血症血液培养结果与临床特征分析及护理启示[J].护理学报,2012,20:45-49.

