慢性收缩性心力衰竭患者右房室瓣收缩期位移与肾功能状态的关系研究
靳亚阁,张菲斐
慢性收缩性心力衰竭(CHF)是一种严重的临床综合征,不仅表现为心脏功能衰退,还常伴有肾功能异常。慢性心力衰竭患者出现肾功能不全称之为心肾综合征(CRS),因其明显增加了CHF患者的死亡率,近年来逐渐引起临床重视。CRS是指心脏和肾脏之间存在复杂的交互影响,当其中一个器官对另一器官的功能损害不能代偿时形成恶性循环,最终导致两者共同损害[1]。CRS的发生机制极为复杂,治疗较为棘手,且预后不良。因此,如何早期发现并及时治疗,对改善预后具有重要意义。目前临床尚无特异指标预测CRS的发生,近年来研究发现右室功能变化与CHF患者发生CRS的关系密切[2]。本研究采用右房室瓣收缩期位移(TAPSE)作为反映右室收缩功能的指标,探讨TAPSE变化对肾小球滤过率(eGFR)及其他肾功能指标的影响,为筛选CRS的临床预测因子提供试验依据。
1 资料与方法
1.1 临床资料选取2011年6月—2012年6月在郑州大学第一附属医院心内科住院治疗的CHF患者共98例,其中男56例,女42例;平均年龄(45.3±12.6)岁。缺血性心肌病56例、扩张型心肌病21例、酒精性心肌病13例、围生期心肌病5例、急性重症心肌炎3例。均符合Framingham心力衰竭诊断标准[3],心功能分级依据NYHA心功能分级标准[4]。 病例排除标准:(1)高血压心脏病、肥厚性心肌病、瓣膜性心脏病及原发于心包疾病的心力衰竭者;(2)单侧或双侧肾动脉狭窄者;(3)既往患有肾小球肾炎等原发性肾脏疾病者;(4)原发于肺及肺血管疾病引起的右心力衰竭者;(5)心脏移植术后、恶性肿瘤、重症结核及感染性疾病、甲状腺疾病、严重肝脏疾病、入院时肌酐值>707 μmol/L及规律透析者;(6)有消化道出血、严重脱水、休克等血容量严重不足者,入院时伴有其他创伤或进行外科手术者。
1.2仪器与方法
1.2.1TAPSE测定采用M型超声在右房室瓣与右室游离壁交界处取样测量TAPSE,TAPSE的参考值>20 mm,右心功能不全时<16 mm[5]。依据TAPSE水平将入选者分为两组:右室功能不全组(TAPSE<16 mm),右室功能正常组(TAPSE≥16 mm)。
1.2.2彩色多普勒超声使用美国超声心动图学会推荐的方法,取心尖四腔心切面,用改良的Simpson单平面法计算左室射血分数(LVEF),将LVEF≤45%定义为左心功能不全。常规测量左室舒张末内径(LVDd)、右室舒张末内径(RVDd),应用右房室瓣反流速度法估测肺动脉收缩压(PASP)。
1.2.3eGFR采用改良MDRD方程计算,eGFR=175×Scr-1.234×年龄-0.179×0.79(女性)。eGFR<90 ml·min-1·(1.73 m2)-1定义为肾功能不全。
1.2.4N端B型钠尿肽前体(NT-proBNP)及常规肾功能指标测定于入院第2天清晨抽取空腹血测定尿素氮(BUN)、肌酐(Cr)、尿酸(UA)及胱抑素C(CysC)。
1.2.5平均动脉压(MAP)于入院当日患者安静休息至少5 min后,采用Korotkoff听诊法测量右上肢肱动脉的收缩压和舒张压;MAP=舒张压+1/3脉压。

2 结果
2.1临床资料比较两组患者的年龄、性别构成、心功能分级、心力衰竭病因及心房纤颤发生率比较,差异均无统计学意义(P>0.05,见表1)。

表1 两组患者临床资料比较
注:*为t值
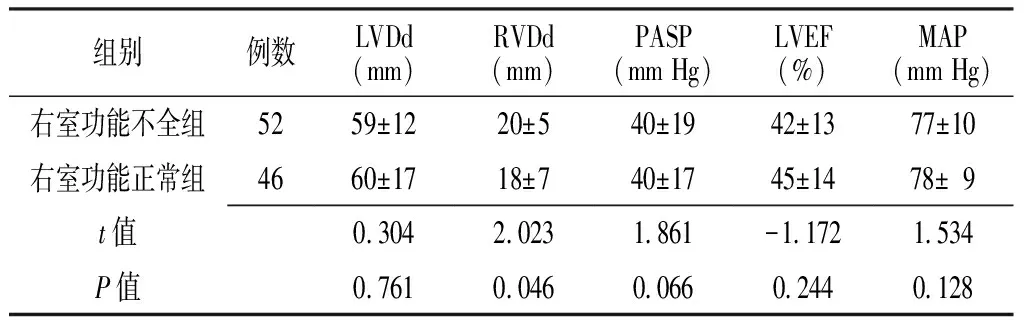
2.2心脏超声指标及MAP比较两组患者LVDd、PASP、LVEF及MAP比较,差异均无统计学意义(P>0.05);RVDd比较,差异有统计学意义(P<0.05,见表2)。

Table2Comparison of echocardiography indicators and MAP between two groups
组别例数LVDd(mm)RVDd(mm)PASP(mmHg)LVEF(%)MAP(mmHg)右室功能不全组5259±1220±540±1942±1377±10右室功能正常组4660±1718±740±1745±1478±9t值0 3042 0231 861-1 1721 534P值0 7610 0460 0660 2440 128
注:LVDd=左室舒张末内径,RVDd=右室舒张末内径,PASP=肺动脉收缩压,LVEF=左室射血分数,MAP=平均动脉压
2.3NT-proBNP及常规肾功能指标比较两组患者NT-proBNP水平间差异无统计学意义(P>0.05),两组患者肾功能不全发生率、eGFR、BUN、Cr、UA及CysC水平间差异有统计学意义(P<0.05,见表3)。

表3 两组患者肾功能及NT-proBNP比较
注:*为 χ2值;eGFR=肾小球滤过率,BUN=尿素氮,Cr=肌酐,UA=尿酸,CysC=胱抑素C,NT-proBNP= N端B型钠尿肽前体
2.4Logistic回归分析将所有患者的肾功能状态作为因变量,按照eGFR小于或大于90 ml·min-1·(1.73 m2)-1将肾功能状态定义为二分类变量,所有患者的LVDd、RVDd、PASP、LVEF、MAP、TAPSE及NT-proBNP为备选自变量,采用二分类Logistic回归分析从中筛选危险因素,结果显示只有TAPSE进入回归模型中,故TAPSE降低是CHF患者发生肾功能不全的危险因素(P<0.05,见表4)。
2.5抗心力衰竭药物使用情况比较右室功能不全组患者静脉袢利尿剂(呋塞米)>80 mg/d使用率高于右室功能正常组,β-受体阻滞剂使用率低于右室功能正常组,差异均有统计学意义(P<0.05),两组间血管紧张素转换酶抑制剂(ACEI)/血管紧张素受体阻滞剂(ARB)、地高辛及螺内酯使用率比较,差异均无统计学意义(P>0.05,见表5)。

表4 二分类Logistic回归分析结果
注:TAPSE=左房室瓣收缩期位移
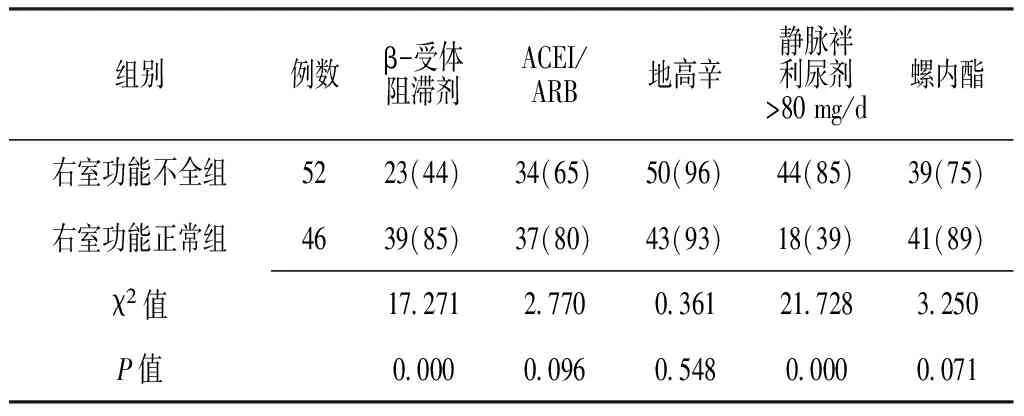
表5 两组抗心力衰竭药物使用率比较〔n(%)〕
注: ACEI=血管紧张素转化酶抑制剂;ARB=血管紧张素受体阻滞剂
3 讨论
TAPSE系右房室瓣环沿右室长轴方向的收缩期位移,与右室射血分数及右室面积变化率呈正相关,能反映右室心肌纤维在长轴方向上的变化特征。诸多研究显示TAPSE与右心功能有良好相关性,明确了其在评价右心功能中的价值[6]。本研究以肾功能状态为因变量,以LVDd、RVDd、PASP、LVEF、MAP、TAPSE及NT-proBNP为备选自变量进行二分类Logistic回归分析,显示仅有TAPSE进入回归模型,说明TAPSE降低较之其他指标更能准确地预测CHF患者肾功能不全的发生。这与目前一些研究中将CHF患者出现肾功能恶化归因于前向血流动力学异常,如LVEF和MAP下降[7]不同。在急性失代偿性心力衰竭患者中肾损害的机制主要是心排出量减低和全身低血压所致的肾灌注不足,但Weinfeld等[8]在治疗慢性心力衰竭期间出现肾功能恶化的研究中并没有发现肾功能恶化与心脏指数、系统性血管阻力或其他血流动力学指标之间有关联。
在ESCAPE试验的回顾性研究中发现右房压力升高是惟一与肾功能恶化有关的因素,而右房压力升高是右室功能不全的直接后果[9]。研究人员在克利夫兰诊所进行的经膀胱测量腹内压的研究显示,增加腹内压可加重肾功能障碍,减少腹内压可改善肾功能[10]。本研究显示TAPSE降低提示右室收缩功能减退,后者导致右室舒张末容量及压力增高,相应的血流动力学后果便是右房压进行性升高、腹腔脏器淤血及腹内高压,而且此类患者出现肾功能不全的比例明显提高。但无论是利用心导管测量右房压,还是经膀胱测量腹内压,均为侵入性操作,重度心力衰竭及老年患者不易耐受,且操作过程相对复杂,不易推广。本研究采用TAPSE作为反映右房压和腹内压的间接指标,进行二分类Logistic回归分析显示肾功能不全的发生与TAPSE关系最密切,而与LVDd、LVEF、MAP、NT-proBNP等无明显相关性。
目前右心室功能受损与CRS的关系已逐渐成为心力衰竭研究的热点,已有研究发现右心室舒张末压升高与腹内压升高、肾静脉淤血及肾小管间质纤维化的关系[11-13]。国外的一些研究早已证实肾小管间质纤维化程度与eGFR降低程度呈正相关[14]。大量肾活检资料也再次证实肾小管间质纤维化程度与肾功能及预后密切相关[15-16]。关于肾脏淤血导致肾小管间质纤维化从而使eGFR下降的详细机制尚有待于进一步研究,但如能在心力衰竭早期右室功能尚未受损时及时有效地减轻肾淤血,防止肾小管间质纤维化的发生与发展,也许能延缓肾功能恶化进展,避免CRS出现,改善CHF的预后。
本研究同时发现右室功能不全组患者大剂量呋塞米的使用率明显高于右室功能正常组,β-受体阻滞剂的使用率明显低于右室功能正常组。对于伴有右室功能不全的CHF患者,使用大剂量利尿剂减轻静脉淤血,往往同时伴随短期内症状与肾功能的改善,这可解释两组间利尿剂使用量的差别。但因伴右室功能不全者往往存在静脉压高、水钠潴留和周围水肿,患者难以达到“干体重”,极大地限制了β-受体阻滞剂的应用,这解释了两组间β-受体阻滞剂使用率的差别。心力衰竭治疗中利尿剂使用问题一直被视为一把双刃剑,长期使用大剂量利尿剂对心力衰竭预后影响尚不明确,只有进行长期随访观察,了解利尿剂用量、右室功能改善与eGFR升高之间动态变化关系,才能为利尿剂使用问题提供更可靠的依据。
综上所述,TAPSE作为一个评价右室收缩功能的良好指标,其降低与CHF患者CRS的发生关系密切。虽然其详细机制有待进一步研究,但因两者之间良好的相关性及TAPSE的可操作性,使该指标具有一定的应用前景,值得临床推广使用。
1Ronco C,Haapio M,House AA,et al.Cardiorenal syndrome[J].J Am Coll Cardiol,2008,52(19):1527-1539.
2Kjaergaard J,Akkan D,Iversen KK,et al.Right ventricular dysfunction as an independent predictor of short-and long-term mortality in patients with heart failure[J].Eur J Heart Fail,2007,9(6-7):610-616.
3Mckee PA,Castelli WP,McNamara PM,et al.The natural history of congestive heart failure:the Framingham study[J].N Engl J Med,1971,285(26):1441-1446.
4陆再英.内科学[M].北京:人民卫生出版社,2008:169-170.
5Rudski LG,Lai WW,Afilalo J,et al.Guidelines for the echocardiographic assessment of the right heart in adults:a report from the American Society of echocardiography endorsed by the European Association of Echocardiography,a registered branch of the European Society of Cardiology,and the Canadian Society of Echocardiography[J].J Am Soc Echocardiogr,2010,23(7):685-713.
6Ghio S,Recusani F,Klersy C,et al.Prognostic usefulness of the tricuspid annular plane systolic excursion in patients with congestive heart failure secondary to idiopathic or ischemic dilated cardiomyopathy[J].Am J Cardiol,2000,85(7):837-842.
7Maxwell AP,Ong HY,Nicholls DP.Influence of progressive renal dysfunction in chronic heart failure[J].Eur J Heart Fail,2002,4(2):125-130.
8Weinfeld MS,Chertow GM,Stevenson LW.Aggravated renal dysfunction during intensive therapy for advanced chronic heart failure[J].Am Heart J,1999,138(2 Pt 1):285-290.
9陈益和,译;唐福林,校.充血性心力衰竭与肺动脉插管作用的评估研究——ESCAPE试验[J].美国医学会杂志:中文版,2006(4):223.
10Testani JM,Khera AV,St John,et al.Effect of right ventricular function and venous congestion on cardiorenal interactions during the treatment of decompensated heart failure[J].Am J Cardiol,2010,105(4):511-516.
11Malbrain MA,Deeren D,De Potter TJ.Intra-abdominal hypertention in the critically ill:it is time to pay attention[J].Curr Opin Crit Care,2005,11(2):156-171.
12Mullens W,Abrahams Z,Francis GS,et al.Importance of venous congestion for worsening of renal function in advancd decompenstated heart faiure[J].J Am Coll Cardiol,2009,53(7):589-596.
13游琼,吴铿.二甲双胍对糖尿病心肌病慢性充血性心力衰竭及心肌灌注的影响[J].中国全科医学,2011,14(2):601.
14Nath KA.Tubulointerstitial change as a major determinant in the progression of renal damage[J].Am J Kidney Dis,1992,20(1):1-17.
15Nangaku M.Chronic hypoxia and tubulointerstitial injury:a final common pathway to end-stage renal failure[J].J Am Soc Nephrol,2006,17(1):17-25.
16张芃.肾上腺髓质素与糖尿病肾病肾小管间质病变的关系研究[J].实用心脑肺血管病杂志,2012,20(10):1661.

