机械循环支持技术在救治心跳骤停重症先天性心脏病婴幼儿4例报告
洪小杨,周更须,刘宇航,刘颖悦,高海涛,王 辉,封志纯
机械循环支持技术在救治心跳骤停重症先天性心脏病婴幼儿4例报告
洪小杨,周更须,刘宇航,刘颖悦,高海涛,王 辉,封志纯
目的介绍采用机械循环支持技术救治心跳骤停重症先天性心脏病婴幼儿的经验。方法回顾总结2012年10月至2013年6月本院利用机械循环支持救治4例心跳骤停先心病重症婴幼儿的临床救治情况和预后。病例1诊断室间隔完整型大血管转位,术前严重低氧、高乳酸血症,心跳骤停1次,心肺复苏同时急诊建立体外循环,行大动脉调转手术治疗,术后切换为体外膜肺氧合(ECMO)辅助;病例2诊断室缺术后残余分流,重度肺动脉高压,左室功能不全,室缺残余分流修补术后出现心跳骤停、高乳酸血症,心肺复苏同时床旁紧急行ECMO辅助;病例3诊断完全型肺静脉异位引流(心上型),术前严重低氧血症、高乳酸血症,心跳骤停2次,急诊建立体外循环并行完全肺静脉异位引流矫治术,术后切换为ECMO辅助;病例4诊断为肺动脉闭锁、动脉导管未闭,行右室流出道重建术后严重低心排,心肺复苏1次,床边ECMO辅助。结果4例患儿3例顺利撤离ECMO,病例3术后出现多脏器功能衰竭,无法撤离ECMO死亡。结论对于出现心跳骤停重症先心病婴幼儿,及时快速建立循环辅助,纠正低氧低灌注对机体的进一步损伤,是救治心跳骤停重症先天性心脏病患儿的有效手段。
机械循环支持,体外膜肺氧合,心跳骤停,先天性心脏病,心肺复苏
机械循环支持(mechanical circulatory support,MCS)技术主要包括心肺转流(cardiopulmonary bypass,CPB)技术与体外膜肺氧合(extracorporeal Membrane Oxygenation,ECMO)技术,ECMO是从CPB技术发展而来,能够在较长时间内,部分或全部代替患者心肺功能,维持机体各器官的供氧,对严重的心肺功能衰竭患者进行长时间心肺支持的生命支持技术。1971年,Hill[1]首次使用CPB设备对1例多脏器损伤合并急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)的24岁患者进行救治,并取得成功。通过临床工作者的长期不懈努力,尤其是ECMO技术在设备、管理上取得了长足进步并取得了较好的临床效果。在中国,相对于CPB技术的开展,ECMO在临床上应用开展较晚,林茹等[2]报道了2007年至2011年期间对12例重症患儿进行ECMO治疗。临床上对于心跳骤停患儿,首先是立即进行心肺复苏(cardiopulmonary resuscitation,CPR),但总有一些极度危重患儿对CPR反应不良,此时临床上可能需要更积极救治手段。MCS自然就成了下一步的选择。目前在国内利用MCS救治经心肺复苏重症患儿仍极少见开展,具体MCS种类、治疗时机和适应证的选择关系到临床伦理学方面问题。本院在2012年10月至2013年6月应用MCS对4例出现心跳骤停患儿进行救治,现介绍分析如下。
1 资料与方法
1.1 一般资料 病例1,男,生后13天,体重3.3 kg,入院诊断“室间隔完整型大动脉转位(transposition of great arteries/intact ventricular septum/patent ductus arteriosus,TGA/IVS/PDA)”,入院时已存在严重低氧血症,给予前列腺素E1持续泵入无明显改善,出现心跳骤停1次,心肺复苏同时入手术室急诊建立CPB,行“大动脉调转术”(arteries switch operation,ASO),术后出现低心排综合征及肺出血,无法停止CPB,延迟关胸,将CPB切换为ECMO支持,并在ECMO支持下转入监护室。
病例2,女,1岁9月,体重10 kg,入院诊断“室间隔缺损修补术后残余分流,重度肺动脉高压(左右室压差10 mm Hg),左心功能不全”,射血分数(EF)40%,入院后行“室缺残余分流修补术”,术后出现肺动脉高压危象,严重左心功能不全(EF值降至15%~20%),术日当晚出现心跳骤停1次,床边心肺复苏同时紧急行ECMO安装术。
病例3,男,生后45天,体重4 kg,入院诊断“完全性肺静脉异位引流(TAPVC,心上型),重度肺动脉高压”,入院即存在严重低氧血症、低血压,出现心跳骤停2次,心肺复苏同时入手术室急诊手术建立CPB,行“TAPVC矫治术”,术后无法停CPB,延迟关胸,将CPB切换ECMO支持,ECMO支持下转入监护室。
病例4,男,7个月,体重8.5 kg,入院诊断“肺动脉闭锁、动脉导管未闭”,行右室流出道重建术,术后出现低心排综合征,心跳骤停1次,心肺复苏同时床旁经胸安装ECMO支持。
1.2 MCS设备和耗材
1.2.1 CPB设备与耗材 采用Terumo System 1系统,包括变温水箱、宁波菲拉尔婴儿套包、动静脉插管;Terumo RX05氧合器。
1.2.2 ECMO设备与耗材 采用Medtronic ECMO系统,包括离心泵、空氧混合器,变温水箱,Terumo CDI 101氧饱和度监测仪。全部患儿均使用Medtronic小儿套包,包括离心泵头、中空纤维模式氧合器,裁剪预充ECMO管道时在静脉端接入CDI 101氧饱和度探头。根据病情需要在ECMO循环管路中接入持续肾代替治疗(CRRT)系统。
1.3 MCS建立及管理 病例1、3患儿建立机械循环支持地点为手术室。手术结束,排除存在心脏畸形未纠正,3次尝试停CPB失败后,经ECMO治疗小组紧急讨论决策,家长知情同意后,即直接将CPB切换为ECMO。保留原上腔静脉插管并退入右心房、保留升主动脉插管,停止CPB同时直接与ECMO系统管路连接,半量鱼精蛋白中和,保持ACT时间150~200 s,延迟关胸,关闭皮肤,ECMO辅助下转运至监护室。病例2术日当晚出现严重低心排综合征,心跳骤停,心肺复苏同时紧急床边行ECMO安装术。切开颈部皮肤后暴露右颈总动脉和右颈内静脉,静脉给予肝素(0.5 mg/kg),查ACT>150 s,右颈总动脉插入14 Fr插管,床边超声确定插管头端位于头臂干开口处;右颈内静脉插入14 Fr静脉插管,床边超声确定其位于右房内。病例4术后次日出现心脏骤停,心肺复苏同时紧急床旁ECMO安装术,再次正中打开胸骨,分别经升主动脉和右房插入12 Fr主动脉插管和18 Fr静脉插管。CPB支持时根据疾病和手术要求,进行CPB常规管理。ECMO支持期间根据患儿血压、CVP等血流动力学指标调节ECMO流量和容量,逐渐减少甚至停用血管活性药物,ECMO流量维持50~100 ml/(kg·min),气血比为1∶1,氧浓度0.5~0.6,持续监测静脉氧饱和度,维持其在60%~70%之间,红细胞比容0.35左右;监测ECMO循环管路动、静脉端压力,动端压力可维持<150 mm Hg,静脉端压力能维持>-10 mm Hg。保持机械通气,采用同步间歇指令通气模式,维持高呼气末正压(6~8 cmH2O)、低频率(20~25次/min)、低氧浓度(0.3~0.5)及较长吸气时间模式(0.6~0.7 s)以维持肺泡开放。每6 h监测血气一次,根据血气情况维持内环境稳定,出现明显水钠潴留、尿量减少肾功能不全症状,甚至急性肾功能衰竭[尿素氮(BUN)>28.56 mmol/L,肌酐(Cr)>530.4 μmol/L,血钾>6.5 mmol/L]时给予CRRT,连接方法为与ECMO管路并联,连接ECMO离心泵后动脉端至离心泵前的静脉端,治疗时血流量为5~10 ml/(kg·min),置换液治疗量为15 ml/(kg·min),超滤速度一般为2 ml/(kg·min),实际治疗中可根据患儿血流动力学指标进行调节。每日床旁胸片,心脏超声评估患儿肺部及心功能恢复情况,如心肺功能会有所恢复则逐渐降低ECMO流量,同时逐渐增加血管活性药物用量、适当增长ACT时间,当辅助流量降低至全流量10%,观察1 h左右,复查动静脉血气,满意则撤离ECMO。拔出动、静脉插管后关胸或修补颈总动脉及颈内静脉。
2 结 果
4例患儿中,存活3例,死亡1例(病例3),病例1、病例2、病例4开始ECMO治疗后乳酸水平即迅速下降,ECMO辅助时间分别为96 h、83 h、96 h后撤离。病例3共辅助118 h,持续高乳酸血症,酸中毒始终难以纠正,多脏器功能衰竭(肝、肾、心脏、胃肠道),家属放弃治疗,撤离ECMO后死亡。在ECMO辅助过程中,4例患儿均出现膜肺血浆渗漏,病例1、3及4更换膜肺1次,病例2出现血浆渗漏时考虑患儿心功能基本恢复,予撤离ECMO,未更换膜肺。病例1及病例3均在开始ECMO治疗后第三天出现尿量少、Cr、BUN增高等肾功能衰竭表现,予CRRT治疗,病例4开始ECMO同时即予CRRT治疗。详见表1。
3 讨 论
MCS技术主要包括CPB和ECMO技术,CPB技术目前已经很好地应用于国内先心病患儿术中生命支持,而由CPB技术发展而来的ECMO技术开展则较为滞后。对于一些极度危重的先天性心脏病患儿,无论术前或术后,出现心跳骤停后往往对CPR反应不良,此时则需要更积极手段,MCS技术就成为重症医学专家的选择。但需机械循环支持的患者,预后并不尽如人意。据体外生命支持组织(Extracorporeal Life Support Organisation,ELSO)所提供数据,成人和婴幼儿ECMO循环辅助的生存率分别为32%,45%[3-4],Meert等[5]报道了由15家医院组成的多中心研究资料,共有353例患者在院内出现心跳骤停并接受了ECMO支持,49%的患者存活出院。对出现心跳骤停的极度危重先心病婴幼儿,在进行CPR同时应用MCS技术(CPB或ECMO)救治,在短时间内需要考虑MCS种类、建立方式、治疗时机和适应证是一个巨大挑战。
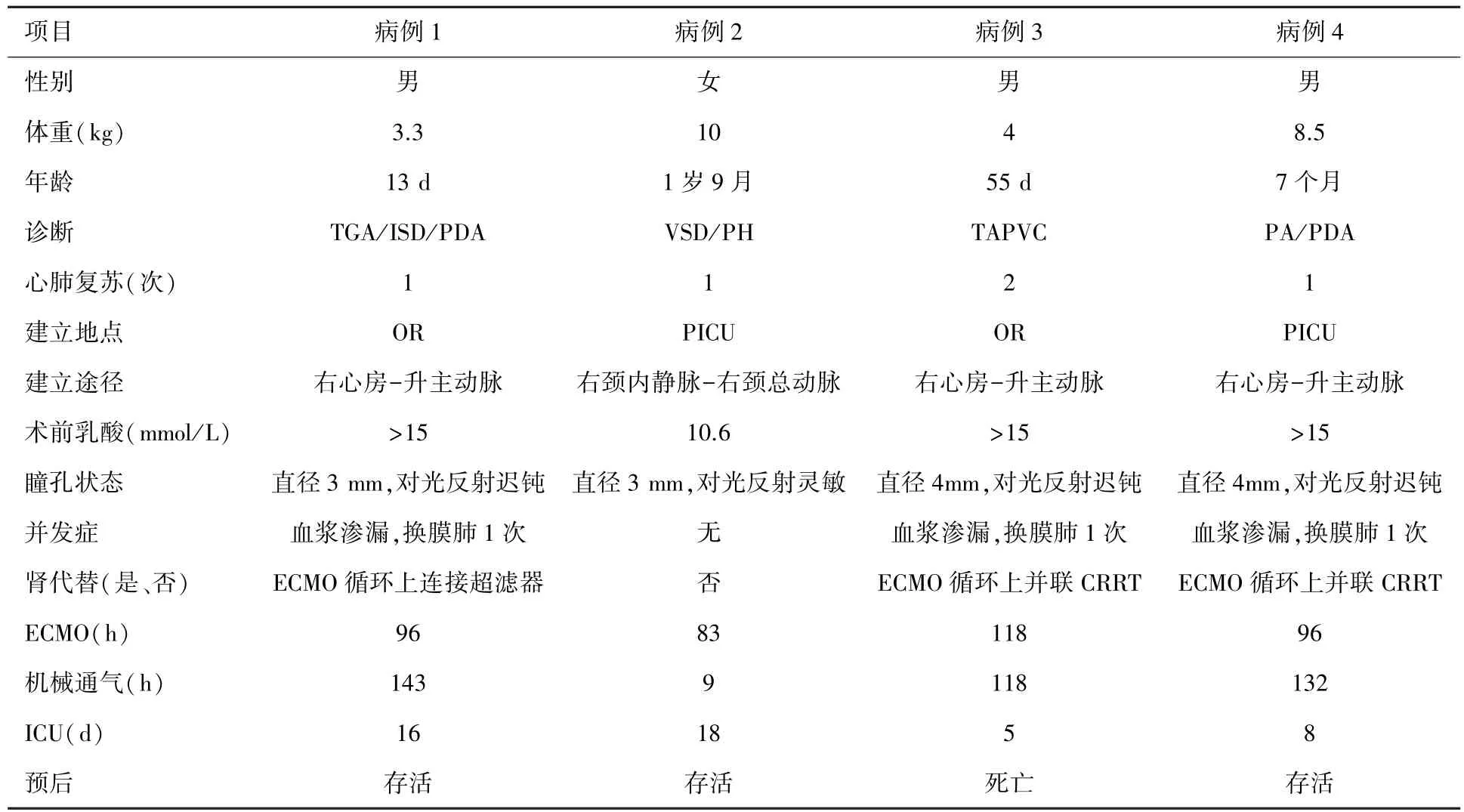
表1 4例ECMO救治患儿临床资料
首先是MCS种类的选择,本文中,病例1、3 CPR后选择CPB进行支持,因这两例患者均为术前患儿,于手术室快速建立CPB支持同时也为下一步心脏畸形矫治创造条件。而病例2、4为术后患儿,选择床旁ECMO辅助。需要ECMO循环支持的重症患儿,是否能成功建立ECMO和正确把握开始ECMO的时机,是成功救治此类重症患儿的关键。在本文中,病例1、3和4都是经胸插管建立ECMO,病例2床旁紧急手术经右颈总动脉、右颈内静脉插管建立ECMO。只要插管型号、种类选择适当,以上两种方式均能快速建立ECMO,并在可接受压力范围内达到满意支持流量。正确把握开始ECMO治疗的时机,需要对患儿各系统功能进行快速、全面和精确的评估。与ECMO救治呼吸衰竭应用方面不同,目前ECMO在循环衰竭危重患儿,尤其是经过心肺复苏患儿的应用,并没有被大家普遍接受的明确适应证与禁忌证,患儿的心肺功能是否具有可恢复性,往往需要在ECMO辅助过程中不断评估。在本组资料中,决定采用机械循环支持前,判断患儿心肺功能是否具有可恢复性有相当大难度,而神经功能评估,只能通过观察瞳孔反射及自主呼吸初步判断。病例1与病例2能够存活,可能与有效心肺复苏和及时建立循环支持(病例1为体外循环支持,心肺复苏与开始循环支持时间<1 hour)有关,而病例3由于监护人因素,从开始心肺复苏至建立循环支持间隔时间较长(约3 h),未能迅速建立有效循环支持。对于经过心脏手术治疗患儿而言,血清中乳酸水平是能够预示危重症患儿预后,与重症患儿死亡率关系密切[6-9]。本组4例患儿开始机械循环支持前乳酸水平均大于10 mmol/L(其中病例1、3、4>15 mmol/L),得到有效循环支持后,存活病例1、2、4均能迅速下降至5 mmol/L以下,而病例3在ECMO辅助期间,即使始终保持SvO2>70%,乳酸水平始终>9 mmol/L,无明显下降,此现象可能因其术前未能及时得到有效循环支持,组织缺氧损伤严重,ECMO支持后虽然保证足够氧供,但机体出现氧利用障碍有关。与机械循环支持前的血清乳酸水平相比,在建立有效循环支持后乳酸水平的动态变化可能是更敏感指示预后的指标,但这仍需要更多的病例研究来支持。
据文献报道,出血和肾功能不全仍是ECMO治疗期间最常见的并发症,出血发生率为29%左右,而肾功能不全与院内死亡高度相关[10-12]。病例1、3和 4均经胸插管建立ECMO,病例2经颈部动、静脉插管,ECMO期间对于凝血监测策略是调整ACT时间150~200 s之间,每日监测血常规,输注血小板维持其水平>50×109/L。除病例2之外,经胸插管的病例1、3、4在ECMO支持期间,即使维持ACT 150~180 s之间,胸部正中切口仍持续渗血。病例1、3、4例患儿在ECMO支持过程中,均出现BUN、Cr升高等肾功能损伤,病例1、3在ECMO第三天出现明显少尿[<1ml/(kg·h)]予以CRRT治疗,病例4由于复苏时间较长,建立ECMO同时即予CRRT治疗。3例患儿均能维持循环稳定,并取得满意的肾代替效果。与传统的单纯在ECMO回路连接超滤器进行CRRT相比较,本单位采用ECMO管路上并联CRRT治疗,能够精确控制CRRT的血流速度及超滤速度,维持患儿容量和循环稳定,对于低龄、低体重患儿意义尤其重大。在机械并发症方面,本组3例患儿均在ECMO治疗80 h前后出现膜肺血浆渗漏,氧合能力下降的情况,这主要与ECMO耗材的质量相关,目前,在国内进行婴幼儿ECMO治疗可供选择耗材不多,只有Medtronic儿童套包可供选择,而其中的中空纤维膜肺使用寿命有限,约70 h左右开始出现血浆渗漏,其中1例膜肺使用35 h即出现膜肺血浆渗漏(病例4),目前,如果想进行较长时间ECMO辅助(>5 d)只能通过更换膜肺解决,要提高婴幼儿长时间ECMO辅助的管理水平,还需要有适合婴幼儿使用的膜肺。
本院对CPR反应不良的先天性心脏病重症患儿快速应用MCS救治进行了尝试,4例患儿中共有3例存活。从初步经验来看,对于出现心跳骤停患儿,及时有效心肺复苏,在准确充分评估心、肺及神经系统功能情况下,快速建立MCS(包括CPB与ECMO),为心功能进一步恢复赢得时间,应该能够提高此类患儿的救治成功率。
[1]Hill JD,O'Brien TG,Murray JJ,et al.Prolonged extracorporeal oxygenation for acute post-traumatic respiratory failure(shocklung syndrome).Use of the Bramson membrane lung[J].N Engl J Med,1972,286(12):629-634.
[2]Lin R,Zhang CM,Tan LH,et al.Emergency use of extracorporeal membrane oxygenation in pediatric critically ill patients.Zhonghua Er Ke Za Zhi,2012,50(9):649-652.
[3]Ayad O,Dietrich A,Mihalov L.Extracorporeal membrane oxygenation[J].Emerg Med Clin North Am,2008,26(4):953-959.
[4]Karagiannidis C,Philipp A,Buchwald D.Extracorporeal membrane oxygenation[J].Dtsch Med Wochenschr,2013,138(5):188-191.
[5]Meert KL,Metheny N.Placement of postpyloric tubes using electromagnetic guidance[J].Pediatr Crit Care Med,2009,10(2):271-273.
[6]Hannan RL,Ybarra MA,Whilte JA,et al.Patterns of lactate values after congenital heart surgery and timing of cardiopulmonary support[J].Ann Thorac Surg,2005,80(4):1468-1473.
[7]Hatherill M,Sajjanhar T,Tibby SM,et al.Serum lactate as a predictor of mortality after paediatric cardiac surgery[J].Arch Dis Child,1997,77(3):235-238.
[8]Hatherill M,Waggie Z,Purves L,et al.Mortality and the nature of metabolic acidosis in children with shock[J].Intensive Care Med,2003,29(2):286-291.
[9]Dietl CA,Wernly JA,Pett SB,et al.Extracorporeal membrane oxygenation support improves survival of patients with severe Hantavirus cardiopulmonary syndromes[J].J Thorac Cardiovasc Surg,2008,135(3):579-584.
[10]Oliver WC.Anticoagulation and coagulation management for ECMO[J].Semin Cardiothorac Vasc Anesth,2009,13(3):154-175.
[11]Khaja WA,Bilen O,Lukner RB,et al.Evaluation of heparin assay for coagulation management in newborns undergoing ECMO[J].Am J Clin Pathol,2010,134(6):950-954.
[12]Combes A,Leprince P,Luyt CE,et al.Outcomes and longterm quality-of-life of patients supported by extracorporeal membrane oxygenation for refractory cardiogenic shock[J].Crit Care Med,2008,36(5):1404-1411.
Mechanical circulatory support in resuscitation of pediatric patients with complex congenital heart defects committed with acute heart arrest,4 cases report
Hong Xiao-yang,Zhou Geng-xu,Liu Yu-hang,Liu Ying-yue,Gao Hai-tao,Wang Hui,
Feng Zhi-chun
Affiliated Bayi Children's Hospital of the General Hospital of Beijing Military Region,Beijing 100007;Affiliated Bayi Children's Hospital of Bayi Clinical Medical College,Nanfang Medical University,Beijing 100007,China
Zhou Geng-Xu,Email:cardiacsurgeon@126.com
ObjectiveTo introduce the experiences of mechanical circulatory support(MCS)in treatment of infants with complex congenital heart disease committed with cardiac arrest.MethodsMCS was adopted to treat 4 infants with complex congenital heart disease committed with cardiac arrest from October 2012 to June 2013,and clinical datas were reviewed.Case 1 was diagnosed as transposition of great arteries with intact ventricular septum.The patient had severe hypoxemia,lactic acidosis and acute cardiac arrest before surgery;cardiopulmonary resuscitation as well as arterial switch operation were performed with emergency cardiopulmonary bypass(CPB).After surgery,CPB was switched to ECMO.Case 2 was diagnosed as residual shunt after ventricular septal defect repairing,severe pulmonary hypertension and left ventricular dysfunction.After the residue shunt repaired,this patient had cardiac arrest and lactic acidosis.Cardiopulmonary resuscitation was performed and emergency bedside ECMO was setup.Case 3 was diagnosed as total anomalous pulmonary venous drainage(supracardiac type).This patient had severe hypoxemia,lactic acidosis and cardiac arrest 2 times before surgery,and urgent defect correction surgery was performed under CPB and switched to ECMO support.Case 4 was diagnosed as pulmonary atresia and patent ductus arteriosus.After operation,this patient had cardiac arrest and lactic acidosis.Cardiopulmonary resuscitation and bedside emergency ECMO were performed.ResultsAmong these 4 patients,3 cases successfully weaned from ECMO,and case 3 died due to multiple organ failure.ConclusionFor infants with complex congenital heart disease and cardiac arrest,application of emergency ECMO support to correct hypoxia and hypoperfusion is a lifesaving effective treatment.
Mechanical circulatory support(MCS);Extracorporeal membrane oxygenation(ECMO);Cardiac arrest;Congenital heart disease;Cardiopulmonary resuscitation
R654.1
A
1672-1403(2013)03-0165-05
2013-06-24)
2013-07-13)
100007北京,北京军区总医院附属八一儿童医院
封志纯,Email:zhjfengzc@126.com

