粗级碳酸锂提纯工艺过程研究*
李燕茹,朱亮,袁建军,沙作良,杨美洁,左玥华
(天津科技大学天津市海洋资源与化学重点实验室,天津 300457)
粗级碳酸锂提纯工艺过程研究*
李燕茹,朱亮,袁建军,沙作良,杨美洁,左玥华
(天津科技大学天津市海洋资源与化学重点实验室,天津 300457)
摘 要碳酸锂产品在陶瓷、冶金、能源、医药等行业应用广泛,实际应用中对碳酸锂产品的纯度要求很高。由于生产技术和盐湖卤水自身条件的限制,直接提取的碳酸锂产品都很难达到要求。基于实际应用的需求,以从卤水制备而得的粗级碳酸锂产品为原料,通过氢化分解法对其提纯,研究了氢化反应中的二氧化碳气体流速、氢化时间、氢化温度及固液比4个氢化条件对粗级碳酸锂溶解的影响。结果表明,采用这项简单工艺可使粗级碳酸锂产品的纯度由88%提高到99%以上,一次性产率达到75%以上。
关键词:碳酸锂;提纯工艺;氢化分解法
碳酸锂(Li2CO3)是制备各种锂化合物的原料,是锂盐产品中产量最大、用途最广的产品。其中高纯碳酸锂在电子技术、高纯试剂、有机合成、药物、特殊玻璃的添加剂、食品保存和人造矿泉水的添加剂等方面有着重要用途。近些年,国内外对碳酸锂产品质量的要求越来越高,而大多初级产品都达不到要求,所以研究针对不同情况的粗锂提纯方法很有必要。目前,由粗级碳酸锂产品(即纯度低于95%)制备高纯碳酸锂产品的纯化方法主要有苛化法、重结晶法、电解法、氢化沉淀法以及氢化分解法。苛化法能够有效去除钙、镁杂质,但对石灰乳纯度的要求很高;重结晶法简单易行,但是碳酸锂溶解度很小,需要能耗较大,生产周期也较长;电解法得到的碳酸锂产品能够达到很高的纯度且流程较短,但此方法对膜的要求较高,电耗也大;氢化沉淀法能够更好地控制产品粒度,但是制备过程中对氢氧化锂的纯度要求很高,这就使生产成本增加;氢化分解法具有较高的操作可行性,回收率优于氢化沉淀法[1-2],其分解过程容易产生黏壁现象,但是如果控制好反应条件就可以避免。因此,笔者对氢化分解法提纯碳酸锂产品进行了实验研究。
1 实验部分
1.1 原料与仪器
原料:利用盐湖卤水自制粗级碳酸锂产品[组成(质量分数):Li+,16.74%;Mg2+,2.29%;Na+,1.08%;,78.45%;Cl-,0.45%;,0.014%;K+,0.122%;B2O3,0.107%];CO2(99.99%以上,天津市泰源工业气体有限公司)。
仪器:DW-3型数显电动搅拌器、SYC型智能超级恒温水槽、LZB-F型玻璃转子流量计、SHB-IV双A型循环水式多用真空泵、WFX-120型原子吸收分光光度计。
1.2 实验过程及结果分析
由原料组成可知,粗锂产品中主要杂质为镁,由于镁与锂的性质很相似,单靠氢化分解法不能达到提纯碳酸锂的目的。针对这一点,笔者将整个实验大体分为三步:氢化过程、除镁过程和蒸发分解过程。
1.2.1 氢化过程
1)氢化温度。称取10 g的粗级碳酸锂产品于500 mL结晶器中,固液质量比为1∶20,CO2气体流速为1 L/min,分别选择氢化温度为10、15、20、25、30、40℃,氢化150 min后抽滤,测定液相中锂、镁离子含量,考察氢化温度对碳酸锂及杂质镁的溶解过程的影响,实验结果见图1。

图1 氢化温度对碳酸锂和杂质镁溶解的影响
温度对化学反应速率和气液传质均有影响。温度升高反应速率会加快,但反应物CO2和Li2CO3以及产物LiHCO3的溶解度又都随温度的升高而减小,使传质推动力减小,从而导致反应速率减慢。由图1可见,随着温度的升高,溶解到溶液中的锂离子越少,与此同时碳酸镁的溶解度不断增大,因此越来越多的杂质镁离子溶解到溶液中。分析实验数据可知,高温不利于氢化反应的进行。结合实际生产中对节能的考虑,实验选择在室温(20℃,下同)下进行氢化反应。
2)氢化时间及CO2气体流速。称取10 g的粗级碳酸锂产品于500 mL结晶器中,氢化温度为室温,固液质量比为1∶20,分别选择CO2气体流速为0.5、1、1.5、2、3、4 L/min,针对每一个CO2气体流速下分别控制其氢化时间为30、50、70、90、120、150 min进行实验,抽滤后分析液相中锂、镁离子含量,考察氢化时间及CO2气体流速对碳酸锂及杂质镁的溶解过程的影响,实验结果见图2。
CO2气体流速加快,则单位时间进入反应器的气体量增加,液体中的气泡量增多,所以气液接触面增大,进而使氢化反应速率增大,即达到溶解平衡所需的时间越短。从图2可见,CO2气体流速越大、氢化时间越长,溶解到溶液中的锂、镁离子越多,但是这2个条件对锂离子的溶解影响比对镁离子影响大。综合考虑,实验选择最佳氢化反应时间为150 min、CO2最佳气体流速为1 L/min。

图2 CO2气体流速及氢化反应时间对碳酸锂和杂质镁溶解过程的影响
3)固液质量比。称取10 g的粗级碳酸锂产品于500 mL结晶器中,氢化温度为室温,氢化时间为150 min,CO2气体流速为1 L/min,分别按固液质量比为1∶10、1∶20、1∶30、1∶40、1∶50进行实验,抽滤后分析液相中锂、镁离子含量,考察固液质量比对碳酸锂及杂质镁的溶解过程的影响,实验结果见图3。

图3 固液质量比对碳酸锂及碳酸镁溶解度及对氢化反应中锂的损失率和镁去除率的影响
由图3可见,随着液固比的增大,液相中锂、镁离子浓度逐渐减小;锂离子的损失率呈现不断减小的趋势但减小幅度越来越小;而镁离子的去除率呈先增大后趋于稳定又增大的趋势。这是由于随着反应物中水的比例增加,更多的CO2溶解于水中,与Li2CO3反应更充分,使得Li2CO3中越多的Li+转化到液相中,且液体比例的增加有利于除掉杂质镁。但是考虑到后期需要蒸发提取碳酸锂,若液体比例太大会增加成本,因此选择适宜的固液质量比为1∶20。
缺镁发生原因:首先,酸性土壤和轻砂土中镁容易流失,尤其是山坡地,土壤中的交换性镁含量降低。其次,钾肥和磷施用过多,影响橘树对镁的吸收,容易引起缺镁。此外,果园中过多使用硫磺及石硫合剂药剂,容易使土壤显酸性,导致缺镁。
1.2.2 除镁过程
经过氢化过程,溶液中残留0.086%(质量分数)的镁离子,为了得到高纯度碳酸锂产品需要在蒸发分解之前除镁,笔者研究了利用氢氧化钠溶液除掉氢化之后溶液中的镁离子的过程,实验结果见图4。
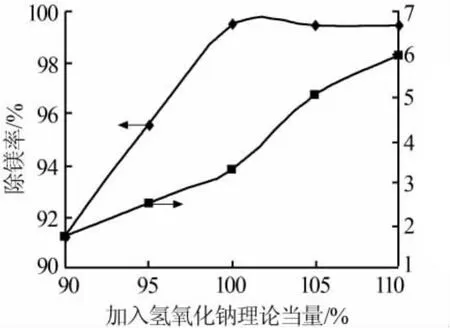
图4 加入氢氧化钠的量对除镁率和锂损失率的影响
由图4可知,氢氧化钠的加入可以很好地除掉溶液中的镁杂质,且过程中锂的损失率很小,这主要是因为溶液中的镁离子的质量分数很小(0.086%),加入除镁的氢氧化钠量也很小,因此对溶液酸碱度几乎没有影响,过程中损失的锂离子也是母液夹带。由实验结果可知,加入除镁氢氧化钠的理论当量(加入量占理论加入量的分数)以100%为宜。
1.2.3 蒸发分解过程
粗级Li2CO3经过氢化过程后转变为LiHCO3,再经除镁,现只需将LiHCO3经高温分解即可得到高纯度Li2CO3产品。整个蒸发分解过程是由LiHCO3热分解和Li2CO3反应结晶2个过程组成。
根据热力学参数计算可知,LiHCO3热分解的理论温度为4.25℃[3],但是低温下其分解速度很慢,且碳酸氢锂分解过程是吸热过程,升高温度有利于溶质的扩散,加快晶体生长的速率。因此,提高反应温度有利于蒸发分解过程的进行,但是实验过程控制不当又很容易发生黏壁现象,而且温度超过90℃会导致反应异常剧烈,且放出大量CO2气体发生“冒槽”事故。因此,实验选择适宜的分解温度为90℃。
在分解-结晶过程中会有CO2放出,搅拌速率也会有很大的影响。搅拌速率越快,液体湍动越强,越有利于CO2不断从反应体系中逸出,所以加快搅拌有利于碳酸氢锂的分解。且实际应用过程中碳酸锂产品的粒度越小越好,所以也可以通过加快搅拌速率的方法得到粒度相对小的产品。综合考虑,实验选择适宜的搅拌速率为500 r/min。
取300 g除镁后的碳酸氢锂溶液于500 mL结晶器中,控制恒温水浴的温度为90℃,搅拌速率为500 r/min,蒸发水的质量分别为100、150、200、250、270 g,高温抽滤,并多次用90℃热水清洗,取出烘干,考察了水蒸发率对产品产率和纯度的影响,实验结果见图5。

图5 水蒸发率对产品产率和纯度的影响
2 结论
与其他粗级碳酸锂产品提纯工艺过程相比,氢化分解法操作过程简单,与其他除杂过程结合效果很好。采用该方法能够使粗级碳酸锂产品的纯度由88%提升至99%以上,整个过程的一次性产率可达75%以上,而且蒸发分解之后的剩余卤液可用于循环提纯产品,通过余液的循环利用可以提高产品的产率。因此,利用氢化分解法提纯碳酸锂产品优势显著。实验过程中,镁离子质量分数最低只能降到0.012%,其他杂质离子单单依靠氢化分解法也很难除去,因此要想得到更高纯度的碳酸锂产品还需将氢化分解法与其他高级除杂方法相结合,例如过程中加入离子交换树脂对杂质离子进行分离[4]。
参考文献:
[1]伊文涛,闫春燕,马培华,等.碳酸锂碳化反应动力学研究[J].化工矿物与加工,2006,35(12):21-24.
[2]Yi Wentao,Yan Chunyan,Ma Peihua,et al.Refining of crude Li2CO3via slurry phase dissolution using CO2[J].Separation and Purification Technology,2007,56(3):241-248.
[3]贾之慎.无机及分析化学[M].北京:高等教育出版社,2008.
[4]吴鉴.氢化分解法从工业级碳酸锂提纯制备电池级碳酸锂[D].昆明:昆明理工大学,2011.
联系方式:lyr-gpz@126.com
中图分类号:TQ131.11
文献标识码:A
文章编号:1006-4990(2013)08-0015-03
收稿日期:2013-02-10
作者简介:李燕茹(1987—),女,硕士,主要研究方向为海卤水资源的综合利用。
*基金项目:自然科学基金重点项目(12JCZDJC28200、12JCZDJC30000)。
Research on purifying process of coarse lithium carbonate
Li Yanru,Zhu Liang,Yuan Jianjun,Sha Zuoliang,Yang Meijie,Zuo Yuehua
(Tianjin Key Laboratory of Marine Resources and Chemistry,Tianjin University of Science and Technology,Tianjin 300457,China)
Abstract:Lithium carbonate(Li2CO3)is widely used in the fields of ceramics,metallurgy,energy,and pharmaceutical etc..A lot of practical applications of Li2CO3need high purity,but the Li2CO3that extracts directly from the salt lake brine are difficult to meet the requirements due to existing technology and the limitations of the salt lake brine itself.Based on the practical requirements,carbonation-decomposition method to get high-purity Li2CO3from the coarse Li2CO3products was studied.The effects of carbonation conditions,such as CO2flow rate,carbonation time,carbonation temperature,and the ratio of solid to liquid,on the dissolution of coarse Li2CO3were also investigated.Results showed through the simple process the purity of Li2CO3could increase from 88%to more than 99%,and the yield of the all process could reach more than 75%.
Key words:lithium carbonate;purifying process;carbonation-decomposition method

