HPLC测定2,5’-二溴-4,5,2’-三羟基二苯甲酮原料药的含量及有关物质
李勇,冯秀娥,梁泰刚,李青山
(山西医科大学药学院,太原 030001)
HPLC测定2,5’-二溴-4,5,2’-三羟基二苯甲酮原料药的含量及有关物质
李勇,冯秀娥,梁泰刚,李青山*
(山西医科大学药学院,太原 030001)
目的 建立HPLC测定海洋来源活性化合物2,5’-二溴-4,5,2’-三羟基二苯甲酮原料药(LM49)的含量及有关物质的方法。方法 采用Diamonsil C18(250 mm×4.6 mm,5 μm)色谱柱,甲醇-乙腈-水(磷酸调pH至3.0)(70∶10∶20)为流动相,检测波长为261 nm,流速0.8 mL·min-1,柱温25 ℃。结果 主峰能与杂质峰达到良好分离,LM49在浓度1.0~100 mg·L-1内线性关系良好(r=0.999 9),最低检测限为0.02 mg·L-1,平均回收率为99.8%(RSD=0.88%)。结论 本法简便、快速、准确,可用于LM49原料药的含量及有关物质的测定。
高效液相色谱法;2,5’-二溴-4,5,2’-三羟基二苯甲酮;有关物质;含量测定
2,5’-二溴-4,5,2’-三羟基二苯甲酮(LM49)为课题组自主合成、具有全新结构的海洋来源溴酚化合物,其对过氧化氢损伤的人脐静脉内皮细胞有显著的保护作用[1],提示该化合物对心脑血管疾病有较强的应用开发前景。由于LM49为本课题组自主合成,目前还没有建立含量测定和有关物质的检测方法。原料药的质量标准建立与质量控制是其后续系统研发工作的基础,为使LM49的质量可控并为后续研究提供质量稳定的样品,本实验采用HPLC对LM49原料药的含量及有关物质的检查进行了研究,结果表明,所建立的方法准确、专属性强、灵敏度高、分离度好,可有效检测原料药中LM49的含量并对有关物质进行控制。
1 仪器与试药
Agilent 1200高效液相色谱仪(美国Agilent公司);BT25S型电子天平(德国Sartorius);LM49对照品(以邻甲氧基苯甲酰氯与1,2-二甲氧基苯为起始原料自制,经3次重结晶,面积归一化法测定其纯度≥99.85%);LM49供试品(自制,批号:20120302,20120511,20120723);甲醇、乙腈为色谱纯;超纯水(用磷酸调节pH至3.0),其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Diamonsil C18(250 mm×4.6 mm,5 μm),流动相:甲醇-乙腈-水(70∶10∶20)(水用磷酸调pH至3.0),流速0.8 mL·min-1,检测波长261 nm,柱温25 ℃,进样量20 μL。
2.2 对照品溶液和供试品溶液的配制
取室温下减压干燥至恒重的LM49对照品和LM49供试品(批号:20120511)各约5 mg,精密称定,分别置50 mL量瓶中,加甲醇溶解并定容至刻度,摇匀,即得100 mg·L-1的对照品贮备液和供试品贮备液,置于4 ℃冰箱中保存。
2.3 检测波长的确定
精密量取5.0 mL对照品贮备液,用甲醇稀释并定容至10 mL,配制成50 mg·L-1的溶液,进行DAD检测,结果表明,在261 nm处有最大吸收,确定261 nm为检测波长。
2.4 系统适用性试验
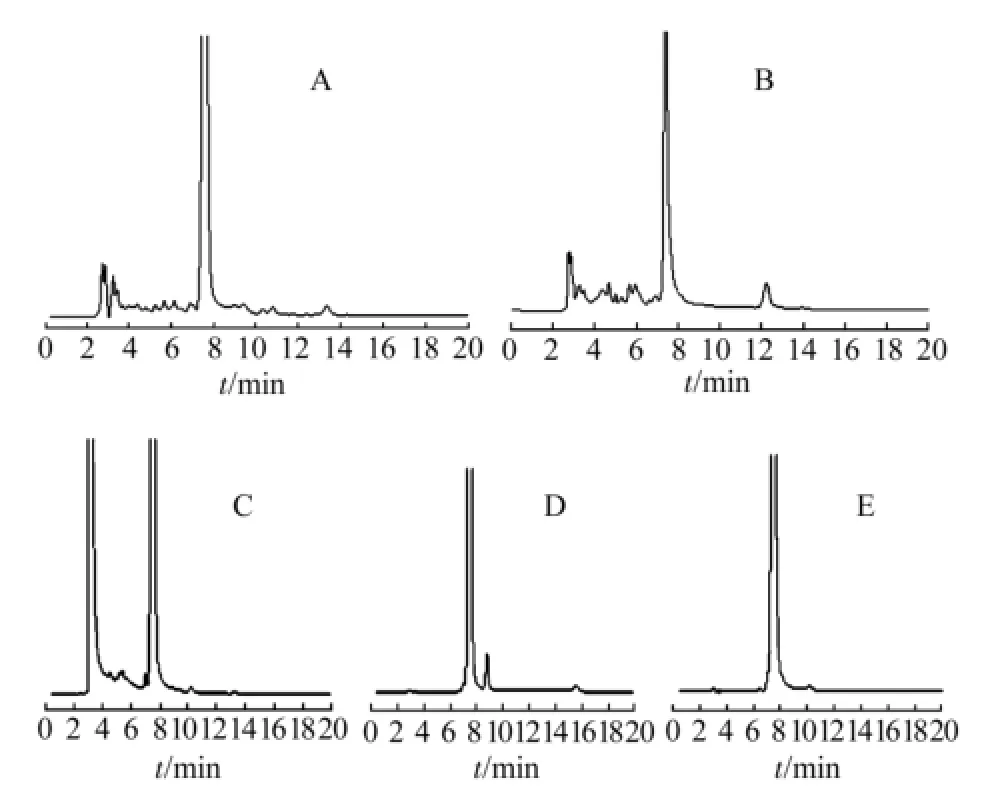
按“2.1”项下色谱条件进样测定,LM49的保留时间为7.48 min,理论板数按LM49计算不低于8 000,与相邻杂质的分离度>1.5,分离良好,峰形对称,结果见图1。

图1 系统适用性试验相关HPLC色谱图A-LM49对照品溶液;B-LM49供试品溶液;C-LM49对照品/原料/中间体混合溶液;1-LM49;3,4-原料;2-原料中的杂质;5,6-中间体Fig 1 HPLC chromatograms of system suitability of LM49 A-LM49 reference substance; B-LM49 test sample; C-LM49/raw materials/intermediates; 1-LM49; 3,4-raw materials; 2-impurity of raw material; 5,6-intermediates
2.5 线性关系和方法学研究
2.5.1 线性关系 分别精密量取对照品贮备液适量,用甲醇稀释成浓度为1.0,5.0,25,50,75,100 mg·L-1的溶液,按“2.1”项下色谱条件进样测定,以浓度(C)为横坐标,色谱峰面积(A)为纵坐标,进行线性回归,回归方程为:A=37.546C-27.8,r=0.999 9。结果表明,本品在1.0~100 mg·L-1内线性关系良好。
2.5.2 检测限及定量限 精密量取对照品贮备液适量,逐级稀释,按“2.1”项下色谱条件进样测定,记录信噪比(S/N)为3,10的色谱图。结果LM49的最低检测浓度为0.02 mg·L-1,最低检测限为0.4 ng;最低定量浓度为0.05 mg·L-1,最低定量限为1 ng。
2.5.3 精密度 精密量取对照品贮备液适量,用甲醇稀释至浓度为50 mg·L-1的对照品溶液,按“2.1”项下色谱条件进样测定,1 d内连续进样6次,考察日内精密度,RSD为0.67%;取上述溶液,每天进样1次,连续测定5 d,考察日间精密度,RSD为1.08%。表明精密度良好。
2.5.4 重复性 取同一批供试品(批号:20120511) 2.5 mg,共5份,精密称定,置于50 mL量瓶中,分别用甲醇溶解并定容至刻度,摇匀。按“2.1”项下色谱条件,按含量测定方法测定,结果其平均含量为99.26%,RSD为0.51%,表明方法重复性良好。
2.5.5 稳定性 取浓度为50 mg·L-1(批号:20120511)的供试品溶液,按“2.1”项下色谱条件进样测定,分别测定其在室温下放置0,2,4,8,12,24 h及3 d后的峰面积,以峰面积考察溶液的稳定性,RSD为1.46%,结果表明,室温放置3 d的供试品溶液稳定性良好。
2.5.6 回收率 称取减压干燥至恒重的同一批供试品(批号:20120511)5.07 mg,用甲醇溶解并定容至50 mL量瓶中。精密量取供试品溶液1.0 mL于10 mL量瓶中,共9份。分别加入对照品溶液(100 mg·L-1)各0.6,1.0,1.4 mL,各3份,加甲醇稀释至刻度,定容,摇匀,经0.45 μm微孔滤膜滤过,取续滤液,按“2.1”项下色谱条件测定,记录峰面积,计算平均回收率,结果见表1。
2.6 含量测定
取本品3批,用甲醇配制成质量浓度为100 mg·L-1的供试品液,另精密称取LM49对照品5.0 mg,置于50 mL量瓶中,用甲醇溶解并定容至刻度,摇匀,配制成浓度为100 mg·L-1的对照品液,分别精密量取20 μL注入液相色谱仪,记录色谱图,按外标法计算含量[2]。结果批号为20120302,20120511,20120723的样品含量分别为100.1%,99.3%,100.4%,RSD分别为0.56%,0.62%,0.44%。

表1 LM49的回收率测定(n=9)Tab 1 The recovery determination of LM49 (n=9)
2.7 专属性试验
为考察HPLC的专属性,根据合成工艺、化合物结构特点及贮存条件,对LM49进行了酸、碱、氧化、高温、强光照射等加速破坏实验[3-6]。取LM49供试品(批号:20120511)适量,用甲醇制成100 mg·L-1的溶液,取样2 mL,共5份。其中1份加2 mL 0.1 mol·L-1的盐酸溶液,加热回流2 h,冷却至室温,用0.1 mol·L-1的氢氧化钠溶液中和至中性;1份加2 mL 0.1 mol·L-1的氢氧化钠溶液,加热回流2 h,冷却至室温,用0.1 mol·L-1的盐酸中和至中性。其中1份加30%过氧化氢溶液0.5 mL,加热回流1 h,冷却至室温。1份80 ℃加热回流1 h。另外1份置于4 500 Lx照度下放置72 h。按“2.1”项下色谱条件进样测定。结果见图2。由加速破坏性实验结果可知,所建HPLC方法能有效检测出各破坏性实验产生的降解产物,且降解产物均能与主峰达到良好分离,表明对有关物质检查的专属性良好。
2.8 有关物质的检查
精密称取LM49样品5.0 mg于50 mL量瓶中,加甲醇溶解并定容至刻度,摇匀,作为供试溶液,精密量取供试溶液1.0 mL,置于100 mL量瓶中,加甲醇溶解并定容至刻度,摇匀,作为对照液。精密量取对照液20 μL,注入液相色谱仪,调节检测器的灵敏度,使主成分的色谱峰高约为满量程的30%。再精密量取供试溶液20 μL注入液相色谱仪,记录色谱图至对照品主峰保留时间的2.5倍。量取供试溶液色谱图中各杂质峰的峰面积总和,用主成分自身对照法计算有关物质的量。结果3批样品的有关物质含量分别为0.34%,0.45%和0.48%。
3 讨论
LM49易溶于甲醇,因此选用不同配比的甲醇-水组成流动相,由于LM49含有酚羟基,呈弱酸性,考察了不同pH值对化合物色谱行为的影响,最终发现用磷酸调节水相的pH为3.0时,色谱峰形及分离度均较好,化合物保留时间适中。流动相中加入乙腈,使色谱峰的对称性得到了进一步优化,最终确定流动相的配比为甲醇-乙腈-水(70∶10∶20)(水用磷酸调节pH至3.0)。
本实验为LM49建立了简便、快速、准确、专属的HPLC方法,为其质量控制及有关物质检查提供了可靠的依据。
REFERENCES
[1] ZHAO W Y, FENG X E, BAN S R, et al. Synthesis and biological activity of halophenols as potent antioxidant and cytoprotective agents [J]. Bioorg Med Chem Lett, 2010, 20(14): 4132-4134.
[2] Ch.P(2010)Vol (Ⅱ中国药典2010年版. 二部) [S]. 2010: Appendix 30.
[3] LEI H Y, ZHANG C H, HUO L R, et al. RP-HPLC determination of YF-13-1 and its related substances [J]. Chin J Pharm Anal(药物分析杂志), 2012, 32(8): 1394-1397.
[4] WANG J, LI X N, ZHANG J M, et al. RP-HPLC determination of TM 208 and its related substances [J]. Chin J Pharm Anal(药物分析杂志), 2011, 31(1): 99-102.
[5] ZHENG J Q, HAN J Y, LI H L. Determination of content and related substances of methylparaben sodium by HPLC [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2012, 29(1): 72-76.
[6] MA Y L, TANG L, LIANG T G, et al. Determination of crude drug 4-O-methyl benzenesulfonyl-2(3H)-benzoxazolone and its related substances by HPLC [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2012, 29(9): 833-835.
Determination of 2,5’-Dibromo-4,5,2’-trihydroxydiphenylmethanone and Its Related Substances by HPLC
LI Yong, FENG Xiu’e, LIANG Taigang, LI Qingshan*(School of Pharmaceutical Sciences, Shanxi Medical University, Taiyuan 030001, China)
OBJECTIVE To establish an HPLC method for the determination of 2,5’-dibromo-4,5,2’-trihydroxydiphenylmethanone(LM49) and its related substances. METHODS HPLC method was carried on a column of Diamonsil C18column (250 mm × 4.6 mm, 5 μm) with the mobile phase of methanol-acetonitrile-water (adjusted to pH 3.0 with phosphoric acid) (70∶10∶20) at the flow rate of 0.8 mL·min-1and the detection wavelength was set at 261 nm. The column temperature was 25 . ℃RESULTS LM49 was completely separated from the impurities. A good linearity(r=0.999 9) of LM49 was obtained at the concentration range of 1.0-100 mg·L-1. The minimal detection limit was 0.02 mg·L-1. The average recovery of method was 99.8%(RSD=0.88%). CONCLUSION The analytical method is simple, rapid, sensitive and accurate for the determination of LM49 and its related substances.
HPLC; 2,5’-dibromo-4,5,2’-trihydroxydiphenylmethanone; related substances; content determination
R917.101
B
1007-7693(2013)10-1104-04
2012-12-21
国家“863”计划项目(2013AA092903);山西省自然科学基金(2013011060-2);山西医科大学科技创新基金(01201116);山西医科大学博士启动基金(B03201213)
李勇,男,硕士 Tel: 15903460874 E-mail: yong5130@126.com*
李青山,男,博士,博导 Tel: (0351)4690322 E-mail: sxlqs2012@163.com

