酶联免疫法测定去氨加压素血药浓度及其药动学
裴泽军,孙欣,王亚平 (无锡市第二人民医院,江苏 无锡214002)
加压素(vasopressin,又称抗利尿激素)是一种多肽激素,在下丘脑的视上核和室旁核中合成后经下丘脑—垂体束到达神经垂体释放[1]。去氨加压素是天然加压素的结构类似物,即1-半胱氨酸脱去氨基和以8-D-精氨酸取代8-L-精氨酸。去氨加压素既是血管收缩素又是抗利尿激素。在收缩血管作用方面主要通过刺激血管平滑肌内的血管加压素V1受体而产生血管平滑肌显著收缩,其作用强度甚至超过去甲肾上腺素和血管紧张素II。在抗利尿作用方面主要是通过刺激肾集合管中的血管加压素V2受体,提高远曲小管和集合管对水的通透性,促进水的再吸收,因此能起到维持血浆渗透压的稳定作用,是尿液浓缩和稀释的关键性调节激素。
去氨加压素应用于临床已经有多年,但对其深入研究却并不多,尤其在药动学方面许多参数缺乏且国内外的数据也存在较大差异。为此,我们通过利用人去氨加压素(dDAVP)ELISA试剂盒进行去氨加压素的血药浓度测定与药动学研究,取得了满意的效果,获得了dDAVP的相关药动学参数。
1 材料与方法
1.1 材料 人去氨加压素(dDAVP)ELISA试剂盒(CUSABIO公司;批号20120131);酶标仪KHB ST-360;醋酸去氨加压素注射液(深圳翰宇药业股份有限公司,规格:1 mL∶4μg,批号20110705)。
1.2 方法
1.2.1 受试者选择 选择受试者8名,男女各半,入选标准:年龄(49.4±5.2)岁,身高(166.2±7.4)cm,体质量(64.2±5.6)kg,体重指数(BMI)范围:18.5~23.90。试验前经检查心电图、血压、血生化等各项指标均正常,病史询问无药物过敏史和药物依赖史,无其他慢性及精神病史。本试验方案经医院医学伦理委员会讨论并批准,受试者均自愿参加并签署知情同意书。
1.2.2 给药方法及血样采集 受试者给予试药前各抽取静脉血2 mL作对照。将醋酸去氨加压素注射液16μg加入0.9%氯化钠注射液50 mL中,给受试者予以静脉滴注并控制滴速使在20 min内给药结束,完成后分别在0,20,40,60,80,100,120,140,160,180,200 min各抽取静脉血2 mL,离心沉淀吸取上清血清,置-80℃冰箱保存备检。
1.2.3 血药浓度测定方法 用人去氨加压素(dDAVP)ELISA试剂盒进行检测,按操作说明书对标准品及检测样品进行稀释、加样、温育、洗涤、加酶、显色、测定(以空白调零,450 nm波长依序测量各孔的吸光度(OD值)。测定应在加终止液后15 min以内进行)。样本结果从标准曲线读取。
2 结果
2.1 标准曲线的建立 配制20,60,100,140,180 pg·mL-1不同质量浓度的标准液后进行检测并用SPSS 18.0软件绘制标准曲线图。标准曲线的回归方程:Y=92.264X+9.655 5,R2=0.998 1,线性范围:2~400 pg·mL-1,定量下限:2 pg·mL-1。
2.2 稳定性、精密度及回收试验 以空白健康人血清精密配置去氨加压素含量为50,100,150 pg·mL-1的样品各5份,置-80℃冰箱保存。分别在6,12,24 h及3,5,10 d室温融冻,按“1.2.3”方法进行含量测定,结果表明样品在-80℃冰箱保存10 d内稳定。但不可重复融冻,重复融冻会使含量下降明显,实验表明反复融冻3次及以上含量平均下降超过16%。另经连续日内、日间测定计算日内、日间精密度,结果见表1。
另取空白健康人血清精密配置去氨加压素含量为50,100,150 pg·mL-1的样品各5份,以同一血清作空白对照,按“1.2.3”方法进行含量测定,将实际测定含量除以理论含量计算回收率,平均回收率为:100.96%,结果见表1。
2.3 实验结果 受试者血清按“1.2.3”方法进行DDAVP的血药浓度检测,用SPSS 18.0软件对8名受试者检测结果的平均值作药时曲线图(图1)并计算药动学参数,得:t1/2=(81.1±10.9)min;Cmax=(175.1±8.8)pg·mL-1;AUC0→200=(18 415±964)pg·h-1·mL-1;ClT=(52.8±2.6)mL·min-1。
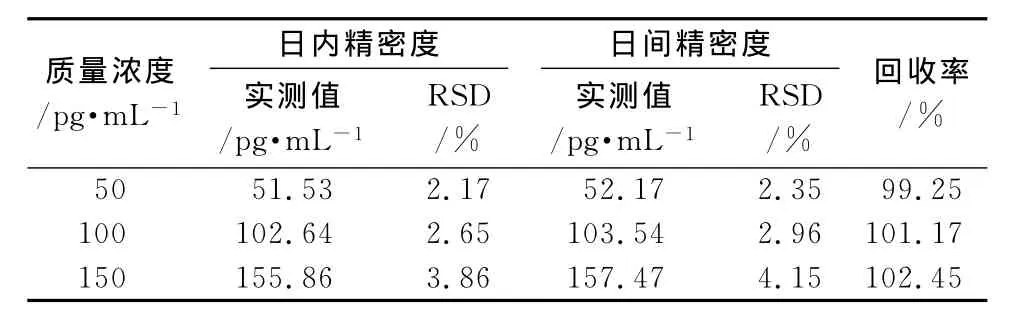
表1 精密度及回收率试验结果(n=5)Tab 1 Results of precision and recovery(n=5)
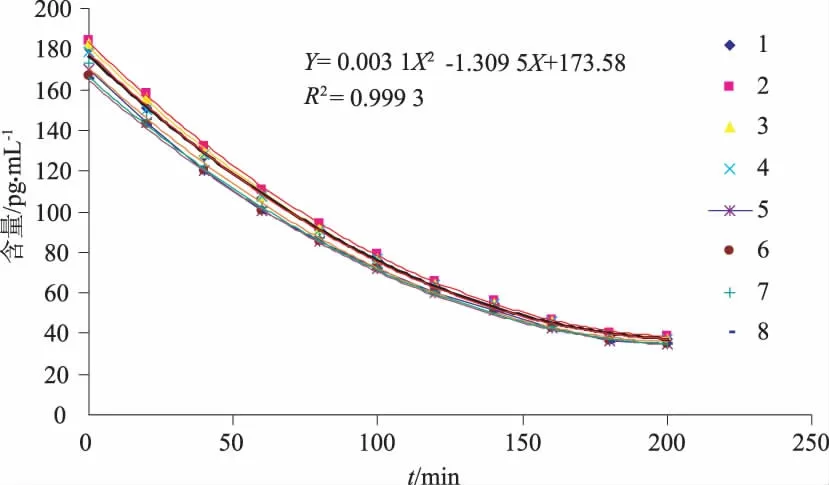
图1 去氨加压素药-时曲线图Fig 1 The drug-time curve of desmopressin
3 讨论
ELISA法即酶联免疫检测方法,其检测原理主要是通过抗原(或抗体)与酶标记的抗体(或抗原)结合,再进行显色反应,通过测定比色来计算含量。因此,ELISA法具有特异性强、灵敏度高、重复性好等特点[2]。
ELISA法测定人血清去氨加压素的试剂盒是用纯化的人精氨酸加压素抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入精氨酸加压素(AVP),再与辣根过氧化物酶(HRP)标记的羊抗人抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物 3,3’,5,5’-四甲基联苯胺(TMB,3,3,5,5 –tetramethylbenzidine)显 色。TMB在HRP的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的精氨酸加压素(AVP)呈正相关。用酶标仪在450 nm波长下测定吸光度(OD值),通过标准曲线计算样品中AVP浓度。
目前去氨加压素的药代动力学研究较少,其国内外的数据差异也较大,如:国内资料显示其t1/2为3~4 h[3],而国外资料显示其t1/2为50~158 min[4],我们创新性地用ELISA法进行了dDAVP的药动学研究,研究结果则显示其t1/2为(81.1±10.9)min。同时,通过我们研究填补了去氨加压素其他的一些药动学参数的空白:20 min静脉滴注dDAVP16μg后的Cmax=(175.1±8.8)pg·mL-1;AUC0→200=(18 415±964)pg·h·mL-1;说明其在组织体液中有很好的分布;ClT=(52.8±2.6)mL·min-1,说明其消除速率较快。
研究证明ELISA法检测去氨加压素血浓的方法特异性、灵敏度、稳定性都很好,且操作简单、方便。从而为进一步开展去氨加压素的临床研究提供良好的借鉴作用。
[1]张金男,高宇飞,赵丛海,等.神经外科术后中枢性尿崩症ADH变化曲线及其临床意义[J].吉林大学学报,2006,32(6):1087-1090.
[2]郭羽中,张真铭.ELISA法检测 HBsAg实验条件的优化[J].国际检验医学杂志,2011,32(6):656-657.
[3]陈新谦,金有豫,汤光.新编药物学[M].16版,北京,人民卫生出版社,2007:545-546.
[4]卫生部合理用药专家委员会.中国医师药师临床用药指南[M].重庆,重庆出版社,2009:1044-1045.

