经小脑水平裂—小脑桥脑裂治疗三叉神经痛解剖入路的基础研究
常书锋,孙君军,郑 鲁,史保中,段勇刚,王 永
三叉神经痛(trigeminal neuralgia,TN),是在三叉神经单支或多支分布范围内间歇性、反复性、阵发性剧烈疼痛,是最常见的神经性疼痛。多于50岁以后起病,以单侧Ⅱ、Ⅲ支为主,平均年发病率为4/10万[1]。分为原发性TN和继发性(症状性)TN,原发性TN的治疗经过40多年的发展,目前微血管减压术(microvascular decompression,MVD)已成为首选的治疗方法。本试验研究小脑水平裂(cerebellar horizontal fissure,CHF)、小脑桥脑裂(cerebello-pontine fissure,CPF)与三叉神经、小脑动脉、岩静脉(petrosal vein,PV)等之间的关系,为临床经枕下乙状窦后CHF-CPF入路MVD治疗TN提供解剖学基础。
1 材料与方法
1.1材料应用福尔马林固定后的正常成人头颅湿标本10个(男性8个、女性2个),共计20侧,用红色及蓝色乳胶灌注湿标本动、静脉系统,固定1周。
1.2方法在手术显微镜下模拟枕下乙状窦后CHF-CPF入路进行解剖:采用侧卧位,乳突后斜切口,开直径约3.0 cm的圆骨窗,于乙状窦和横窦交界处呈十字形切开硬膜,观察并测量未分开CHF-CPF时PV主干与REZ的关系及距离;分开CHF-CPF后再观察并测量PV主干与REZ的关系及距离;测量分开CHF-CPF前、后PV主干与三叉神经的关系及增加可操作手术野的距离。
1.3方法小脑组织的解剖暴露:沿眉弓上缘至枕外粗隆上1 cm水平锯开颅盖骨,小心去除硬脑膜,避免牵拉血管移位。自大脑脚水平切除大脑组织,保留小脑、脑干;打开小脑幕,观察PV主干及桥小脑角池蛛网膜;小心剥离蛛网膜,观察岩上窦、PV主干、属支与REZ的关系,显露REZ,显微镜下解剖研究CHF-CPF,再用圆规或游标卡尺辅助测量其与小脑动脉和PV及其属支的关系距离,及其与三叉神经的关系及距离。然后从前向后逐一切断脑神经和血管,在紧贴颞骨岩部尖端处切断三叉神经,在枕骨大孔处切断延髓和两侧椎动脉,取出脑干和小脑进行观察、测量、照相。
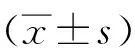
2 结果
2.1分离CHF-CPF对术野暴露的影响分离前CHF-CPF时手术暴露野最远点至乙状窦与横窦交界处硬膜的距离:左侧(3.62±1.47) mm,右侧(3.73±1.54) mm,均值(3.67±1.51) mm。分离后手术暴露野最远点至乙状窦与横窦交界处硬膜的距离:左侧(18.41±3.64) mm,右侧(18.63±3.95) mm,均值(18.52±3.80) mm,较分离前距离统计学具有差异性(P<0.01)(表1)。分离前REZ暴露困难,分离后REZ暴露良好。
2.2术野内组织结构暴露情况见表2。
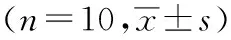
表1 小脑水平裂—小脑桥脑裂分离后手术野暴露最宽径数据测量比较 mm
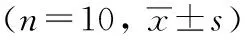
表2 小脑小平裂—桥脑裂与其周围结构关系的测量数据 mm
3 讨论
TN属于神经系统的一种功能性疾病,患者及家属对手术期望值高,因而如何提高手术疗效、降低手术后并发症一直是手术医师关注的焦点。众多文献表明[2-4],如PV处理不当,可能会出现严重后果,有学者对49家开展三叉神经痛MVD的医疗单位进行调查显示,其中有14家医疗单位发生过手术死亡,PV切断所致小脑和脑干坏死是最为常见的死亡原因[5]。有鉴于此,众多学者想了很多办法以保全PV,如在神经内镜辅助下微血管减压术[6-7]以及 Fujimaki 等[8]报道的经CHF入路,还有国内郑鲁教授等[9]提出经CHF-CPF联合入路治疗TN,可最大限度地保留PV及其属支,提高手术疗效、降低并发症。
3.1 CHF-CPF的解剖学特点CHF也称为岩裂,是小脑半球最大的水平裂隙,自后向前将小脑半球分为上下几乎相等的两部分,其前外侧端与CPF相接。CPF位于桥脑小脑角处,分为上肢和下肢,呈V型,顶点与CHF相接,两肢之间夹着小脑绒球,其上肢末段正对着REZ[10],本组观察小脑上动脉的皮层段横跨部分CHF,小脑前下动脉绒球小结段穿行于CPF上下唇。PV分支走行于桥脑裂表面。因小脑上动脉皮层段的原因,CHF分离受限。本组研究证实分开前均不能暴露REZ,分开此间隙后,即可暴露REZ,测量数据表明:分开前后增加的手术野最大宽径均值为(14.85±2.29) mm,总体平均暴露手术野最大宽径(18.52±3.80) mm,使分开该间隙前大部分看似阻挡手术入路的PV及小脑组织不再妨碍手术操作,使手术通道变得较大,能在该PV及其分支与其他结构的间隙内得以完成减压手术,而不需再切断PV。
3.2 CHF-CPF、REZ与PV三者之间的关系岩静脉是又称Dandy静脉,其解剖特点是:干短壁薄,呈游离悬空状跨越蛛网膜下脑间隙,在三叉神经外上方、内耳门上方走行,至近岩骨嵴处穿出蛛网膜注入岩上窦,PV大多干粗短,干短者管径较粗,干长者管径较细,作为MVD中的主要路障血管及责任血管之一,术者在牵拉小脑时一定要注意岩静脉这一解剖特征,需先探查PV,如较粗则不能过分牵拉,需电凝后切断以增加操作空间,避免出血,减少并发症,如较细则可考虑保留[11]。20侧岩静脉主干19支均位于三叉神经根背外侧面(86.4%),3支位于三叉神经根腹外方(13.6%),3支(13.6%)岩静脉主干及8支(15.7%)属支与三叉神经根接触,1支(4.6%)岩静脉主干及2支(3.9%)属支压迫神经根,与文献报道一致[12]。临床大量手术资料已明确PV的辨认与处理是MVD手术中的非常关键和有一定手术难度的一个步骤,对于术中是否保留或如何处理PV,特别是PV本身作为责任血管时则处理更加棘手[11]。本组研究测量:分离CHF-CPF后手术暴露野最远点至乙状窦与横窦交界处硬膜的距离(18.52±3.80) mm,CHF-CPF交界点与PV主干的距离(13.6±1.59) mm,未接触PV主干距REZ距离(5.64±1.68) mm,在分开CHF-CPF时增大了操作空间,容易发现责任血管,最大限度地保留PV,防止并发症,增加手术安全性。
3.3 CHF-CPF与REZ的关系三叉神经在桥脑上下缘的中间与脑干相连,小脑向前发出的唇样突起遮盖三叉神经后根与桥脑的连接处,其硬膜内部分从桥脑的外侧部发出后,斜向上行至岩尖。本组将CHF-CPF交界点作为一个测量点,是因其在CHF-CPF中相对恒定,是重要解剖标志。测量CHF-CPF交界点与REZ(19.42±4.57) mm,岩上窦与REZ的距离(12.39±4.81) mm,未接触PV主干距REZ距离(5.64±1.68) mm。本组实验证实在分开CHF-CPF后,其下方正对着REZ,对手术操作区暴露理想,不需牵拉PV,即可完成减压操作。
3.4 CHF-CPF与小脑动脉的关系三叉神经在桥小脑角区与小脑和脑干的血管关系密切,Rhoton称之为桥小脑角上神经血管复合体,其中是重要的血管是SCA[10],其皮层段横跨部分小脑水平裂,与REZ距离较近,常接触、压迫神经根。本组研究提示:与三叉神经最近的是SCA,本组20支SCA主干均起自基底动脉上段,45%(9/20)与REZ接触、10%(2/20)对REZ压迫;55%(11/20)未接触,其主干距REZ最近距离(4.62±1.68) mm,与CHF-CPF交界点最近距离(14.40±6.77) mm。正常生理情况下,因蛛网膜黏连,加之SCA内侧小脑中脑裂池的凸起处的视野阻挡,不容易被术者于直视下清楚观察。本研究提示:在分开CHF-CPF后,REZ暴露区增大,可直视下进行MVD,在彻底减压的同时不至于造成责任血管的遗漏或损伤,尤其有利于发现REZ腹侧的血管。AICA与REZ稍远,本组20%(4/20)与REZ接触、5%(1/20)对REZ压迫;75%(15/20)未接触,其主干距REZ最近距离(7.47±2.81) mm,与CHF-CPF交界点最近距离(19.67±7.40) mm,其与REZ关系不很密切,MVD手术时相对容易分离。PICA与CHF-CPF及REZ较远,MVD时注意分辨即可。
3.5经CHF-CPF入路手术中注意事项本研究提供了CHF、CPF自身解剖数据,同时测量其与三叉神经、PV及其分支、小脑动脉等重要解剖结构之间的距离,观测到PV的是MVD手术的主要路障血管,辨认与处理是非常关键的步骤,同时SCA是与REZ关系最密切的血管,也是主要的责任血管,在主干和分支结合处是最易发生神经压迫的部位。在整个MVD手术中需注意以下几方面:首先,在打开硬脑膜后,先辨认出小脑水平裂,因小脑上动脉皮层段分支横跨其上,在其边缘处开始打开小脑水平裂,尽可能不切断此分支,注意分离深度不要超过11.75 mm,以免损伤小脑组织,在分离长约30 mm左右时就接近水平裂及桥脑裂交界处了,这时注意调整方向,稍向枕骨大孔方向找到小脑桥脑裂,此时分离深度要变浅,约7.49 mm,以免损伤桥脑,再向前分离19.42 mm左右即到REZ。对于桥脑裂上下唇的PV分支,一如经翼点入路打开外侧裂的过程处理外侧裂静脉的原则和方法。其次,因桥小脑角区解剖结构复杂、空间狭小,重要神经、血管、小脑及脑干相毗邻,手术难度增大,因此要求术者掌握桥小脑角区解剖规律。本研究表明:PV距离小脑水平裂—桥脑裂最近,并与三叉神经根关系密切,因此对PV及其分支的处理一定要慎重,因考虑到面、听神经不宜过骚扰,以免出现听力下降甚至丧失以及面瘫等并发症,为了暴露REZ,必要时可切断细小分支,以达到手术目的。再次,本研究在模拟入路情况下,表明分开水平裂—桥脑裂后手术暴露野最远点至乙状窦与横窦交界处硬膜的距离为(18.52±3.80) mm,考虑到活体组织有弹性及脑脊液释放减压等情况,因此理论上均可达到手术野需要的暴露,个别情况下如仍不能满足,可试从小脑上及多角度探查,切忌向分开的水平裂两侧牵拉过度,以免损伤小脑深部组织。
参考文献:
[1] Yoshimasu F,Kurland LT,Elveback LR.Tic douloureux in Rochester,Minnesota, 1945~1969[J].Neurol,1972,22:952.
[2] Samii M,Gunther T,Laconetta G,et al.Microvascular decompression to treat hemifacial spasm:long term results for a consecutive series of 143 patients[J].Neurosurg,2002,50:712-719.
[3] Cruccu G,Gronseth G,Alksne J,et al.AAN-EFNS guidelines on trigeminal neuralgia managemen[J]. Eur J Neurol, 2008, 15:1013-1028.
[4] 赵卫国,濮春华,蔡瑜,等.1002例颅神经疾病微血管减压手术疗效和并发症分析[J]. 上海交通大学学报(医学版),2006, 26(7):778-780.
[5] 陈国强,李锐,郭京. 三叉神经痛微血管减压术导致患者死亡的手术并发症[J].立体定向和功能性神经外科杂志, 2004, 17(1):44-46.
[6] Charalampaki P,Kafadar AM,Grunert P,et al.Vascular decompression of trigeminal and facial nerves in the posterior fossa under endoscope-assisted keyhole conditions[J].Skull base, 2008, 18:117-128.
[7] Helbig GM,Callahan JD,Cohen GA.A Variant intraneural vein-trigeminal nerve relationships:an observation during microvascular decompression surgery for trigeminal neuralgia[J].Neurosurg, 2009, 65:958-961.
[8] Fujimaki T,Kirino T.Combined transhorizontal supracerebellar approach for microvascular decompression of trigeminal neuralgia [J].Br J Neurosurg, 2000, 14(6):531-534.
[9] 郑鲁,楚燕飞,姚智强,等.小脑水平裂—小脑桥脑裂入路治疗三叉神经痛[J].中华神经外科杂志, 2010, 26(7): 640-642.
[10] Roton著.刘庆良译.Rhoton颅脑解剖与手术入路[M].北京:中国科学技术出版社,2010:441, 447, 448, 454, 520, 521, 523.
[11] Mclaughlin MR,Jannetta PJ,Clyde BL,Subach BR,Comey CH,Resnick DK.Microvascular decompression of cranial nerves: lessons learned after 4400 operations[J].J Neurosurg,1999,90:1-8.
[12] 朱亚文,乔威.三叉神经根与周围血管关系及其临床意义[J].中国临床解剖学杂志,2006, 24(6):600-604.

