柠檬酸络合法制备质子化层状钙钛矿K0.5La0.5Bi2Ta2O9及其光解水制氢性能
陈 威 高寒阳 杨 俞 林培宾 袁 坚上官文峰,* 苏佳纯 孙洋洲
(1上海交通大学燃烧与环境技术中心,上海200240;2中海油新能源投资有限责任公司,北京100016)
柠檬酸络合法制备质子化层状钙钛矿K0.5La0.5Bi2Ta2O9及其光解水制氢性能
陈 威1高寒阳1杨 俞1林培宾1袁 坚1上官文峰1,*苏佳纯2孙洋洲2
(1上海交通大学燃烧与环境技术中心,上海200240;2中海油新能源投资有限责任公司,北京100016)
采用柠檬酸络合法制备铋层钙钛矿K0.5La0.5Bi2Ta2O9(KLBT),通过酸化处理得到质子化层状钙钛矿H1.9K0.3La0.5Bi0.1Ta2O7(HKLBT)光催化剂,并通过热重-差热(TG-DSC)、X射线衍射(XRD)、紫外-可见漫反射(DRS)、X射线光电子能谱(XPS)等技术对其进行了表征和分析.考察了前驱体KLBT的不同焙烧温度对HKLBT制氢活性的影响.结果表明,柠檬酸络合法能在较低温度下合成高结晶度纯相HKLBT,前驱体经900°C焙烧制备的HKLBT催化剂活性最高,在纯水中的产氢速率达236.6 μmol·h-1;长时间活性测试表明HKLBT具有完全分解水并同时产氢产氧能力,且具有较好的稳定性.
光催化;水分解;层状钙钛矿;酸化
1 引言
能源危机和环境恶化是制约未来社会和人类发展的重大问题,目前世界大多数国家都在开发清洁的可再生能源以应对此挑战.其中,光催化分解水制氢将太阳能直接转化为氢能,实现人工光合作用,为解决全球的能源问题提供了极好的技术途径.1-3近年来,Ta、Nb基的层状钙钛矿氧化物如H2La2/3Ta2O7、4K[Ca2Nan-3NbnO3n+1]、5KSr2TaNb2O10,6因其较高的导带电位和独特的层状结构(电子和空穴分别在不同层间富集从而达到分离的效果)在完全分解水方面表现出优异的性能.Kuroda等7报道了使用酸处理含有铋层结构的钙钛矿氧化物Bi2SrTa2O10,通过选择性的剥落铋可以形成质子化的层状钙钛矿氧化物H1.8[Sr0.8Bi0.2Ta2O7],并认为酸化处理可以应用到其他铋层氧化物,从而制备新型层状钙钛矿氧化物.这为新型光催化材料的设计和制备提供一个新的途径.
柠檬酸络合法(PC)是基于柠檬酸和乙二醇与金属离子的缩聚反应,从而在较低温度下合成具有高比表面积和高结晶度的材料,克服了传统固相法过高的反应温度造成比表面积过低的缺点.8目前PC法被广泛应用于光催化材料,尤其是固相法难以合成或需要较高温度过长反应时间的材料的合成制备.9本文使用柠檬酸络合法合成铋层钙钛矿氧化物K0.5La0.5Bi2Ta2O9,通过HCl酸化方法部分剥落铋形成质子化的新型层状钙钛矿氧化物H-K0.5La0.5Bi2Ta2O9用于光催化制氢.探讨了K0.5La0.5Bi2Ta2O9的不同合成温度对H-K0.5La0.5Bi2Ta2O9制氢活性的影响,分析了催化剂的活性位置,并结合X射线光电子能谱(XPS)考察了催化材料在反应过程中的稳定性.
2 实验部分
2.1 光催化材料的制备
所用试剂:TaCl5(美国Acros公司,99.9%); K2CO3、Bi(NO3)3·5H2O、La2O3、Bi2O3、Bi2O3、Ta2O5(99.99%)、甲醇、乙二醇均为国药集团化学试剂有限公司,分析纯,所有试剂未进行进一步纯化.
2.1.1 Bi层氧化物K0.5La0.5Bi2Ta2O9的制备
柠檬酸络合法制备铋层氧化物K0.5La0.5Bi2Ta2O9:10,11称取2.15 g TaCl5置于50 mL甲醇中,然后加入25 g一水合柠檬酸,溶解后依次加入0.124 g K2CO3, 0.555g La(NO3)3·nH2O,(3.02 g Bi(NO3)3·5H2O,完全溶解后加入30 mL乙二醇,在130°C油浴中搅拌均匀直至棕色凝胶生成,350°C焙烧1 h后结碳,置于Al2O3板650°C焙烧2 h除碳,转移至坩埚中800-1100°C焙烧6 h得到K0.5La0.5Bi2Ta2O9(记为KLBT).
固相法制备铋层氧化物K0.5La0.5Bi2Ta2O9:12取0.124 g K2CO3,0.244 g La2O3,1.40 g Bi2O3,1.33 g Ta2O5,混合研磨后900°C焙烧12 h,取出研磨,然后于1150°C焙烧2 h得到K0.5La0.5Bi2Ta2O9.
2.1.2 质子化H-K0.5La0.5Bi2Ta2O9的制备
取0.8 g K0.5La0.5Bi2Ta2O9加入到200 mL 3 mol· L-1HCl中静置72 h(每24 h更换一次新鲜盐酸溶液),过滤、洗涤、干燥后得到H-K0.5La0.5Bi2Ta2O9(记为HKLBT).
2.2 催化剂表征
XRD分析在日本理学Rigaku X射线粉末衍射仪(CuKα靶,λ=0.15406 nm,40 kV,20 mA)进行X射线粉末衍射表征.元素分析(ICP)由美国热电公司的ICAP6300定量分析.紫外-可见漫反射(DRS)分析在日本岛津公司UV-2450紫外-可见分光光度计上进行,热重-差热(TG-DSC)由德国NETZSCH公司STA449F3进行表征.采用美国Quanta Chrome公司NOVA1000进行BET测试.XPS在日本岛津-Kratos公司生产的Axis UltraDLD多功能光电子能谱仪上进行,Al靶,Kα(hν=1486.69 eV)射线,采用污染碳C 1s (Ea=284.6 eV)作能量校正.
2.3 光催化剂的活性评价
光解水产氢性能测试在自制的真空上照式石英玻璃反应器(350 mL)中进行.反应前将光催化剂样品及50 mL纯水加入到反应器中,然后将反应器抽成真空.反应中利用磁力搅拌使得光催化剂更好的分散,并用冷却水维持反应体系处于室温(20-25°C).光源采用北京畅拓科技有限公司250 W高压汞灯,生成的气体由气相色谱定量检出(华爱色谱9160,TCD检测器,5A分子筛填充柱,氩气为载气).
3 结果与讨论
3.1 TG和XRD结果分析
图1为KLBT凝胶经350°C焙烧1 h结碳后样品的热重-差热曲线.图中350-700°C之间出现明显的失重峰,DSC对应出现显著的放热,这归于前驱体表面积碳的燃烧.700°C以后样品不再失重,而750-900°C之间仍出现小的放热,这很可能是因为KLBT晶体开始形成,大于900°C的放热可归因于晶体的长大及结晶度的提高.图2为不同焙烧温度下KLBT的XRD衍射图谱.由图看出,当焙烧温度达到800°C,层状钙钛矿KLBT已经出现,随着焙烧温度的升高,KLBT的结晶度提高,颗粒增大,比表面降低(表1).当焙烧温度达到1100°C时,样品开始出现K2LaTa5O15,可见高温会导致KLBT的铋层的破坏,生成Bi2O3和K2LaTa5O15.较之固相烧结法制备的样品(图2f),柠檬酸法可以在远低于1150°C下获得纯相KLBT.图3为离子交换后H-KLBT的XRD图.酸化后样品由斜方晶系转变为四方晶系,前驱体KLBT的焙烧温度越高,对应的H-KLBT的结晶度越高.

图1 KLBT前驱体的TG-DSC曲线Fig.1 TG-DSC curves of KLBT precursor
3.2 质子化HKLBT组成分析
由于酸化处理会导致KLBT部分元素的脱除,因此酸化后有必要进行元素分析.ICP显示酸化后K:La:Bi:Ta(摩尔比)由原来的0.5:0.5:2:2变为0.30: 0.51:0.09:2,即一部分的K、Bi在酸化过程中剥脱掉,这是因为铋层被破坏,层状钙钛矿氧化物由双层变为单层.TG测试(图4)显示,HKLBT的脱氢温度约285°C,失重约2.8%.由于受热后氢是以脱水的方式脱除,以此计算可得完全脱出1.81个H,而根据ICP计算,酸化后的HKLBT中H的理论值为1.9,二者近似.酸化过程可以由方程(1)来描述:

图2 不同焙烧温度制备KLBT的XRD图谱Fig.2 XRD patterns of KLBT calcined at different temperaturesT/°C:(a)650,(b)800,(c)900,(d)1000,(e)1100;(f)solid state

表1 不同前驱体焙烧温度制备HKLBT的产氢活性Table 1 Photocatalytic activity for hydrogen on HKLBT precursor at different temperatures evolution

3.3 紫外-可见漫反射分析
图5为不同焙烧温度下制备的质子化HKLBT的紫外-可见漫反射光谱图.不同温度焙烧制得的HKLBT的吸收边均在315 nm附近,没有明显改变,仅800°C时有微弱的蓝移,推测是因为800°C制备的HKLBT颗粒较小,形成量子尺寸效应.13另外, XRD虽然显示1100°C焙烧及固相法制备的样品中有部分的K2LaTa5O15生成,但由于K2LaTa5O15的带隙与HKLBT近似,其吸收边也没明显改变.
3.4 不同前驱体焙烧温度对HKLBT制氢活性的影

图3 不同焙烧温度制备的KLBT酸化后得到HKLBT的XRD图谱Fig.3 XRD patterns of HKLBT from KLBT calcined at different temperaturesT/°C:(a)800,(b)900,(c)1000,(d)1100;(e)solid state
表1为不同焙烧温度制备的HKLBT在纯水中的产氢活性.当焙烧温度为900°C时产氢活性达到最大,为236.6 μmol·h-1,低于或高于此温度活性都会下降.一般来说,光催化材料的结晶度及比表面积是影响催化活性的关键因素.14当焙烧温度为800°C时,HKLBT虽有较大的比表面积(表1),但结晶度较低(图3).高的比表面积虽能提供较多的反应位,但低结晶度造成的缺陷往往成为光生载流子的复合中心,致使活性下降.而焙烧温度过高(超过1000°C)时,虽然材料具有高的结晶度,但比表面积过低,活性位不足.当焙烧温度为1100°C时,BET下降到仅有0.14 m2·g-1,产氢量下降为900°C时的1/2.另外,与固相法相比,由于柠檬酸法能在较低温度下(900°C)合成高结晶度的HKLBT,因此柠檬酸法制备的HKLBT显示出更好的活性.
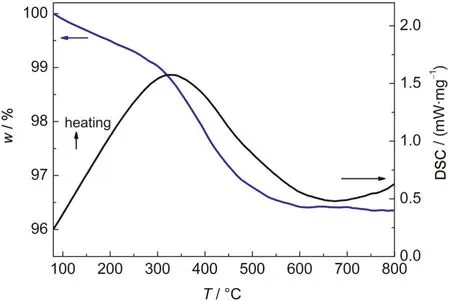
图4 HKLBT的TG-DSC图谱Fig.4 TG-DSC curves of HKLBT
3.5 层状化合物HKLBT活性位探究

图5 不同焙烧温度制备HKLBT的紫外-可见漫反射光谱图Fig.5 UV-Vis DRS of HKLBT calcined at different temperatures
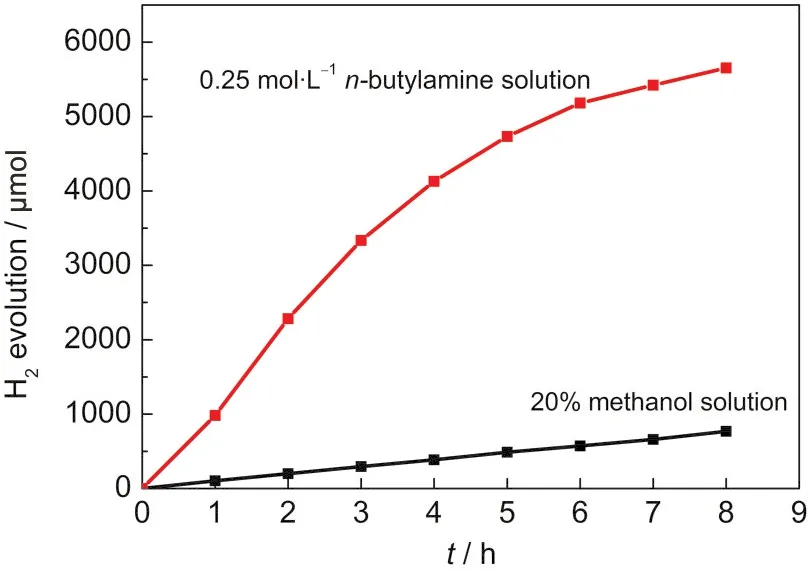
图6 不同牺牲试剂下HKLBT的产氢活性Fig.6 Photocatalytic activity of HKLBT for hydrogen in different sacrificial reagents0.1 g catalyst,50 mL solution,250 W high press mercury lamp, λ>200 nm
研究认为4,6某些层状化合物具有高活性的原因归于其电子和空穴分别在不同层间或层间和表面富集,从而达到分离的效果.为考察HKLBT反应位在层间还是表面,本研究选取丁胺和甲醇两种牺牲试剂进行产氢实验.图6为HKLBT在丁胺-水溶液和甲醇-水溶液中的制氢活性.测试表明HKBT在丁胺溶液中的制氢活性达到1010 μmol·h-1,为纯水的4.3倍,而在甲醇溶液中活性仅107 μmol·h-1,甚至低于纯水中的活性.一般认为15有机胺较强的亲水性容易进入层状化合物的层间,广泛用于层间修饰.因此,推测造成二者产氢活性的差异来自于是否能进入HKLBT的层间.将HKLBT置入丁胺-水和甲醇-水(50/50,体积比)溶液24 h后,XRD显示(图7)丁胺溶液浸泡后的HKLBT层间距由0.990 nm增加为1.115 nm,而甲醇溶液浸泡后的层间距没有改变.对应的TG(图8)测试也显示甲醇-水溶液浸泡后HKLBT的失重与原HKLBT相比几乎没有改变,而丁胺浸泡后的失重显著增加.这说明丁胺可以进入层间而甲醇不能,证实了层状HKLBT光催化反应可能主要在层间发生,这为下步对HKLBT进行修饰提供了指导.
3.6 HKLBT完全分解水测试及稳定性考察

图7 不同牺牲试剂浸泡24 h后HKLBT的XRD谱Fig.7 XRD patterns of HKLBT dipping in different sacrificial reagents for 24 h(a)without treatment,(b)methanol,(c)n-butylamine

图8 不同牺牲试剂浸泡24 h后HKLBT的TG曲线图Fig.8 TG curves of HKLBT dipping in different sacrificial reagents for 24 h
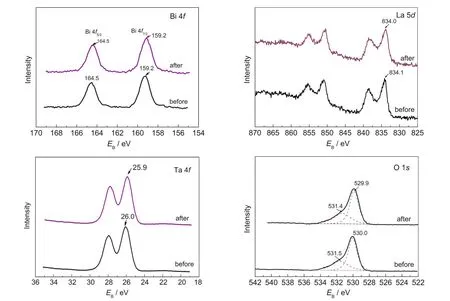
图10 连续光解水反应前后HKLBT的XPS图Fig.10 XPS of HKLBT before and after photocatalytic reaction of water
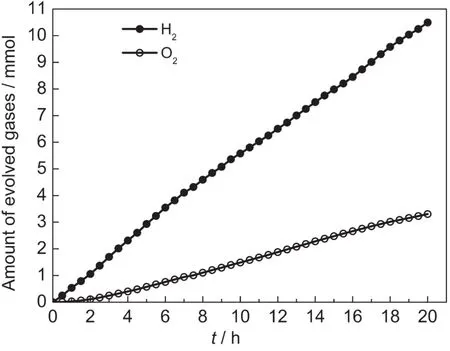
图9 HKLBT完全分解水连续测试Fig.9 Time course of overall water splitting on HKLBT0.2 g catalyst,50 mL pure water,250 W high press mercury lamp, λ>200 nm
为确定产氢反应为光催化反应而非光化学或光腐蚀反应以及考察HKLBT的稳定性,样品在纯水中20 h时的连续产氢如图9所示.在反应初期,仅有氢气产生而没有观察到氧气的生成,2 h以后氧气开始出现,并呈现增加的趋势,稳定时H2:O2(体积比,下同)约为2.9,高于2的理论值.光催化产氢反应中氢氧比偏离计量比甚至没有氧气生成在以前的研究中也有报道,16一方面是因为生成氧吸附在催化剂表面(尤其在反应初期),另一方面因为生成一分子氧气需要4个空穴,而氢气仅需要2个电子,相对于氢气来说氧的生成更困难.17,18也有报道认为生成的氧气会不可逆的生成或HO2·造成检测不到氧气或氢氧比偏离计量比.19,20然而,20 h连续反应产生了10.5 mmol H2及3.3 mmol O2,分别为催化剂量(约0.35 mmol)的30和9倍,因此可以证实产氢反应为光催化反应.为表征催化剂的稳定性,对反应前后的样品进行XPS测试如图10所示:Ta 4f轨道结合能为26.0 eV,与KTaO3中Ta(26.1 eV)近似,21Bi 4f轨道结合能分别为159.2 eV(Bi 4f2/7)及164.5 eV (Bi 4f2/5),与BiTaO4中Bi一致,22表示存在Bi-Ta键.而La 5d结合能为834.0 eV,与钙钛矿La0.3Sr0.7CoO3中 La 5d(834.0 eV)近似,23这说明质子化过程虽然出现部分元素的剥离,但仍为具有完整结构的钙钛矿HKLBT,这与XRD一致.对O 1s图谱进行解叠处理可以得到两个峰,晶格氧峰(530.0 eV)及吸附氧峰(531.5 eV),二者相差1.5 eV.一般认为,表面吸附氧中酸性羟基与碱性羟基的O 1s峰值比晶格氧的O 1s峰值要分别高约1.1和2.5 eV,24因此催化剂表面吸附氧主要为酸性羟基氧,这可能是因为氧吸附主要在层间,与质子形成酸性羟基氧.对比反应前后的XPS图谱,各元素的结合能改变在0.1 eV以内,说明反应过程催化剂各元素化学态稳定.
4 结论
采用柠檬酸络合法制备铋层钙钛矿K0.5La0.5Bi2Ta2O9,并通过酸化处理得到质子化层状钙钛矿H1.9K0.3La0.5Bi0.1Ta2O7光催化剂.较之固相烧结法,柠檬酸络合法能在较低的温度下合成高结晶度的HKLBT.当前驱体KLBT制备温度为900°C时,酸化后获得的HKLBT具有最高的光解纯水产氢活性.连续测试表明HKLBT具有完全分解纯水同时产氢产氧的能力,且具有较好的稳定性.
(1) Maeda,K.;Domen,K.J.Phys.Chem.C 2007,111,7851.doi: 10.1021/jp070911w
(2) Chen,X.;Shen,S.;Guo,L.;Mao,S.Chem.Rev.2010,110, 6503.doi:10.1021/cr1001645
(3) Li,Y.X.;Wang,J.X.;Peng,X.Q.;Lu,G.X.;Li,S.B.Int.J. Hydrog.Energy 2010,35,7116.doi:10.1016/j.ijhydene. 2010.02.017
(4) Shimizu,K.;Itoh,S.;Hatamachi,T.;Kodama,T.;Sato,M.; Toda,K.Chem.Mater.2005,17,5161.doi:10.1021/cm050982c
(5) Shangguan,W.;Yoshida,A.J.Mater.Sci.2001,36,4989.doi: 10.1023/A:1011877414129
(6)Huang,Y.;Li,Y.;Wei,Y.;Huang,M.;Wu,J.Sol.Energy Mater. Sol.Cells 2011,95,1019.doi:10.1016/j.solmat.2010.12.017
(7) Tsunoda,Y.;Shirata,M.;Sugimoto,W.;Liu,Z.;Erasaki,O.; Kuroda,K.Inorg.Chem.2001,40,5768.doi:10.1021/ ic010266m
(8)Yan,S.;Huang,Q.D.;Lin,J.D.;Yuan,Y.Z.;Liao,D.W.Acta Phys.-Chim.Sin.2011,27,2406. [闫 石,黄勤栋,林敬东,袁友珠,廖代伟.物理化学学报,2011,27,2406.]doi:10.3866/ PKU.WHXB20110929
(9)Yoshino,M.;Kakihana,M.Chem.Mater.2002,14,3369. doi:10.1021/cm0109037
(10)Kakihana,M.;Milanova,M.;Arima,M.;Okubo,T.;Yashima, M.;Yoshimura,M.J.Am.Ceram.Soc.1996,79,1673.doi: 10.1111/jace.1996.79.issue-6
(11) Maeda,K.;Terashima,H.;Kase,K.;Domen,K.Appl.Catal.A: Gen.2009,357,206.doi:10.1016/j.apcata.2009.01.024
(12) Karthika,C.;Ravishankara,N.;Maglioneb,M.;Vondermuhllb, R.;Etourneaub,J.;Varmaa,K.Solid State Communications 2006,139,268.doi:10.1016/j.ssc.2006.06.019
(13) Li,C.;Yuan,J.;Han,B.;Shangguan,W.Int.J.Hydrog.Energy 2011,36,4271.doi:10.1016/j.ijhydene.2011.01.022
(14) Kudo,A.;Miseki,Y.Chem.Soc.Rev.2009,38,253.doi: 10.1039/b800489g
(15) Tsunoda,Y.;Sugimoto,W.;Sugahara,Y.Chem.Mater.2003,15, 632.doi:10.1021/cm0200893
(16) Jiang,L.;Wang,Q.;Li,C.;Yan,J.;Shangguan,W.Int.J. Hydrog.Energy 2010,35,7043.doi:10.1016/j.ijhydene. 2009.12.187
(17) Betley,T.;Wu,Q.;Voorhis,T.;Nocera,D.G.Inorg.Chem. 2008,47,1849.doi:10.1021/ic701972n
(18) Kanan,M.;Nocera,D.Science 2008,32,1072.doi:10.3321/ j.issn:1006-9275.2008.07.010
(19) Kiwi,J.;Morrison,C.J.Phys.Chem.1984,88,6146.doi: 10.1021/j150669a018
(20) Kiwi,J.;Grätzel,M.J.Phys.Chem.1984,88,1302.doi: 10.1021/j150651a012
(21) McGuire,G.;Schweitzer,K.;Carlson,T.Inorg.Chem.1973, 12,2450.doi:10.1021/ic50128a045
(22) Shi,R.;Lin,J.;Wang,Y.;Xu,J.;Zhu,Y.J.Phys.Chem.C 2010, 114,6472.
(23) Galenda,A.;Maria,M.;Krishnan,V.;Bertagnolli,H.Chem. Mater.2007,19,2796.
(24)Chen,W.;Dong,X.F.;Chen,Z.S.;Chen,S.Z.;Lin,W.M. Acta Phys.-Chim.Sin.2009,25,1107.[陈 威,董新法,陈之善,陈胜洲,林维明.物理化学学报,2009,25,1107.]doi: 10.3866/PKU.WHXB20090624
July 6,2012;Revised:July 27,2012;Published on Web:August 1,2012.
Polymerizable Complex Synthesis of Protonated Form of Layered Perovskite K0.5La0.5Bi2Ta2O9for Water Splitting into Hydrogen
CHEN Wei1GAO Han-Yang1YANG Yu1LIN Pei-Bin1YUAN Jian1SHANGGUAN Wen-Feng1,*SU Jia-Chun2SUN Yang-Zhou2
(1Research Center for Combustion and Environmental Technology,Shanghai Jiao Tong University,Shanghai 200240,P.R.China;2CNOOC New Energy Investment Co.Ltd.Beijing 100016,P.R.China)
The protonated layered perovskite oxide H1.9K0.3La0.5Bi0.1Ta2O7(HKLBT)was prepared from K0.5La0.5Bi2Ta2O9(KLBT)by H ion-exchange,and subsequently characterized by thermogravimetric analysis (TG-DSC),X-ray diffraction(XRD),UV-Vis diffuse reflectance spectroscopy(DRS),and X-ray photoelectron spectroscopy(XPS).The effects of the calcining temperature on the materialʹs photocatalytic activity were also investigated.Results showed that HKLBT with high crystalline quality could be synthesized at low temperatures and that HKLBT prepared from KLBT calcined at 900°C exhibited the greatest photocatalytic activity,with an average water splitting hydrogen evolution rate of 236.6 μmol·h-1in pure water.The time course of water splitting indicated HKLBT has ability to split water into hydrogen and oxygen with long-term stability.
Photocatalysis;Water splitting;Layered perovskite;Acid treatment
10.3866/PKU.WHXB201208011
∗Corresponding author.Email:Shangguan@sjtu.edu.cn;Tel:+86-21-34206020.
The project was supported by the National Key Basic Research Program of China(973)(2009CN220000)and National Natural Science Foundation of China(20973110).
国家重点基础研究发展规划项目(973)(2009CN220000)及国家自然科学基金(20973110)资助
O643

