索拉非尼联合华蟾素片治疗中晚期原发性肝癌的临床疗效观察
冯丽华 陈毅德 郑志高 高应勤
厦门市第二医院肿瘤内科,福建 厦门 361000
原发性肝癌是临床上最常见的恶性肿瘤之一,全球发病率逐年增长[1],据统计我国肝癌发病人数占全球约55%[2],对人民健康构成了严重威胁。由于肝细胞癌起病隐匿,进展迅速,且常伴肝硬化,一旦发现多已为中晚期,大多数失去了手术机会。自然生存率不超过半年,5年生存率低于5%,目前尚无特别有效的治疗手段[3]。以细胞信号传导为理论基础的靶向治疗是近期研究热点,索拉非尼(sorafenib)是已被证实可延长晚期肝细胞癌患者总生存期的药物,中药华蟾素已应用于多种肿瘤的辅助治疗,鉴于以上因素及方便患者治疗,本研究观察口服索拉非尼联合华蟾素片治疗原发性中晚期肝癌的临床疗效、不良反应以及患者生活质量,现将结果报道如下。
1 资料与方法
1.1 一般资料
选择2009年1月—2012年7月经我院确诊为原发性肝癌中晚期的59例患者,符合“原发性肝癌诊断标准”[4]。治疗方案经过会诊,均为无手术及肝动脉化疗栓塞术(transcatheter arterial chemoembolization,TACE)指征或不愿接受手术及TACE治疗、手术后复发的晚期肝细胞癌,并取得患者及家属同意接受治疗和随访。Karnofsky评分60分以上,肝功能Child-Pugh分级为A至B级,预计生存期3个月以上,均有可测量病灶。将患者随机分为联合组(n=30)和对照组(n=29)。联合组男性25例,女性5例,平均年龄56.4岁;给予索拉非尼(德国拜耳公司生产)400 mg,每日2次,华蟾素片(安徽金蟾生化股份有限公司生产)4片,每日3次。对照组男性25例,女性4例,平均年龄55.8岁;给予单药索拉非尼400 mg,每日2次。每月为1个治疗周期,每2个周期行MRI等检查评价疗效。两组间性别、年龄、肿瘤大小及合并肝硬化、门脉癌栓、远处转移情况、Karnofsky评分、疼痛评分等一般资料经统计学处理,差异均无统计学意义(P>0.05),具有可比性。
1.2 观察指标
1.2.1 疗效评估标准
按照美国癌症研究所提出的实体瘤反应评价标准(RECIST)[5],将疗效分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD),以CR+PR+SD计算临床获益率(clinical benefit rate,CBR)。
1.2.2 不良反应评价
不良反应分级参照NCI-CTCAE National Cancer Institute-Common Terminology Criteria for Adverse Events 3.0版。
1.2.3 生活质量评价
参照Karnofsky评分标准,凡KPS计分提高≥10分为改善,下降≥10分为恶化,提高或下降在10分内为稳定[6]。
1.2.4 止痛疗效评价标准
疼痛强度采用数字评估法(number rating scales,NRS),0为无痛,1~3为轻度疼痛,4~6为中度疼痛,7~10为重度疼痛。止痛疗效评价标准:CR为治疗后 完全无痛;PR为疼痛较给药前明显减轻,睡眠基本不受干扰,能正常生活;轻度缓解(minimal remission,MR)为疼痛较给药前减轻,但仍感明显疼痛,睡眠仍受干扰;无效(no remission,NR)为与治疗前比较无疼痛减轻。以CR+PR计算疼痛缓解率 。
1.3 统计学处理
采用SPSS 17.0统计学软件进行数据分析,两组间率的比较采用χ2检验,P<0.05为差异有统计学意义。
2 结 果
2.1 两组临床疗效比较
联合组C B R(7 6.7%)明显高于对照组(51.7%),差异有统计学意义(P<0.05,表1)。

表1 两组临床疗效比较Tab.1 Comparison of CBR between treatment group and control group(n)
2.2 两组不良反应比较
两组主要不良反应均为手足皮肤反应(hand-foot skin reaction)、腹泻、高血压、骨髓移植和肝功能异常等,本研究中患者均未因不良反应而退出治疗。联合组较对照组腹泻发生率高,但差异无统计学意义(P>0.05),且两组腹泻多为1~2级,多在服用的前几周明显,且经过口服易蒙停、补充肠道有益菌群和黏膜保护剂等治疗后均可控制,且随着时间延长,多可耐受,未见其他明显的不良反应。联合组白细胞(white blood cell,WBC)、总胆红素(total bilirubin,TBIL)和谷丙转氨酶(alanine aminotransferase,ALT)指标较对照组有明显的改善,差异有统计学意义(P<0.05,表2)。
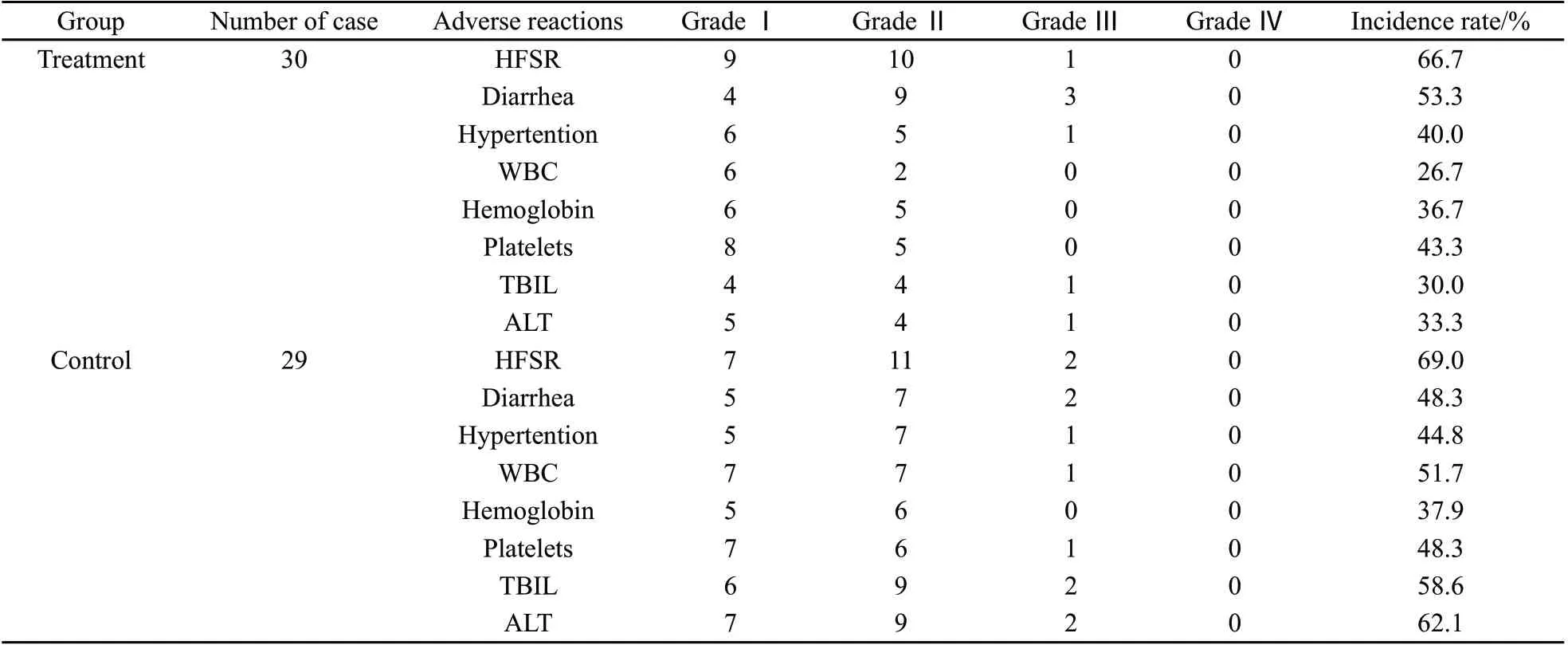
表2 两组不良反应比较Tab.2 Comparison of adverse reactions between treatment group and control group(n)
2.3 两组生活质量比较
联合组Karnofsky评分改善率(60.0%)明显优于对照组(31.0%),差异有统计学意义(P<0.05,表3)。
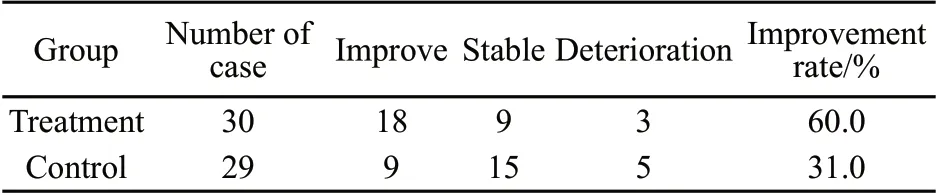
表3 两组生活质量情况比较Tab.3 Comparison of the life quality between treatment group and control group(n)
2.4 镇痛效果
联合组疼痛缓解率(73.3%)明显高于对照组(48.3%),差异有统计学意义(P<0.05,表4)。

表4 两组疼痛缓解率比较Tab.4 Comparison of cancer pain relief rate between treatment group and control group(n)
3 讨 论
索拉非尼是一种口服的多靶点的多激酶抑制剂,通过抑制多种酪氨酸激酶而起到阻断肿瘤细胞增殖和血管形成的作用[7]。国际多中心的两项Ⅲ期临床研究均显示,索拉非尼能有效地阻止肝癌患者病情恶化,显著延长晚期肝癌患者的生存时间[8-9]。采用中西医结合的方法治疗晚期恶性肿瘤是我国特有的方法之一,其中华蟾素目前已被临床广泛应用于晚期恶性肿瘤的治疗。陈华等[10]研究发现,华蟾素注射液对人肝癌HepG-2细胞增殖具有抑制作用。郑培实等[11]体外研究发现,索拉非尼联合华蟾素对离体肝癌细胞株SMMC-7721有协同抑制作用。
本研究结果显示,联合组CBR为76.7%,明显高于对照组,较苑珩珩等[12]研究中的CBR(63.3%)有所增加,同时联合组白细胞、肝功能和疼痛等情况明显改善,生活质量也明显提高。并且两药均为口服用药,简单、方便,患者依从性好,避免长时间住院点滴,减轻了患者及家属的经济负担。因此,索拉非尼联合华蟾素片可作为中晚期肝癌的一种较好的治疗选择。
[1]ALVESl R C, ALVES D, GUZ B, et al.Advanced hepatocellular carcinoma.Review of targeted molecular drugs[J].Ann Hepatol, 2011, 10(1): 21-27.
[2]PARKIN D M, BRAY F, FERLAY J, et al.Estimating the world cancer burden: globocan 2000[J].Int J Cancer, 2001, 94(2): 153-156.
[3]曹宇华, 罗和生.华蟾素治疗晚期肝癌的临床疗效研究[J].中国医学文摘, 2007, 16(1): 18-19.
[4]中国抗癌协会肝癌专业委员会.原发性肝癌诊断标准[J].中华肝脏病杂志, 2000, 8(3): 135.
[5]THERASSE P, ARBUCK S G, EISENHAUER E A, et al.New guidelines to evaluate the response to treatment in solid tumors[J].J Natl Cancer Inst, 2000, 92(3): 205-216.
[6]孙燕, 石远凯.临床肿瘤内科手册[M].5版.北京: 人民卫生出版社, 2010: 239-242.
[7]ZHU A X.Development of sorafenib and other molecularly targeted agents in hepatocellular carcinoma[J].Cancer, 2008, 112(2): 250-259.
[8]LLOVET J M, RICCI S, MAZZAFERRO V, et al.Sharp investigators study group sorafenib in advanced hepatocellular carcinoma[J].N Engl J Med, 2008, 359(7): 378-390.
[9]CHENG A L, KANG Y K, CHEN Z, et al.Efficacy and safety of sorafenib in patients in the Asia-Pacific region with advanced hepatocellular carcinoma: a phase Ⅲ randomized, double blind, placebo-controlled trial[J].Lancet Oncol, 2009, 10(1): 25-34.
[10]陈华, 孙宇, 崔晓楠.华蟾素注射液对人肝癌HepG-2细胞DNA拓扑异构酶Ⅰ的影响[J].中国癌症杂志, 2010, 20(3): 197-201.
[11]郑培实, 张阳, 蒋葵, 等.索拉非尼联合华蟾素对离体肝癌细胞株SMMC-7721的协同抑制效应观察[J].山东医药, 2011, 51(19): 69-70.
[12]苑珩珩, 白玉贤, 张婷婷, 等.以索拉非尼为基础治疗晚期肝细胞癌的疗效和不良反应临床观察[J].中国癌症杂志, 2012, 22(1): 52-55.

