离子液体-水混合介质中合成N、F共掺杂宽光域响应多孔TiO2光催化剂及性能
陈孝云 陆东芳 黄锦锋 卢燕凤 郑建强
(1福建农林大学材料工程学院,福州350002;2福建农林大学园林学院,福州350002)
离子液体-水混合介质中合成N、F共掺杂宽光域响应多孔TiO2光催化剂及性能
陈孝云1,*陆东芳2黄锦锋1卢燕凤1郑建强1
(1福建农林大学材料工程学院,福州350002;2福建农林大学园林学院,福州350002)
以TiCl4为钛源,离子液体-水为混合溶剂,采用液相水解-沉淀法制得浅黄色的N、F共掺杂宽光域响应多孔TiO2光催化剂(TiONF).以苯酚为模型物,考察了TiONF在紫外光区、可见光区及太阳光下催化活性.采用X射线光电子能谱(XPS)、紫外-可见漫反射光谱(DRS)、透射电镜(TEM)、X射线衍射(XRD)、傅里叶变换红外(FTIR)光谱及低温N2吸附-脱附等技术对TiONF的结构进行表征.结果表明,在离子液体-水混合介质中合成适量N、F共掺杂的TiO2在紫外光区、可见光区及太阳光下均表现出较高的活性,且高于纯水介质中合成TiONF的活性.离子液体-水混合介质有利于N、F进入TiO2晶格中;N、F共掺杂后在TiO2表面生成Ti―O―N键,形成新的能级结构,使催化剂的吸收红移至450-530 nm,诱发TiO2可见光催化活性;同时,N、F共掺杂提高了TiO2表面羟基数量;还提高了TiO2相转变温度,减缓了相转变速率.另外,在离子液体-水混合介质中合成的TiONF较纯水介质中合成的TiONF粒子小、分散性好、比表面积大.
TiO2;N-F共掺杂;离子液体;光催化剂;可见光
1 引言
近年来利用TiO2光催化氧化技术解决日益严重的水、空气、土壤等环境污染问题的研究发展非常迅速.1-5但从应用角度看,目前还存在不少问题,如光催化剂光谱响应范围在<380 nm时,对太阳能利用率低;6-9以电驱动的紫外光源其电-光转换效率低(<25%),大部分电能转化为热能转移出反应体系未被利用,反应系统总能量利用率低;10常规TiO2光催化剂的量子效率低等.11因此,研制太阳光响应光催化剂拓展其光谱响应范围(>380 nm),提高光催化量子效率成为世界范围的研究热点.12-14过渡金属离子掺杂、2贵金属沉积、4半导体复合、11染料敏化、12催化剂还原处理(TiOx)(x<2)13等方法均可不同程度地提高TiO2可见光催化活性.但催化剂的紫外光区活性、稳定性、光吸收效率、使用寿命等仍难以保证.8
非金属离子(N、S、C、F)掺杂对提高TiO2可见光响应能力具有较好的效果.6-9,14-19但目前研究主要是以水为溶剂,采用沉淀-溶胶法、液相水解法、水热法、喷溅热解法等19-22合成(N、S、C、F)掺杂TiO2可见光催化剂,而这些传统化学方法对其进行掺杂改性所制备的TiO2可见光催化剂效果还不甚理想.而关于在非水溶剂中或者含水较少的溶剂中合成(N、S、C、F)掺杂的报道还很少见到,近年来一些学者以绿色离子液体为溶剂合成纳米TiO2,展现出良好的效果,23-28因离子液体低的表面能可以使在其中的物质具有很好的稳定性,在离子液体中进行的反应相当于在纯的配体中进行,24,25离子液体不仅起到结构导向剂作用,还能够控制产物的形貌及影响产物的物相,26,28为介孔材料的合成提供了一个崭新的平台.
本文以TiCl4为钛源,在离子液体-水混合介质中合成N、F共掺杂宽光域响应TiO2光催化剂.采用XPS、DRS、TEM、XRD、FTIR及低温N2物理吸附-脱附等技术对催化剂的结构进行表征.系统研究了N、F共掺杂对TiO2微观结构及光催化活性的影响.
2 实验部分
2.1 离子液体的制备29
第一步,阳离子的合成:在250 mL的三口烧瓶中依次加入0.2 mol N-甲基咪唑(AR,阿拉丁), 0.24 mol溴代正丁烷(AR,阿拉丁),在磁力搅拌下, 70°C油浴中加热反应1 h后,得到白色粘稠液体[Bmim]Br,称为液体A.
第二步,阴离子交换:在第一步反应得到的液体A中加入0.2 mol六氟磷酸钾(AR,阿拉丁),加入100 mL水作为反应溶剂,在室温下磁力搅拌2 h,停止静置,液体分成两层,上层为水溶液,下层为无色透明溶液[Bmim]PF6.采用分液漏斗分离[Bmim]PF6与水,重复水洗操作至无Br-检出(往分离出来的水层溶液滴加0.1 mol·L-1的AgNO3无沉淀产生)为止.
2.2 光催化剂的制备
在恒温水浴(25°C)和强力搅拌的条件下,将10 mL的TiCl4(AR,阿拉丁)缓慢滴加到装有离子液体[Bmim]PF6和蒸馏水混合溶液的三口烧瓶中,以300 r·min-1的速率搅拌30 min后,升温至80°C并保持30 min,再以浓NH3·H2O(AR,阿拉丁)调节溶液pH=7,继续反应30 min.将固相产物于室温下陈化10 h,然后用蒸馏水洗涤,洗至无Cl-检出(滴加0.1 mol·L-1的AgNO3无白色沉淀产生),再用乙醇(AR,阿拉丁)洗2次,并转移到陶瓷坩埚,加入一定量的氟化铵(AF)(AR,阿拉丁)(控制n(Ti)/n(AF)=1:0.10, 1:0.25,1:0.50,1:0.75)和乙醇,并在搅拌下反应2 h,室温下陈化10 h,85°C真空干燥,研磨后移入坩埚反应器中,以10°C·min-1的升温速率升温至指定温度并恒温焙烧2 h,制得浅黄色的TiONF光催化剂.纯水介质中合成N、F共掺杂TiO2的方法同离子液体-水混合介质中合成N、F共掺杂TiO2(标记为TiONF-H),空白对照试样TiO2在相同条件下不加AF制得.对照试样P-25 TiO2催化剂为德国Degussa公司生产.
2.3 光催化剂的结构表征
利用美国物理电子公司生产的PHI5700型光电子能谱仪测试TiONF的表面组成、化学态及元素含量,X射线源采用Al Kα(hv=1486.6 eV)射线,采用污染碳C 1s(Ea=284.62 eV)作能量校正.利用紫外-可见漫反射光谱分析TiONF粉末的能阈结构以及对光的吸收性能,DRS的测试在装有积分球的TU-1901型紫外-可见分光光度计上进行,以BaSO4做参比.利用日本理学D/max-r B型X射线衍射仪分析TiONF粉体晶型结构,测定条件为室温Cu Kα射线,管电压45 kV,管电流40 mA;根据Scherrer公式计算晶粒平均尺寸.利用美国尼力高公司生产的Nicolet-380型傅里叶变换红外光谱仪研究TiONF界面变化情况,采用KBr压片法.利用荷兰飞利浦公司生产的TECANAI 10高分辨透射电子显微镜观察TiONF粒子形貌与大小,制样方法是将少量样品溶于乙醇,采用浸涂法将样品涂覆到碳膜铜网上.利用北京彼奥德公司生产的SSA4300孔隙及比表面积分析仪,以液氮为吸附介质,77.4 K时测试不同压力下的吸附体积,样品测试前200°C脱气2 h;按照BET方程计算TiONF催化剂比表面积;根据BJH公式计算孔径分布.以甲基红为指示剂,采用正丁胺滴定法测定TiONF真空干燥粉末的表面酸度.30
2.4 光催化剂的活性测试
光催化反应在自制石英/玻璃夹套式反应器(250 mL)中进行,31石英/玻璃管内置8 W低压汞灯(λML=365 nm)为紫外光光源或350 W球型氙灯(λML= 500 nm,以玻璃滤光管滤去λML<450 nm的光)为可见光光源,向反应器外层夹套通入冷却水以使反应温度维持在(25±1)°C,反应器外层以铝箔包覆,以避免其它光干扰.在光催化反应前避光磁力搅拌30 min,以使浓度为0.05 g·L-1的苯酚水溶液在催化剂表面达到吸附平衡,并以80 mL·min-1速率通入空气,起搅拌和补充溶解氧作用,催化剂用量为1.0 g· L-1.每20 min取样5 mL,离心分离,取上层清液以TU-1901型紫外-可见分光光度计于270 nm处测量吸光度,根据郎伯-比尔定律定量测得苯酚浓度.
太阳光活性测试:称0.1 g TiONF催化剂倒入直径为15 cm的平皿,加0.05 g·L-1的苯酚溶液100 mL,在磁力搅拌下吸附30 min,然后用保鲜膜封住平皿口,放在太阳光下照射.日期是2011年6月23日,时间为9:30-16:00,温度为27-36°C.
3 结果与讨论
3.1 光催化剂的XPS分析
图1为离子液体-水混合介质中合成的TiONF前驱体经600°C焙烧后的XPS谱.图中出现了Ti2p1/2、Ti 2p3/2、Ti 2s、Ti 3s、Ti 3p、O 1s、F 1s、C 1s和N 1s谱峰,其中C 1s为有机碳污染峰;981.3和1113.1 eV的峰分别为O和Ti的俄歇电子峰;从图1(c)TiONF和TiO2样品N 1s的高分辨率XPS谱中,可以看出TiONF样品在401.3 eV出现一个较宽且不对称的N 1s谱峰,说明样品中存在不同化学态的氮.按照结合能增加的顺序可依次解析出晶格氮(399.8 eV)和吸附N2(401.7 eV)两个峰,说明存在Ti―N结合键,N进入TiO2晶格中.Pelaez等17采用溶胶-凝胶法合成的N、F共掺杂TiO2,Ti―N结合能为399.5 eV;Li等32采用两步合成法制备的N、F共掺杂TiO2, Ti―N结合能为399.9-400.2 eV;Ling等33制备的B、N共掺杂TiO2,Ti―N结合能为399.5 eV.从图1(b) F 1s高分辨XPS谱可以看出,只有688.3 eV的峰,未出现685.5 eV F的吸附峰,20由此可见F通过化学键与TiO2相结合.从图1(d)TiONF和TiO2样品O 1s的高分辨率XPS谱可以看出,O 1s谱峰形状的不对称性,说明样品中存在不同化学态的氧.按照结合能增加的顺序可依次解析出晶格氧(529.8 eV)和羟基氧(531.1 eV)两个峰,按峰面积大小计算出晶格氧和羟基氧的比例,结果见表1,从表中可以看出,N、F共掺杂提高了TiO2表面羟基氧数量,TiO2晶格氧的比例降低.而表面羟基是光生空穴的捕获剂,捕获光生空穴后可生成活性物种·OH自由基,·OH在吸附相和溶液相中都易引发物质的氧化反应,从而提高光催化氧化效率.34,35从表2催化剂表面酸度测定结果可以看出,N、F共掺杂后TiO2粒子表面酸度有较大幅度的提高.苏雅玲等36认为是F掺杂促进TiO2粒子表面氧空穴的产生,致使TiO2粒子表面酸度与Ti3+增加,并认为TiO2粒子表面酸度与Ti3+增加有利于减少电子-空穴复合率,从而提高其光催化活性;黄冬根等20认为,F原子掺杂使TiO2的TiO6八面体结构发生变化,导致形成许多新的表面酸点,粒子的表面酸度增大.表3为TiONF光催化剂的XPS元素分析结果.从表中可以看出,各样品中Ti含量基本相同,随着N-F掺杂量的增加TiO2晶格的O含量明显减少;且晶格中N、F含量随焙烧温度的升高逐渐减少,当焙烧温度为900°C时就检测不到TiO2晶格中的N和F.对照纯水介质中合成的TiONF,发现在相同合成条件下,进入TiO2晶格中的N、F量明显少于离子液体-水混合介质中合成的TiO2晶格.其原因可能是离子液体在其中起到结构导向作用.
3.2 光催化剂的DRS分析

图1 离子液体-水混合介质中合成的TiONF(a)、F 1s(b)、N 1s(c)和O 1s(d)的XPS谱Fig.1 XPS spectra of(a)TiONF,(b)F 1s,(c)N 1s,and(d)O 1s synthesized in ionic liquid-water mixture solvent
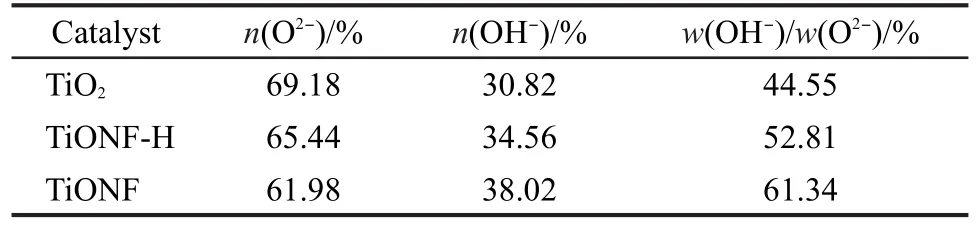
表1 TiO2、TiONF-H和TiONF光催化剂中羟基氧和晶格氧含量Table 1 Amount of OH-and O2-of TiO2, TiONF-H,and TiONF catalysts

表2 不同n(Ti):n(AF)的TiO2、TiONF-H和TiONF光催化剂表面酸点的量Table 2 Amount of surface acid sites of TiO2,TiONF-H, and TiONF catalysts with different n(Ti):n(AF)values
图2(a)为600°C焙烧制得不同N、F共掺杂量TiONF光催化剂的DRS谱.由图可以看出,随着N、 F掺杂量的增大TiO2在可见光区域(λ≥380 nm)的吸收增强,从而参与光催化反应的光子数量增加.由DRS曲线的拐点可以看出,TiONF光催化剂的吸收阈值发生明显改变.除了在约380 nm处出现锐钛矿相的特征吸收阈值外,在450-530 nm处因N、F掺杂而产生第二个拐点,且随N、F掺杂量的增大第二拐点光吸收阈值向长波移动量增加.第二拐点的出现表明TiO2中出现新的能级结构.即N、F离子掺杂导致TiO2晶格发生局部微变,形成一个禁带宽度较小的新能级,而新能级在λ≥380 nm的光照射下就能发生电子跃迁.Yu等16认为是TiO2中掺入F原子后,在光的照射下形成一个由Ti3+组成的浅势,使TiO2的带隙能变窄.对照纯水介质中合成的TiONF的DRS谱图,发现在离子液体-水混合介质合成的TiO2第一拐点光吸收阈值向短波移动.其原因可能是来自量子尺寸效应的影响,量子尺寸效应理论认为,半导体粒径越小,带隙越宽,吸收带边蓝移量越大,而XRD测试结果也证实了在离子液体-水混合介质中合成TiONF晶粒子尺寸比纯水介质中合成的TiONF晶粒子尺寸小.从DRS的一阶求导图(图2 (b))中可求出各条件下制备的TiONF光催化剂的吸收阈值,并以其为依据,根据带隙能公式Eg=1240/λ计算出的催化剂禁带宽度,37结果见表4.
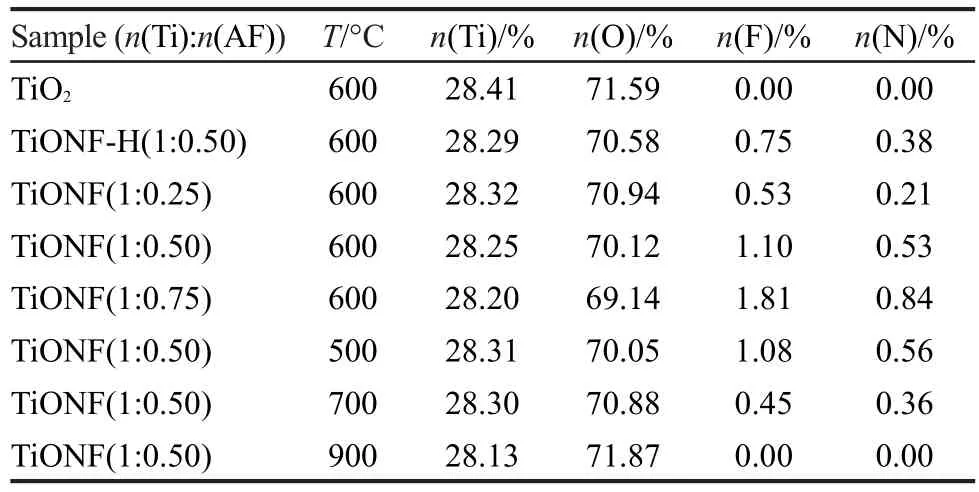
表3 不同n(Ti):n(AF)的TiO2、TiONF和TiONF-H光催化剂的XPS元素含量分析结果Table 3 XPS elements analysis result of TiO2,TiONF,and TiONF-H catalysts with different n(Ti):n(AF)values

图2 不同N、F共掺杂量TiONF光催化剂的(a)漫反射光谱和(b)漫反射光谱的一阶求导图Fig.2 (a)Diffuse reflectance spectra and(b)the first derivative of diffuse reflectance spectra of TiONFcatalysts with different N-F co-doping

表4 TiO2、TiONF-H和TiONF光催化剂的物理性质Table 4 Characteristics of TiO2,TiONF-H,and TiONF catalysts
图3为不同温度下焙烧制得TiONF光催化剂的DRS谱.从图可看出,当较低温度焙烧时,TiONF光催化剂的拐点跃迁阈值以及对可见光吸收和紫外光的吸收基本一致.当焙烧温度高于600°C时,随焙烧温度的升高,催化剂黄色逐渐减弱,对可见光区的吸收逐渐减弱;当焙烧温度达700°C时,TiONF光催化剂的第一拐点吸收阈值开始红移,当焙烧温度达900°C时样品为白色,此时对可见光已无吸收,其吸收阈值与金红石相TiO2基本相同.
3.3 光催化剂的FTIR分析
图4为600°C下制得TiONF光催化剂的FTIR分析结果.谱图中主要在3450、1630、1080和550 cm-1处出现四个吸收带.其中3450和1630 cm-1分别为表面吸附的水分子或TiO2催化剂表面O―H伸缩和弯曲振动峰,N、F共掺杂可引起吸附水或羟基的伸缩振动特征峰变宽,并随掺杂量的增加特征吸收峰加宽,可归因于掺杂N、F与H的相互作用所致.31这进一步证实了XPS分析结果,N、F共掺杂后TiO2表面羟基数量增多.550 cm-1为Ti―O伸缩振动峰, N、F共掺杂后Ti―O伸缩振动特征峰向低波数移动,同时在1080 cm-1出现Ti―O―N特征吸收峰,且随掺杂量的增加,吸收峰强度加强.Liu等31采用TiCl4水解法制备的N掺杂TiO2可见光催化剂Ti―O―N键的FTIR特征吸收峰出现在1059 cm-1.而本文与之相比Ti―O―N吸收峰向高波速偏移,其原因可能是受晶格中电负性较强的F的影响,使Ti―O―N键的特征吸收峰向高波速偏移.对照纯水介质中合成的TiONF,发现在纯水介质中合成的TiONF在1080 cm-1处Ti―O―N特征吸收峰明显弱于离子液体-水混合介质中合成的TiONF.这也进一步证实了XPS分析结果,离子液体的存在有利于N进入TiO2晶格中.
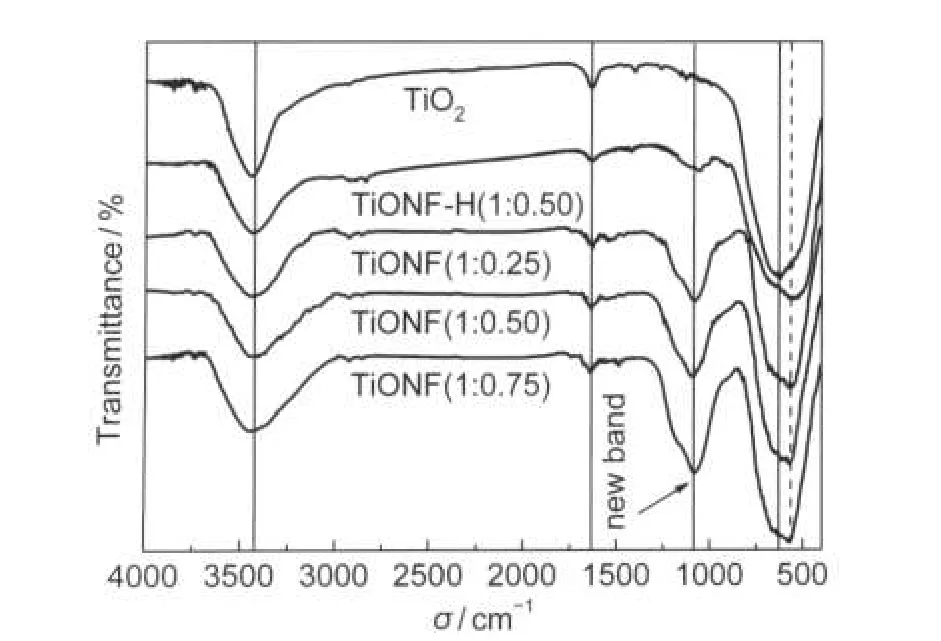
图4 TiO2、TiONF-H和TiONF光催化剂的FTIR谱Fig.4 FTIR spectra of TiO2,TiONF-H,and TiONF catalysts
3.4 光催化剂的XRD分析
图5为不同温度下制得TiONF和TiO2的XRD谱.可以看出,谱图中未出现因N、F共掺杂而引起锐钛矿或金红石相TiO2特征峰移动现象.TiONF前驱体为无定型结构,经400°C焙烧时就已基本转变为锐钛矿相;经600°C焙烧时,锐钛矿晶核生长趋于完善,具有较高的结晶度;800°C焙烧时开始有少量金红石相(6%)出现;900°C焙烧时为锐钛矿与金红石相(45%)的混晶结构.而相同条件下TiO2经800°C焙烧时金红石相约占26%,900°C焙烧时已基本转变为金红石相.比较图5(a)和5(b)可以发现, N、F共掺杂提高了锐钛矿相TiO2向金红石相转变的温度,减缓了相转变速率.这一结论与Yu等16和Li等21,22的结果一致.N、F共掺杂抑制TiO2金红石相生成的原因可能是:32N、F离子与Ti4+生成配位体,而这种配位体的存在能阻止锐钛矿相TiO6八面体的螺旋形链向金红石相TiO6八面体的直链转变,22故而抑制了金红石相的生成.
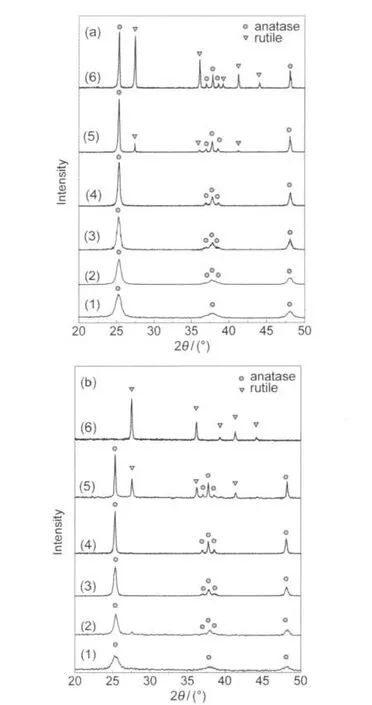
图5 不同温度下离子液体-水混合介质中制得TiONF(a)和TiO2(b)的XRD谱Fig.5 XRD patterns of TiONF(a)and TiO2(b) synthesized in ionic liquid-water mixture solvent at different temperaturesn(Ti):n(AF)=1:0.50;T/°C:(1)400,(2)500,(3)600, (4)700,(5)800,(6)900
3.5 光催化剂的BET及孔径分析
图6为TiO2、TiONF-H和TiONF光催化剂的N2吸附-脱附等温线和孔径分布.由图6(a)可知,三种样品都具有IV型吸附-脱附等温线和滞后环.在相对压力较低时,吸附量随着相对压力升高而逐渐增加,此时N2分子以单层或多层吸附在孔内表面;当N2相对压力为0.75-0.85时,吸附量产生突跃,这是由于N2在介孔孔道中发生毛细凝结所致,曲线中所形成滞后环证明催化剂存在介孔结构,主要是纳米粒子堆积而形成的间隙结构;当N2相对压力大于0.95时,吸附量基本不变,说明吸附已达到饱和.用BJH方法对吸附-脱附等温线进行计算,得到孔径分布曲线如图6(b)所示,由图可知TiONF样品孔径主要分布在2-10 nm间(最可几孔径在4.5 nm左右), TiO2样品孔径主要分布在1.5-7 nm之间(最可几孔径在3.5 nm左右),TiONF-H样品孔径主要分布在1.5-6 nm间(最可几孔径在3.0 nm左右).由BET计算结果见表4,TiONF催化剂的比表面积为172.3 m2·g-1,高于未掺N、F的TiO2催化剂的比表面积(138.4 m2·g-1),高于纯水中合成TiONF-H催化剂的比表面积(78.8 m2·g-1),高于纯水中合成TiO2催化剂的比表面积(43.8 m2·g-1).由此可见,在离子液体-水混合介质中合成的TiONF孔径、孔容积和比表面积明显增加,明显高于在纯水介质中合成的TiONF.另外,掺杂N、F后TiO2孔径、孔容积和比表面积明显增加,这可能与N、F的掺杂抑制TiO2晶体的生长有关.

图6 TiO2、TiONF和TiONF-H光催化剂的吸附等温线(a)及孔径分布图(b)Fig.6 Nitrogen adsorption isotherms(a)and pore size distribution curves(b)for TiO2,TiONF,and TiONF-H catalystsn(Ti):n(AF)=1:0.50
一般认为,TiO2的比表面积对其光催化活性影响较大,比表面积越大,表面活性中心及表面电荷传输速率随之增加,反应活性也随之提高.39介孔TiO2因其具有较高的比表面积和发达的孔道结构,且孔径尺寸在一定范围内可调,表面易于改性等特点,可以有效地增强TiO2的光催化活性,40将TiO2制成介孔结构有利于反应物和生成物扩散速度的提高,同时还可以利用介孔结构的吸附力场对目标污染物分子进行捕着,提高光催化降解效率.因此在离子液体-水混合介质中合成的N、F共掺杂TiO2可以提高TiO2的光催化效率.
3.6 光催化剂的TEM分析
图7为600°C下焙烧制得纯水介质中及离子液体-水混合介质中合成TiONF的TEM照片,从图中可以看出,纯水介质中制备的TiONF颗粒团聚较严重,颗粒较大(12-20 nm),但在离子液体-水混合介质中合成的TiONF光催化剂的粒子分散性较好,颗粒较小(7-8 nm).这与XRD的分析结果基本相符,而较小的粒度对光催化剂活性起到促进作用.
3.7 光催化剂的活性
从图8(a)、图9(a)催化剂的可见光活性测试结果可以看出,N、F共掺杂后TiO2的可见光催化活性显著提高,TiONF(n(Ti):n(AF)=1:0.5,600°C焙烧)活性最高,100 min内即可实现对苯酚完全去除,而未掺杂N、F的TiO2、P-25以及在纯水介质中合成的TiONF在120 min内对苯酚降解率只有21.7%、16.9%、95.5%.另外,结合DRS实验可知,第二吸收阈值向长波方向移动并不能保证催化剂的可见光活性增强,而是存在一个最佳值.其原因是,N、F共掺杂后新形成的能级与体相TiO2形成复合半导体结构,两者价带电势差可使TiO2价带光生空穴向新形成能级迁移,从而有效降低光生电子-空穴复合几率,进而提高催化剂活性;当N、F掺杂量增加时,新形成的能级向上移动,禁带宽度减小,从而使跃迁到导带上的电子容易与新能级上的空穴复合,即N、 F掺杂量过大时新形成能级成为电子-空穴的复合中心,从而使催化剂活性降低.37图8(b)、图9(b)催化剂紫外光活性测试结果表明,采用本方法制得的TiO2催化剂不仅在可见光区保持较高活性,其紫外光区活性亦高于P-25和未掺杂N、F的TiO2.从图10太阳光活性实验可以看出,N、F掺杂后TiO2光催化剂的活性显著提高,TiONF(n(Ti):n(AF)=1:0.5,600 °C焙烧)在测试时间内能实现对苯酚完全去除,而未掺杂N、F的TiO2及P-25对苯酚的去除率都在35%以下,在纯水介质中合成的TiONF对苯酚的去除率为81.8%.对照在纯水介质中合成的TiONF活性,发现离子液体-水混合介质中合成的TiONF在可见光区、紫外光区及太阳光下的活性都高于纯水介质中合成的TiONF.由此表明,采用本方法制备N、F掺杂TiO2,不仅有利于拓展TiO2光响应范围,同时也可有效提高催化剂紫外光区活性.

图7 TiONF-H和TiONF光催化剂的TEM图Fig.7 TEM images of(a)TiONF-H and(b) TiONF catalystsn(Ti):n(AF)=1:0.50

图8 不同N、F掺杂量TiONF的光催化活性Fig.8 Photocatalytic activity of TiONF with different N-F co-dopings(a)visible light;(b)UV light

图9 不同焙烧温度制得TiONF的光催化活性Fig.9 Photocatalytic activity of TiONF calcined at different temperatures n(Ti):n(AF)=1:0.50;(a)visible light,(b)UV light

图10 太阳光下TiONF的光催化活性Fig.10 Photocatalytic activity of TiONF under solar light(a)TiONF with different N-F co-dopings at 600°C;(b)TiONF calcinated at different temperatures with n(Ti):n(AF)=1:0.50
4 结论
以TiCl4为钛源,在离子液体-水混合介质中,采用液相水解-沉淀法制得N、F共掺杂宽光域响应多孔TiO2光催化剂.研究表明,在离子液体-水混合介质中合成适量N、F共掺杂的TiO2在紫外光区、可见光区及太阳光下均表现出较高的活性,且高于纯水介质中合成TiONF的活性.离子液体-水混合介质有利于N、F进入TiO2晶格中;N、F共掺杂在TiO2表面生成Ti―O―N键,形成新的能级结构,使催化剂的吸收红移至450-530 nm,诱发TiO2可见光催化活性;同时,N、F共掺杂提高了TiO2表面羟基数量;还提高了TiO2相转变温度,减缓了相转变速率.另外,在离子液体-水混合介质中合成的TiONF较纯水介质中合成的TiONF粒子小、分散性好、比表面积大.
(1) Yu,J.G.;Zhou,M.H.;Cheng,B.;Zhao,X.J.J.Mol.Catal. A-Chem.2006,246(1-2),176.
(2)Wawrzyniak,B.;Morawski,A.W.Appl.Catal.B-Environ. 2005,62(1-2),150.
(3) Liu,S.X.;Chen,X.Y.;Chen,X.Chin.Chem.Lett.2006,17 (4),529.
(4) Mori,K.;Maki,K.;Kawasaki,S.;Yuan,S.;Yamashita,H. Chem.Eng.Sci.2008,63,5066.
(5) Balek,V.;Li,D.;Šubrt,J.;Večernıková,E.;Hishitab,S.; Mitsuhashib,T.;Hanedab,H.J.Phys.Chem.Solid 2007,68 (5-6),770.
(6) Chen,Y.M.;Zhong,J.;Chen,F.;Zhang,J.L.Chin.J.Catal. 2010,31(1),120.[陈艳敏,钟 晶,陈 锋,张金龙.催化学报,2010,31(1),120.]
(7)Wu,Y.M.;Xing,M.Y.;Tian,B.Z.;Zhang,J.L.;Chen,F. Chem.Eng.J.2010,162,710.
(8) Chen.P.;Gu,M.Y.;Jin,Y.P.Progress in Chemistry 2005,17 (1),8.[程 萍,顾明元,金燕苹.化学进展,2005,17(1),8.]
(9)Tang,Y.C.;Huang,X.H.;Yu,H.Q.;Hu,C.Progress in Chemistry 2007,19(2-3),225.[唐玉朝,黄显怀,俞汉青,胡春.化学进展,2007,19(2-3),225.]
(10) Lu,W.S.;Xiao,G.S.;Li,D.Z.;Fu,X.Z.;Wang,X.X.Chin.J. Inorg.Chem.2005,21(10),1495.[鲁文升,肖光参,李旦振,付贤智,王绪绪.无机化学学报,2005,21(10),1495.]
(11) Ihara,T.;Miyoshi,M.;Iriyama,Y.;Matsumoto,O.;Sugihara,S. Appl.Catal.B 2003,42(4),403.
(12) OʹRegan,B.;Grätzel,M.Nature 1991,353(6346),737.
(13) Nakamura,I.;Negishi,N.;Kutsuns,S.;Ihara,T.;Sugihara,S.; Takeuchi,K.J.Mol.Catal.A-Chem.2000,161(1-2),205.
(14)Ashia,R.;Ohwaki,T.;Ohwak,K.;Aoki,K.;Taga,Y.Science 2001,293(5528),269.
(15) Hattori,A.;Tada,H.J.Sol-Gel.Sci.Technol.2001,22(1-2),47.
(16)Yu,J.C.;Yu,J.G.;Ho,W.K.;Jing,Z.T.;Zhang,L.Z.Chem. Mater.2002,14(9),3808.
(17) Pelaez,M.;Cruz,A.A.;Stathatos,E.;Falaras,P.;Dionysiou,D. Catal.Today 2009,144,19.
(18) Lee,S.H.;Yamasue,E.;Ishihara,K.N.;Okumura,H.Appl. Catal.B-Environ.2010,93(3-4),217.
(19) Li,X.H.;Liu,S.X.Acta Phys.-Chim.Sin.2008,24(11), 2019.[李晓辉,刘守新.物理化学学报,2008,24(11),2019.]
(20) Huang,D.G.;Liao,S.J.;Dang,Z.Acta Chim.Sin.2006,64 (17),1805.[黄冬根,廖世军,党 志.化学学报,2006,64 (17),1805.]
(21) Li,D.;Haneda,H.;Hishita,S.;Ohashi,N.;Labhsetwar,N.K. J.Fluorine Chem.2005,126(1),69.
(22) Li,D.;Haneda,H.;Labhsetwar,N.K.;Hishita,S.;Ohashi,N. Chem.Phys.Lett.2005,401(426),579.
(23)Yoo,K.S.;Choi,H.;Dionysiou,D.D.Catal.Commun.2005,6, 259.
(24) Liu,Y.;Li,J.;Wang,M.J.;Li,Z.Y.;Liu,H.T.;He,P.;Yang,X R.;Li,J.H.Crystal Growth&Design 2005,5(4),1643.
(25)Alammar,T.;Birkner,A.;Shekhah,O.;Mudring,A.V.Mater. Chem.Phys.2010,120,109.
(26) Liu,H.;Liang,Y.G.;Hu,H.J.;Wang,M.Y.Solid State Sci. 2009,11,1655.
(27) Yu,N.;Gong,L.;Song,H.J.;Liu,Y.;Yin,D.H.J.Solid State Chem.2007,180,799.
(28) Choi,E.H.;Hong,S.I.;Moon,D.J.Catal.Lett.2008,123 (1-2),84.
(29)Wang,Z.Z.;Zhu,G.M.;Chen,B.Q.Chem.Eng.2007,141(6), l4. [王振中,朱光明,陈北强.化学工程师,2007,141(6),l4.]
(30) Benesi,H.A.J.Phys.Chem.1957,61,970.
(31) Liu,S.X.;Chen,X.Y.;Chen,X.Chin.J.Catal.2006,27(8), 697. [刘守新,陈孝云,陈 曦.催化学报,2006,27(8),697.]
(32) Li,Y.X.;Jiang,Y.;Peng,S.Q.;Jiang,F.Y.J.Hazard.Mater. 2010,182,90.
(33) Ling,Q.C.;Sun,J.Z.;Zhou,Q.Y.Appl.Surf.Sci.2008,254, 3236.
(34)Fox,M.A.;Dulay,M.T.Chem.Rev.1993,93,341.
(35)Hoffmann,M.R.;Martin,S.T.;Choi,W.Y.;Bahnemann,D.W. Chem.Rev.1995,95,693.
(36) Su,Y.L.;Li,Y.;Du,Y.X.;Lei,L.C.Acta Phys.-Chim.Sin. 2011,27(4),939.[苏雅玲,李 轶,杜瑛珣,雷乐成.物理化学学报,2011,27(4),939.]
(37) Chen,X.Y.;Liu,S.X.Acta Phys.-Chim.Sin.2007,23(5), 701. [陈孝云,刘守新.物理化学学报,2007,23(5),701.]
(38) Jiang,H.F.;Zhou,Z.X.;Liu,X.Q.;Meng,G.Y.Photographic. Sci.Photochem.2007,25(3),223.[江宏富,周作兴,刘杏芹,孟广耀.感光科学与光化学,2007,25(3),223.]
(39) Zhang,Z.;Wang,C.;Rama,Z.J.Phys.Chem.B 1998,102(52), 10871.
(40) He,X.;David,A.Angew.Chem.Int.Edit.2002,41,214.
August 16,2011;Revised:October 10,2011;Published on Web:October 25,2011.
Preparation and Properties of N-F Co-Doped TiO2Photocatalyst with Wide Range Light Response and Multipore Structure from Ionic Liquid-Water Mixture Solvent
CHEN Xiao-Yun1,*LU Dong-Fang2HUANG Jin-Feng1LU Yan-Feng1ZHENG Jian-Qiang1
(1College of Material Engineering,Fujian Agriculture and Forestry University,Fuzhou 350002,P.R.China;2College of Landscape Architecture,Fujian Agriculture and Forestry University,Fuzhou 350002,P.R.China)
A yellow N-F co-doped TiO2photocatalyst(TiONF)exhibited high activity over a wide light spectrum range and a multipore structure was prepared by a hydrolysis-precipitation method using an ionic liquid([Bmim]PF6)-water mixture as the solvent and TiCl4as the precursor.Photocatalytic activity was investigated by the photocatalytic degradation of phenol under ultraviolet(UV),artificial visible(Vis),and solar light irradiation.X-ray photoelectron spectroscopy(XPS),UV-Vis diffuse reflectance spectroscopy (DRS),transmission electron microscopy(TEM),X-ray diffraction(XRD),Fourier transform infrared(FTIR), spectroscopy,and N2adsorption-desorption were used for catalyst characterization.The results show that TiONF synthesis in an ionic liquid-water mixture solvent with suitable N-F doping gives high activity under UV,Vis,and solar light irradiation,and the activities are higher than those obtained by synthesis in pure water.The ionic liquid-water mixture solvent leads to N and F being incorporated into the TiO2lattice and N-F co-doping can increase the amount of surface OH-on TiO2.The new bandgap formed by N-F doping can induce a second adsorption edge(450-530 nm),which can be excited by Vis irradiation and induce Vis activity.N-F co-doping retards the phase transformation.In addition,an ionic liquid-water mixture as a solvent benefits the dispersion of TiO2,increases the SBETand reduces the particle size.
TiO2;N-F co-doping;Ionic liquid;Photocatalyst;Visible light
10.3866/PKU.WHXB201228161www.whxb.pku.edu.cn
*Corresponding author.Email:chenxy_dicp@126.com;Tel:+86-13178389782.
The project was supported by the National Natural Science Foundation of China(31000269),Talent Training Program for Distinguished Young Scholars in Universities of Fujian Province,China(JA11072)and Education Department Foundation of Fujian Province,China(JA10121).
国家自然科学基金(31000269),福建省高等学校杰出青年科研人才培育计划(JA11072)和福建省教育厅基金(JA10121)资助项目
O643

