石墨烯掺杂LiFePO4电极材料的合成及其电化学性能
徐 科 申来法 米常焕 张校刚
(南京航空航天大学材料科学与技术学院,南京210016)
石墨烯掺杂LiFePO4电极材料的合成及其电化学性能
徐 科 申来法 米常焕 张校刚*
(南京航空航天大学材料科学与技术学院,南京210016)
采用水热辅助法合成石墨烯改性的LiFePO4多孔微球电极材料.并对材料进行了X射线衍射(XRD),扫描电子显微镜(SEM),透射电子显微镜(TEM),傅里叶变换红外(FT-IR)光谱,充放电等表征.从结果可以看出在2 mol·L-1LiNO3电解液体系中单纯包碳的LiFePO4微球在1C、50C倍率时的比容量分别为137、64 mAh·g-1,而石墨烯改性的LiFePO4微球的比容量分别为141、105 mAh·g-1,表现出较好的倍率特性.恒流循环充放电测试60次后两种材料容量保持率分别为70.2%、83.7%.说明掺杂石墨烯构成的三维导电网络能明显改善LiFePO4的电化学性能.
LiFePO4;石墨烯;水热法;锂离子电池
1 引言
能源是人类社会发展与稳定的重要支柱,现在随着化石燃料的消耗,能源危机也不断加剧,同时新能源的开发与利用也越来越迫切.电池作为一种储能设备在新能源的转换和利用中发挥了不可替代的作用.其中锂离子电池性能优越,具有较高的能量密度,循环寿命长,而且无污染,成为研究的热点.1990年,Sony公司制备了LiCoO2为正极材料,石墨为负极材料的二次电池,锂离子电池不断发展壮大,应用领域越来越广泛.科研人员不断研究探索更好的锂离子电池电极材料,以达到其在多领域的要求.正极材料中有层状过渡金属氧化物(LiCoO2, LiNiO2),尖晶石结构的LiMn2O4,以及橄榄石型聚阴离子化合物(LiFePO4,LiMnPO4,LiCoPO4)等.
LiFePO4作为聚阴离子型锂离子电池正极材料,具有绿色环保、安全性能好、成本低等优点.自从1997年Goodenough等1,2发现以来,备受关注.然而LiFePO4自身较差的离子导电性和电子导电性,一直制约其广泛的应用.目前提高其导电性的方法主要有包覆高导电性材料,3-8掺杂金属离子,9以及颗粒纳米化10-12等.Kostecki等13发现,磷酸亚铁锂的电子电导率随包覆碳sp2/sp3成键比的增加而增加. Xia等14,15率先研究了水系电解液中LiFePO4的电化学性能并系统解释了其反应机理,而且将包碳的LiFePO4应用于水系电解质中,有效地缓解了其循环过程中容量损失.16Zhang等17用导电性良好的聚吡咯(PPy)合成了LiFePO4-PPy复合物,有效地改善其在水系环境中的倍率特性.近年来发现的石墨烯片层中碳原子均为sp2杂化,有较高的导电性,相较于其他的炭材料(如CNT,碳纤维)二维(2D)片层结构的石墨烯可以比较容易实现对电极材料的包覆,形成性能良好的导电层.因而被广泛应用于碳基复合电极材料.Su等18用石墨烯为导电剂与LiFePO4进行物理混合发现其倍率特性有了明显提高.证明石墨烯的片层结构比较容易形成性能良好的导电层.
本实验以CH3COOLi·2H2O,Fe(NO)3·9H2O和NH4H2PO4为原料,柠檬酸为螯合剂同时又作为还原剂,采用水热辅助法合成了多孔LiFePO4纳米微球结构.我们在此基础上掺杂了导电性良好的石墨烯材料.成功制备了石墨烯掺杂的LiFePO4纳米微球.并分别对其在水系电解液中的电化学性能进行了测试.
2 实验
2.1 原料和试剂
CH3COOLi·2H2O,分析纯,广东省化学试剂工程技术研究开发中心;Fe(NO)3·9H2O、K2S2O8,、KMnO4均为分析纯,石墨粉为光谱纯,中国医药(集团)上海化学试剂公司;NH4H2PO4,≥99.0%,成都科龙化工试剂厂;P2O5、C6H8O7·H2O,分析纯,上海久亿化学试剂有限公司;H2SO4,95.0%-98.0%,南京化工试剂有限公司;H2O2,30%,上海中试化工公司.
2.2 水热辅助合成石墨烯掺杂LiFePO4
将CH3COOLi·2H2O、Fe(NO3)3·6H2O、NH4H2PO4C6H8O7·H2O(摩尔比为1.03:1:1:1)加入70 mL蒸馏水中,磁力搅拌直至形成透明溶液.将所得溶液转入聚四氟乙烯内衬的高压反应釜中,180°C反应8 h后自然冷却.在80°C下将水分蒸干,得到浅绿色固体.将其与葡萄糖在玛瑙研钵中研磨混合,在N2气氛保护下700°C煅烧10 h制得样品,标记为LFP/C.
氧化石墨(GO)采用石墨粉为原材料,通过Hummers化学氧化法19制得.称取一定质量的氧化石墨(m(GO)/m(LiFePO4)=0.15),超声分散在70 mL蒸馏水中,再按上述方法依次加入其它原料经水热还原,晶化后所得产物标为LFP/C-G.
2.3 样品表征
XRD采用德国Bruker D8 advance-X射线衍射仪,CuKα靶,管电压为40 kV,管电流40 mA,扫描速率为10(°)·min-1,2θ角范围为10°-90°.SEM测试采用德国Leo 1430 VP扫描电子显微镜,发射电压设置为20 kV.TEM测试采用美国FEI公司TECNAI-20型透射电子显微镜.FT-IR仪器采用360 Nicolet AVATAR傅立叶变换红外光谱仪,KBr压片(样品中的活性物质:KBr的质量比例为100:1),扫描波数范围为400-4000 cm-1.分辨率为4 cm-1.拉曼测试采用Jobin Yvon.Co.LabRom-1B型拉曼光谱仪.
电化学性能测试采用CHI660B型电化学工作站,将活性材料粉末、乙炔黑和聚四氟乙烯(PTFE)按质量比80:10:10的比例混合均匀,然后涂抹在泡沫镍片上,60°C烘干后用压片机在10 MPa左右压成薄片,制成工作电极浸入2 mol·L-1LiNO3溶液的三电极体系中,饱和甘汞电极为参比电极,Pt电极为辅助电极.电池体系的恒流充放电区间为-0.4-0.6 V.循环伏安及交流阻抗测试在相同电化学体系中,且所有的电化学测试都在室温((25±1)°C)下进行.
3 结果与讨论
3.1 XRD物相分析
图1为LFP/C和LFP/C-G的XRD图谱及LiFePO4标准图谱,从图1中可以看出,LFP/C和LFP/C-G与标准图谱的(PDF 83-2092)卡片晶体结构相符,没有FeP2、氧化铁、磷酸锂等杂峰出现,说明样品LFP/C和LFP/C-G均为橄榄石型LiFePO4结构.20且在LFP/ C-G样品的XRD谱图中,11°左右未发现GO的特征峰,19说明GO已被还原.

图1 LFP/C与LFP/C-G的XRD图Fig.1 XRD patterns of LFP/C and LFP/C-GLFP/C:carbon coated LiFePO4;LFP/C-G:graphene modified LiFePO4
3.2 形貌分析
图2为LFP/C和LFP/C-G的SEM及TEM照片.从图中可以看出两样品为均匀的多孔微球结构,微球直径约为2-3 μm.从图2(b)可以看出LFP/C-G样品的LiFePO4微球表面被石墨烯片层结构覆盖.由于石墨烯片大小不均匀,较小的片层紧贴在微球的表面,而较大的石墨烯片可将微球包裹.图2(c-e)为LFP/C-G的TEM图,图2(c)中可以观察到包裹在微球表面的石墨烯(如箭头所示),图2(d)所示LiFePO4微球由直径为50 nm左右的小颗粒团聚而成,在微球中形成明显的孔道结构.图2(e)图为微球上单个颗粒放大图,其表面包覆的石墨化碳层为5-10 nm左右(如图中箭头所示).内部晶格间距约为0.31 nm,对应LiFePO4晶体结构中的(020)晶面.纳米尺度的LiFePO4可以有效减少锂离子在其中的扩散路径,提高锂离子的传输效率.纳米颗粒聚集形成的孔道又可以使电解液更容易进入内部,21与活性物质良好地接触,有利于离子及电子的交换.而石墨化碳均匀地填充在小颗粒聚集形成的孔道中,将石墨烯(图2(c)中箭头所示为石墨烯)与LiFePO4紧密结合.内层导电石墨化碳与外层石墨烯紧密接触,使不同石墨结构的碳结合形成具有三维空间结构的导电网络,从而有效提高电子的传输速率.
3.3 FT-IR光谱分析

图2 LFP/C(a)与LFP/C-G(b)的SEM图及LFP/C-G的TEM图(c-e)Fig.2 SEM images of LFP/C(a)and LFP/C-G(b),TEM images of LFP/C-G(c-e)
图3为GO和LFP/C-G的红外图谱,从GO的红外图谱可以看出上面含有丰富的羟基,羧基等官能团,与文献报道相符.19,22其中3617、3418及3166 cm-1处为羟基的三个振动峰,分别对应GO的羟基基团、夹层中H2O及内部的-COH基团.1630 cm-1处水的摇摆振动峰及1402 cm-1处-COH面内摇摆振动峰可进一步确认上述官能团的存在.1732和1120 cm-1分别对应GO中C=O的伸缩振动峰及C-O的伸缩振动峰.LFP/C-G的红外图谱可以看出LiFePO4明显的特征峰,1139、1096和1057 cm-1处的吸收峰对应于PO3-4四面体不对称伸缩振动.971 cm-1处的吸收峰对应于P-O对称伸缩振动,636和468 cm-1处的吸收峰对应于P-O不对称弯曲振动. 501、551、578和647 cm-1的吸收峰对应于P-O对称振动和不对称弯曲振动.23同时可以看出3617、3166 cm-1振动峰消失,且3418 cm-1峰强明显减小,说明GO中的羟基消失,GO被还原.1732和1120 cm-1的C=O、C-O振动峰也消失,结合XRD图谱可以说明GO已经被完全还原.

图3 GO和LFP/C-G的FT-IR谱图Fig.3 FT-IR spectra of GO and LFP/C-G
3.4 拉曼图谱
LFP/C、LFP/C-G的拉曼光谱如图4所示.图中两者在1351和1582 cm-1处都有拉曼峰.1351 cm-1对应碳的sp2拉曼峰,1582 cm-1对应碳的sp3结构拉曼峰.24,25947、1048 cm-1为PO3-4的伸缩振动峰.23LFP/ C-G峰强减小是由于石墨烯的加入所构成的三维网状碳结构能更好地包覆LiFePO4,因此使其裸露部分减少.从图4中可以看出LFP/C-G样品D峰、G峰的峰宽及半峰宽比LFP/C的都要大.说明加入石墨烯使碳层的石墨化程度明显提高.
3.5 电化学性能测试

图4 LFP/C和LFP/C-G的拉曼谱图Fig.4 Raman spectra of LFP/C and LFP/C-G
图5为LFP/C和LFP/C-G在2 mol·L-1LiNO3体系中的循环伏安图谱,扫描速率为2 mV·s-1,扫描电压范围-0.4-0.8 V(vsSCE).在此电压范围中可以看到有一对明显的氧化还原峰,分别对应锂离子的嵌入和脱出.图中LFP/C-G样品的峰电流相对LFP/ C样品的峰电流有了明显增强,LFP/C-G样品的氧化还原峰的积分面积大于LFP/C样品的积分面积,说明LFP/C-G样品比LFP/C样品在此体系下的电化学活性更高.氧化还原峰的峰间距变小说明石墨烯的加入使电极的可逆性增加.图6为LFP/C与LFP/ C-G在相同电极体系下的放电曲线.从图6中可以看出掺杂石墨烯的LiFePO4样品比包碳的LiFePO4样品倍率特性有明显的提高.在2 mol·L-1LiNO3溶液中LFP/C与LFP/C-G样品在1C下的放电平台大约在0.2 V左右,这与循环伏安图谱相符,比容量分别为137、141 mAh·g-1,在大电流密度50C的条件下其放电容量为64、105 mAh·g-1.大电流密度的容量保持率分别为46.7%、74.5%.
在较小的电流密度下由于电压降缓慢,离子及电子容易进入电极材料的细小孔道等细微结构中发生反应.26在大电流密度下电化学反应较快,在材料的部分区域不能及时进行电子、离子交换,引起容量的损失.这需要给电子、离子交换提供更好的通道.在本实验中,掺杂石墨烯包碳后的LFP/C-G样品比包碳的LFP/C样品大电流容量保持率有了明显提高.首先在LFP/C-G样品外层包覆的石墨烯增加了电极材料的表面积,使材料与电解液可以更好地接触.同时包覆在LiFePO4外层的石墨烯中碳原子为sp2杂化结构,相比石墨化碳具有良好的电子导电性.石墨烯与LiFePO4颗粒表面的石墨化碳紧密结合形成性能良好的导电网络更有利于电子传输(如图7所示).进一步证实电极材料表面的微观结构可以有效改善材料的电化学活性及在高电压下的热力学性能.27最后在水热反应中,石墨烯片将LiFePO4前驱体包覆,减少了高温反应中微球之间的团聚,有利于孔道的保持,三维自组装形成的多级孔道结构便于离子的交换有效增强其电化学性能.28
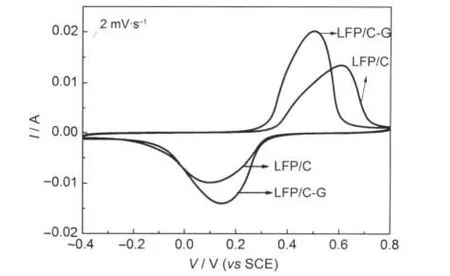
图5 LFP/C和LFP/C-G的循环伏安图Fig.5 Cyclic voltammograms of LFP/C and LFP/C-G
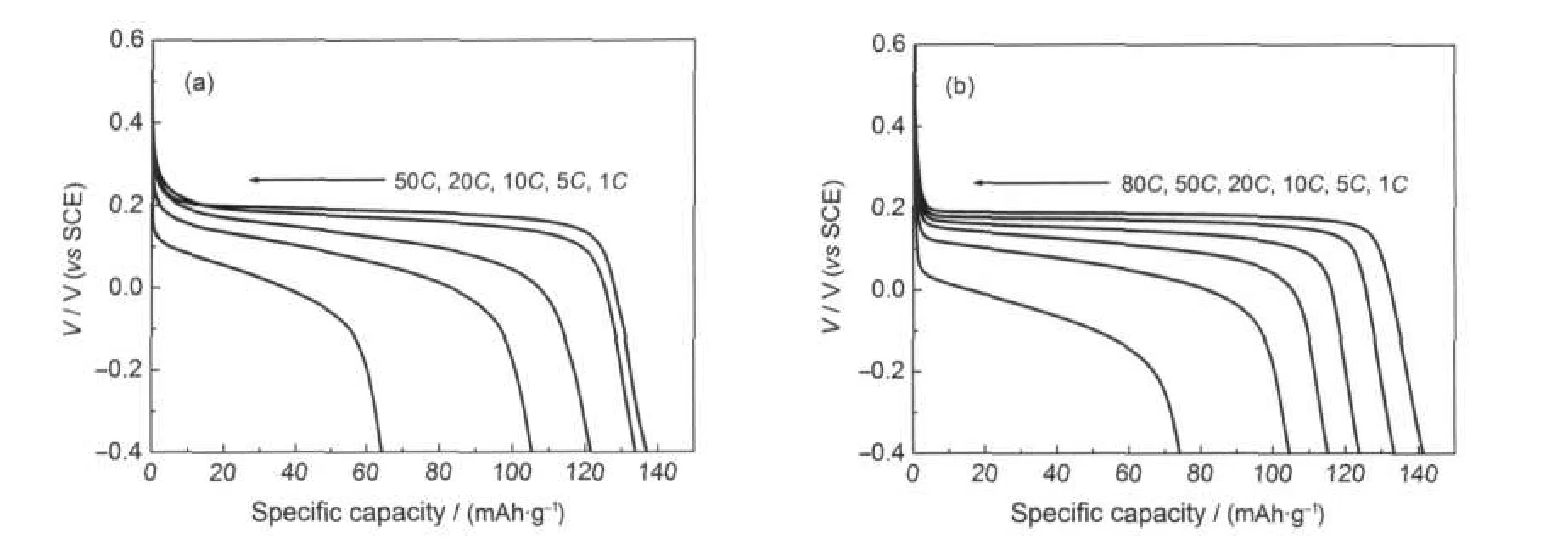
图6 LFP/C(a)和LFP/C-G(b)在不同电流密度下的充放电曲线Fig.6 Charge-discharge curves of LFP/C(a)and LFP/C-G(b)at different current densities
为了进一步分析LFP/C和LFP/C-G样品的电化学性能,我们对其进行了交流阻抗测试.图8是LFP/ C和LFP/C-G样品在相同电化学体系中,电流密度为1C循环5次后的交流阻抗图谱.从图中可以看出,谱图在高频区为半圆形,低频区逐渐过渡为一条直线.高频区的半圆是Li+穿过界面的表面电阻和双电层电容;低频区的直线是对应Li+的扩散阻抗及相应电容.29LFP/C-G半圆半径的减小,说明石墨烯的加入有效减小了材料的界面阻抗,从而极大提高了LFP/C-G的脱嵌Li+的化学动力学性能.这与上面所测的交流阻抗图谱结果相一致.总之,高导电性的石墨烯于石墨化碳组成的三维导电网络有效提高了LFP/C-G的储锂性能.

图7 LFP/C-G的导电网络结构原理图Fig.7 Schematic illustration of the structure of the LFPG conducting network
图9为样品LFP/C和LFP/C-G的循环寿命图,可以看出在水溶液体系下LiFePO4容量衰减较快.这是由于在电化学反应过程中水中溶解氧及OH−离子的影响所致.14相应的化学方程式如下所示:
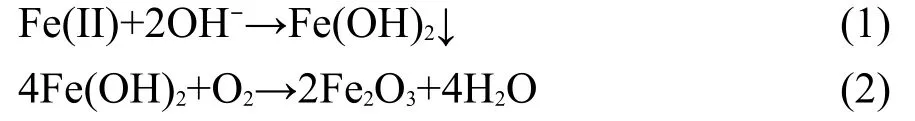
上述副反应使LiFePO4表面生成的Fe(OH)2及Fe2O3材料的电化学活性降低.石墨烯掺杂包碳的LiFePO4样品循环充放60次后的容量保持率为83.7%,包碳的样品其在循环充放60次后容量保持率为70.2%. Xia等16认为碳层的存在可以阻挡水中溶解的氧气及OH-离子对LiFePO4材料的破坏会有效缓解其在水溶液体系中的容量衰减.石墨烯的加入使电极材料导电性增强,加快了电子及离子传输,使充放电反应顺利进行.同时石墨烯片层与石墨化碳紧贴在LiFePO4表面,进一步减少了LiFePO4裸露程度,阻碍了溶液中溶解的氧气及OH-离子的接触,从而较大程度减缓了副反应的破坏,增强了电极材料的循环稳定性.

图8 LFP/C和LFP/C-G的交流阻抗谱图Fig.8 Nyquist plots of LFP/C and LFP/C-G

图9 LFP/C与LFP/C-G的充放电循环性能Fig.9 Cycle-life plots of LFP/C and LFP/C-G
4 结论
采用水热辅助法合成了掺杂石墨烯的碳包覆LiFePO4多孔纳米微球材料,相比单纯碳包覆的LiFePO4样品,其具有更好的倍率特性和较好的循环性能.在电流密度为50C时,容量可以达到105 mAh·g-1.在水系体系中,1C电流密度下循环充放60次后两样品的容量保持率分别为83.7%、70.2%.石墨烯在其中起了关键性的作用,不但改善了LiFePO4的导电性,并且有效缓解了水中的氧气和OH-离子对电极材料的影响,从而进一步改善了LiFePO4材料在水溶液体系中的循环稳定性.
(1)Padhi,A.K.;Nanjundaswamy,K.S.;Masquelier,C.;Okada,S.; Goodenough,J.B.J.Electrochem.Soc.1997,144,1188.
(2) Padhi,A.K.;Nanjundaswamy,K.S.;Masquelier,C.;Okada,S.; Goodenough,J.B.J.Electrochem.Soc.1997,144,1609.
(3) Ravet,N.;Goodenough,J.B.;Besner,S.;Simoneau,M.; Hovington,P.;Armand,M.Proceedings of the 196th ECS Meeting,Honolulu,HI,Oct 1999;pp 17-22.
(4) Belharouak,I.;Johnson,C.;Amine,K.Electrochem.Commun. 2005,7,983.
(5)Takeuchi,T.;Tabuchi,M.;Nakashima,A.;Nakamura,T.;Miwa, Y.;Kageyama,H.;Tatsumi,K.J.Power Sources 2005,146,575.
(6) Chen,Z.Y.;Zhu,H.L.;Ji,S.;Fakir,R.;Linkov,V.Solid State Ionics 2008,179,1810.
(7) Chen,Z.H.;Dahn,J.R.J.Electrochem.Soc.2002,149,A1184.
(8) Zhang,D.;Cai,R.;Zhou,Y.K.;Shao,Z.P.;Liao,X.Z.;Ma,Z. F.Electrochim.Acta 2010,55,2653.
(9) Chung,S.Y.;Bloking,J.T.;Chiang,Y.M.Nat.Mater.2002,1, 123.
(10)Wang,Y.;Wang,Y.;Hosono,E.;Wang,K.;Zhou,H.Angew. Chem.Int.Edit.2008,47,7461.
(11) Qian,J.F.;Zhou,M.;Cao,Y.L.;Ai,X.P.;Yang,H.X.J.Phys. Chem.C 2010,114,3477.
(12) Liu,J.L.;Jiang,R.R.;Wang,X.;Huang,T.;Yu,A.S.J.Power Sources 2009,194,536.
(13) Kostecki,R.;Schnyder,B.;Alliata,D.;Song,X.;Kinoshita,K.; Kotz,R.Thin Solid Films 2001,396,36.
(14)He,P.;Zhang,X.;Wang,Y.G.;Cheng,L.;Xia,Y.Y. J.Electrochem Soc.2008,155,A144.
(15) Luo,J.Y.;Cui,W.J.;He,P.;Xia,Y.Y.J.Nat.Chem.2010,2, 760.
(16) He,P.;Liu,J.L.;Cui,W.J.;Luo,J.Y.;Xia,Y.Y.Electrochim. Acta 2011,56,2351.
(17) Chen,S.Y.;Gao,B.;Su,L.H.;Mi,C.H.;Zhang,X.G.J.Solid State Electrochem.2009,13,1361.
(18) Su,F.Y.;You,C.H.;He,Y.B.;Lv,W.;Cui,W.;Jin,F.M.;Li, B.H.;Yang,Q.H.;Kang,F.Y.J.Mater.Chem.2010,20,9644.
(19)Hummers,W.S.;Offeman,R.E.J.Am.Chem.Soc.1958,80, 1339.
(20) Wang,D.Y.;Li,H.;Shi,S.Q.;Huang,X.J.;Chen,L.Q. Electrochim.Acta 2005,50,2955.
(21)Shi,Z.C.;Ye,W.L.;Wang,Q.;Li,Y.X.;Yang,Y.Electrochim. Acta 2008,53,2665.
(22) Szabo,T.;Berkesi,O.;Dekany,I.Carbon 2005,43,3186.
(23) Burba,C.M.;Frech,R.J.Electrochem Soc.2004,151,A1032.
(24) Julien,C.M.;Zaghib,K.;Mauger,A.;Massot,M.;Salah,A.A.; Selmane,M.;Gendron,F.J.Appl.Phys.2006,100,063511.
(25) Dresselhaus,M.S.;Dresselhaus,G.Light Scattering in Solids, 3rd ed.;Springer:Berlin,1982;p 3.
(26) Morishita,T.;Soneda,Y.;Hatori,H.;Inagaki,M.Electrochim. Acta 2007,52,2478.
(27)Appapillai,A.T.;Mansour,A.N.;Cho,J.;Yang,S.H.Chem. Mater.2007,19,5748.
(28) Mai,L.Q.;Yang,F.;Zhao,Y.L.;Xu,X.;Xu,L.;Luo,Y.Z.Nat. Commun.2011,2,381.
(29) Shen,L.F.;Yuan,C.Z.;Luo,H.J.;Zhang,X.G.;Yang,S.D.; Lu,X.Nanoscale 2011,3,572.
July 26,2011;Revised:October 12,2011;Published on Web:October 20,2011.
Synthesis and Electrochemical Performance of Graphene Modified LiFePO4Cathode Materials
XU Ke SHEN Lai-Fa MI Chang-Huan ZHANG Xiao-Gang*
(College of Material Science and Engineering,Nanjing University of Aeronautics and Astronautics,Nanjing 210016,P.R.China)
Graphene-modified mesoporous LiFePO4microsphere composites were synthesized by a hydrothermal method and subsequent annealing.X-ray diffraction(XRD),scanning electron microscopy (SEM),transmission electron microscopy(TEM),Fourier transform infrared(FT-IR)spectroscopy,and galvanostatic charge-discharge techniques were used to characterize the morphology,structure and electrochemical performance of the resulting composites.The graphene-modified LiFePO4microspheres exhibited a high discharge capacity of 141 mAh·g-1at 1C,and 105 mAh·g-1at 50C,while LiFePO4/C only delivered 137 mAh·g-1at 1C,64 mAh·g-1at 50C in an aqueous electrolyte of 2 mol·L-1LiNO3.The graphene-modified LiFePO4exhibited excellent cyclability compared with LiFePO4/C,with a capacity retention of about 83.7%after 60 cycles versus about 70.2%for LiFePO4/C.The improved electrochemical performance is attributed to the formation of a three-dimensional(3D)graphene network.
Lithium iron phosphate;Graphene;Hydrothermal;Li-ion battery
10.3866/PKU.WHXB201228105 www.whxb.pku.edu.cn
*Corresponding author.Email:azhangxg@163.com;Tel:+86-25-52112918;Fax:+86-25-52112626.
The project was supported by the National Key Basic Research Program of China(973)(2007CB209703),National Natural Science Foundation of China(20873064,21173120,21103090),Jiangsu Innovation Program for Graduate Education,China(CXZZ11_0204),and Outstanding Doctoral Dissertation in Nanjing University ofAeronautics andAstronautics,China(BCXJ11-10).
国家重点基础研究发展计划项目(973)(2007CB209703),国家自然科学基金(20873064,21173120,21103090),江苏省普通高校科研创新计划(CXZZ11_0204)及南京航空航天大学博士学位论文创新与创优基金资助(BCXJ11-10)
O646

