注射用头孢唑肟钠与维生素B6注射液在5%葡萄糖注射液中的配伍稳定性考察
陆 华,程道海,刘滔滔(广西医科大学第一附属医院药剂科,南宁 530021)
注射用头孢唑肟钠属于第3代头孢菌素,具有广谱抗菌作用,并且对多种革兰阳性菌和革兰阴性菌产生的广谱β-内酰胺酶(包括青霉素酶和头孢菌素酶)稳定,因此临床应用广泛,用于敏感菌所致的下呼吸道感染、尿路感染、腹腔感染、盆腔感染等疾病的治疗。某院护士在给患者静脉滴注含有维生素B6注射液0.1 g的5%葡萄糖注射液100 mL过程中,临时在输液器的墨菲氏滴管中加入经0.9%氯化钠注射液溶解后的注射用头孢唑肟钠1支(规格为1.0 g)后,约数分钟后溶液出现乳白色浑浊及沉淀,立即停用,咨询药剂科查因。查阅国内《400种中西药注射剂临床配伍应用检索表》[1]显示,注射用头孢唑肟钠与维生素B6均可使用5%葡萄糖注射液作溶媒配伍使用,但未见二者可以相互配伍;搜索国内的专业文献期刊,也未见有关注射用头孢唑肟钠和维生素B6存在配伍禁忌的报道。为确保临床用药的安全性和有效性,笔者模拟上述临床使用的用药浓度和配制方法,对注射用头孢唑肟钠和维生素B6在5%葡萄糖注射液中的配伍稳定性进行研究,现将结果报道如下。
1 仪器与试药
1.1 仪器
DF110电子分析天平(江苏常熟衡器厂);pHS-3C型精密pH计(上海雷磁仪器厂);LC-10ATvp高效液相色谱仪(日本岛津公司)。
1.2 试药
注射用头孢唑肟钠(韩国钟根堂制药公司产,规格:1.0 g,批号:MA024A);维生素B6注射液(徐州莱恩药业有限公司产,规格:2 mL∶0.1 g,批号:1012241);5%葡萄糖注射液(石家庄四药有限公司产,规格:100 mL∶5 g,批号:110226801);0.9%氯化钠注射液(徐州莱恩药业有限公司产,规格:10 mL∶90 mg,批号:0907081);头孢唑肟钠对照品(上海瑞齐生物科技有限公司,标示量:93.6%);甲醇为色谱纯,磷酸、磷酸二氢钾为分析纯。
2 方法
2.1 溶液的配制
(1)A液:维生素B6注射液1支(规格:2 mL∶0.1 g)+5%葡萄糖注射液1瓶(规格:100 mL∶5 g),混匀;(2)B液:注射用头孢唑肟钠1支(规格:1.0 g)+0.9%氯化钠注射液5 mL,溶解后加至5%葡萄糖注射液1瓶(规格:100 mL∶5 g)中,混匀;(3)C液:注射用头孢唑肟钠1支(规格1.0 g)+0.9%氯化钠注射液5 mL,溶解后加至A液中,混匀。
2.2 外观和pH值变化
配制A、B、C液,分别于室温下放置0、10、30、60、120 min后,观察3种溶液的外观并同时测定5个时间点溶液的pH值。有关方法参照2010年版《中国药典》进行测定。
2.3 采用高效液相色谱法测定溶液中头孢唑肟钠在上述时间点的含量变化
2.3.1 色谱条件[2,3]。色谱柱:Thermo Hypersil ODS-2(4.6 mm×250 mm,5 μm),流动相:0.02 mol·L-1磷酸二氢钾溶液(用磷酸调pH值至3.6)-甲醇(85∶15);柱温:25 ℃;流速:1 mL·min-1;检测波长:254 nm;进样量:20 μL。
2.3.2 系统适用性试验。取B液,用5%葡萄糖注射液稀释成含头孢唑肟0.1 mg·mL-1的溶液(按标示量计)注入高效液相色谱仪,结果头孢唑肟钠峰形较好,理论板数以头孢唑肟钠峰计不低于2500。按上述方法稀释同样倍数A液,考察维生素B6峰或其他杂质峰对头孢唑肟峰的影响,并且单独以5%葡萄糖注射液作空白考察。结果维生素B6和溶剂峰对头孢唑肟钠峰无干扰,头孢唑肟钠峰与其他杂质峰的分离度符合要求。高效液相色谱图见图1。
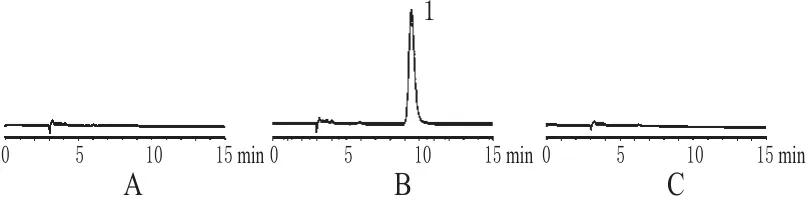
图1 高效液相色谱图Fig 1 HPLC chromatograms
2.3.3 标准曲线的制备。准确称取干燥至恒重的头孢唑肟钠对照品50 mg,置于50 mL容量瓶中,用水溶解并稀释至刻度,即得含量为1 mg·mL-1的贮备液。用5%葡萄糖注射液分别稀释成含头孢唑肟钠0.033、0.05、0.067、0.1、0.133、0.2 mg·mL-1的定标液,按“2.3.1”项下条件进样测定,记录色谱。以浓度(c)为横坐标,相应峰面积(A)为纵坐标,进行线性回归,获得标准曲线的回归方程:A=4×107c+214206(r=0.9990)。结果表明,头孢唑肟钠检测浓度在0.033~0.2 mg·mL-1范围内线性关系良好。
2.3.4 精密度试验。配制含头孢唑肟钠100 μg·mL-1对照品溶液,按“2.3.1”项下色谱条件分别进样测定5次,计算精密度,结果平均RSD为0.44%。
2.3.5 回收率试验。分别取低、中、高3种不同浓度的头孢唑肟钠对照品溶液,按“2.3.1”项下色谱条件,每个浓度平行进样测定3次,计算回收率,结果见表1。
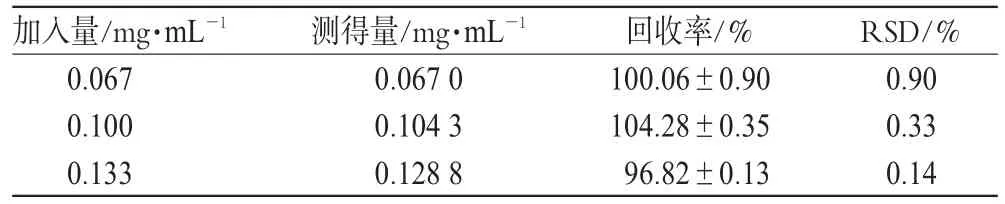
表1 回收率试验结果(n=3)Tab 1 Results of recovery test(n=3)
2.3.6 测定C液中头孢唑肟钠含量变化。取新鲜配制C液于0 min用5%葡萄糖注射液稀释成含头孢唑肟钠0.1 mg·mL-1的溶液(按标示量计),按“2.3.1”项下色谱条件,注入高效液相色谱法仪,记录峰面积数值,并以其作为相对参考值100%;随后分别取室温放置10、30、60、120 min的C液,同法进行测定。如溶液出现浑浊或有沉淀产生,则溶液需预先经0.45 μm微孔滤膜过滤。记录各时间点的峰面积并与0 min的峰面积进行比较,计算出相对含量,以考察配伍溶液中头孢唑肟在不同时间点的含量变化。
3 结果
3.1 外观与pH值变化
A液和B液在室温放置2 h外观均为澄清、无色液体,pH值稳定,说明维生素B6注射液和注射用头孢唑肟钠在5%葡萄糖溶媒中稳定。C液除在0、10 min时澄清、无色外,在30、60、120 min均出现白色浑浊液体,并有沉淀产生,且随着时间延长,沉淀增多;C液30 min后的pH值也发生显著改变,结果见表2。

表2 3种溶液在不同时间点的pH值变化Tab 2 pH value changes of 3 kinds of samples at different time points
3.2 C液中头孢唑肟钠含量变化
配伍C液于不同时刻取样按”2.3.6”项下方法进样测定,结果见表3。
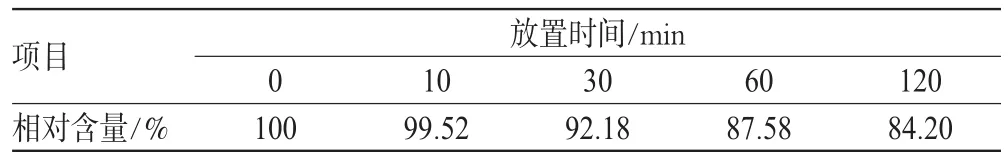
表3 C液中头孢唑肟钠在不同时间点的峰面积和相对含量变化Tab 3 Peak area and relative content change of ceftizoxime sodium in solution C at different time points
由表3可知,C液中头孢唑肟含量在10 min时变化不明显,30 min开始明显下降,120 min时相对含量仅为84.20%,说明头孢唑肟钠的含量在观察期内明显下降。
4 讨论
色谱条件的选择,笔者经过试验,确定以0.02 mol·L-1磷酸二氢钾溶液(用磷酸调pH值至3.6)-甲醇(85∶15)作为流动相。结果,该条件方法简单,头孢唑肟峰钠形、分离度和稳定性均较好。
模拟临床用药浓度和配制方法,根据临床输液正常的消耗时间,并参考文献提供的配伍稳定性考察方法[4],得出的结果是注射用头孢唑肟钠与维生素B6在5%葡萄糖注射液中混合10 min内外观、pH值、含量无明显变化,但从30 min开始,3指标均有明显改变:外观出现白色浑浊或沉淀;pH值发生改变(由4.65升至5.42);头孢唑肟含量下降(混合30 min降低至92.18%,2 h降至84.2%)。可见从30 min开始混合液的3项指标同步发生变化。混合液pH值的升高,可能是由于头孢唑肟钠与维生素B6结合后生成沉淀析出,溶液中维生素B6这一偏酸性物质减少导致。
有文献报道[5],注射用头孢唑肟钠与维生素B6注射液加入5%葡萄糖注射液进行配伍试验,结果外观无变化,紫外吸收峰无偏移,认为临床可配伍。但笔者发现该文献中的头孢唑肟钠和维生素B6的试验浓度要明显低于本文(本文使用的溶媒5%葡萄糖为100 mL,而该报道使用的为500 mL),药物浓度过低导致发生配伍不稳定性的现象不明显,如析出细小的颗粒肉眼看不见、药物含量改变不大。参考有关文献及相关说明书,发现头孢唑肟钠一般使用50~100 mL的5%葡萄糖注射液作为溶媒进行溶解[5],或要求在30~120 min内滴注完毕(参考西南药业有限公司头孢唑肟钠说明书),所以本文中的溶媒量为100 mL,与临床的常规使用量相符。
维生素B6为水溶性盐酸吡多辛,参与氨基酸及脂肪的代谢,2010年版《中国药典》规定其注射液的pH值为2.5~4.0,而《中国药典》规定的注射用头孢唑肟钠的酸碱度应在6.0~8.0,两药配伍后溶液的pH值发生了改变,且都不在二者允许的稳定范围内,溶液产生白色浑浊和沉淀,药物含量下降,可见注射用头孢唑肟钠在溶液中的稳定性与pH值有关。因此,临床应用时应避免将两药混合伍用。护士在给予患者进行输液治疗时,不应为图方便随意将一种药物通过输液器墨菲氏滴管加入到已含有其他药物的溶媒中,应该仔细查阅与配伍变化相关的专业文献和药品说明书,确定无配伍禁忌后再实施配伍,以确保患者安全用药。有关二者配伍后出现的沉淀为何物及其理化性质还有待进一步研究。
[1]宗希乙,沈建平,林建设,等.400种中西药注射剂临床配伍应用检索表[M].北京:中国医药科技出版社,2007:1.
[2]国家药典委员会编.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2010:201-205.
[3]郭 静,周学琴.注射用头孢唑肟钠在复方氨基酸注射液中稳定性的研究[J].现代医院,2009,9(9):60.
[4]刘瑞琴,杨继章,叶 楠.注射用头孢地嗪钠与注射用甲硝唑磷酸二钠配伍稳定性考察[J].中国药房,2011,22(2):151.
[5]张建忠.头孢唑肟在输液中与6种注射剂配伍的稳定性研究[J].中国现代应用药学杂志,1999,16(5):59.

