HPLC法同时测定复方儿茶酊中儿茶素与原儿茶素的含量
龙潇鸿,范卫东,郑娇妮
(1.重庆医科大学附属第二医院,重庆400010;2.重庆市第四人民医院药剂科,重庆400014)
HPLC法同时测定复方儿茶酊中儿茶素与原儿茶素的含量
龙潇鸿1*,范卫东1#,郑娇妮2
(1.重庆医科大学附属第二医院,重庆400010;2.重庆市第四人民医院药剂科,重庆400014)
目的:建立同时测定复方儿茶酊中儿茶素与原儿茶素含量的方法。方法:采用高效液相色谱法。色谱柱为YMC ODS(250 mm×4.6 mm,5μm),流动相为0.04 mol·L-1枸橼酸溶液-N,N-二甲基甲酰胺-四氢呋喃(45∶8∶2,V/V/V),流速为1.0 mL·min-1,检测波长为280 nm,柱温为35℃。结果:儿茶素与原儿茶素的检测浓度分别在0.051 8~0.259 0、0.010 1~0.203 0 mg·mL-1(r均为0.999 9)范围内与各自峰面积积分值呈良好的线性关系;平均加样回收率分别为101.63%和100.49%,RSD分别为1.27%和1.12%(n均为9)。结论:本方法简便、准确、稳定,能有效控制复方儿茶酊的质量。
高效液相色谱法;复方儿茶酊;儿茶素;原儿茶素;含量测定
复方儿茶酊主要由儿茶、黄柏、冰片等常用中药组成,具有收湿敛疮、清热解毒的作用,同时对烧伤具有抗菌消肿、活血止痛、促进创面愈合的功效,临床主要用于治疗各种原因引起的烧烫伤[1],至今约有30余年的临床应用历史。本方君药儿茶味苦、性寒,功能收湿生肌敛疮,《本草正》曰:“用治湿烂诸疮”。因此,对本方儿茶中主要有效成分儿茶素、原儿茶素的含量进行有效控制尤为必要。笔者采用高效液相色谱(HPLC)法对本方中儿茶素、原儿茶素的含量进行了测定,以为该制剂的质量控制提供依据。
1 仪器与试药
LC-20AT型HPLC仪、AW-200型电子天平(日本岛津公司);KQ-250B型超声仪(巩义市予华仪器有限责任公司,功率:250 W,频率:40 kHz)。
儿茶素、原儿茶素对照品(中国食品药品检定研究院,批号分别为877-200001、879-200203);甲醇为色谱纯,其他试剂均为分析纯;复方儿茶酊(批号:20100920-1、20100920-2、20100920-3)及缺儿茶的阴性样品均由重庆医科大学药物分析实验室制备。
2 方法与结果[2~5]
2.1 色谱条件
色谱柱:YMC ODS(250 mm×4.6 mm,5μm);流动相:0.04 mol·L-1枸橼酸溶液-N,N-二甲基甲酰胺-四氢呋喃(45∶8∶2,V/V/V);流速:1.0 mL·min-1;检测波长:280 nm;柱温:35℃。
2.2 溶液的制备
2.2.1 对照品溶液 精密称定儿茶素对照品0.002 59 g,置于10 mL量瓶中,以50%甲醇定容,制得每1 mL含0.259 mg的儿茶素对照品溶液;精密称定原儿茶素0.002 03 g,置于10 mL量瓶中,以50%甲醇定容,制得每1 mL含0.203 mg的原儿茶素对照品溶液。
2.2.2 供试品溶液 精密移取样品1 mL,置于100 mL量瓶中,加50%甲醇至刻度,摇匀,用微孔滤膜(0.45μm)滤过,取续滤液,即得。
2.2.3 阴性对照溶液 取缺儿茶的阴性样品0.5 g,按“2.2.2”项下方法制备阴性对照溶液,即得。
2.3 系统适用性试验
分别取阴性对照溶液、儿茶素对照品溶液、原儿茶素对照品溶液、供试品溶液各适量,按上述色谱条件进样测定,对系统适用性参数进行考察。结果,儿茶素和原儿茶素的理论板数分别为5 689、7 526;分离度为5.36。供试品溶液中儿茶素和表儿茶素的峰与其他峰能达到基线分离,且阴性对照无干扰。色谱见图1。
2.4 线性关系考察
分别取儿茶素对照品溶液2.0、4.0、6.0、8.0、10.0 mL,加50%甲醇溶解并定容至10 mL量瓶中,得一系列儿茶素对照品溶液。精密吸取上述儿茶素对照品溶液各10μL,分别注入液相色谱仪,按上述色谱条件进样测定。以儿茶素峰面积积分值(X)为横坐标,进样浓度(Y,mg·mL-1)为纵坐标,绘制标准曲线,得儿茶素的回归方程为Y=0.000 172X+2.255 312(r=0.999 9,n=5)。结果表明,儿茶素进样浓度在0.051 8~0.259 0 mg·mL-1范围内与峰面积积分值呈良好线性关系。
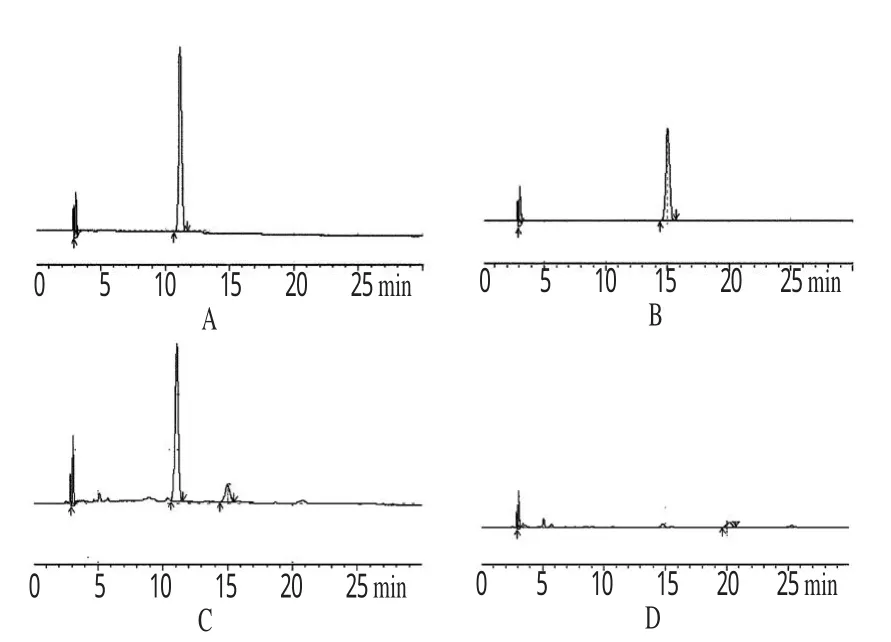
图1 高效液相色谱图A.儿茶素对照品;B.原儿茶素对照品;C.供试品;D.阴性对照Fig 1 HPLC chromatogramsA.catechin control;B.epicatechin control;C.test samples;D.negative control
分别取原儿茶素对照品溶液 0.5、1.0、2.0、4.0、6.0、8.0、10.0 mL,加50%甲醇溶解并定容至10 mL量瓶中,得一系列原儿茶素对照品溶液。精密吸取上述原儿茶素对照品溶液各10 μL,分别注入液相色谱仪,按上述色谱条件进样测定。以原儿茶素峰面积积分值(X)为横坐标,进样浓度(Y,mg·mL-1)为纵坐标,绘制标准曲线,得原儿茶素的回归方程为Y=0.000 176X+0.159 399(r=0.999 9,n=7)。结果表明,原儿茶素进样浓度在0.010 1~0.203 0 mg·mL-1范围内与峰面积积分值呈良好线性关系。
2.5 精密度试验
取儿茶素对照品溶液与原儿茶素对照品溶液各适量,重复进样6次,记录峰面积。结果,儿茶素、原儿茶素峰面积的RSD分别为2.3%、2.1%(n均为6),表明仪器精密度良好。
2.6 稳定性试验
精密移取同一供试品溶液(批号:20100920-1)适量,分别于0、4、8、12、18、24 h进样10μL,记录峰面积。结果,儿茶素、原儿茶素峰面积的RSD分别为0.56%、0.98%(n均为6),表明供试品溶液在24 h内稳定。
2.7 重复性试验
精密移取同一批(批号:20100920-1)样品适量,按“2.2.2”项下方法平行制备6份供试品溶液,计算各组分含量。结果,儿茶素和原儿茶素含量的RSD分别为0.15%、1.52%(n均为6),表明本方法重复性良好。
2.8 加样回收率试验
精密移取0.1 mL儿茶素含量为9.04 g·L-1的样品(批号:20100920-1),置于10 mL量瓶中,平行9份,每3份分别加入儿茶素对照品溶液2.5、3.0、3.5 mL,按“2.2.2”项下方法制备供试品溶液,再按上述色谱条件测定,计算儿茶素的加样回收率,结果见表1。
精密移取0.1 mL原儿茶素含量为1.32 g·L-1的样品(批号:20100920-1),置于10 mL量瓶中,平行9份,每3份分别加入原儿茶素对照品溶液1.5、2、2.5 mL,按“2.2.2”项下方法制备供试品溶液,再按上述色谱条件测定,计算原儿茶素的加样回收率,结果见表2。
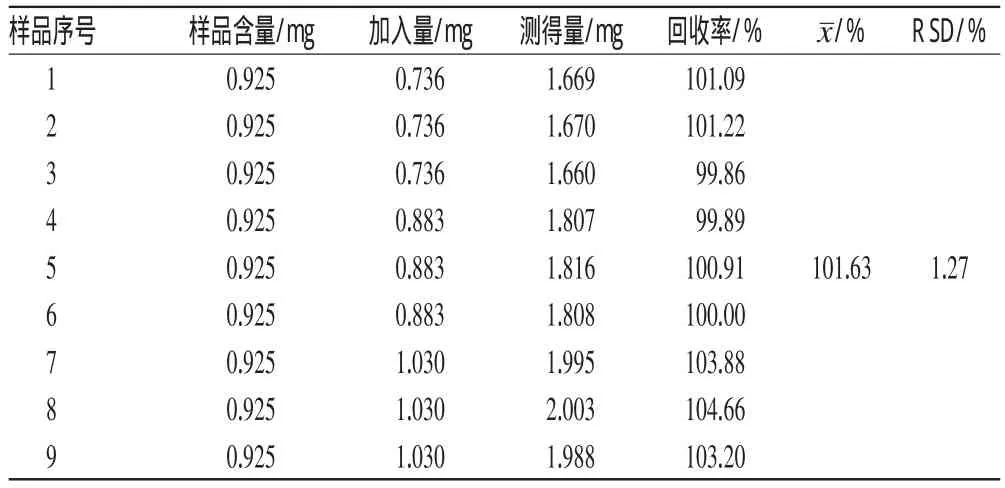
表1 儿茶素的加样回收率试验结果(n=9)Tab 1 Results of recovery test of catechin(n=9)
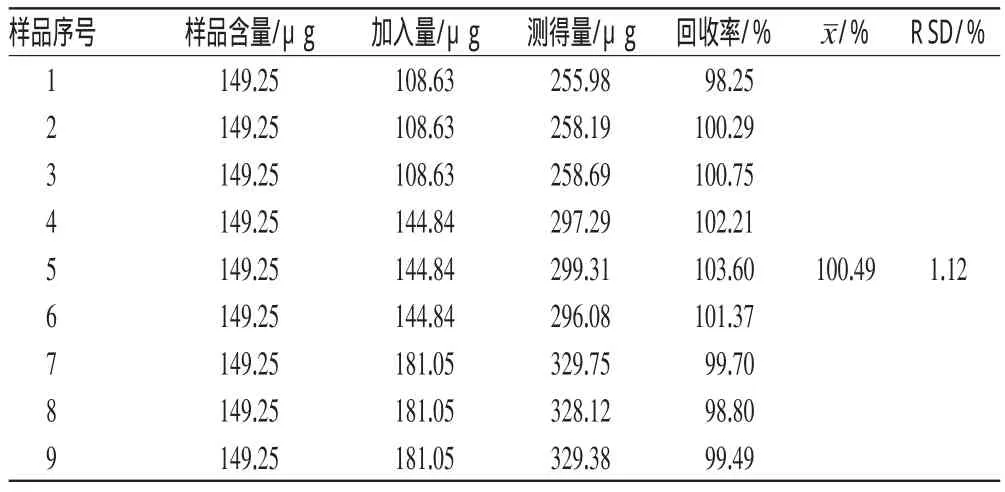
表2 原儿茶素的加样回收率试验结果(n=9)Tab 2 Resultsof recovery test of epicatechin(n=9)
2.9 样品含量测定
取3批样品,分别按“2.2.2”项下方法制备供试品溶液,各进样10μL,照上述方法测定3批复方儿茶酊中儿茶素、原儿茶素的峰面积,按标准曲线法计算含量,结果见表3。
3 讨论
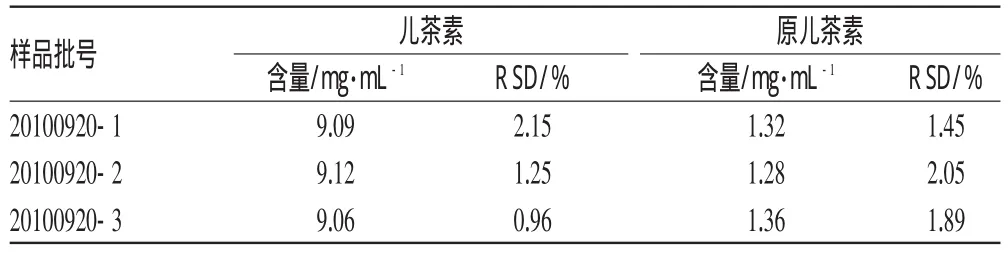
表3 样品含量测定结果(n=3)Tab 3 Results of content determination of samples(n=3)
复方儿茶酊用药后在创面形成一层药膜,可立即解除烧灼感,使患者获得清凉感而止痛;可以减少渗出和体液蒸发,减少补液和抗生素的应用;该药收敛迅速形成痂皮,使创面与该药接触处呈湿润状态,对烧伤后间生态组织有保护作用,促使上皮组织再生修复,因此在临床应用多年,口碑较好。
本方法简便、稳定、专属性强、灵敏度高,能有效控制复方儿茶酊的质量;并对于含儿茶的制剂,本法同样适用于其中儿茶素与原儿茶素含量的测定,从而为此类品种的质量控制提供了一种有效方法。
[1] 王权龙.复方儿茶酊治疗烧伤35例[J].陕西中医,2010,31(10):1 365.
[2] 国家药典委员会.中华人民共和国药典(一部)[S].2010年版.北京:中国医药科技出版社,2010:9.
[3] 曲银锋,李松武,刘乃强,等.HPLC法测定小儿泻速停颗粒中儿茶素和表儿茶素的含量[J].食品与药品,2009,11(5):39.
[4] 高剑锋,易以木,邱 娟,等.HPLC法测定复方儿茶软膏中儿茶素和表儿茶素含量[J].药物分析杂志,2007,27(7):1 105.
[5] 王 勤,侯铁军.HPLC法测定锁阳中原儿茶酸的含量[J].中国药房,2007,18(15):1 170.
Content Determination of Catechin and Epicatechin in Compound Catechu Tinctureby HPLC
LONG Xiao-hong,FAN Wei-dong
(The Second Affiliated Hospital of Chongqing Medical University,Chongqing 400010,China)
ZHENG Jiao-ni
(Dept.of Pharmacy,Chongqing Fourth People’s Hospital,Chongqing 400014,China)
OBJECTIVE:To establish the method for the content determination of catechin and epicatechin in Compound catechu tincture.METHODS:HPLC method was adopted.The determination was performed on YMC ODS(250 mm×4.6 mm,5μm)column with mobile phase consisted of 0.04 mol·L-1citric acid solution-N,N-dimethylformamide-tetrahydrofuran(45∶8∶2,V/V/V)at the flow rate of 1.0 mL·min-1.The detection wavelength was 280 nm and column temperature was 35℃.RESULTS:The linear range of catechin and epicatechin were 0.051 8~0.259 0 mg·mL-1(r=0.999 9)and 0.010 1~0.203 0 mg·mL-1(r=0.999 9).The average recoveries were 101.63%(RSD=1.27%,n=9)and 100.49%(RSD=1.12%,n=9).CONCLUSION:The method is simple,accurate and stable for quality control of Compound catechu tincture.
HPLC;Compound catechu tincture;Catechin;Epicatechin;Content determination
R283.662;R927.2
A
1001-0408(2012)43-4093-03
DOI 10.6039/j.issn.1001-0408.2012.43.24
2012-01-30
2012-09-14)

