β-环糊精修饰二氧化钛光催化降解甲基橙的研究
朱方彤,邓 琳,高海鹰
(东南大学 市政工程系,江苏 南京210096)
1 引言
印染废水具有种类多、水量大、有机物成分复杂、可生化降解性差等特点,其中含有的有毒成分可以削弱有机污染物的微生物矿化作用,引起水生生态系统微生物的减少,进一步导致水体生态系统的破坏[1,2]。其中属于偶氮染料的甲基橙是具有代表性的一种。甲基橙易溶于水,性质十分稳定,用传统的生物降解方法难降解,因此研究偶氮类染料的光降解有着十分重要的意义。
以二氧化钛为代表的半导体催化技术,在环境污染控制领域有着巨大实际应用前景以及社会经济效益。普遍认为如果目标化合物能尽可能接近二氧化钛表面,就能更有利于光解效率,但二氧化钛缺乏对目标污染物的主动吸附驱动力。因此,提高目标污染物在二氧化钛表面的吸附率是进一步提高光降解效率的有效手段。程大莉[3]等以竹炭作为纳米二氧化钛粒子的载体物质,制备了二氧化钛/竹炭复合材料,并以苯酚为模型物质对其光催化性能进行了研究。研究表明:此复合材料对苯酚具有较强的吸附性能。Dingning[4]等研究组以十六烷基三甲基溴化铵为活性剂,制备得到 WO3/TiO2复合颗粒,复合后的二氧化钛通过提高罗丹明B在二氧化钛表面的吸附率从而使罗丹明B的光降解达到更好的效果。然而,借助于改性β-环糊精修饰二氧化钛提高其光催化性能的研究鲜有报道。本研究采用3-氯丙基三乙氧基硅烷、β环糊精和二氧化钛等,合成出新型P25-S1-CD,以甲基橙作为目标污染物,考察P25-S1-CD对有机物的光催化效果。
2 材料与方法
2.1 试剂与仪器
试剂选用P25锐钛矿含量为78%和金红石矿含量为22%;氢氧化钠(NaOH),盐酸(HCl),甲基橙从国家医药公司(中国上海)购得;甲苯;3-氯丙基三乙氧基硅烷;丙酮;甲醇等。所用化学试剂都是分析纯,均从国家医药公司(中国上海)购得;实验中使用二次蒸馏水。
仪器选用自制的光化学反应器;UV-1061分光光度计(日本SHIMADZU)。
2.2 检测方法
甲基橙吸收光谱由UV-1061分光光度计(日本SHIMADZU)记录,甲基橙的特征吸收峰为464nm。采用分光光度法测定溶液中染料最大吸收峰的吸光度变化。吸光度值差异换算为溶液中染料浓度的变化。在6个100mL容量瓶中,用5mL玻璃管分别加入0.00,1.00,2.00,3.00,4.00,5.00mL甲基橙标准溶液(C=1mmol/L),再用去离子水稀释至刻度,摇匀。在所选定的波长(464nm)下,用3cm比色皿,以空白试剂调零后,逐个测定以上各标准溶液的吸光度。得到吸光度与浓度关系的公式y=0.2217x+0.00329,R2=0.9999。
2.3 β环糊精修饰二氧化钛试剂的制备
在200mL甲苯中,加入4g二氧化钛与4mL的3-氯丙基三乙氧基硅烷,在N2保护下,120℃回流搅拌反应12h,冷却,过滤。固体物质依次采用丙酮、甲醇、二次水和丙酮洗涤数次,滤干后,将产物于100℃真空干燥8h后得到物质A。0.5g的β-CD与0.1g的NaOH加入100mL的DMF中,搅拌1h,然后过滤,在滤液中加入物质A 2g。混合物在N2保护下115℃回流搅拌反应3d。冷却过滤所得固体物质依次采用丙酮、甲醇、二次水和丙酮洗涤数次,滤干后于100℃真空干燥8h后于干燥器中备用[5]。
2.4 光催化试验
试验在自制的光化学反应器中进行,反应器容积为0.5L,中心光源为15W低压汞灯(特征波长为254nm),中心光源置于一端封闭的石英套管中,中间夹层通过水循环对系统进行冷却,保持相对稳定的温度,磁力搅拌使催化剂悬浮于反应液中。圆形反应器中有一个15W低压汞灯,通循环冷却水以保持相对稳定的温度。所有的光催化实验溶液放置在光化学反应装置中进行,每间隔30min取一次10mL反应溶液进行检测。
3 结果与讨论
3.1 P25-S1-CD与P25对甲基橙光降解效果的比较
为检验P25-S1-CD对甲基橙的光解效果,在pH值为中性,甲基橙初始浓度为40μmol/L,投加量为0.2g/L的条件下,将P25-S1-CD与P25对甲基橙光降解效率进行对比,其结果如图1所示。
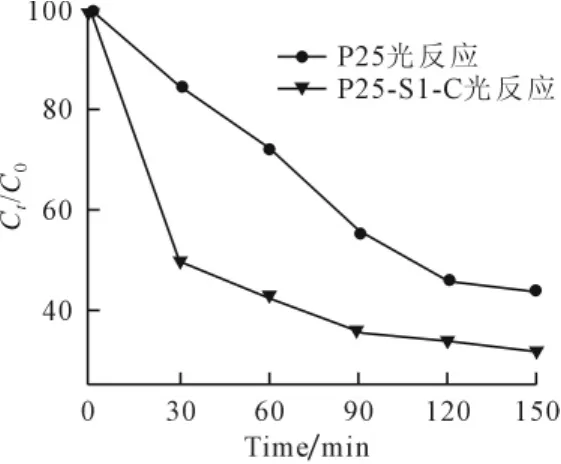
图1 P25-S1-CD、P25对甲基橙光降解效果比较
由图1可知,经过150min的光反应,投加P25的甲基橙溶液其降解率为56%,而投加P25-S1-CD的甲基橙溶液降解率为69%。实验结果说明与未改性的P25相比,P25-S1-CD可有效提高甲基橙溶液的光催化降解率。降解率提高的原因可能是P25-S1-CD吸附甲基橙的能力增强,从而提高其光降解效率。
3.2 P25-S1-CD投加量对甲基橙光降解的影响
为研究P25-S1-CD投加量对甲基橙光降解效果,在pH值为中性,甲基橙初始浓度为40μmol/L的条件下,对投加量为0.05g/L-0.4g/L的一系列溶液进行光催化反应,结果如图2所示。

图2 P25-S1-CD投加量对甲基橙光降解的影响
由图2可知,P25-S1-CD的投加量在0.05g/L~0.4g/L变化时,甲基橙的光降解率随投加量的增加而增大。当P25-S1-CD的投加量由0.05变为0.4g/L时,经过150min甲基橙的光降解率由25%提高到89%。原因可能是随着投加量的增加,可供利用的P25-S1-CD的量增加,当投入量较少时,对甲基橙的吸附弱,而随着投入量的增加,对甲基橙分子的吸附能力逐渐加强,反应的固-液接触面增大,所以甲基橙在P25-S1-CD表面发生吸附和光催化能力加强,所以甲基橙的光降解率随之提高。
3.3 初始pH值对甲基橙光降解的影响
为研究在不同pH值条件下P25-S1-CD的吸附效果,在甲基橙初始浓度为40μmol/L、投加量均为0.2g/L的条件下,用 HCl和NaOH调整到需要的pH值,对pH值为4、6、7、8、10的一系列溶液进行光催化反应,结果如图2所示。
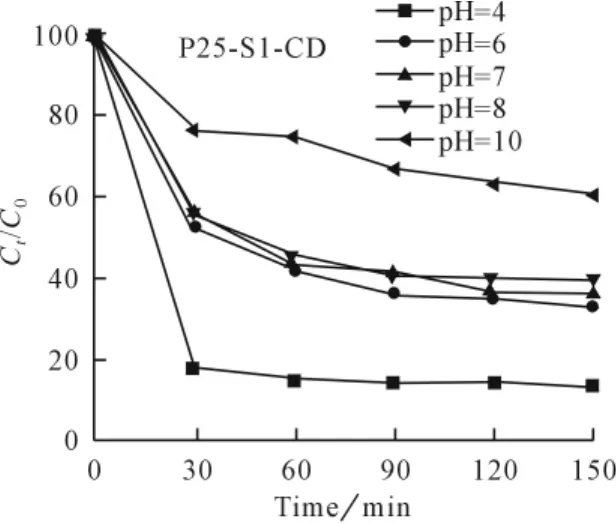
图3 初始pH值对甲基橙光降解的影响
由图3可知,投加P25-S1-CD的溶液中,碱性溶液pH值为10时,150min后甲基橙的光催化降解率仅为39%,而在酸性溶液中pH=4时,甲基橙的光催化降解率为87%。可见,pH值的影响非常明显。其他实验条件一定的情况下,随着pH值的不断升高,P25-S1-CD的光催化效率逐渐下降。pH值的改变可以影响到P25-S1-CD对染料的吸附,进而对染料的光降解产生巨大影响。溶液初始pH值的变化会影响半导体离子的表面电荷、能级等性质,同时也会影响甲基橙分子在溶液中的存在形式以及不同形式甲基橙分子在溶液中的存在量,从而影响反应物表面的吸附,最终影响光催化剂性能[6]。Mills A[7]等也论述了碱性条件下,极大的抑制了染料在二氧化钛表面的吸附,从而出现抑制光降解现象,而在酸性的条件下,可强化阴离子型染料在二氧化钛表面的吸附,起到促进光降解的作用。
3.4 甲基橙初始浓度对甲基橙光降解影响
为研究不同的甲基橙初始浓度下的光催化降解效果,在pH值为中性,投加量为0.2g/L,对10~50μmol/L的初始浓度的一系列甲基橙溶液进行了光催化反应,结果如图4所示。
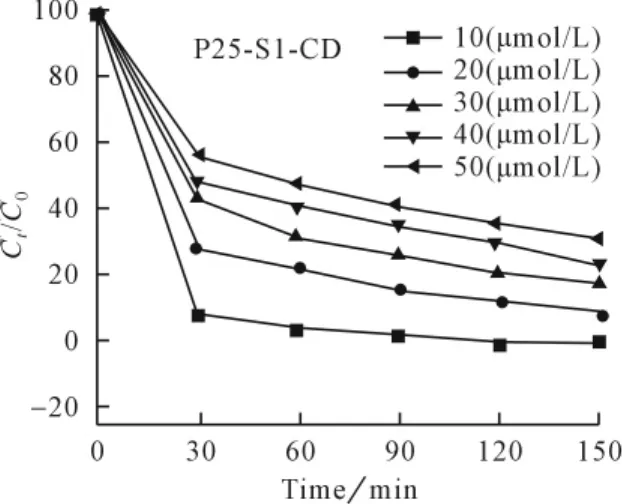
图4 甲基橙初始浓度对甲基橙光降解的影响
由图4可知,甲基橙的起始浓度在10~50μmol/L时,光催化效率随着初始浓度增加而减少,由于初始浓度越高,溶液中所含离子的数量越多,与P25-S1-CD表面的接触机会也越多,从而被吸附的离子数量也会相应增加,所以单位面积P25-S1-CD吸附容量增加,但是由于溶液中离子增加的绝对数远大于P25-S1-CD吸附离子的增加数,所以吸附率反而降低[8]。吸附率降低,导致光催化降解率越低。在10~50μmol/L浓度范围内,随着底物吸附量提高,相对来说催化剂表面的氧分子及氢氧根离子吸附量就会越少,于是出现浓度越高降解率越低的现象。由于大量的甲基橙覆盖于催化剂表面,减少了二氧化钛表面的羟基和氧分子的数量,所以光激发甲基橙后导致羟基自由基等活性物质生成量减少。另一种可能是高浓度甲基橙削弱的了光的强度,使得能照射于二氧化钛表面的光能减少,这也必然导致二氧化钛表面活性物质相应减少,因此导致浓度越高光解速率越慢的结果[9,10]。
3.5 温度对甲基橙光降解的影响
为研究不同温度的甲基橙的光催化降解效果,在pH值为中性,投加量为0.2g/L,对温度变化分别为20℃、30℃、40℃、50℃的一系列甲基橙溶液进行了光催化反应,结果如图5所示。
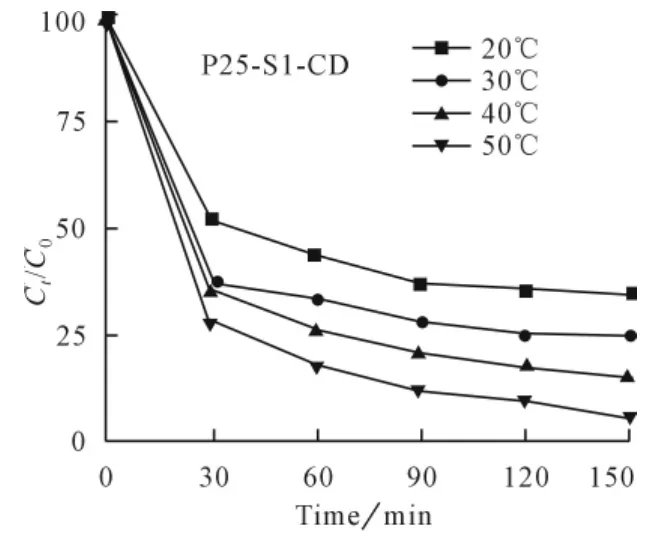
图5 温度对甲基橙光降解的影响
由图5可知,温度由20℃上升到50℃,P25-S1-CD的光降解率随着温度的升高而升高。P25-S1-CD经过150min光催化反应后,降解率达到85%;温度上升到50℃时,经过120min光催化反应后,降解率达到了90%。
3.6 P25-S1-CD光降解甲基橙动力学研究
对甲基橙初始浓度试验结果进行处理,发现甲基橙浓度Ct的对数值ln(Ct)与反应时间t存在较好的线性关系,实验时甲基橙的初始浓度分别为10、20、30、40、50μmol/L。以上每个浓度下的甲基橙初始降解速率等于对应的准一级反应动力学常数与其初始浓度的乘积,所得数据按照Langmuir-Hinshelwood动力学模式拟合,该模式对应的方程如下:
R=-dC/dt=kreKsC0/(1+KsC0)
式中,R代表底物的起始降解速率;C0表示底物的起始浓度;kre表示反应速率常数;Ks为朗格缪尔吸附常数。由公式可以看出,1/R与1/C0是线性关系,线性方程的截距为1/kre。以上的计算结果详见表1。
由表1可知,甲基橙光降解的起始速率随初始浓度的增加而加快,其反应动力学常数kre为0.283。赵德明等在复合纳米TiO2光催化氧化苯酚的动力学研究中也得到了类似的结果[11~13]。
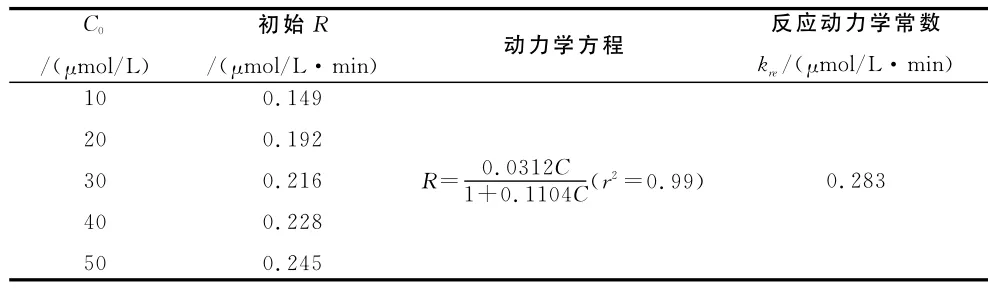
表1 甲基橙光降解动力学分析
4 结语
试验研究表明与未改性的P25相比,经过β环糊精修饰二氧化钛P25-S1-CD可有效提高甲基橙的光催化降解率。在一定范围内加大体系中P25-S1-CD的投加量、降低初始pH值、降低甲基橙的初始浓度、提高反应温度会提高体系甲基橙的光催化降解效果。在甲基橙的初始浓度为10~50μmol/L范围内,对甲基橙光降解浓度变化按照Langmuir-Hinshelwood动力学模式进行拟合,得出甲基橙的光降解规律为准一级反应。
[1] 张林生,蒋岚岚.染料废水的脱色方法 [J].化工环保,2000,20(1):14~18.
[2] 时桂杰.光催化氧化处理水中污染物的研究进展及发展趋势[J].环境科学与技术,1988,21(3):1~4.
[3] 程大莉,蒋身学,张齐生.化钛/竹炭符合材料的吸附——光催化降解苯酚的动力学研究[J].浙江林学院学报,2010,27(2):205~209.
[4] Ke D,Liu H,Peng T,et al.Preparation and photocatalytic activity of WO3/TiO2nanocomposite particles[J].Materials Letters,2008,62(3):447~450.
[5] Liu M,Da S-L,Feng Y-Q,et al.Study on the preparation method and performance of a newβ-cyclodextrin bonded silica stationary phase for liquid chromatography[J].Anal Chim Acta,2005(533):89~95.
[6] Zhan Xueyan,Song Dandan,Zeng Shengnian,et al.Progress in the study on TiO2photocatalytic osidation determiting organic pollutants[J].Chem Res Appl,2002,14(4):387.
[7] Mills A,Davies R H,Worsley D.Water purification by semiconductor photocatalysis[J].Chemical Society Reviews,1993,22(6):417~425.
[8] 段小月,刘伟于,艳艳卢,等.电吸附法去除水中刚果红的研究[J].环境污染与防治,2012,34(1):56~59.
[9] Tang W Z,Huren A.UV/TiO2photocatalytic oxidation of commercial dyes in aqueous solutions[J].Chemosphere,1995,31(9):4157~4170.
[10] So C M,Cheng M Y,Yu JC,et al.Degradation of azo dye Procion Red MX-5Bby photocatalytic oxidation[J].Chemosphere,2002,46(6):905~912.
[11] 赵德明,惠 祥.合纳米TiO2光催化氧化苯酚的动力学[J].中国给水排水,2004,20(1):48~49.
[12] Davide Vione,Juliana Feitosa-Felizzola,et al:phototransformation of clarithromycin in surface waters:kinetics,model predictions and degradation pathways[J].WaterResearch,2009(6):211~213.
[13] N Doucet,O Zahraa,Kinetics of the photocatalytic degradation of benzene[J].Catalysis Today,2007(122):168~177.

