纳氏试剂比色法测定水体中氨氮常见问题与处理办法
杨燕 陈静
(临沂市环境监测站,山东 临沂 276000)
1 纳氏试剂的正确配制,影响方法的灵敏度
纳氏试剂由Nessler于1856年发明,有2种配制方法,常用HgCl2与KI反应的方法配制,其反应过程如下:

显色基团为[HgI4]2-,它的生成与I-浓度密切相关。开始时,Hg2+与I-按反应(1)式生成红色沉淀HgI2,迅速与过量I-按反应(2)式生成[HgI4]2-淡黄色显色基团;当红色沉淀不再溶解时,表明I-不再过量,应立即停止加入HgCl2,此时可获得最大量的显色基团。若继续加入HgCl2,反应(3)式和(4)式就会显著进行,促使显色基团不断分解,同时产生大量HgI2红色沉淀,从而引起纳氏试剂灵敏度的降低。
按照国家标准,纳氏试剂有2种配制方法,第一种方法利用KI、HgCl2和KOH配制,第二种方法利用KI、HgI2和KOH配制。两种方法均可产生显色基团[HgI4]2-,一般常用第一种方法配制。依据上述纳氏试剂配制反应原理,根据反应方程(5)式和(6)式我们得出HgCl2与KI的最佳用量比为0.41∶1(即82gHgCl2溶于20gKI溶液),以此比例配制的纳氏试剂经多次实验检验,灵敏度均能达到实验要求。配制过程中,HgCl2一般溶解较慢,为加快反应速度,节省反应时间,可在低温加热中进行配制,还可防止HgI2红色沉淀提前出现。
2 正确了解酒石酸钾钠掩蔽原理,正确配置可提高实验的准确度。
水体中常见金属离子有 Ca2+、Mg2+、Fe2+、Mn2+等,若含量较高,易与纳氏试剂中OH-或I-反应生成沉淀或浑浊,影响比色。因而在加入纳氏试剂前,需先加入酒石酸钾钠,以掩蔽这些金属离子,其掩蔽原理如下:
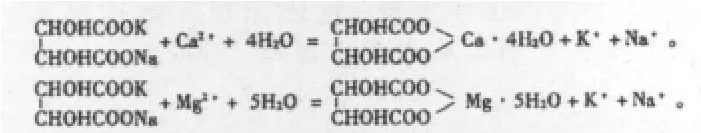
若向过滤后的实际水样中加入酒石酸钾钠出现浑浊,但标准曲线组却未出现浑浊的现象,这与酒石酸钾钠试剂不合格有关,非水样干扰问题。当酒石酸钾钠试剂中含有较多Ca2+、Mg2+杂质时,与实际水样中 Ca2+、Mg2+共同反应,生成较多量的酒石酸钙或酒石酸镁,从而析出使过滤水样变浑浊;由于蒸馏水中Ca2+、Mg2+痕量,因此未出现浑浊现象,此时应更换酒石酸钾钠试剂,重新测定。
酒石酸钾钠配制方法较为简单,但对于不合格试剂,由于铵盐含量较大,只靠加热煮沸并不能完全除去,可采取以下2种方法:1、向定容后的酒石酸钾钠溶液中加入5ml纳氏试剂,沉淀后取上层清液使用。2、向酒石酸钾钠溶液中加少量碱,煮沸蒸发至50ml左右后,冷却并定容至100ml。我们认为,第二种方法优于第一种方法,即使铵盐含量很高的酒石酸钾钠,经处理后空白值也能满足实验要求。
3 商品试剂纯度以及实验用品的纯净度能够较大的影响氨氮实验的测定
3.1 商品试剂纯度
纳氏试剂比色法实验所用试剂主要有KNaC4H6O6.4H2O、KI、HgCl2、KOH。某些市售分析纯试剂常达不到要求,甚至部分地区、部分厂家出产的优级纯也达不到实验要求,从而给实验造成较大影响,其中影响实验结果的试剂主要是KNaC4H6O6.4H2O和HgCl2。
不合格酒石酸钾钠会导致实验空白值高和实际水样浑浊,影响测定。不纯试剂从外观上难以鉴别,只有通过预实验检验才能判定是否符合要求。
HgCl2为无色结晶体或白色颗粒粉末,变质的HgCl2试剂常见红色粉末夹杂其中。若试剂中含有少量红色粉末的试剂还可使用,但仍要避免称取红色粉末配制反应试剂。
3.2 滤纸对空白值的影响,适当选用滤膜过滤
氨氮实验需将水样过滤后测定,所以实验还需做过滤空白对照实验,以扣除滤纸影响。由于滤纸一般都含有铵盐,因而可引起过滤空白值升高。有实验表明,不同滤纸或同种滤纸但不同张之间铵盐含量差别很大,有些含量较高的滤纸虽多次用水洗涤,但仍达不到实验要求。因此使用前需对每一批次滤纸进行抽检,淋洗时要少量多次。我们选用经稀HCl浸泡并洗净的0.45μm醋酸乙酯纤维滤膜过滤水样,解决了用滤纸过滤产生的高空白问题。不仅过滤空白值低,而且重复性好,所以推荐使用滤膜过滤。
4 反应条件控制影响实验的最终结果
4.1 反应温度对实验的影响
温度影响纳氏试剂与氨氮反应的速度,并显著影响溶液颜色。实验表明,反应温度为25℃时,显色最完全;5℃~15℃吸光度无显著改变,但其显色不完全;当温度达30℃时,溶液褪色,吸光度出现明显偏低现象。因而实验显色温度应控制在20℃~25℃,以保证分析结果的可靠性。
4.2 反应时间对实验的影响
实验表明,反应时间在10分钟之前,溶液显色不完全;10~30分钟颜色较稳定;30~45分钟颜色有加深趋势;45~90分钟颜色逐渐减褪。因而,用纳氏试剂光度法测定水中氨氮时,显色时间应控制在10~30分钟,以尽快的速度进行比色,达到分析的精密度和准确度。
4.3 反应体系PH对实验的影响
由氨氮反应原理可知,OH浓度影响反应平衡。水样PH的变化对颜色的强度有明显影响,水样呈中性或碱性,得出的测定结果相对偏差符合分析要求,呈酸性的水样无可比性,所以对于废水样应特别注意调节体系的pH值,最好将溶液显色PH控制在11.8~12.4,以保证结果的精密度和准确度。PH太低时,显色不完全,过高时溶液会出现浑浊,当PH为13时显色较完全,且不产生浑浊,因此溶液PH值宜选为13。
5 样品的稀释
纳氏试剂光度法测定氨氮,当水样氨氮浓度大于2.0mg/L时,则需将水样稀释后测定,称为“事前稀释”。这种稀释方法相对准确,但测定前不好预料,不利于大批量样品的及时分析。另一种稀释方法是直接将显色后的样品进行稀释比色,称为“事后稀释”。对于难以预料的超出浓度测定线性范围含量的含氨氮废水样品,用2种稀释方法得到的对比实验结果,相对误差满足环境监测分析要求。对比结果还表明,若用无氨水作稀释溶剂,事后稀释以负误差居多,但配制一定量的空白溶液作稀释溶剂可抵消一部分负误差。
小结
由实验和讨论可知,纳氏试剂光度法测定氨氮应注意和解决5种常见问题:(1)试剂的正确配制决定着方法灵敏度,特别要注意理解纳氏试剂配制原理,正确掌握纳氏试剂配制要领。(2)对配置试剂的纯度和过滤滤纸要注意检查。(3)反应条件,如温度、时间、体系PH决定反应速度、反应平衡和反应生成物的稳定性,应控制反应在最佳条件下进行。(4)水体中溶解态无机或有机物以及不溶态悬浮物对纳氏试剂光度法测定氨氮均有干扰,应根据不同情形选择不同方法加以消除,特别应注意酒石酸钾钠掩蔽失效现象。(5)对于超过检测上限含量水样的稀释测定问题,因事前、事后稀释2种方法相对误差均满足分析要求,对于大批量测定情况,可采取事后稀释测定。
[1]朱学君.水中氨氮的测定方法小结及结果分析.聊城市环境监测中心[J].科技信息,2008-09-20.
[2]林建国.用去离子水替代无氨水测定氨氮的研究.柳州职业技术学院[J].安徽农业科学,2008-03-20.

