艾迪注射液联合FOLFOX 4方案治疗复发转移性大肠癌的疗效观察
刘 威 钟小溱 王科明 王朝霞 王继荣
1.南京医科大学第二附属医院普外科,江苏南京 210011;2.南京医科大学第二附属医院肿瘤科,江苏南京 210011
艾迪注射液联合FOLFOX 4方案治疗复发转移性大肠癌的疗效观察
刘 威1钟小溱1王科明2王朝霞2王继荣2
1.南京医科大学第二附属医院普外科,江苏南京 210011;2.南京医科大学第二附属医院肿瘤科,江苏南京 210011
目的观察和比较艾迪注射液联合FOLFOX4(亚叶酸钙+氟尿嘧啶+奥沙利铂)方案与单纯FOLFOX4方案治疗转移性或复发性晚期大肠癌的疗效及毒副反应。 方法将经病理组织学及影像学确诊为转移性或复发性晚期大肠癌患者108例作为研究对象,将其分为艾迪注射液联合FOLFOX4方案组 (联合治疗组)56例及单纯FOLFOX4方案组(对照组)52例。每例患者至少治疗2个周期进行疗效评价。 结果联合治疗组可评价疗效56例:完全缓解(CR)2例,部分缓解(PR)22 例,稳定(SD)24 例,有效率为 42.86%,临床获益率(CR+PR+SD)为 85.71%,疾病进展时间(TTP)为(8.4±0.2)个月,中位生存期(MST)为 15.6 个月;对照组可评价疗效 52 例:CR 1 例,PR 18 例,SD 21 例,有效率为36.54%,CR+PR+SD 为 76.92%,TTP 为(7.9±0.6)个月,MST 为 14.9个月;两组疗效比较差异无统计学意义(P > 0.05)。联合治疗组生活质量Karnofsky评分提高率为78.57%,对照组提高率为55.69%,两组比较差异有统计学意义(P<0.05)。联合治疗组白细胞减少的发生率、消化道反应(恶心呕吐、腹泻)发生率显著少于对照组(P<0.05)。 结论复发转移性大肠癌使用FOLFOX4方案化疗时加用艾迪注射液,虽在临床疗效上未见明显提高,但患者的化疗不良反应明显减轻。
艾迪注射液;大肠癌;化疗;减毒
大肠癌是世界上最常见的恶性肿瘤之一。由于生活方式、饮食结构等因素的改变,大肠癌在我国发病率呈上升趋势。无法手术切除、复发或转移的大肠癌患者,5年生存率仍低于10%。化疗是复发或转移性大肠癌的主要治疗手段,以化疗为主的综合治疗对于这部分患者延长生存期起着重要作用[1]。复发或转移性大肠癌主要以全身化疗为主,过去几十年中大肠癌化疗的主要药物是氟尿嘧啶,从20世纪90年代后期随着奥沙利铂、伊立替康等新药的问世,大肠癌患者的疗效和生存率明显提高。化疗,特别是联合化疗不良反应较重,会影响化疗如期进行。有文献报道,中药制剂艾迪注射液能减轻化疗的不良反应。2007年1月~2010年12月56例复发、转移性大肠癌患者在FOLFOX4方案化疗同时加用艾迪注射液,监测患者临床疗效,动态观察恶心、呕吐、腹泻、骨髓、肝肾功能等,观察终点对数据整理分析,现总结如下:
1 资料与方法
1.1 纳入标准
①细胞学或病理诊断为大肠癌;②体能状况KPS≥60分;③有明确观察指标;④预期生存时间≥3个月;⑤无重要器官功能严重损害,心电图、肝肾功能及血常规正常,无化疗禁忌。此临床观察经南京医科大学第二附属医院伦理委员会审查通过,所有患者均知情同意。
1.2 一般资料
选择2007年1月~2010年12月我院收治的不能手术及术后复发、转移的大肠癌108例,男58例,女50例;年龄32~76岁,中位年龄65岁;结肠癌68例,直肠癌40例;其中86例有多个器官转移,转移部位:肝脏32例,肺18例,骨10例,远处淋巴结 22例,腹盆腔 20例,其他 5例;初治62例,复治46例。将108例患者分为联合治疗组和对照组,两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性,见表1。
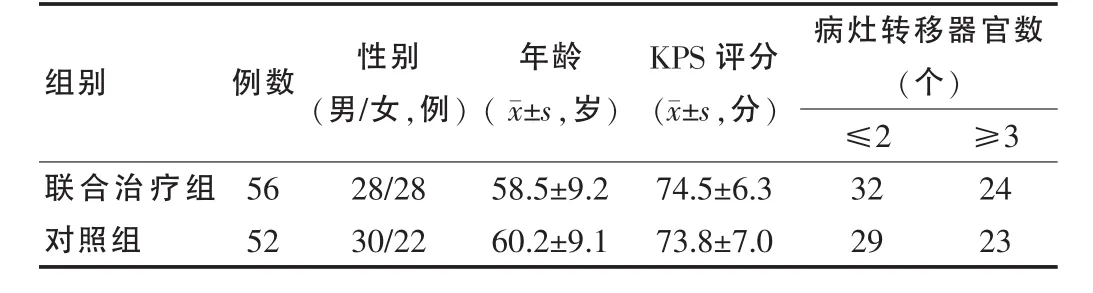
表1 两组患者一般资料比较
1.3 方法
联合治疗组:艾迪注射液(贵州益佰制药股份有限公司,10 mL×5 支,批准文号:国药准字 Z52020236)50~80 mL,静脉滴注,d1~10。 FOLFOX4:奥沙利铂(OXA)85mg/m2,静脉滴注2 h,d1;四氢叶酸钙(LV)200 mg/m2,静脉滴注 2 h,d1~2;氟尿嘧啶(5-Fu)400mg/m2,静脉注射,600mg/m2持续静脉泵入22 h,d1~2。14 d 重复。28 d 为 1 个周期。对照组:仅用 FOLFOX4。每完成2个周期化疗后评定疗效,所有患者均至少完成2个周期。托烷司琼或格拉司琼止吐,用药期间叮嘱患者忌冷食冷饮,忌接触冷物,注意手足保暖,减少对末梢神经的副作用。每周期化疗前后均检查血、尿、便常规、肝肾功能、心电图等。
1.4 疗效评定标准
在化疗前、化疗结束后1个月,行CT、MRI、B超等确定并测量病灶大小。采用实体瘤疗效评价标准(RECIST)[2]评定疗效:完全缓解(CR)、部分缓解(PR)、稳定(SD)与进展(PD)。临床有效率RR=CR+PR,临床获益率CBR=CR+PR+SD。治疗前后KPS评分变化依据WHO标准评定:上升≥10分为好转,无增减为稳定,减少≥10分为恶化,总有效率=好转+稳定。不良反应按WHO不良反应分级标准判断,分为0~Ⅳ度[3]。
1.5 统计学方法
采用SPSS 15.0软件进行统计分析,计量资料采用成组设计t检验,以及采用Kaplan-Meier方法进行生存分析。计数资料的比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组近期疗效及KPS评分比较
两组患者各自完成2~6个周期,均能评价疗效。联合治疗组 56例,其中 CR 2例(3.57%),PR 22 例(39.29%),SD 24例(42.86%),PD 8例 (14.29%),RR 为 42.86%,CBR 为85.71%;疾病进展时间(TTP)为(8.4±0.2)个月,中位生存期(MST)为15.6个月。单独化疗对照组52例,CR 1例(1.92%),PR 18例(34.62%),SD 21 例 (40.38%),PD 12 例 (23.08%),RR 为36.54%,CBR为 76.92%;TTP 为(7.90±0.55)个月,MST 为14.9 个月。两组间比较差异无统计学意义(P>0.05)。见表2。两组患者治疗后症状均有改善,Karnofsky评分比较:联合治疗组总有效率为78.57%,对照组总有效率为55.69%,差异有统计学意义(P < 0.05)。 见表 3。
2.2 不良反应
两组患者共完成化疗432个周期,联合治疗组224周期,平均完成4.0个周期,对照组208周期,平均完成4.0个周期。两组毒副反应发生情况见表4。
3 讨论
大肠癌是国内外常见的恶性肿瘤,由于生活方式及饮食结构等因素的改变,其发病率逐年上升,其中约80%为进展期大肠癌。化疗是不能手术、转移及复发大肠癌的主要治疗手段。FOLFOX4为治疗晚期大肠癌的一线化疗方案[4]。但化疗的毒副反应如恶心、呕吐、白细胞下降、血小板下降、腹泻、神经毒性、肝肾功能损害等,往往使肿瘤患者对化疗的依从性和耐受性明显下降,因此着眼于提高化疗疗效的同时,需寻求减轻不良反应的有效措施[5]。

表2 两组疗效比较[n(%)]

表3 两组KPS评分比较(例)
纯中药制剂艾迪注射液主要成分有去甲斑蝥素、人参、刺五加、黄芪。斑蝥素有破血散结、攻毒蚀疮的功用,可抑制肿瘤新生血管形成;抑制癌细胞DNA和RNA的生物合成,从而抑制癌细胞的生长分裂,诱导肿瘤细胞凋亡;同时能逆转多药耐药。另外含有的斑蝥酸钠还可促进骨髓造血干细胞向粒-单核细胞分化,从而提升白细胞[6-7]。化疗同时加用艾迪注射液不仅联合抗癌,艾迪还促进骨髓造血干细胞分化、成熟,促进粒细胞的释放,对骨髓具有保护作用。人参皂苷和刺五加多糖有补气安神、扶正固本的功效,能增强NK、LAK和巨噬细胞的活性,诱导IL、TNF及IFN等细胞因子产生,从而提高免疫力。另外一种重要成分是黄芪多糖,具有补气健脾的功效,具有较强的解毒功能,可增强淋巴细胞增生,增强T细胞抗肿瘤活性[8-10]。
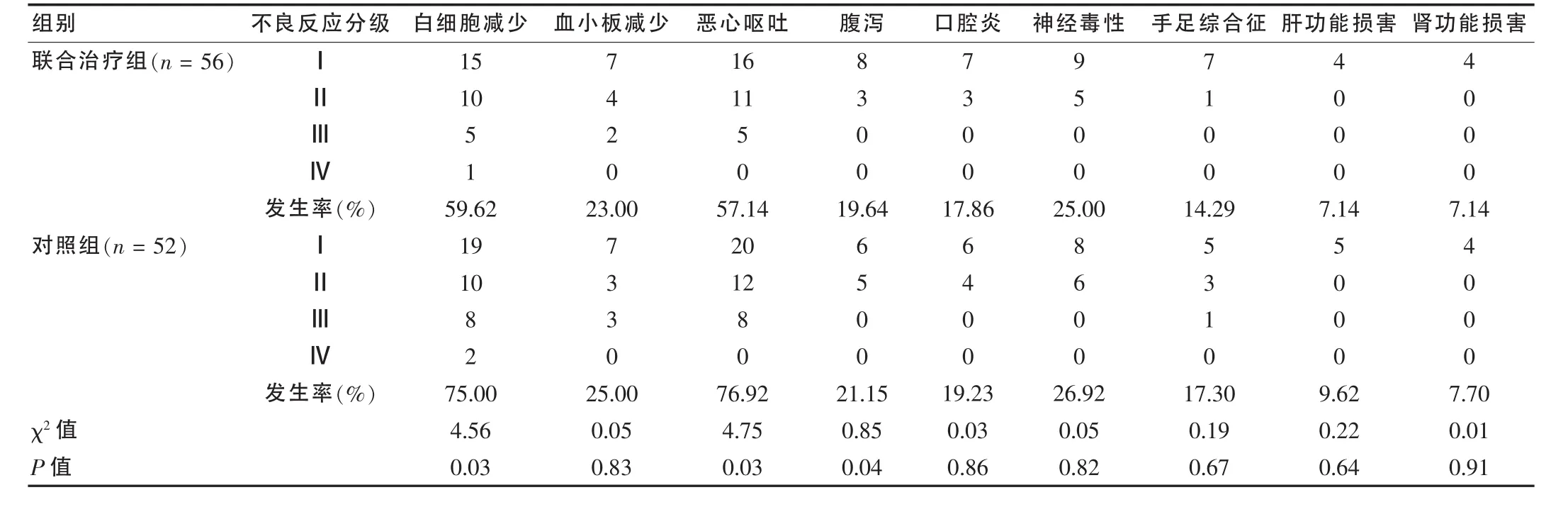
表4 两组毒副反应比较(例)
本研究应用艾迪注射液联合FOLFOX4化疗,结果显示,联合治疗组在CBR、TTP、MST方面略优于对照组,但无统计学差异;临床有效率高于对照组,但差异不明显;不过在改善生活质量KPS评分、胃肠道反应及白细胞下降等方面,联合治疗组明显好于对照组,两组间差异有统计学意义(P<0.05)。由此认为,艾迪注射液联合FOLFOX4化疗,可减轻大肠癌患者化疗所引起的恶心、呕吐、厌食及腹泻等胃肠道反应,同时能维持白细胞稳定,使患者生活质量改善,精神状况明显好转,提高患者化疗耐受性及治疗信心,且毒副作用轻微,使用安全、方便,值得临床推广使用。
[1]Chibaudel B,Tournigand C,AndréT,et al.Therapeutic strategy in unresectablemetastatic colorectal cancer[J].Ther Adv Med Oncol,2012,4(2):75-89.
[2]Fabel M,Wulff A,Heckel F,et al.Clinical lymph node staging influence of slice thickness and reconstruction kernel on volumetry and RECIST measurements[J].Eur JRadiol,2012,81(11):3124-3130.
[3]孙燕.内科肿瘤学[M].北京:人民卫生出版社,2001:90.
[4]Simpson D,Dunn C,Curran M,et al.Oxaliplatin:a review of its use in combination therapy for advanced metastatic colorectal cancer[J].Drugs,2003,63(19):2127-2156.
[5]周际昌.实用肿瘤内科学[M].北京:人民卫生出版社,2003:555.
[6]周英武,彭桂英,葛东宇,等.人参皂苷Rg1对BALB/c小鼠免疫调节作用的实验研究[J].中华中医药杂志,2011,26(5):1232-1234.
[7]宋斌,万楚成,李章志,等.艾迪注射液联合VAD方案治疗老年多发性骨髓瘤的临床研究[J].中国医药导报,2012,9(7):69-70,80.
[8]王鸿彪,林英城.人参皂甙Rg3抗肿瘤作用研究进展[J].医学综述,2009,15(3):323-326.
[9]刘明华,任美萍,陈健平,等.黄芪皂苷抗肿瘤活性研究[J].中药药理与临床,2009,25(2):68-70.
[10]杜佳新,顾玉红,张博,等.刺五加有效成分的抗肿瘤作用研究与评价[J].中国医院用药评价与分析,2010,10(3):199-200.
Observation of curative effect on Aidi Injection in combination w ith FOLFOX4 regimen chemotherapy in the treatment of patientsw ith advanced colorectal cancer
LIUWei1 ZHONG Xiaoqin1 WANG Keming2 WANG Zhaoxia2 WANG Jirong2
1.Department of General Surgery,the Second Affiliated Hospital of Nanjing Medical University,Jiangsu Province,Nanjing 210011,China;2.Department of Oncology,the Second Affiliated Hospital of Nanjing Medical University,Jiangsu Province,Nanjing 210011,China
Objective To observe and compare the efficacy and toxicity of Aidi Injection in combination with FOLFOX4 regimen (L-OHP plus 5-Fu/Lv)and FOLFOX4 regimen in the treatment of patients with advanced colorectal cancer.Methods108 patientswith advanced colorectal cancer diagnosed pathologically and imageology were divided into 56 cases ofAidi Injection in combinationwith FOLFOX4 regimen group(coalition group)and 52 casesof FOLFOX4 regimen group(control group).Each patient was given at least 2 cycles and the efficacy and toxicity were then evaluated.Results56 cases could be evaluated in coalition group:there were 2 cases of CR,22 cases of PR,24 cases of SD,the effective rate was 42.86%,CR+PR+SD was 85.71%,TTPwas(8.4±0.2)months,MSTwas 15.6months;52 cases could be evaluated in control group:there were 1 case of CR,18 cases of PR,21 cases of SD,the effective rate was 36.54%,CR+PR+SD was 76.92%,TTP was(7.9±0.6)months,MST was 14.9 months.In coalition group,the overall response rate was 41.07%and thatwas 36.54%in control group.The difference of effect between the two groupswas insignificant(P>0.05).Karnofsky score increase rate of life quality in coalition group was 78.57%and thatwas 55.69%in control group,with significant difference(P<0.05).The incidence rates of leucopenia,gastrointestinal reaction,hepatotoxicity and renal toxicity in coalition group were significantly lower than those in control group(P<0.05).ConclusionAidi Injection can reduce toxic effects of FOLFOX4 regimen chemotherapy while enhancing patients'tolerance to chemotherapy and improving patients'quality of life.
Aidi Injection;Colorectal cancer;Chemotherapy;Attenuation
R735.35
A
1673-7210(2012)12(a)-0080-03
江苏省卫生厅科研项目资助(课题编号:H200913);江苏省高等学校大学生实践创新训练计划项目。
刘威(1989-),男,汉族,江苏盐城人,住院医师;研究方向:消化道肿瘤的综合治疗。
王继荣(1972-),女,汉族,江苏海安人,南京医科大学2010级劳动卫生与环境卫生学在读博士研究生,副主任医师;研究方向:消化道肿瘤的基础与临床研究。
2012-09-26 本文编辑:张瑜杰)

