大剂量复方苦参注射液联合化疗治疗晚期非小细胞肺癌疗效观察
于振刚,王炳辙(潍坊市人民医院呼吸内科,山东潍坊 261041)
肺癌是常见的恶性肿瘤,发病率呈逐年增高的趋势。很多患者诊断出非小细胞肺癌(non-small-cell lung cancer,NSCLC)时,多属晚期而失去手术治疗的最佳时机。现对2010年1月—2011年8月在我科收治的90例晚期NSCLC患者采用大剂量复方苦参注射液联合吉西他滨+卡铂(GC)方案对稳定瘤体、缓解疼痛、减轻不良反应、改善Karnofsky评分方面进行观察、比较,现报道如下。
1 资料与方法
1.1 临床资料
选择呼吸科2010年1月—2011年8月确诊的晚期NSCLC患者共90例,所有患者均为初诊,血常规、肝肾功能及心电图检查正常,Karnofsky评分≥60分,预计生存期超过2个月,有可测量的病灶,可以评价近期疗效,经伦理委员会同意,患者或家属签署知情同意书。以随机抽样法分为治疗组(复方苦参注射液联合GC方案化疗)和对照组(单纯GC方案化疗),其中治疗组50例,男性30例,女性20例,年龄40~78岁,中位年龄56岁;鳞癌30例,非鳞癌20例,Ⅲ期32例,Ⅳ期18例。对照组40例,男性25例,女性15例,年龄43~76岁,中位年龄58岁;鳞癌28例,非鳞癌12例;Ⅲ期25例,Ⅳ期15例。所有患者神智清楚,治疗合作,能够准确描述疼痛症状。治疗组50例患者中,轻度疼痛20例,中度疼痛18例,重度疼痛12例;对照组40例患者中,轻度疼痛16例,中度疼痛13例,重度疼痛11例。
1.2 治疗方法
2组均采用GC方案化疗,具体用量及用法为:吉西他滨1 000 mg·m-2,静脉注射,d1~8;卡铂 300 mg·m-2,d1。以上为第1周期用药,第2周期后进行疗效评定。治疗组在化疗同时应用复方苦参注射液(山西振东制药有限公司生产)20 mL静脉滴注,每日1次,连用14 d,休息14 d后复查血常规、肝功能(ALT及AST、胆红素、白蛋白)、肾功能(肌酐、尿素氮、尿酸)正常,进行第2个疗程治疗,2个疗程后进行疗效评定。
1.3 评判标准
1.3.1 实体瘤疗效评价:每化疗2个周期后复查增强CT检查,测量原发灶或转移灶大小。采用世界卫生组织(WHO)实体瘤疗效评价标标准[1]判定:完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD),并观察2组中位无疾病进展时间(progressionfree survival,PFS)。
1.3.2 疼痛程度:按照WHO数字疼痛分级法(NRS)[2]评估疼痛程度:1~3分为轻度疼痛,4~7分为中度疼痛,8~10分为重度疼痛。疼痛缓解疗效评价:完全缓解(CR)为治疗后完全无痛;部分缓解(PR)为疼痛较给药前明显减轻,睡眠基本上不受干扰,能正常生活;轻度缓解(MR)为疼痛较给药前减轻,但仍感明显疼痛,睡眠仍受干扰;无效(NR)为与治疗前比较无减轻。CR+PR+MR为有效病例。
1.3.3 不良反应:按照WHO《抗癌药物急性及亚急性毒性分级标准》中的0~Ⅳ度评定毒性[3]。
1.3.4 生存质量:以Karnofsky功能状态评分标准为指标,凡治疗后Karnofsky评分提高10分以上者为有效,下降10分或以上者为无效(恶化),介于两者之间者为稳定[4]。
1.4 统计学处理
使用SPSS 13.0统计软件进行分析,计量资料采用t检验,计数资料以率表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 疗效评价
治疗组完全缓解9例,部分缓解22例,稳定13例,进展6例;对照组完全缓解4例,部分缓解10例,稳定16例,进展10例。2组疗效比较,χ2=6.48,P<0.05,差异有统计学意义,治疗组优于对照组;2组PFS比较,t=3.73,P<0.01,差异有统计学意义,治疗组优于对照组,见表1。
表1 2 组临床疗效比较[例(%),]Tab1 Comparison of clinical efficacy between two groups[cases(%),]
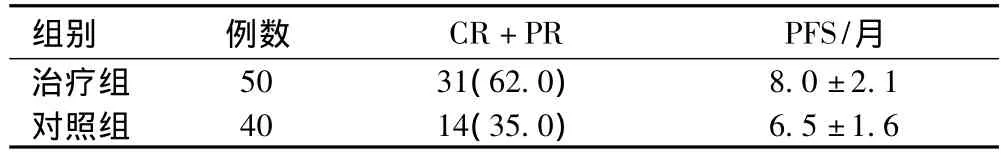
表1 2 组临床疗效比较[例(%),]Tab1 Comparison of clinical efficacy between two groups[cases(%),]
2.2 疼痛缓解程度
治疗组疼痛完全缓解12例,部分缓解25例,轻度缓解12例,无效1例。对照组疼痛完全缓解4例,部分缓解9例,轻度缓解17例,无效10例。2组疼痛缓解有效率比较,χ2=8.92,P<0.01,差异有统计学意义,治疗组明显优于对照组;2组每日疼痛频率、持续时间及应用镇痛药次数比较,治疗组均低于对照组,差异有统计学意义,见表2、3。

表2 2组疼痛缓解有效率比较[例(%)]Tab2 Comparison of effective rate in pain relief between two groups[cases(%)]
表3 2组疼痛评分及疼痛缓解具体情况()Tab3 Comparison of pain scores and pain relief between two groups()
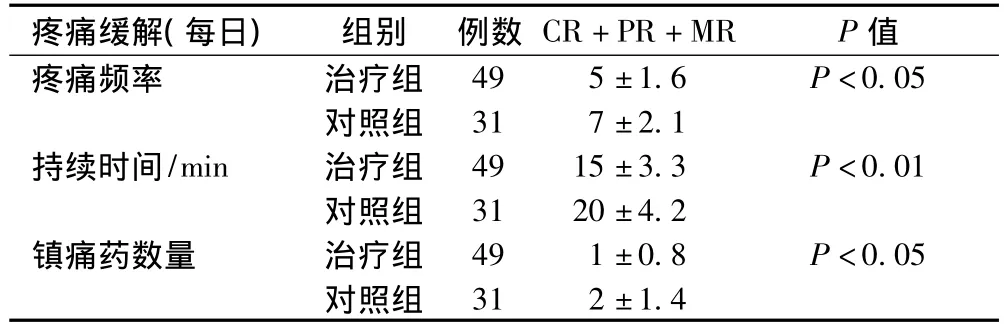
表3 2组疼痛评分及疼痛缓解具体情况()Tab3 Comparison of pain scores and pain relief between two groups()
2.3 不良反应
主要不良反应为Ⅰ~Ⅱ度的消化道反应和骨髓抑制,2组均以白细胞计数、血小板计数下降为主,2组比较,差异有统计学意义(χ2=6.75,P <0.05;χ2=11.48,P <0.01);血红蛋白有所下降,但2组比较,差异无统计学意义(χ2=2.72,P>0.05);消化道反应以恶心、呕吐、腹泻、便秘为主,治疗组较对照组发生率低,差异有统计学意义(χ2=4.72,P<0.05;χ2=10.3,P<0.01);肝、肾损害方面,治疗组较对照组发生率低,差异有统计学意义(χ2=4.69,P <0.05),见表4。
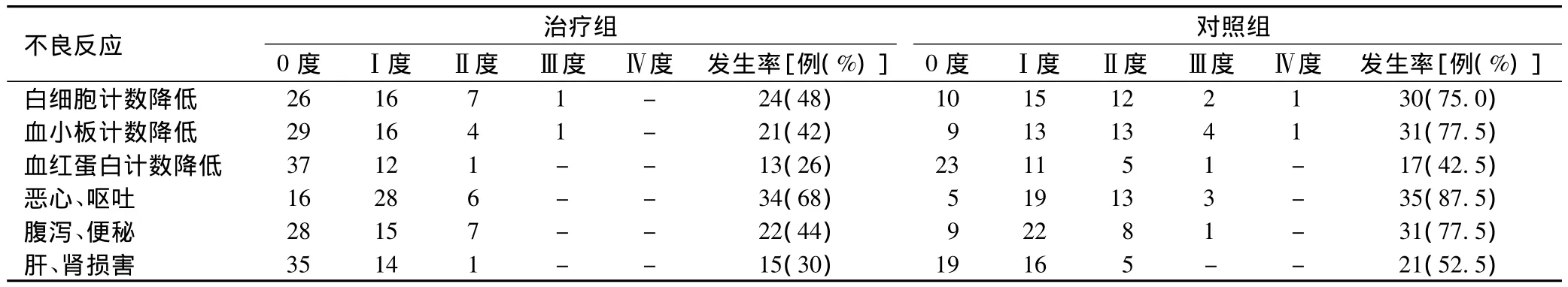
表4 2组不良反应比较(例)Tab4 Comparison of adverse reactions between two groups(cases)
2.4 生活质量改善
生活质量改善方面,治疗组有效27例,稳定19例,无效4例;对照组有效 13例,稳定 17例,无效10例。治疗组Karnofsky评分升高例数较对照组明显增多,有效率分别为54%和32.5%(χ2=4.16,P<0.05),有效 +稳定率分别为 92%和75%(χ2=4.89,P <0.05),差异均有统计学意义,见表5。
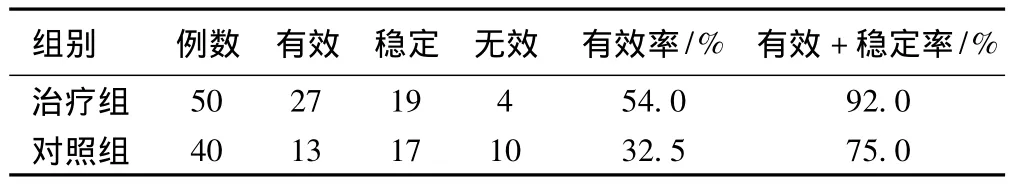
表5 2组Karnofsky评分变化比较(例)Tab5 Comparison of Karnofsky score changes between two groups(cases)
3 讨论
全身化疗是肺癌晚期主要治疗手段之一,但化疗药的诸多不良反应影响治疗效果。本研究中,吉西他滨是一种胞嘧啶核苷衍生物,属周期特异性抗肿瘤药,主要作用于G1/S期,具有自我增效作用,作为第3代化疗药,对NSCLC的单药有效率高达20% ~24%,本实验联合卡铂有效率可达28%,但同时可加重骨髓抑制,限制了其的使用剂量,同时也限制了患者的化疗获益[5]。如何减少化疗不良反应、提高疗效、改善生活质量、延长生存期,是临床上经常遇见的问题。
复方苦参注射液是以苦参和白土苓为原料提炼而成。苦参清热燥湿解毒,白土苓解毒祛湿,二者合用可以解毒利湿、健脾扶正,其抗肿瘤作用机制有:(1)接杀伤肿瘤细胞;(2)直接作用于靶细胞的DNA而发挥抗肿瘤作用;(3)通过影响细胞周期而发挥抗肿瘤作用;(4)可以诱导肿瘤细胞产生凋亡[6]。有研究表明,复方苦参注射液在术后治疗及联合化疗、放疗治疗肿瘤方面均具有抑制肿瘤、缓解癌痛、降低放化疗毒性、改善生活质量的功效,是一种高效的纯中药抗肿瘤制剂[7]。实验研究发现,复方苦参可通过下调抑凋亡基因Bcl-2、上调促凋亡基因Bax的表达,诱导A549和SMMC-7721细胞的凋亡,并可减少肿瘤细胞VEGF-A的分泌,抑制其迁徙及生长能力[8];有临床试验显示,以苦参碱为主要组方的抗肿瘤抗生素A(ACAPHA)可明显降低食管癌者的肿瘤增生,亦可不同程度地减少化学诱导肺肿瘤多样性及瘤负荷[9]。我们观察大剂量复方苦参注射液联合GC方案治疗晚期NSCLC取得了较好的临床疗效,有效率达62%,与对照组比较疗效显著。
WHO推荐的《癌症三阶梯止痛治疗原则》,由于其长期使用的不良反应大、依赖性强,使得疗效受到限制。对苦参碱镇痛作用构效关系的研究提示,苦参碱l位的氨基基团是其具有镇痛作用的关键,可以通过投射到脊髓的下行抑制性强啡肽能神经元激动脊髓上的Κ受体,从而发挥其镇痛作用,另外可能与影响Ca2+内流和减少NO生成,发挥镇痛作用[10]。通过热板法、酸刺激扭体法实验[10,11],结果表明复方苦参注射液可作用于中枢起明显的镇痛作用,强度与盐酸哌替啶(杜冷丁)相似;电刺激法实验表明,复方苦参可使小鼠的疼痛阈值显著提高。本实验发现大剂量复方苦参注射液在缓解癌性疼痛方面效果显著,可明显降低癌性疼痛频率,缩短癌性疼痛持续时间,并可减少镇痛药的应用;可减轻化疗的不良反应,明显提高患者的Karnofsky评分,不仅适用于轻、中度癌性疼痛[12],亦可作为重度癌性疼痛患者的辅助用药,尤其适用于晚期或终末期癌性疼痛患者,本文与有些研究[13,14]结果类似。
复方苦参注射液说明书中的参考剂量为12 mL·d-1,200 mL为1个疗程。有研究提示,增大剂量能显著提高其抑制肿瘤和缓解疼痛的功效,然而剂量超过30 mL·d-1时,会出现寒战、发热等不良反应[15]。本研究结果表明,复方苦参注射液按照20 mL·d-1的剂量给药,不仅有良好的治疗效果,且不良反应少见,与诸多学者的研究结果类似[12,13]。但亦有学者应用复方苦参注射液60 mL加入5%葡萄糖注射液500 mL中静脉滴注,每日1次,未发现明显不良反应,分析其原因可能与患者应用复方苦参注射液的总疗程时间短有关[16]。本研究基于晚期NSCLC患者的姑息治疗,以安全为首要考虑因素,采用20 mL·d-1的大剂量给药,可辅助提高晚期NSCLC的化疗疗效,明显缓解疼痛,减轻化疗不良反应,改善患者的一般状况,提高生活质量,且无明显不良反应,提高患者的临床获益。但因本研究所选病例数相对少,临床观察时间较短,远期疗效尚不明确,有关复方苦参注射液在临床上能否应用更大的剂量与疗程,尚需进一步的临床观察。
[1]孙 燕,石远凯.临床肺癌内科手册[M].第5版.北京:人民卫生出版社,2007:147-156.
[2]闫康鹏,罗华友.癌性疼痛的治疗现状及展望[J].昆明医学院学报,2009,S2:108.
[3]孙 燕.临床肿瘤内科手册[M].第3版.北京:人民卫生出版社,1996:23-45.
[4]刘姣林,纳木恒,张 瑾.复方苦参注射液对肺癌化疗中减毒增效作用的临床观察[J].中国肿瘤临床与康复,2011,18(2):162.
[5]陆新岸.复方苦参注射液联合同步放化疗治疗局部晚期非小细胞肺癌30例[J].河北中医,2010,32(10):1542.
[6]李道睿,林洪生.大剂量复方苦参注射液治疗中晚期恶性肿瘤的有效性和安全性[J].中华肿瘤杂志,2011,33(4):291.
[7]Zhen Yang,Song Gao,Taijun Yin,et al.Biopharmaceutical and pharmacokinetic characterization of matrine as determined by a sensitive and robust UPLC-MS/MS Method[J].J Pharm Biomed Anal,2010,51(5):1120.
[8]Zhang Y,Zhang H,Yu P,et al.Effects of matrine against the growth of human lung cancer and hepatoma cells as well as lung cancer cell migration[J].Cytotechnology,2009,59(3):191.
[9]Gao G,Law FC.Physiologically based pharmacokinetics of matrine in the rat after oral administration of pure chemical and ACAPHA[J].Drug Metab Dispos,2009,37(4):884.
[10]侯延辉,彭晓冬.苦参碱类生物碱对中枢神经系统影响的研究现状[J].宁夏医科大学学报,2009,31(4):551.
[11]刘 安,魏 静,谭镇岳.复方苦参注射液缓解癌痛的临床与实验研究[J].吉林中医药,2005,25(6):54.
[12]陈小彬.复方苦参注射液联合化疗治疗晚期消化道肿瘤临床观察[J].当代医学,2009,15(12):59.
[13]王 娜,周雍明,杨宗艳.复方苦参注射液治疗80例老年晚期肺癌的临床疗效观察[J].中国医院用药评价与分析,2009,9(5):387.
[14]林明雄,曹 科,王艺璇,等.复方苦参注射液联合硫酸吗啡控释片治疗晚期癌痛的临床观察[J].中国医院用药评价与分析,2011,11(5):461.
[15]林丽珠,周岱翰,陈 瑶,等.复方苦参注射液对肺癌和肝癌细胞抑瘤作用研究[J].中药新药与临床药理,2009,20(1):21.
[16]刘宗亮,李亚峰.大剂量复方苦参注射液治疗非小细胞肺癌34例疗效观察[J].山东医药,2011,51(5):78.

