甲地孕酮联合格拉司琼预防化疗所致消化道反应的疗效观察
李春艳,张 芳,李庆云
(焦作市第二人民医院肿瘤内科,河南焦作454001)
在恶性肿瘤患者的化疗中,恶心呕吐是最常见的毒副反应,也是很多肿瘤患者惧怕化疗的原因之一。化疗诱发的恶心呕吐可引起代谢紊乱、营养失调、体能下降,不仅影响患者的生活质量,也常使化疗不能顺利进行。作者选择2009年1月至2010年12月收治的76例接受含顺铂、阿霉素及环磷酰胺联合化疗的恶性肿瘤患者,随机分为2组,比较甲地孕酮+格拉司琼+甲氧氯普胺与格拉司琼+甲氧氯普胺预防化疗所致恶心呕吐的效果。
1 资料与方法
1.1 一般资料 76例均为住院患者,入组标准:1)经组织病理学或细胞学证实为恶性肿瘤;2)KPS评分≥60分;3)入组时未接受激素类药物治疗;4)无严重心脏病、高血压、糖尿病史,无营养吸收障碍和血栓现象;5)血常规及肝、肾功能正常;6)预计生存期≥3个月;7)未接受肠内或肠外高营养;8)化疗前排除其他原因所致恶心呕吐。76例患者中,男性43例,女性33例;年龄25~78岁,中位年龄54岁;肿瘤类型:食管癌18例,乳腺癌17例,胃癌16例,肺癌16例,恶性淋巴瘤6例,卵巢癌3例。将76例患者随机分为治疗组和对照组,每组38例,2组患者在年龄、性别、病种、KPS评分比较差异均无统计学意义(P均>0.05)。所有患者治疗前均记录体质量和每天进食量。
1.2 方法
1.2.1 化疗方案 由于病种不同所用化疗方案也不同,所用化疗方案至少含有下列一种药物:1)DDP 60~80 mg·m-2(分 2~3 d给予);2)ADM 30~50 mg·m-2或EPI 50 ~80 mg·m-2;3)CTX 750 ~1 000 mg·m-2。如 PF、CAF、TA、ECF、NP、TP、CHOP、ABVD、CD、PD等方案,至少用2周期。同一患者2周期化疗方案及剂量相同。出现Ⅲ或Ⅳ度骨髓抑制时给予相应处理。
1.2.2 止吐方案 治疗组止吐方案:化疗前1天开始口服甲地孕酮160 mg·d-1,连续10 d;格拉司琼3 mg·d-1,化疗前20 min静脉注入 ;甲氧氯普胺20 mg·d-1,肌肉注射。对照组止吐方案:格拉司琼+甲氧氯普胺(剂量用法同治疗组)。每周期后对恶心呕吐和食欲变化情况进行评价,2周期后对KPS评分及体质量进行评价。
1.3 疗效评定标准 恶心:无,为0度;有,但不影响进食及日常生活为Ⅰ度;有恶心,并影响进食及日常生活为Ⅱ度;因恶心而卧床为Ⅲ度。呕吐:无,为0度;每天呕吐1~2次为Ⅰ度;每天呕吐3~5次为Ⅱ度;每天呕吐超过5次为Ⅲ度。末次化疗后24 h内出现的恶心呕吐为急性恶心呕吐;24 h以后出现的恶心呕吐为迟发性恶心呕吐;下周期化疗前出现的恶心呕吐为预期性恶心呕吐。进食量变化:治疗后每天进食量≥100 g为增加;日进食量变化<100 g为稳定;日进食量减少≥100 g为减少。
1.4 生活质量评估 依据KPS评分标准,治疗后KPS评分增加≥10分为改善,增加或减少<10分为稳定,减少≥10分为下降。
1.5 体质量评估 治疗后体质量增加≥5%为增加,增加或减少<5%为稳定,减少≥5%为下降。
1.6 统计学处理 用SPSS 13.0进行统计分析,计数资料比较采用χ2检验,检验水准α=0.05。
2 结果
2.1 止吐疗效 毎周期化疗后评价止吐效果,2周期后评价疗效。每组38例,2周期各76例次均可评价,治疗组Ⅱ度以上急性恶心、急性呕吐及迟发性恶心呕吐发生率分别为5.3%(4/76)、9.2%(7/76)及 6.6%(5/76);对照组Ⅱ度以上急性恶心、急性呕吐及迟发性恶心呕吐发生率分别为 23.7%(18/76)、28.9%(22/76)及21.1%(16/76)。2组比较差异均有统计学意义(P均<0.05)。对照组有2例在第2周期前出现预期性恶心呕吐。详见表1。
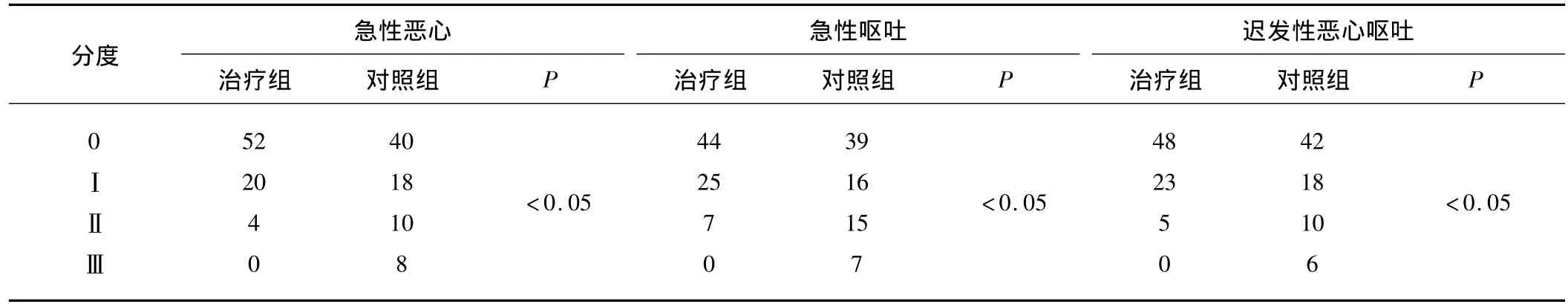
表1 2组患者止吐疗效比较
2.2 2组患者生活质量评估 治疗2周期后评价患者食欲、KPS评分及体质量变化情况。体质量增加2组比较差异无统计学意义(P>0.05),食欲及KPS评分增加2组比较差异均有统计学意义(P均<0.05)。详见表2。
2.3 毒副反应 2组患者毒副反应相近,便秘(3例及4例)、疲倦(各3例)、轻微头晕(各2例),未见锥体外系症状。治疗组有1例女性患者服用甲地孕酮后出现不规则阴道出血,1例出现血糖稍高,停药后渐恢复正常,不影响治疗。
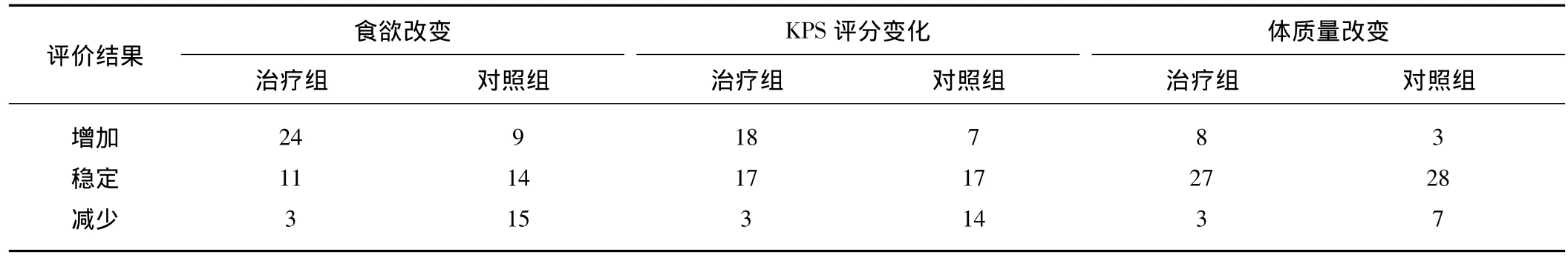
表2 2组患者生活质量比较例
3 讨论
化疗是治疗恶性肿瘤患者最常用、有效的方法,DDP、ADM及CTX是最常用的广谱抗肿瘤药物,且这3种药物为中、高度催吐风险药物,急性恶心呕吐发生率达30% ~100%[1-2]。化疗药物诱发恶心呕吐的机制非常复杂,目前尚不完全清楚,与以下因素有关:1)多数化疗药物可刺激胃肠道黏膜,引起黏膜损伤,导致黏膜上的嗜铬细胞释放5-HT3与5-HT3受体结合产生神经冲动,由迷走传入神经传入呕吐中枢导致呕吐;2)化疗药物及其代谢产物刺激催吐化学感受区 ,这两方面与急性呕吐有关;3)感觉、精神因子刺激大脑皮质通路,这是预期性呕吐的重要机制;4)迟发性呕吐可能与P物质介导有关,P物质通过结合神经激肽1(NK-1)受体致吐[3]。NK-1受体拮抗剂阿瑞吡坦对迟发性呕吐有突出作用[4],但该药在我国尚未上市。格拉司琼是一种高选择性的5-HT3受体拮抗剂,可选择性地阻滞5-HT3与中枢神经系统的化疗受体感受区和上消化道传入迷走神经的5-HT3受体结合,使之不发生呕吐,故对化疗所致急性恶心呕吐有很好的疗效。
甲地孕酮为半合成孕激素衍生物,以往多用于治疗晚期乳腺癌和子宫内膜癌[5],目前多项研究表明,甲地孕酮有促进脂肪合成和蛋白同化作用,可改善恶性肿瘤患者的食欲,增加体质量,提高患者的生活质量及对放化疗的耐受。作者曾用甲地孕酮治疗中晚期癌症患者[6],可明显改善患者的生活质量。敬新蓉等[7]用甲地孕酮联合NP方案治疗晚期非小细胞肺癌,甲地孕酮联合化疗组骨髓抑制及生活质量改善方面明显优于单用化疗组。张恩宁等[8]用甲地孕酮联合昂丹司琼预防胃肠道肿瘤化疗所致呕吐,较单用昂丹司琼有更好的预防效果,可明显改善患者的食欲。本观察用甲地孕酮联合格拉司琼预防高、中度催吐风险化疗药所致恶心呕吐及迟发性恶心呕吐,结果显示,治疗组比对照组无论是急性恶心、呕吐,还是迟发性恶心呕吐发生率均明显降低,差异均有统计学意义(P均<0.05),2组毒副反应相近,均可耐受。
总之,甲地孕酮联合格拉司琼预防高、中度催吐风险化疗药物所致恶心呕吐比单用格拉司琼更有效,并可明显改善患者的生活质量,值得临床推广应用。
[1]Hesketh PJ,Kris MG,Grunberg SM,et al.Proposal for classifying the acute emetogenicity of cancer chemotherapy[J].Clin Oncol,1997,15(1):103 -109.
[2]Jordan K,Kasper C,Schmoll HJ.Chemotherapy-induced nausea and vomiting:current and new standards in the antiemetic prophylaxis and treatment[J].Eur J Cancer,2005 ,41(2):199 -205.
[3]张晓静,张频.肿瘤化疗所致恶心呕吐的发生机制和药物治疗的研究进展[J].癌症进展,2006,4(4):348 -354.
[4]Grélot L,Dapzol J,Estève E,et al.Potent inhibition of both the acute and delayed emetic responses to cisplatin in piglets treated with GR205171,a novel highly selective tachykinin NK1 receptor antagonist[J].Br J Pharmacol,1998,124(8):1643 - 1650.
[5]Gibson LJ,Dawson CK,Lawrence DH,et al.Aromatase inhibitors for treatment of advanced breast cancer in postmenopausal women[J].Cochrane Database Syst Rev,2007 ,(1):CD003370.
[6]李春艳,张芳,孙晓芙,等.甲地孕酮对中晚期癌症患者生活质量的影响[J].新乡医学院学报,2005,22(4):374 -375.
[7]敬新蓉,陈健,钟国成.甲孕酮联合长春瑞滨顺铂治疗晚期非小细胞肺癌临床观察[J].中国肿瘤临床,2008,35(4):189-192.
[8]张恩宁,曲维庆,刘磊,等.甲地孕酮联合昂丹司琼对胃肠道肿瘤化疗所致呕吐预防效果的临床观察[J].中华肿瘤防治杂志,2009,16(17):1329 -1331.

