颅内动脉瘤患者血清差异蛋白质谱表达模型的研究
周 杰,陈礼刚,李定君,黄昌仁,刘洛同,明 扬,张 苓,李 昊
(泸州医学院附属医院神经外科,四川泸州646000)
颅内动脉瘤一旦破裂会带来极严重后果,而在其破裂之前如能早期发现并给予积极治疗,可明显降低患者的致残率和病死率,因此,对颅内动脉瘤的筛查及治疗具有重要意义。但目前这方面的研究尚少[1-2]。本实验拟采用表面增强激光解吸/离子化飞行时间质谱(surface-enhanced laser desorption/inionation-time of flight-mass spectra,SELDI-TOF-MS)技术筛选颅内动脉瘤患者血清特异蛋白标记物,建立人工神经网络诊断模型,为早期、无创筛选颅内动脉瘤提供实验依据。
1 资料与方法
1.1 一般资料 纳入病例为2007年7月至2010年12月本院神经外科收治的颅内动脉瘤患者。将45例颅内动脉瘤破裂患者作为破裂组,其中,男26例,女19例;年龄(45.1±7.1)岁。同时期收治的颅内动脉瘤未破裂患者作为未破裂组,其中,男28例,女17例;年龄(46.2±6.5)岁。将45例同时期于本院门诊部体检的健康者作为对照组,其中,男23例,女22例;年龄(47.1±6.9)岁。所有颅内动脉瘤患者经计算机断层扫描血管造影(computed tomography angiography,CTA)、数字减影血管造影(digital subtraction angiography,DSA)检查证实,均无动脉瘤和蛛网膜下腔出血家族史、脑出血及遗传性疾病史。
1.2 主要试剂与仪器 芥子酸、乙腈、三氟乙酸、甲醇、Tris-HCl、磷酸盐缓冲溶液(phosphate buffered solution,PBS)、丙酮及甲酸等均购自美国Sigma公司。金属亲和表面蛋白芯片、PBSⅡ/C型蛋白质指纹图谱仪系统均为美国Ciphergen公司产品。
1.3 标本收集 所有受试者清晨空腹,于前臂静脉采血5mL,4℃下静置30min,2h内送本院检验科蛋白组学实验室。4℃下离心5min(离心半径8cm,3 000r/min),取上清液(即血清)放入-80℃冰箱保存。实验时,从-80℃冰箱中取出样本,冰上融解0.5~1.0h,4℃下离心2min(离心半径8cm,10 000r/min),待用。
1.4 芯片检测 吸取10mL芥子酸溶液(芥子酸溶于50%乙腈和0.5%三氟乙酸所得的饱和溶液)与血清等量混合,芯片活化,吸取2mL混合液点样,晾干后再加入1μL芥子酸,室温下干燥,上机检测。设定参数:从相对分子质量为1.0×106开始检测,检测最大相对分子质量为1.0×108,相对分子质量优化范围为2.0×106~2.0×107,激光强度为210,开始检测灵敏度为9,集中在优化中心,用定量的方法获取数据,设置SELDI参数位置为20,开始位置为20,结束位置为80,每个位置平均5次递增。利用PBSⅡ/C型蛋白质指纹图谱仪对结合在芯片表面的血清蛋白质进行检测。
1.5 数据处理和模型建立 采用Ciphergen Proteinchip软件自动采集实验数据,采用Biomarker Wizard 3.1软件分别分析未破裂组和对照组(各30例)、未破裂组和破裂组 (各30例)的血清蛋白质指纹图谱差异,对实验数据进行聚类分析和统计学处理,以P<0.05为差异有统计学意义。运用人工神经网络模型对检测数据进行分析及优化,分别建立诊断模型。利用测试集样本(各15例)对模型进行双盲法验证,评价模型的准确性。
2 结 果
2.1 差异蛋白的检测 (1)检测未破裂组和对照组血清共获得135个蛋白质峰,两组有54个蛋白质峰表达的差异有统计学意义(P<0.05),其中8个蛋白质峰荷质比分布于2 000~20 000之间,两组比较差异显著(P<0.01)。在未破裂组与对照组血清中筛选差异表达的2个蛋白质峰分别为3 367.7和5 857.5,两组血清蛋白指纹图谱及相应的凝胶电泳图比较见图1。(2)检测未破裂组和破裂组血清共获得265个蛋白质峰,两组有79个蛋白质峰表达的差异有统计学意义(P<0.05),其中14个蛋白质峰荷质比分布于2 000~20 000之间,两组比较差异显著(P<0.01)。在未破裂组与破裂组血清中筛选差异表达的2个蛋白质峰分别为6 642.0和9 127.5,两组血清蛋白指纹图谱及相应的凝胶电泳图比较见图2。
2.2 建立筛选预测模型 (1)以荷质比为2 540.6、3 367.7、5 857.5及8 231.0的4个蛋白质峰作为输入节点建立的模型,其模拟计算的网络误差值最低,其中,以荷质比为2 540.6、3 367.7及5 857.5的差异蛋白对比正常血清表达显著升高(P<0.01);荷质比为8231.0的差异蛋白对比正常血清表达显著降低(P<0.01),见表1。(2)以荷质比为 2 938.2、4 065.3、6 642.0、9 127.5及16 021.6的5个蛋白质峰作为输入节点建立的模型,其模拟计算的网络误差值最低。其中,以荷质比为2 938.2、16 021.6的差异蛋白对比破裂组血清表达显著升高(P<0.01);荷质比为4 065.3、6 642.0及9 127.5的差异蛋白对比破裂组血清表达显著降低(P<0.01),见表2。
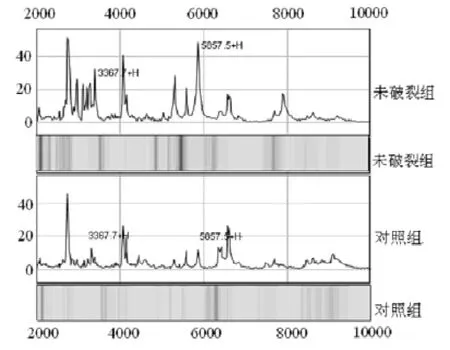
图1 未破裂组和对照组血清的蛋白指纹图谱及凝胶电泳图比较
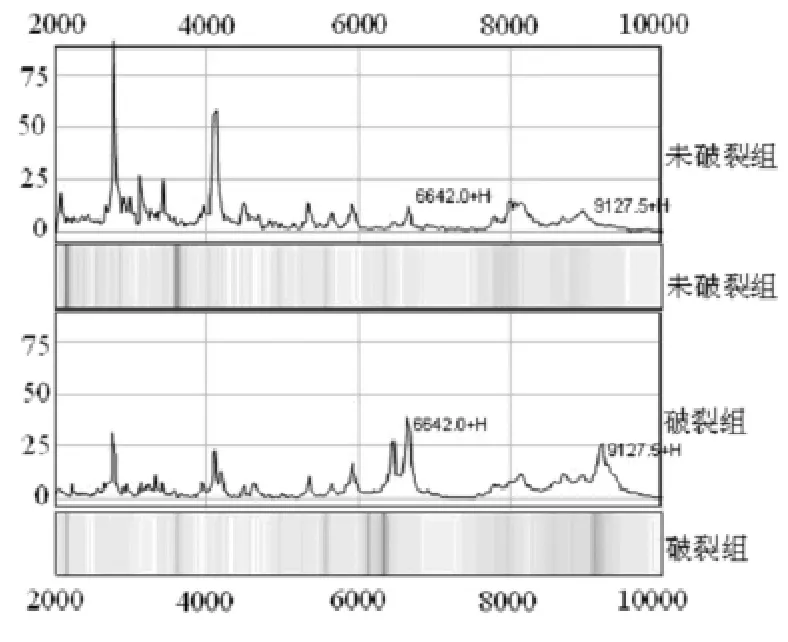
图2 未破裂组和破裂组血清的蛋白指纹图谱及凝胶电泳图比较
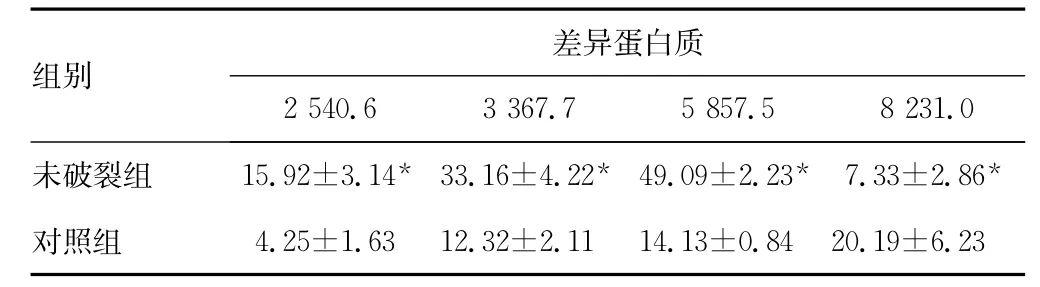
表1 4种差异蛋白质在未破裂组和对照组中的质谱峰值
2.3 人工神经网络诊断模型的双盲法验证 利用建立的人工神经网络诊断模型对测试集中样本(各15例)分别进行双盲法测试。验证结果显示:(1)15例未破裂组患者的血清中(目标输出值0.5~1.0)有1例判错;而在15例对照组患者的血清中(目标输出值0.0~0.5)有1例判错。经统计学分析处理,其灵敏度为93.3%,特异度为93.3%,阳性预测值为93.3%,阴性预测值93.3%。利用结果数据绘制受试者工作特征(receiver operator characteristic curve,ROC)曲线,ROC曲线下面积(area under ROC curve,AUC)为0.920(>0.7),说明该诊断模型准确,见图3。(2)15例未破裂组患者的血清中(目标输出值0.5~1.0)有1例判错;而在15例破裂组患者的血清中(目标输出值0.0~0.5)有2例判错。经统计学分析处理,其灵敏度为93.3%,特异度为86.7%,阳性预测值为87.5%,阴性预测值92.9%。利用结果数据绘制的ROC曲线,AUC为0.858(>0.7),说明该诊断模型准确,见图4。
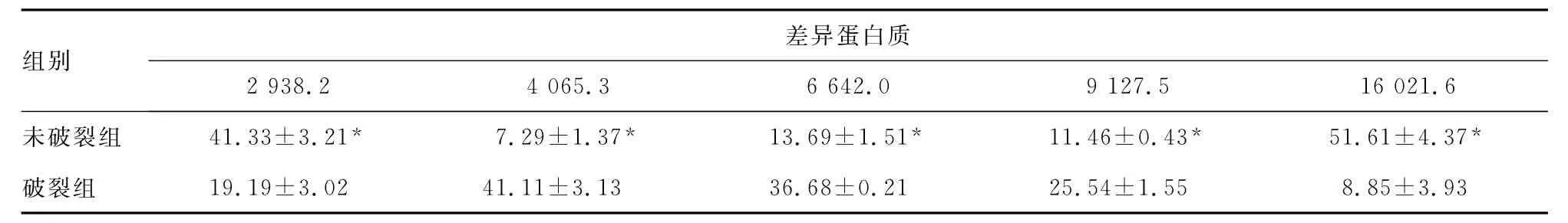
表2 5种差异蛋白质在未破裂动脉瘤和破裂动脉瘤组中的质谱峰值
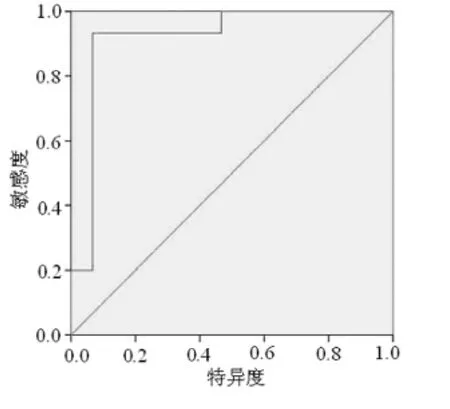
图3 未破裂组与对照组人工神经网络诊断模型的ROC曲线分析
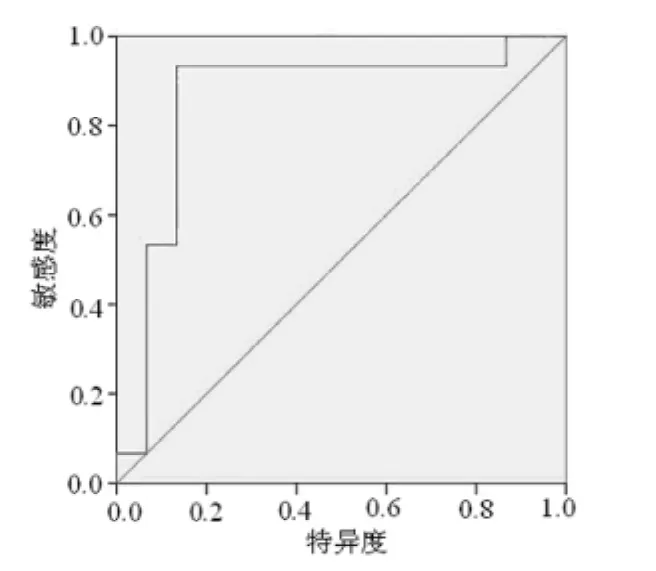
图4 未破裂组与破裂组人工神经网络诊断模型的ROC曲线分析
3 讨 论
目前,对于未破裂动脉瘤的筛选工作开展较少,尚缺乏快捷、行之有效的方法对颅内动脉瘤进行早期筛选和预测。DSA和CTA是目前诊断颅内动脉瘤的主要手段,但它们不能作为颅内动脉瘤的大规模筛选手段[3-4]。近年来越来越多的颅内动脉瘤在例行体格检查或因其他原因行头部磁共振成像、磁共振血管造影(magnetic resonance angiography,MRA)检查时被发现,因MRA无创、无辐射,且在颅内动脉瘤的诊断方面具有一定价值,相对DSA、CTA而言,它更适合用于人群的筛查。但作为筛查手段,MRA存在检查时间长、噪音大、费用高的弊端,且MRA可能漏诊或误诊较小动脉瘤和大动脉瘤[5]。鉴于动脉瘤破裂后的严重后果,确立可靠的无创筛查手段具有重要意义。
目前,尚不清楚颅内动脉瘤的发病机制,它可能与遗传、血流动力学以及后天退行性变等多种因素相关。研究表明基因突变、缺失以及表达异常在颅内动脉瘤的发生、发展过程中发挥重要的作用,因此,从分子水平上研究颅内动脉瘤的发病机制,进而对其进行基因诊断和治疗成为该领域的最新研究方向[6]。蛋白质组学的出现和发展极大地推动了疾病生物标志物的研究,它可以从整体水平上对一个细胞、一种组织中所包含的全部蛋白质进行时间和空间上的动态研究[7-8]。因此,对颅内动脉瘤患者血清蛋白指纹图谱的研究有可能发现特异性颅内动脉瘤诊断的生物标志。SELDI-TOF-MS技术检测的基本原理是基于特殊芯片的表面加强吸附,芯池中的分析物经激光脉冲辐射,解吸形成荷电离子,不同荷质比的离子在仪器漂移管中飞行的时间不同,质量越小,所带电荷越多的离子,其荷质比越小,飞行时间越短,检测器可对其进行检测并绘制成质谱图,经计算机软件处理后形成模拟图谱[9],将对照组与某种疾病或疾病不同阶段的图谱进行比较,可发现和捕捉特异相关蛋白。该技术优点在于:(1)可分析经典技术无法分析的蛋白质,包括疏水蛋白质、等电点过高或过低的蛋白质;(2)获得的图谱单一,重复性好,可用于定量分析;(3)样品无需纯化,可分析复杂的生物样品,增加发现生物学标志的机会;(4)样品需要量少,检测速度快,适合临床诊断及大规模筛选。近年来,它已被广泛用于生物标志物的发现和定义、蛋白质功能分析、肿瘤标志物筛选及药学研究等领域,同时,对颅脑损伤和颅内肿瘤进行的初步研究显示其在这一领域也具有一定的临床应用价值,但目前尚无颅内动脉瘤相关文献的报道[10-14]。
SELDI-TOF-MS技术的应用为大规模人群筛选提供了可能。Zhang等[15]运用SELDI-TOF-MS技术建立的诊断模型检测弥漫性大B细胞淋巴瘤的特异度和敏感度均为94%,检测预后不良患者的特异度为92%,敏感度为94%。吕晶晶等[16]用结直肠腺瘤患者、结直肠良性疾病患者及正常人血清的3种表达差异蛋白质的荷质比建立诊断模型,该模型的诊断准确率为87.70%、灵敏度为71.43%、总特异度为96.25%、阳性预测值为90.91%。本研究结果表明运用SELDI-TOF-MS技术检测未破裂组、破裂组及对照组患者的血清标本,获取相应血清蛋白表达指纹图谱,经统计分析以筛选未破裂组患者血清可能存在的特异蛋白是可行的,未破裂组、破裂组及对照组患者血清蛋白质谱的表达具有显著的差异性。根据不同分组的差异蛋白,运用人工神经网络模型分别建立其诊断模型,其AUC>0.7,说明该方法所建立的诊断模型准确可靠,可以作为未破裂颅内动脉瘤患者的潜在筛选手段。双盲法验证此诊断模型显示其可在短时间内较好地区分未破裂动脉瘤患者、破裂动脉瘤患者及健康者,说明该诊断模型适合于未破裂动脉瘤的筛选工作。
利用SELDI-TOF-MS技术筛选的血清特异蛋白标志物作为筛选颅内动脉瘤实验指标具有重要的潜在价值和一定的应用前景。首先,该方法血清样本容易获得,对患者创伤性小,检查耗时短,费用低,有利于临床高危人群筛选的应用和推广;其次,通过对颅内动脉瘤的蛋白质表达差异情况进行研究,进而对差异蛋白数量、结构、性质、相互关系和生物学功能进行全面分析,明确颅内动脉瘤血清差异蛋白在此疾病发生、发展过程中的作用,从而对颅内动脉瘤进行诊断和筛选,并可对这些“关键”蛋白进行干预,为基因治疗颅内动脉瘤提供临床和实验资料。然而,本研究在诸多方面还需进一步深入,如对实验方法学的完善以及实验条件的标准化,以增强实验可重复性,并进行多中心、大样本的联合研究。通过对这些潜在的生物标志物进行精确鉴定,确定其在动脉瘤发生、发展、破裂过程中的具体作用,为颅内动脉瘤的临床筛选提供可靠的实验依据。
[1] Menghini VV,Brown RD Jr,Sicks JD,et al.Clinical manifestations and survival rates among patients with saccular intracranial aneurysms:population-based study in Olmsted County,Minnesota,1965to 1995[J].Neurosurgery,2001,49(2):251-256.
[2] 翟宝进,刘欣民,李双英,等.颅内动脉瘤患者血清差异表达蛋白质的研究[J].中华神经外科杂志,2010,26(10):891-895.
[3]Joo SP,Kim TS,Kim YS,et al.Clinical utility of multislice computed tomographic angiography for detection of cerebral vasospasm in acute subarachnoid hemorrhage[J].Minim Invasive Neurosurg,2006,49(5):286-290.
[4] 林维斌,何理盛.颅内动脉瘤诊断与治疗的现状及进展[J].福建医药杂志,2007,29(2):98-100.
[5] Yang YJ,Chen WJ,Zhang Y,et al.Diagnostic value of CTA and MRA in intracranial traumatic aneurysms[J].Chin J Traumatol,2007,10(1):29-33.
[6] 杨呈浩,李定君,詹书良.与颅内动脉瘤发病机制相关基因研究现状[J].泸州医学院学报,2007,30(6):541-543.
[7] Lu HB,Zhou JH,Ma YY,et al.Five serum proteins identified using SELDI-TOF-MS as potential biomarkers of gastric cancer[J].Jpn J Clin Oncol,2010,40(4):336-342.
[8] Araki Y,Yoshikawa K,Okamoto S,et al.Identification of novel biomarker candidates by proteomic analysis of cerebrospinal fluid from patients with moyamoya disease using SELDI-TOF-MS[J].BMC Neurol,2010,10:112.
[9] 伍健,黄培林.SELDI蛋白质芯片技术在肿瘤蛋白质组学研究中的应用[J].东南大学学报:医学版,2004,23(5):347-350.
[10]Lin YW,Lin CY,Lai HC,et al.Plasma proteomic pattern as biomarkers for ovarian can cer[J].Int J Gynecol Cancer,2006,16Suppl 1:S139-146.
[11]谭小林,任兴军,王开正,等.食管癌血清差异蛋白质组测定结果分析[J].重庆医学,2011.40(7):641-643.
[12]张蓉,张莉.心理训练对心理应激后陆军特种兵血清蛋白质谱特征的影响[J].解放军医学杂志,2011,35(9):985-987.
[13]李杰,陈茂伟,周怡,等.乙肝肝纤维化血清标记物筛选的初步研究[J].实用医学杂志,2011,27(15):2724-2727
[14]Dursun E,Monari E,Cuoghi A,et al.Proteomic profiling during atherosclerosis progression using SELDI-TOFMS:effect of darbepoetin treatment[J].Acta Histochem,2010,112(5):432-443.
[15]Zhang MZ,Sun ZC,Fu XR,et aI.Analysis of serum proteome profiles of non-Hodgkin lymphoma for biomarker identification[J].J Proteomics,2009,72(6):952-959.
[16]吕晶晶,高春芳,王秀丽,等.SELDI-TOF-MS技术在结直肠腺瘤血清蛋白质指纹图谱筛查模型建立中的应用[J].山东医药,2010,50(34):7-9.

