含莫西沙星方案与含左氧氟沙星方案对耐多药肺结核病的观察
吴树才 高官聚 耿书军 张向丛
耐药和耐多药肺结核病(MDR-PTB)直接威胁人类健康,当前MDR-PTB的增多和广泛传播已成为结核病疫情严重程度的标志[1]。笔者采用含莫西沙星(MXFX)及含左氧氟沙星(LVFX)方案联合母牛分枝杆菌菌苗(M.vcacae)治疗MDRPTB,以评价MXFX的疗效及其安全性,为MDR-PTB的治疗提供依据。
1 资料与方法
1.1 一般资料 病例选择:(1)痰涂片镜检、培养阳性并经菌型鉴定为结核分枝杆菌,经药物敏感试验证实至少同时耐利福平(RFP)、异烟肼(INH)者;(2)X线胸片证实肺内有活动性病变,含或不含空洞;(3)无肝、肾、血液系统疾患、精神病、癫痫、支气管哮喘、糖尿病、职业病等重要并存病史者;(4)对治疗药物无过敏史;(5)自愿接受本试验的患者。分组:采用随机对照试验方法分为治疗组(T组)和对照组(C组),2组在年龄、性别比、病程、耐药情况、体质量、病变严重程度方面差异无统计学意义(P>0.05),具有可比性。2组耐药情况见表1。

表1 2组患者耐药种类 n=39,例(%)
1.2 研究方法
1.2.1 治疗方案:T组:6 MDEZA(C)/612MDE、6MDEBTh/12MDE;C 组:6 VDEZA(C)/12MDE、6DVEBTh/12MDE,其中M:莫西沙星,MXFX,商品名:拜复乐,由德国拜耳公司生产,0.4 g,1次/d;V:左氧氟沙星,LVFX,商品名:利复星,北京双鹤药业股份有限公司生产,0.6~0.8 g,1次/d;D:对氨基水杨酸异烟肼,PSNZ,商品名:力克菲蒺,重庆华邦制药股份有限公司生产,0.4 ~0.6 g,2 次/d;E:乙胺丁醇,EMB,上海信谊药业有限公司生产,0.75~1.0 g,1次/d;Z:吡嗪酰胺,PZA,上海信谊药业有限公司生产,0.5 g,3次/d;Th:丙硫异烟胺,1321Th,上海信谊药业有限公司生产,0.2 g,3次/d;B:利福布丁,RFB,四川明佳欣药业有限责任公司生产,300 mg,1次/d;A:阿米卡星,AK,山东鲁抗制药有限责任公司生产,0.4 g,1次/d,肌内注射;C:卷曲霉素,CP,由和力达药业责任有限公司生产,0.75 g,1次/d,静脉滴注。2组抗痨方案除FQNs外其余药物在配对上相同。所有患者于治疗期间前6个月加用M.vaccae(安徽龙科马制药有限公司生产)22.5 μg,深部肌内注射,1次/15 d,公式中数字表示治疗时间(月)。所有患者全程加用护肝药物,体弱者酌情加用营养支持疗法,有合并症及并存症者予以相应处理。
1.2.2 化疗管理:采用全程监督化疗管理,与患者及家属签订医患合约书,规定住院期间在医务人员面视下服药,出院后由家属遵医嘱监督面视服药,出院后每月随访1次,到疗程结束,随时记录药物不良反应,以确保患者全程规律化疗。
1.3 观察项目 治疗前详细记录患者病史、用药史、症状、体征及并发(存)症等情况,住院期间,每天观察患者一般症状及体征变化,记录药物不良反应,并给予处理。用药前查痰涂片3次,结核菌培养加菌型鉴定及药敏试验各1次,治疗后2、4、6、9、12、18、24个月查痰涂片3次及痰培养1次(无痰或少痰者可采用气雾法进行导痰),治疗前摄胸片及胸部CT 1次,治疗后于满 2、4、6、9、12、18、24 个月各复查胸部 X 线片 1 次,6、12、18、24个月时查胸部CT 1次。
1.4 疗效评定标准 依据2005年中华医学会临床诊疗指南制订的标准评定疗效[2]:(1)细菌学:以连续3个月痰菌阴转,且不再复阳为阴转标准。(2)X线检查:①明显吸收:病变吸收≥1/2;②吸收:病变吸收<1/2;③无改变:病变无变化;④恶化:病变增大或出现新病变;⑤X线好转:明显吸收+吸收;⑥空洞缩小≥1/2为缩小;缩小<1/2为不变;⑦增大≥1/2为增大;⑧空洞消失为闭合。
2 结果
2.1 患者情况 依照标准选例:共纳入78例,T组39例,其中男26例,女13例;C组39例,其中男29例,女10例。因各种原因脱落15例,可评价疗效者63例:T组33例,其中男25例,女8例;年龄26~65岁,平均年龄(45±15)岁;病程0.5~19年,合并空洞者29例;C组30例,其中男21例,女9例;年龄28~65岁,平均年龄(41±14)岁;病程0.5~16.5年;合并空洞者25例。
2.2 临床症状 接受MXFX治疗者咳嗽、咳痰症状改善较快,为6~26 d,平均(16±5)d,而用 LVFX 为15~54 d,平均(35±11)d,差异有统计学意义(χ2=24.0780,P <0.01)。
2.3 痰菌阴转率 治疗满2个月及4个月时,2组比较差异有统计学意义(P<0.05);以后各期T组均大于C组,差异均无统计学意义(P>0.05)。见表2。
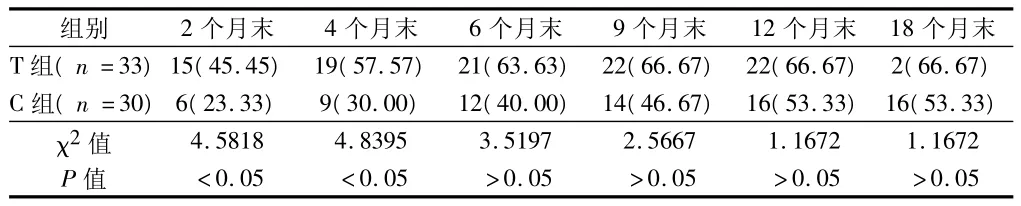
表2 治疗期间不同时间痰菌累积阴转情况 例(%)
2.4 病灶情况 疗程末病灶吸收好转率及空洞闭合率比较,2组差异无统计学意义(P>0.05)。见表3。
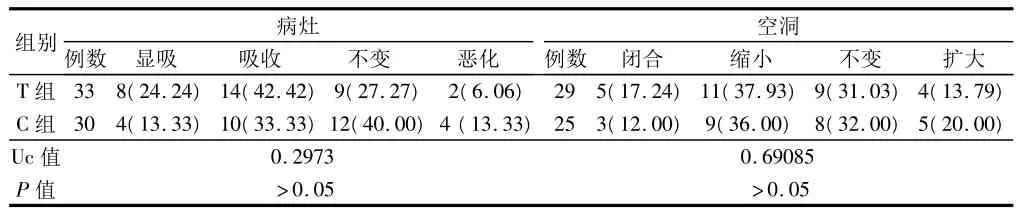
表3 治疗后病灶、空洞变化情况比较 例(%)
2.5 不良反应 共退组15例。T组6例,原因:肝功损害2例,消化道反应(恶心、呕吐、腹部不适、腹泻)不能坚持治疗2例,神经系统症状(严重头晕、失眠、兴奋)1例,白细胞减少1例。C组9例,原因:肝功能损害4例,消化道反应不能坚持治疗2例,神经系统症状2例,用LVFX后Q-T延长1例。其他患者的不良反应为轻度消化道反应,2组各6例,对症治疗后可继续坚持治疗;总的不良反应发生率T组为30.77%(12/39),C组为38.46%(15/39),2组比较差异无统计学意义(χ2=0.5098,P>0.05)。2组均无继发真菌感染及光敏等现象发生,无死亡病例。
3 讨论
MDR-PTB的治疗是国际公认的难题,WHO在20世纪90年代结核病研究和发展战略规划中,提出化疗与免疫疗法相结合的治疗措施[3]。笔者采用含莫西沙星(MXFX)方案并加用M.vaccae治疗MDR-PTB,达到了预期的临床效果。
MXFX是由德国拜耳公司研制开发的一种新型8-甲氧基FQNs,是现有 FQNs中抗 MTB 活性最高的品种[4],FQNs的作用机制为抑制结核菌DNA旋转酶A亚单位,该酶是细菌复制的基础[5],各种FQNs间存在交叉耐药性,近年来随着FQNs类药物的滥用,MTB对FQNs耐药程度越来越严重,明显影响了FQNs的治疗效果,肖和平等[5]提出对耐多药结核病,仍推荐使用最高级的FQNs,以确保其发挥最佳效果,并使耐本类药物的几率降至最低。MXFX具有良好的药代动力学特性,在支气管黏膜、肺组织及肺巨噬细胞内药物浓度显著高于血药浓度[6]不良反应小,这些特点均表明MXFX治疗MDR-PTB的优势作用。
FQNs的临床应答呈现出剂量相关性[7],LVFX已广泛应用于MDR-PTB的治疗,陆宇提出 LVFX临床最大耐受量为800 mg/L,用于治疗结核病效果理想[8],为使C组治疗同样有效,本研究LVFX应用0.6~0.8 g/d,而不是常规用量0.4 g/d。
MTB具有编码调控其“潜伏性”、“特留性”、“突变性”及“致病性”等特征的多种基因,部分细菌呈静止或低代谢状态持留体内[9]。此为长程用药及应用免疫增强剂的依据,此研究用药时间为18个月,M.vaccae可介导保护性免疫反应[10],可以加速MDR-MTB的持续清除,故在治疗期间的前6个月所有患者均加用了M.vaccae。
治疗后最明显的改变是接受MXFX治疗者咳嗽、咳痰症状改善较快,考虑是由于MDR-PTB易继发肺部感染,而MXFX的化学结构是在8位碳原子引入了甲氧基团,增加了对非特异性细菌的结合能力和对细胞膜的穿透破坏能力,而且抗菌后效应强大而持久[11],另一方面与MDR-MTB的快速抑制也有关。痰菌阴转率在治疗满2个月T组为45.45%,C组为23.23%(P<0.05),满4个月分别为为57.57%,40.00%(P <0.05),显示MXFX有比LVFX更快地清除MDR-MTB的作用;而C组的痰菌阴转率在9~12月间仍有变化,如此长的阴转时间为MDR-MTB耐FQNs提供了机会。通过此研究推测MXFX较LVFX不易产生耐药性,6个月后各期痰菌阴转率T组均大于C组,经统计学处理差异无统计学意义(P>0.05),疗和结束时T组阴转率66.67%,C组53.33%,2组对比无统计学意义,需要进一步扩大样本含量。病灶吸收率、空洞闭合率2组比较差异无统计学意义(P>0.05)。此2组患者病灶吸收好转率均较低,考虑与患者患病时间长、肺部存在大面积干酪病变及肺毁损、多发或厚壁纤维空洞、支气管扩张、间质损害等有关,痰菌阴转较病变吸收好转要早,停药后在很长一段时间内病变仍会继续吸收好转。
联合化疗是结核病化学治疗的核心,但多种药物联合不可避免地增加药物不良反应(ADRs)发生的几率[11]。此为正确实施结核病化疗的一大障碍,本实验ADRs发生率 T组为30.76%,C组为38.46%(P >0.05),ADRs不是单纯FQNs所致,是所有使用抗结核药物ADRs的总和。ADRs大多为消化道反应,对症处理后可坚持治疗。由于此类患者对治疗的依从性差,忘记服药、或由于药物ADRs自行停药或减少药物剂量时常发生,故需全程监督管理,及时正确处理ADR,以确保结核化疗的顺利进行。
本研究显示MXFX对MDR-PTB的治疗是有效并且是安全的。目前临床应用的MXFX是德国拜耳公司产品-拜复乐,我国尚不能生产,价格偏贵是其不足,能否于6个月后将MXFX换用国产的3、4代FQNs继续治疗有待进一步研究。
1 朱莉贞,傅瑜,初乃惠,等.利福类联合多种药物长疗程方案治疗耐多药肺结核.中华结核和呼吸杂志,2006,29:520-523.
2 中华医学会主编.临床诊疗指南(结核病分册).第1版.北京:人民卫生出版社,2005.87-91.
3 Broermans JF,Migliori GB,Rieder HL,et al.Recommendations of the world Health organization(WHO),International Union against tuberculosis and lung Disease(IUATU)and Royal Netherlands Fuberculosis Association(KNCV)working group.Eur Respir J,2002,19:765-775.
4 肖和平.耐多药肺结核的化学治疗.辽宁医学,2005,22:635-638.
5 肖和平,唐神结.二线抗结核药物的临床应用.中国防痨,2009,31:612-616.
6 张宇.喹诺酮类抗菌药的研究进展.中国新药杂志,2006,15:1344-1350.
7 李建华,宋丰贵,王华.氟喹诺酮类药物在耐多药结核病治疗中的应用.中国药业,2007,16:25-27.
8 陆宇,朱莉贞,段连山,等.左氧氟沙星的抗结核作用研究.中华结核和呼吸杂志,1999,22:693-695.
9 马宇.结核病的化学治疗及面临的挑战.中国医学科学院学报,2009,31:389-392.
10 初乃惠,罗永艾,朱莉贞,等.化疗加免疫长疗程方案治疗耐多药结核病的随机对照研究.中国防痨,2009,31:10-14.
11 孟静娟.新抗生素莫西沙星国内外研究应用最新进展.微生物学杂志,2007,27:98-101.

