HPLC法同时测定蝎龙酒中芍药苷、羟基红花黄色素A和阿魏酸
王亚洲
(广西医科大学第四附属医院,广西 柳州 545005)
HPLC法同时测定蝎龙酒中芍药苷、羟基红花黄色素A和阿魏酸
王亚洲
(广西医科大学第四附属医院,广西 柳州 545005)
目的建立蝎龙酒(全蝎、当归、白芍、红花、地龙、威灵仙、杜仲等)中芍药苷、羟基红花黄色素A和阿魏酸的测定方法。方法采用反相高效液相色谱法进行定量分析,用Inertsil C8-3柱,乙腈-0.1%磷酸-四氢呋喃(18∶80∶2)为流动相,体积流量为1.0 mL/min,检测波长为340 nm。结果芍药苷、羟基红花黄色素A和阿魏酸的线性范围分别为46.69~466.95 μg/mL、11.13~111.35 μg/mL和4.84~48.4 μg/mL;平均加样回收率分别为101.08%、99.85%和100.34%(n=6)。结论此法简便、准确,具有良好的重复性和回收率,适用于蝎龙酒中3种成分的同时测定。
高效液相色谱法;蝎龙酒;芍药苷;羟基红花黄色素A;阿魏酸
蝎龙酒为广西医科大学第四附属医院院内制剂,处方包括全蝎、当归[1]、白芍[1]、红花[1]、地龙、威灵仙、杜仲等数味中药,有解毒止痛、强筋健骨、活血通经等功效,临床用于治疗各种风湿痹痛所致四肢麻木、腰膝酸痛、骨质增生、跌打损伤、中风后遗症、偏头痛等,疗效明显[2-3],副作用小。原质量标准中仅对白芍进行鉴别,规定总固体量不少于1%,并无定量测定内容。为进一步提高本制剂质量标准,更有效地控制成品质量,本实验参阅有关文献[4-6],经反复摸索,建立一种高效液相色谱测定方法,可以同时测定蝎龙酒中芍药苷、羟基红花黄色素A和阿魏酸3种成分。
1 仪器与试药
LC—10ATvp高效液相色谱仪(SHIMADZU公司);752型紫外分光光度计(南京麒麟公司);AB—L电子分析天平(梅特勒-托利多公司);MP511电子pH计(上海三信公司),B2500S型超声波清洗器(BRANSON公司)。芍药苷对照品(中国药品生物制品检定所,批号110736-200630);羟基红花黄色素A对照品(上海源叶生物科技有限公司,批号20110311);阿魏酸对照品(上海源叶生物科技有限公司,批号20110406);甲醇、乙腈为色谱纯,其他试剂为分析纯,水为重蒸馏水,蝎龙酒(本院制剂室自制,批号:110809、110822、110830)。
2 试验方法与结果
2.1 色谱条件及系统适用性实验Inertsil C8-3柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.1%磷酸-四氢呋喃(18∶80∶2);检测波长340 nm;柱温30℃;体积流量1.0 mL/min;进样量20 μL。在此色谱条件下,芍药苷、羟基红花黄色素A和阿魏酸均能够达到基线分离,其它成分对测定没有干扰。芍药苷保留时间约为8.4 min,羟基红花黄色素A保留时间约为10.7min,阿魏酸保留时间为14.1min。见图1。

图1 供试品(A)、阴性对照品(B)和对照品(C)高效液相色谱图Fig.1 HPLC chromatograms of sample(A),negative sample(B)and mixed reference substances(C)
2.2 对照品溶液的制备称取经五氧化二磷减压干燥至恒质量的芍药苷、羟基红花黄色素A和阿魏酸对照品适量,精密称定,置于棕色量瓶中,加50%甲醇制成每1 mL分别含芍药苷1 867.8 μg、羟基红花黄色素A 445.4 μg和阿魏酸193.6 μg,即得。
2.3 供试品溶液的制备精密称取蝎龙酒10 mL,置于100 mL量瓶中,加甲醇至刻度,0.45 μm微孔滤膜过滤,即得。
2.4 阴性对照品溶液的制备按照处方组成,取除白芍、红花和当归以外的其余药材,按工艺要求制成不含芍药苷、羟基红花黄色素A和阿魏酸的合剂,按照供试品溶液制备项下的方法,即得阴性对照品溶液。
2.5 线性范围考察取上述混合对照品溶液适量,用50%甲醇稀释成6个质量浓度,即得芍药苷质量浓度分别为46.69、93.39、186.78、280.17、373.56、466.95 μg/mL,羟基红花黄色素A质量浓度分别为11.13、22.27、44.54、66.81、89.08、111.35 μg/mL,阿魏酸质量浓度分别为4.84、9.68、19.36、29.04、38.72、48.4 μg/mL的溶液。依次进样,按上述色谱条件测定,再分别以3成分的进样质量浓度为横坐标,以相应的峰面积为纵坐标绘制标准曲线,芍药苷、羟基红花黄色素A和阿魏酸的回归方程分别为:Y=10 216X+769,r=0.999 7(n=6);Y=24 753X+1 975,r=0.999 5(n=6);Y=83 437X-5 612,r=0.999 4(n=6)。结果表明,3成分的线性范围分别为46.69~466.95 μg/mL、11.13~111.35 μg/mL和4.84~48.4 μg/mL。
2.6 进样精密度试验分别取上述混合对照品溶液1 000、500、200 μL,置于10 mL量瓶中,用甲醇定容至刻度,配成高、中、低3种质量浓度。分别在同日内连续进样5次,计算日内精密度,结果芍药苷、羟基红花黄色素A和阿魏酸的RSD值分别为1.21%、1.07%和1.49%(n=5);在5日内连续进样5次,计算日间精密度,结果三者的RSD值分别为1.96%、2.351%和2.14%(n=5),说明本法进样精密度良好。
2.7 重复性试验取同一批(批号:110809)蝎龙酒,按供试品溶液制备方法制得6份,再按照上述色谱条件测定。测得芍药苷、羟基红花黄色素A和阿魏酸的RSD值分别为0.77%、1.26%和1.04%,说明本法重复性良好。
2.8 加样回收率试验取已知含有量的同一批(批号:110809)蝎龙酒6份,分别置于量瓶中,再加入一定量的混合对照品溶液,按供试品溶液制备方法制备成供试品溶液,并按上述色谱条件进行测定。计算结果见表1。
2.9 样品测定按2.3项供试品溶液的制备方法制备3批蝎龙酒供试品溶液,每批进样5次,按上述色谱条件测定,计算供试品溶液的质量浓度,结果见表2。
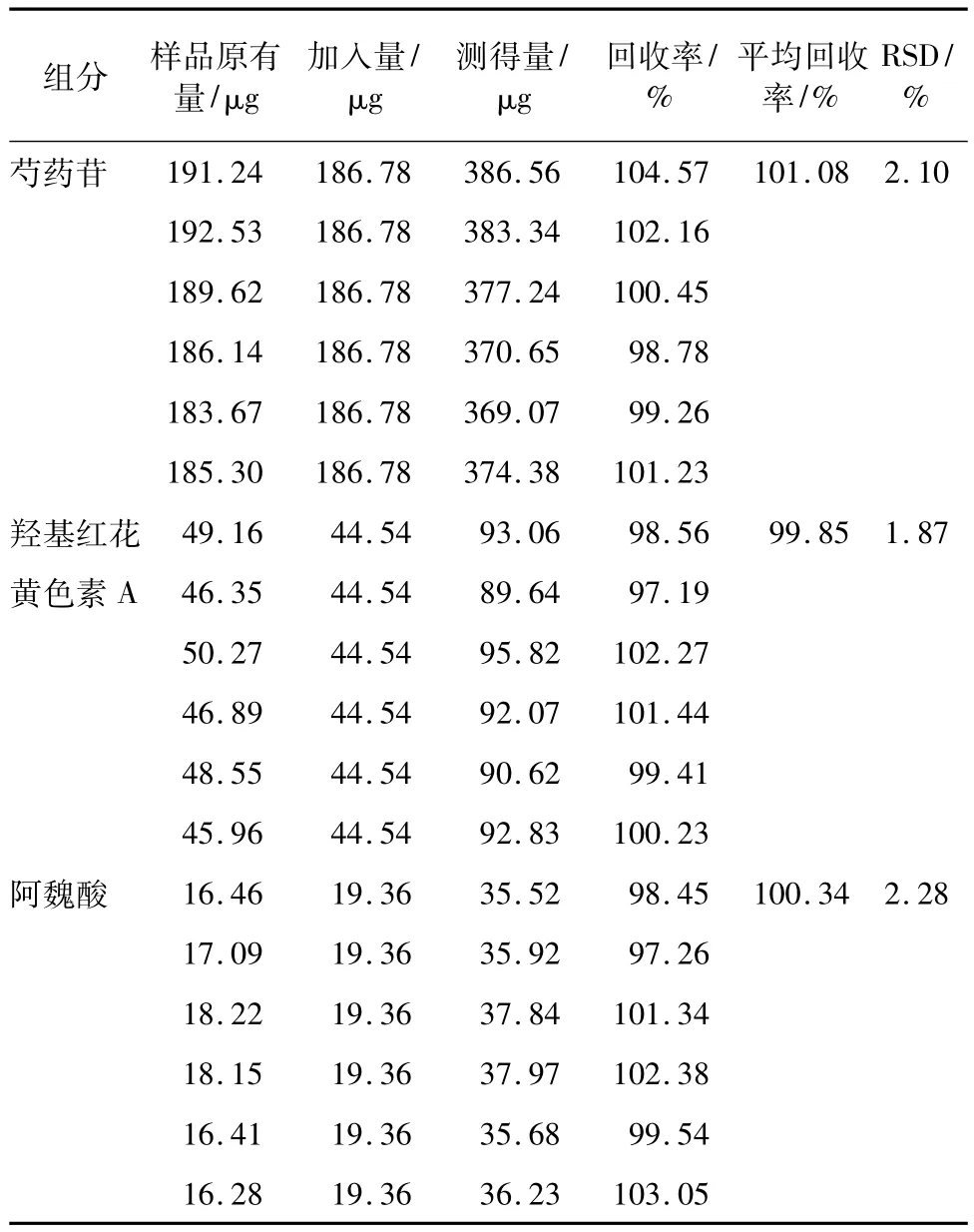
表1 加样回收率试验结果(n=6)Tab.1 Results of recovery tests(n=6)
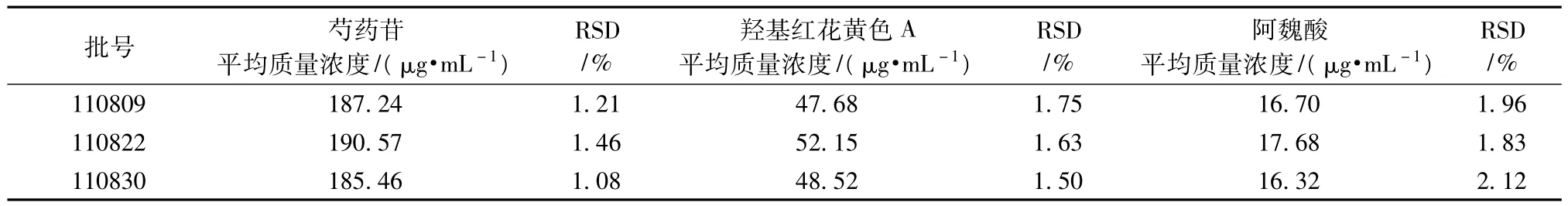
表2 样品测定结果(n=5)Tab.2 Results of sample assay(n=5)
3 讨论
HPLC法同时测定制剂中几种成分,选择合适的检测波长尤为关键。本实验将芍药苷、羟基红花黄色素A和阿魏酸的对照品溶液分别进行全波长紫外扫描,确定芍药苷最大吸收波长为230 nm,羟基红花黄色素A最大吸收波长为403 nm,阿魏酸的最大吸收波长为327 nm。在上述色谱条件下,分别于230 nm、300 nm、327 nm、340 nm和403 nm等处对供试品溶液进行分析,发现阿魏酸最大吸收波长327 nm附近的340 nm处所得的HPLC图谱上各成分峰分离效果较好,杂质干扰峰亦被消除,且能较好地兼顾含有量较小的阿魏酸和羟基红花黄色素A的峰形,因此选择340nm作为检测波长。
参考有关文献[7-9],经过不同流动相的摸索,发现乙腈-0.1%磷酸-四氢呋喃(18∶80∶2)为测定流动相时,3成分的出峰时间更合适,峰形好、无拖尾,且不受杂质峰干扰。在流动相中少量加入的四氢呋喃,很好的改善了峰形。但四氢呋喃容易与流动相中的溶解氧形成有紫外吸收的络合物,此络合物会提高背景吸收(特别是在260 nm以下),导致检测灵敏度的轻微降低[10],所以试验流动相必须预先彻底脱气。四氢呋喃易被氧化从而可能在色谱图中产生倒峰,故添加四氢呋喃的流动相宜现用现配。
反相高效液相色谱法同时测定中药合剂中芍药苷、羟基红花黄色素A和阿魏酸在国内尚未见文献报道,本实验建立的测定方法灵敏度高、专属性好,为其它制剂的HPLC法测定上述3种成分提供了方法参考。相比于文献[11-12]中的调pH再乙醚萃取法,本试验中仅需对合剂稀释即可进行定量测定,操作简便易行。对3批样品分别进行分析,测定结果准确、重复性好,说明本法可作为控制蝎龙酒质量的定量方法。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[2]杨春旭,戴盛明,李桂生.蝎龙酒对血瘀大鼠血液流变学及正常大鼠血小板功能影响的实验研究[J].广西医学,2002,24(6):763-764.
[3]朱灵,杨春旭,黎渊弘,等.蝎龙液浸膏体内外对动物凝血功能及血栓形成的影响[J].现代中药研究与实践,2008,22(4):22-24.
[4]凌明,马安宇.HPLC测定胃肠合剂中芍药苷和黄芩苷的含量[J].中成药,2008,30(9):1311-1313.
[5]黄安军,聂晓玲.HPLC法同时测定乳核内消液中芍药苷和阿魏酸的含量[J].西北药学杂志,2009,24(6):436-437.
[6]倪文澎,钱平,周琴妹,等.RP-HPLC法同时测定养生丸中芍药苷和阿魏酸的含量[J].中国药师,2010,13(8):1114-1116.
[7]李生有.HPLC测定丹夏头痛胶囊中阿魏酸的含量[J].中成药,2007,29(2):附6-附7.
[8]王玉华,郝美玲,王伟.HPLC测定蒙成药檀香清肺二十味丸中羟基红花黄色素A的含量[J].中成药,2008,30(1):143-144.
[9]刘岩,刘顺航,贾佳丽,等.HPLC同时测定广东汤中葛根素和芍药苷的含量[J].中成药,2007,29(6):842-845.
[10]张庆合.高效液相色谱实用手册[M].北京:化学工业出版社,2008,83.
[11]梁陈方,杨春旭,吴洪文,等.高效液相色谱法测定蝎龙酒中阿魏酸的含量[J].时珍国医国药,2009,20(7):1661-1662.
[12]吴洪文,李明艳.高效液相色谱法测定蝎龙酒中芍药苷的含量[J].中国医院药学杂志,2010,30(17):1486.
Simultaneous determination of paeoniflorin,hydroxysafflor yellow A and ferulic acid in Xielong Liquor by HPLC
WANG Ya-zhou
(The No.4 Affiliated Hospital of Guangxi Medical University,Liuzhou 545005,China)
AIMTo establish a method for determining the contents of paeoniflorin,hydroxysafflor yellow A and ferulic acid in Xielong Liquor(Scorpio,Angelicae sinensis Radix,Paeoniae Radix alba,Carthami Flos,Pheretima,Clematidis Radix et Rhizoma,Eucommiae Cortex,etc.).METHODSThe quantitative analysis was carried out by HPLC with an Inertsil C8-3column.The mobile phase was acetonitrile-0.1%phosphoric acid-tetrahydrofuran(18∶80∶2)with a flow rate at 1.0 mL/min.The detection wavelength was set at 340 nm.RESULTSThe linear ranges for paeoniflorin,hydroxysafflor yellow A and ferulic acid were 46.69-466.95 μg/mL,11.13-111.35 μg/mL and 4.84-48.4 μg/mL,respectively.Their average recoveries were 101.08%,99.85%and 100.34%(n=6),respectively.CONCLUSIONThis method is simple and accurate,with good reproducibility and recovery.It is suitable for the determination of the contents of paeoniflorin,hydroxysafflor yellow A and ferulic acid in Xielong Liquor.
HPLC;Xielong Liquor;paeoniflorin;hydroxysafflor yellow A;ferulic acid
R927.2
A
1001-1528(2012)10-1925-04
2012-01-13
广西科技厅攻关基金资助项目(9920028);广西柳州市科技局科技攻关基金资助项目(990608)
王亚洲(1979—),男,硕士,主管药师,从事药品质量控制工作。Tel:(0772)3802560,E-mail:lzpharmacy@163.com

